苏教化学必修2专题4第二单元 化学是社会可持续发展的基础(共18张PPT)
文档属性
| 名称 | 苏教化学必修2专题4第二单元 化学是社会可持续发展的基础(共18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 926.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-20 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
随着经济的发展和科学技术的进步,化学与其他学科齐头并进,迅速发展,成为21世纪自然学科的中心学科。
化学科学发展的历史,是一部人类逐步深入认识物质组成、结构、变化的历史,也是一部合成、创造更多新物质,推动社会经济发展和促进人类文明发展的历史。
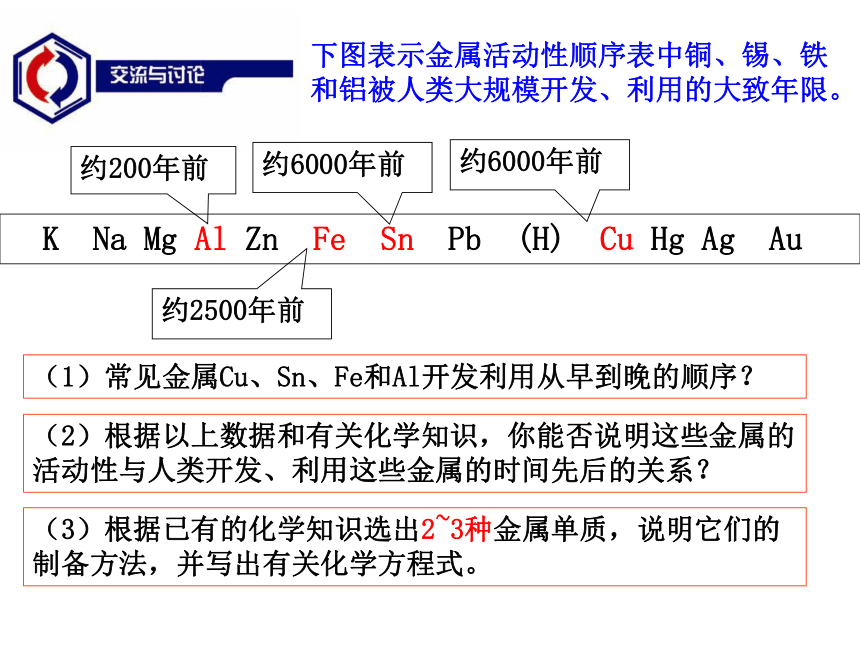
下图表示金属活动性顺序表中铜、锡、铁和铝被人类大规模开发、利用的大致年限。
K Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Au
(2)根据以上数据和有关化学知识,你能否说明这些金属的活动性与人类开发、利用这些金属的时间先后的关系?
(3)根据已有的化学知识选出2~3种金属单质,说明它们的制备方法,并写出有关化学方程式。
(1)常见金属Cu、Sn、Fe和Al开发利用从早到晚的顺序?
1.金属使用的发展历程
金属铜约在6000年前已大规模利用,铁约在2500年前,而铝的使用仅有200年左右,这与____________及_____________有关。
2.金属的活动性与金属冶炼的关系
②冶炼依据:金属的__________不同,冶炼方法不同;
③冶炼方法:_________、____________、__________及__________。
电解法
热还原法
热分解法
富集法
活动性
金属活动性
冶炼技术
一、人类对金属使用的发展过程
CuSO4+Fe === Cu +FeSO4
生物炼铜
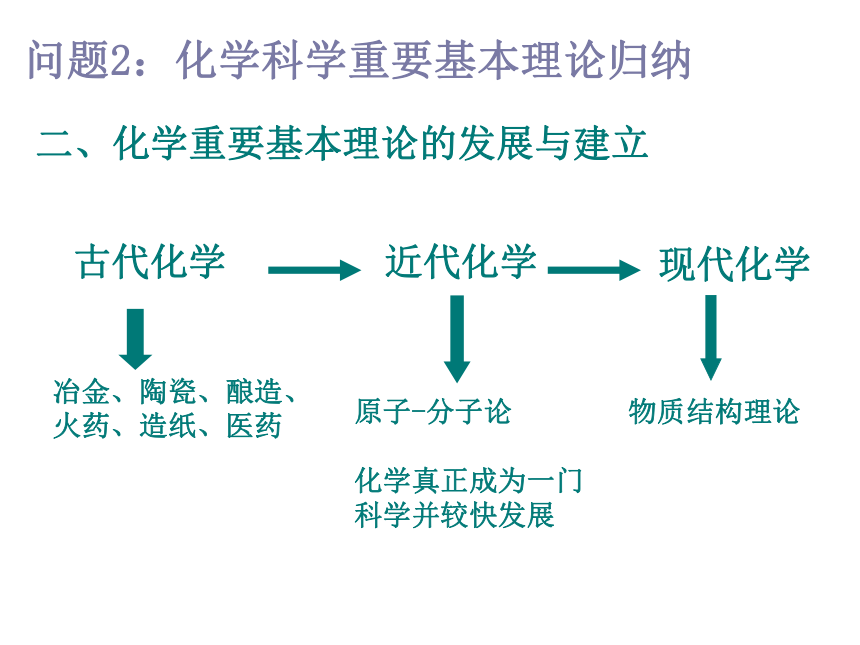
古代化学
冶金、陶瓷、酿造、
火药、造纸、医药
近代化学
原子-分子论
化学真正成为一门科学并较快发展
现代化学
物质结构理论
二、化学重要基本理论的发展与建立
问题2:化学科学重要基本理论归纳
二、化学基本理论的建立与发展
(1)19世纪,
①以 、 和 为中心内容的经典
②1869年 发现了 ;
③提出了 定律,奠定了化学反应的 基础;
④ 的合成彻底动摇了“生命力论”,使有机化学得到迅猛发展。
(2)20世纪
①化学家 提出了 和 的螺旋结构模型,为DNA分子的双螺旋结构模型的提出奠定了基础。
②扫描隧道显微镜的发展,实现了对__________的操纵。
道尔顿原子论
分子结构
原子价键理论
原子分子论
元素周期律
质量作用
动力学
人工尿素
鲍林
氢键理论
蛋白质分子
知识梳理
1
门捷列夫
原子或分子
近代化学阶段
原子学说的创立者
有关原子结构理论的建立
1869 年,俄国科学家门捷列夫将当时已知的 63 种化学元素按原子量大小排列成一个规范的统计表,这个元素周期表揭示了一个非常重要而有趣的规律----元素周期律。门捷列夫根据这个规律纠正了一些错误的原子量,还先后预言了 15 种以上的未知元素。于是,新发现的化学元素就“落户”到了今天元素周期表里来了
元素周期表
近代化学阶段
人工合成出了尿素,彻底动摇了“生命力论”,使有机化学得到了迅速发展。
历史上曾经有人认为,有机化合物只能由生物的细胞在一种特殊力量 生命力的作用下产生,人工合成有机物是不可能的。
1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,由氯化铵和氰酸银反应制得)水溶液得到了尿素[CO(NH2)2]。尿素的人工合成,揭示了人工合成有机物的序幕。
近代化学阶段
建立了物质结构理论-量子化学
使物质世界的秘密进一步揭开,打开了原子的大门,合成物质大量出现。
水晶及其结构
现代化学阶段
鲍林
化学键理论的先驱
现代化学阶段
微观结构观测仪器:
光学显微镜
电子显微镜
扫描隧道显微镜
用硅原子组成的两个汉字“中国”
用STM技术写成的字母“IBM”
问题3:人类对酸碱概念认识的发展
阅读教材P93《人类对酸碱认识的发展》回答下列问题:
(1)人们对酸碱的认识经历了哪些过程?
(2)写出NaHCO3在水溶液中的电离方程式,NaHCO3溶液与盐酸、NaOH溶液反应的离子方程式。依据酸碱质子理论,HCO3-是否可称为酸碱两性物质?
三、人类对酸、碱的认识
(1)阿伦尼乌斯酸碱理论:
酸:电解质电离时产生的阳离子全部是 的化合物是酸,如HCl、H2SO4
碱:电解质电离时产生的阴离子全部是 的化合物是碱。如NaOH
(2)酸碱质子理论:(适用非水溶液和无水条件,范围更大)
酸:凡能 的物质都是酸,如_______、____________等;
碱:凡能______________ 的物质都是碱,如_____、_________等;
酸碱两性物质:若某物质既能 _______ 又能 ,可称为酸碱两性物质。
H+
OH-
给出质子(H+)
给出质子
接受质子
接受质子(H+)
HNO3
CH3COOH
OH-
CH3COO-
(2)写出NaHCO3在水溶液中的电离方程式,NaHCO3溶液与盐酸、NaOH溶液反应的离子方程式。依据酸碱质子理论,HCO3-是否可称为酸碱两性物质?
NaHCO3=== Na+ +HCO3-
H+
OH-
HCO3- + H+===H2O+CO2↑
HCO3- + OH-===H2O+CO32-
给出质子(H+)
接受质子(H+)
HCO3-可称为酸碱两性物质
1.置换反应是金属冶炼的基本原理之一。下列属于通过置换反应得到铁的是( )
A.单质铜与FeCl3 溶液混合 B.CO通过灼热的FeO
C.铜浸入FeCl2 溶液中 D.单质铝与Fe2O3 混合物加热引燃
2.化学真正成为一门科学并较快发展,始于( )
A.舍勒发现氧气 B.质量守恒定律的发现
C.原子?-分子论的问世 D.中国湿法冶金术的推广
3.根据酸碱质子理论,下列说法不正确的是( )
A. 所有的弱酸根都是碱 B. 酸式弱酸根既是酸又是碱
C. 一种物质不可能既是酸又是碱 D. OH- 是碱
4.下列四种物质按酸碱质子理论判断,下列物质属于酸碱两性物质的是( )。
A.HCl B.NaHSO4 C.NaOH D.NaHSO3
随着经济的发展和科学技术的进步,化学与其他学科齐头并进,迅速发展,成为21世纪自然学科的中心学科。
化学科学发展的历史,是一部人类逐步深入认识物质组成、结构、变化的历史,也是一部合成、创造更多新物质,推动社会经济发展和促进人类文明发展的历史。
下图表示金属活动性顺序表中铜、锡、铁和铝被人类大规模开发、利用的大致年限。
K Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Au
(2)根据以上数据和有关化学知识,你能否说明这些金属的活动性与人类开发、利用这些金属的时间先后的关系?
(3)根据已有的化学知识选出2~3种金属单质,说明它们的制备方法,并写出有关化学方程式。
(1)常见金属Cu、Sn、Fe和Al开发利用从早到晚的顺序?
1.金属使用的发展历程
金属铜约在6000年前已大规模利用,铁约在2500年前,而铝的使用仅有200年左右,这与____________及_____________有关。
2.金属的活动性与金属冶炼的关系
②冶炼依据:金属的__________不同,冶炼方法不同;
③冶炼方法:_________、____________、__________及__________。
电解法
热还原法
热分解法
富集法
活动性
金属活动性
冶炼技术
一、人类对金属使用的发展过程
CuSO4+Fe === Cu +FeSO4
生物炼铜
古代化学
冶金、陶瓷、酿造、
火药、造纸、医药
近代化学
原子-分子论
化学真正成为一门科学并较快发展
现代化学
物质结构理论
二、化学重要基本理论的发展与建立
问题2:化学科学重要基本理论归纳
二、化学基本理论的建立与发展
(1)19世纪,
①以 、 和 为中心内容的经典
②1869年 发现了 ;
③提出了 定律,奠定了化学反应的 基础;
④ 的合成彻底动摇了“生命力论”,使有机化学得到迅猛发展。
(2)20世纪
①化学家 提出了 和 的螺旋结构模型,为DNA分子的双螺旋结构模型的提出奠定了基础。
②扫描隧道显微镜的发展,实现了对__________的操纵。
道尔顿原子论
分子结构
原子价键理论
原子分子论
元素周期律
质量作用
动力学
人工尿素
鲍林
氢键理论
蛋白质分子
知识梳理
1
门捷列夫
原子或分子
近代化学阶段
原子学说的创立者
有关原子结构理论的建立
1869 年,俄国科学家门捷列夫将当时已知的 63 种化学元素按原子量大小排列成一个规范的统计表,这个元素周期表揭示了一个非常重要而有趣的规律----元素周期律。门捷列夫根据这个规律纠正了一些错误的原子量,还先后预言了 15 种以上的未知元素。于是,新发现的化学元素就“落户”到了今天元素周期表里来了
元素周期表
近代化学阶段
人工合成出了尿素,彻底动摇了“生命力论”,使有机化学得到了迅速发展。
历史上曾经有人认为,有机化合物只能由生物的细胞在一种特殊力量 生命力的作用下产生,人工合成有机物是不可能的。
1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,由氯化铵和氰酸银反应制得)水溶液得到了尿素[CO(NH2)2]。尿素的人工合成,揭示了人工合成有机物的序幕。
近代化学阶段
建立了物质结构理论-量子化学
使物质世界的秘密进一步揭开,打开了原子的大门,合成物质大量出现。
水晶及其结构
现代化学阶段
鲍林
化学键理论的先驱
现代化学阶段
微观结构观测仪器:
光学显微镜
电子显微镜
扫描隧道显微镜
用硅原子组成的两个汉字“中国”
用STM技术写成的字母“IBM”
问题3:人类对酸碱概念认识的发展
阅读教材P93《人类对酸碱认识的发展》回答下列问题:
(1)人们对酸碱的认识经历了哪些过程?
(2)写出NaHCO3在水溶液中的电离方程式,NaHCO3溶液与盐酸、NaOH溶液反应的离子方程式。依据酸碱质子理论,HCO3-是否可称为酸碱两性物质?
三、人类对酸、碱的认识
(1)阿伦尼乌斯酸碱理论:
酸:电解质电离时产生的阳离子全部是 的化合物是酸,如HCl、H2SO4
碱:电解质电离时产生的阴离子全部是 的化合物是碱。如NaOH
(2)酸碱质子理论:(适用非水溶液和无水条件,范围更大)
酸:凡能 的物质都是酸,如_______、____________等;
碱:凡能______________ 的物质都是碱,如_____、_________等;
酸碱两性物质:若某物质既能 _______ 又能 ,可称为酸碱两性物质。
H+
OH-
给出质子(H+)
给出质子
接受质子
接受质子(H+)
HNO3
CH3COOH
OH-
CH3COO-
(2)写出NaHCO3在水溶液中的电离方程式,NaHCO3溶液与盐酸、NaOH溶液反应的离子方程式。依据酸碱质子理论,HCO3-是否可称为酸碱两性物质?
NaHCO3=== Na+ +HCO3-
H+
OH-
HCO3- + H+===H2O+CO2↑
HCO3- + OH-===H2O+CO32-
给出质子(H+)
接受质子(H+)
HCO3-可称为酸碱两性物质
1.置换反应是金属冶炼的基本原理之一。下列属于通过置换反应得到铁的是( )
A.单质铜与FeCl3 溶液混合 B.CO通过灼热的FeO
C.铜浸入FeCl2 溶液中 D.单质铝与Fe2O3 混合物加热引燃
2.化学真正成为一门科学并较快发展,始于( )
A.舍勒发现氧气 B.质量守恒定律的发现
C.原子?-分子论的问世 D.中国湿法冶金术的推广
3.根据酸碱质子理论,下列说法不正确的是( )
A. 所有的弱酸根都是碱 B. 酸式弱酸根既是酸又是碱
C. 一种物质不可能既是酸又是碱 D. OH- 是碱
4.下列四种物质按酸碱质子理论判断,下列物质属于酸碱两性物质的是( )。
A.HCl B.NaHSO4 C.NaOH D.NaHSO3
