初高中化学衔接点学习江苏省运河中学2019年高一第一学期初高中衔接点教学19ppt
文档属性
| 名称 | 初高中化学衔接点学习江苏省运河中学2019年高一第一学期初高中衔接点教学19ppt |

|
|
| 格式 | zip | ||
| 文件大小 | 342.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-21 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
初高中化学衔接点回顾与强化
龚 源
有位木匠砍了一棵树,把它做了三个木桶。一个装粪,就叫粪桶,众人躲着;一个装水,就叫水桶,众人用着;一个装酒,就叫酒桶,众人品着! 桶是一样的,因装的东西不同命运也就不同。
人生亦如此,有什么样的观念就有什么样的人生, 有什么样的想法就有什么样的生活!
【关于学习方法】
初中学习化学的方法主要是记忆和简单模仿。这种较为机械、死板的方法不适应高中注重能力及创新的要求。改进学习方法,使之适应高中化学的学习,是决定能否学好高中化学的利器。
1.预习法
预习是学习的一种重要方法。通过预习,初步感受新知。从“建构理论”和“最近发展区”理论来看,预习和不预习在接受新知时所得到的学习感受差异很大。
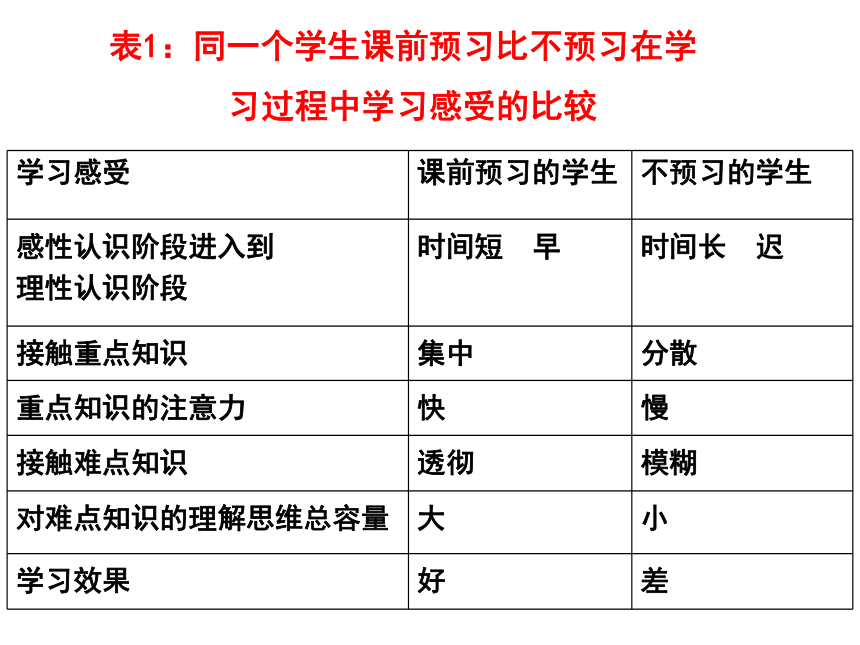
表1:同一个学生课前预习比不预习在学
习过程中学习感受的比较
学习感受 课前预习的学生 不预习的学生
感性认识阶段进入到
理性认识阶段 时间短 早 时间长 迟
接触重点知识 集中 分散
重点知识的注意力 快 慢
接触难点知识 透彻 模糊
对难点知识的理解思维总容量 大 小
学习效果 好 差
2.类比法
在初中化学中,我们接触的知识面是非常有限的。而在高中阶段随着知识面的扩大,将会遇到很多结构相似和性质相似的新物质,因此学习这些新物质的结构与性质时,可以寻找一定的内在变化规律,可以采用“类比法”来学习的。
【例】在初中我们知道:Na2O+CO2=Na2CO3是能够发生的化学反应。若“Na2S”与“Na2O”、“CO2”与“CS2”结构和性质分别相似。
请写出下列反应:Na2S+CS2=————。
Na2CS3
3.归纳法
学习高中化学要善于利用“归纳法”使所学知识规律化和系统化。这样才不会使学生感觉到化学知识紊乱,也会使高中化学知识有序地储存在大脑中。
4.实验法
化学实验探究可以达到将获得的感性知识达到去伪存真、对正确的化学知识加深理解的目的。因此要求我们在高中化学学习阶段要重视实验。要灵活运用实验法学习高中化学知识。一方面可以通过化学实验获得新知;另一方面也可以利用化学实验纠正知识错误;通过化学实验还可以促使动手、动脑的学习习惯的养成。
5.温习法
有人测验了学习后半个月的遗忘情况,结果发现:小学生对于历史知识遗忘52%,中学生对化学遗忘了
58%,大学生对心理学遗忘了75%,数量之大,确实惊人。
古人云:“温故而知新”、“学而时习之”。温习法是学好高中化学的重要法宝。温习既可以克服遗忘,又可以使所学知识清晰化、系统化,对知识的理解进一步加深。下图是德国著名心理学家艾宾浩斯提出的遗忘规律所画的曲线图:
俄罗斯著名教育学家乌申斯基说过:我们应当巩固建筑物,而不应当等着去修补已经崩溃了的建筑物。
要使识记的材料保持住而不发生遗忘或减少遗忘,就必须搞好复习,复习是克服遗忘的重要条件。及时复习,经常复习,同时复习形式也要多样化。
6.典型习题法
“典型习题法”不是“题海战术法”,两者有本质的区别。
“典型习题法”是指对高中化学主干知识进行连贯,对学生基本思维方法进行综合,具有典型代表性的解题方法的化学习题进行训练的方法。
“典型习题法”是具有触类旁通和事半功倍的学习效果的学习方法。
【关于衔接点】
研究初高中化学教材发现:高中化学对初中化学知识进行了合理地延伸与拓展,对初中化学教材许多之处进行很好的链接。由于初高中教学的分离,教学衔接问题是影响中学化学教学效果的因素。
如何理解初高中化学的知识体系的不同及特点;如何剖析初高中化学教材的衔接点、学习方法与思维方法差异等,是顺利实现过渡,有效提高高中化学学业成绩的关键问题。
1.前18号元素的原子序数、元素符号和名称。
2.除了前18号元素外还有哪些常见的元素?
K、Ca、Ti、Cr、Mn、Fe、Co、Ni、Cu、Zn、Ag、Ba、As、Se、Br、I
3.金属活动顺序表
1812年瑞典化学家贝采利乌斯根据实验现象首先提出金属活动顺序。后来俄国化学家贝开托夫又在大量实验和系统研究之后,于1865年发表了金属置换顺序—金属活动顺序表:
K?、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb 、(H) 、
Cu、?Hg?、Ag、Pt、Au
?
4.常见元素及原子团的化合价
5.常见物质(离子)的化学式
物质 化学式 物质 化学式
亚硫酸 溴化亚铁
氧化钡 氢氧化镁
碘化钾 高锰酸钾
硫酸铵 磷酸二氢铵
硫酸铁 碳酸氢钙
硝酸镁 硫化亚铜
写出下列物质的化学式
6.常见元素的相对原子质量
H-1 He-4 C-12 N-14 O-16 Na-23 Mg-24 Al-27
Si-28 P-31 S-32 Cl-35.5 K-39 Ca-40 Fe-56
Cu-64 Zn-65 Ag-108 I-127 Ba-137
7.常见物质的相对分子质量
H2-2 He-4 N2-28 O2-32 Cl2-71 NH3-17 H2O-18
CO2-44 SO2-64 HCl-36.5 HNO3-63 H2SO4-98
NaCl-58.5 NaOH-40 Na2CO3-106 AgCl-143.5 CaCO3-100 BaSO4-233 CuSO4·5H2O-250
酸碱盐溶解性口诀
钾钠铵盐硝酸盐,完全溶解不困难;
盐酸盐中氯化银,水中溶解不得行;
硫酸钡铅不溶外,微溶只有银和钙;
碳酸盐溶钾钠铵,余下沉淀记心间。
8.常见难溶物和微溶物
阴离子
阳离子 OH- NO3- Cl- SO42- S2- SO32- CO32-
H+ 溶 溶 溶 溶 溶 溶
NH4+ 溶 溶 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 — 不 不
Ca2+ 微 溶 溶 微 — 不 不
Mg2+ 不 溶 溶 溶 — 微 微
Al3+ 不 溶 溶 溶 — — —
Zn2+ 不 溶 溶 溶 不 不 不
Fe2+ 不 溶 溶 溶 不 不 不
Fe3+ 不 溶 溶 溶 — — —
Pb2+ 不 溶 微 不 不 不 不
Cu2+ 不 溶 溶 溶 不 不 不
Ag+ — 溶 不 微 不 不 不
初高中化学衔接点回顾与强化
龚 源
有位木匠砍了一棵树,把它做了三个木桶。一个装粪,就叫粪桶,众人躲着;一个装水,就叫水桶,众人用着;一个装酒,就叫酒桶,众人品着! 桶是一样的,因装的东西不同命运也就不同。
人生亦如此,有什么样的观念就有什么样的人生, 有什么样的想法就有什么样的生活!
【关于学习方法】
初中学习化学的方法主要是记忆和简单模仿。这种较为机械、死板的方法不适应高中注重能力及创新的要求。改进学习方法,使之适应高中化学的学习,是决定能否学好高中化学的利器。
1.预习法
预习是学习的一种重要方法。通过预习,初步感受新知。从“建构理论”和“最近发展区”理论来看,预习和不预习在接受新知时所得到的学习感受差异很大。
表1:同一个学生课前预习比不预习在学
习过程中学习感受的比较
学习感受 课前预习的学生 不预习的学生
感性认识阶段进入到
理性认识阶段 时间短 早 时间长 迟
接触重点知识 集中 分散
重点知识的注意力 快 慢
接触难点知识 透彻 模糊
对难点知识的理解思维总容量 大 小
学习效果 好 差
2.类比法
在初中化学中,我们接触的知识面是非常有限的。而在高中阶段随着知识面的扩大,将会遇到很多结构相似和性质相似的新物质,因此学习这些新物质的结构与性质时,可以寻找一定的内在变化规律,可以采用“类比法”来学习的。
【例】在初中我们知道:Na2O+CO2=Na2CO3是能够发生的化学反应。若“Na2S”与“Na2O”、“CO2”与“CS2”结构和性质分别相似。
请写出下列反应:Na2S+CS2=————。
Na2CS3
3.归纳法
学习高中化学要善于利用“归纳法”使所学知识规律化和系统化。这样才不会使学生感觉到化学知识紊乱,也会使高中化学知识有序地储存在大脑中。
4.实验法
化学实验探究可以达到将获得的感性知识达到去伪存真、对正确的化学知识加深理解的目的。因此要求我们在高中化学学习阶段要重视实验。要灵活运用实验法学习高中化学知识。一方面可以通过化学实验获得新知;另一方面也可以利用化学实验纠正知识错误;通过化学实验还可以促使动手、动脑的学习习惯的养成。
5.温习法
有人测验了学习后半个月的遗忘情况,结果发现:小学生对于历史知识遗忘52%,中学生对化学遗忘了
58%,大学生对心理学遗忘了75%,数量之大,确实惊人。
古人云:“温故而知新”、“学而时习之”。温习法是学好高中化学的重要法宝。温习既可以克服遗忘,又可以使所学知识清晰化、系统化,对知识的理解进一步加深。下图是德国著名心理学家艾宾浩斯提出的遗忘规律所画的曲线图:
俄罗斯著名教育学家乌申斯基说过:我们应当巩固建筑物,而不应当等着去修补已经崩溃了的建筑物。
要使识记的材料保持住而不发生遗忘或减少遗忘,就必须搞好复习,复习是克服遗忘的重要条件。及时复习,经常复习,同时复习形式也要多样化。
6.典型习题法
“典型习题法”不是“题海战术法”,两者有本质的区别。
“典型习题法”是指对高中化学主干知识进行连贯,对学生基本思维方法进行综合,具有典型代表性的解题方法的化学习题进行训练的方法。
“典型习题法”是具有触类旁通和事半功倍的学习效果的学习方法。
【关于衔接点】
研究初高中化学教材发现:高中化学对初中化学知识进行了合理地延伸与拓展,对初中化学教材许多之处进行很好的链接。由于初高中教学的分离,教学衔接问题是影响中学化学教学效果的因素。
如何理解初高中化学的知识体系的不同及特点;如何剖析初高中化学教材的衔接点、学习方法与思维方法差异等,是顺利实现过渡,有效提高高中化学学业成绩的关键问题。
1.前18号元素的原子序数、元素符号和名称。
2.除了前18号元素外还有哪些常见的元素?
K、Ca、Ti、Cr、Mn、Fe、Co、Ni、Cu、Zn、Ag、Ba、As、Se、Br、I
3.金属活动顺序表
1812年瑞典化学家贝采利乌斯根据实验现象首先提出金属活动顺序。后来俄国化学家贝开托夫又在大量实验和系统研究之后,于1865年发表了金属置换顺序—金属活动顺序表:
K?、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb 、(H) 、
Cu、?Hg?、Ag、Pt、Au
?
4.常见元素及原子团的化合价
5.常见物质(离子)的化学式
物质 化学式 物质 化学式
亚硫酸 溴化亚铁
氧化钡 氢氧化镁
碘化钾 高锰酸钾
硫酸铵 磷酸二氢铵
硫酸铁 碳酸氢钙
硝酸镁 硫化亚铜
写出下列物质的化学式
6.常见元素的相对原子质量
H-1 He-4 C-12 N-14 O-16 Na-23 Mg-24 Al-27
Si-28 P-31 S-32 Cl-35.5 K-39 Ca-40 Fe-56
Cu-64 Zn-65 Ag-108 I-127 Ba-137
7.常见物质的相对分子质量
H2-2 He-4 N2-28 O2-32 Cl2-71 NH3-17 H2O-18
CO2-44 SO2-64 HCl-36.5 HNO3-63 H2SO4-98
NaCl-58.5 NaOH-40 Na2CO3-106 AgCl-143.5 CaCO3-100 BaSO4-233 CuSO4·5H2O-250
酸碱盐溶解性口诀
钾钠铵盐硝酸盐,完全溶解不困难;
盐酸盐中氯化银,水中溶解不得行;
硫酸钡铅不溶外,微溶只有银和钙;
碳酸盐溶钾钠铵,余下沉淀记心间。
8.常见难溶物和微溶物
阴离子
阳离子 OH- NO3- Cl- SO42- S2- SO32- CO32-
H+ 溶 溶 溶 溶 溶 溶
NH4+ 溶 溶 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 — 不 不
Ca2+ 微 溶 溶 微 — 不 不
Mg2+ 不 溶 溶 溶 — 微 微
Al3+ 不 溶 溶 溶 — — —
Zn2+ 不 溶 溶 溶 不 不 不
Fe2+ 不 溶 溶 溶 不 不 不
Fe3+ 不 溶 溶 溶 — — —
Pb2+ 不 溶 微 不 不 不 不
Cu2+ 不 溶 溶 溶 不 不 不
Ag+ — 溶 不 微 不 不 不
