人教版化学九年级下学期《11.2 化学肥料》 同步练习 含答案
文档属性
| 名称 | 人教版化学九年级下学期《11.2 化学肥料》 同步练习 含答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 68.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-21 00:00:00 | ||
图片预览



文档简介
11.2 化学肥料
一.选择题(共11小题)
1.下列化肥属于复合肥的是( )
A.CO(NH2)2 B.(NH4)2SO4 C.KNO3 D.Ca3(PO4)2
2.重过磷酸钙[Ca(H2PO4)2]是一种常用的化学肥料,它属于( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥
3.如图“滤液”中分离出的氯化铵,在农业上可用作( )
A.钾肥 B.氮肥 C.磷肥 D.复合肥
4.农业生产离不开化肥,下列关于化肥的说法中不正确的是( )
A.铵态氮肥不能与草木灰(含K2CO3)不能混合使用
B.化肥对提高农作物产量具有重要作用,应尽量多施用
C.复合肥料能同时供给作物几种养分,肥效高
D.长期使用硫酸铵、硫酸钾会使土壤酸化、板结
5.下列化肥看外观能与其他化肥区分开的是( )
A.氯化铵 B.硫酸钾 C.磷矿粉 D.尿素
6.某无土栽培所需的营养液成分是含有N、P、K等元素的无机盐,下列可作营养液成分的是( )
A.P2O5 B.KOH C.NH4Cl D.HNO3
7.下列说法中,正确的是( )
A.含有氮元素的物质一定能做氮肥
B.工业炼铁的原理是利用还原剂(CO)将铁从其化合物中置换出来
C.能与酸反应产生气体的物质一定含CO32﹣
D.pH等于6的溶液可能是盐溶液
8.下列关于化肥的说法正确的是( )
A.尿素与熟石灰混合研磨后能嗅到刺激性气味
B.氯化钾(KCl)和磷酸氢二铵[(NH4)2HPO4]都属于复合肥料
C.化肥对提高农作物的产量具有重要作用
D.化肥的过度使用会造成土壤酸化,可用碱性的碳酸钠改良
9.如图是某同学鉴别NH4HCO3、NH4C1、KCl三种化肥的过程,其中试剂甲和乙分别可能是( )
A.甲:熟石灰; 乙:稀盐酸
B.甲:水; 乙:氢氧化钠溶液
C.甲:氢氧化钠溶液; 乙:水
D.甲:稀盐酸; 乙:氯化钠溶液
10.化学学习让我们有很多收获,下列归纳总结正确的是( )
A 鉴别方法 B实验现象
①NH4NO3和(NH4)2SO4固体:加熟石灰混合研磨后闻气味②检验铜、铁、银的活动性:三种金属分别放入FeCl2溶液 ①肥皂水滴入硬水中,产生的泡沫较少,浮渣较多②生锈的铁钉浸泡在足量的稀盐酸中。铁锈会消失,一段时间后有气泡产生
C 反应原理不同 D 化学式排序
①盛有石灰水的试剂瓶内壁出现白膜②用炭火烘干石灰浆抹过的墙壁,墙壁反而更潮湿 ①溶液pH由大到小:HCl、NaCl、Na2CO3②硫元素质量分数由高到低:Na2S、Na2SO3、Na2SO4
A.A B.B C.C D.D
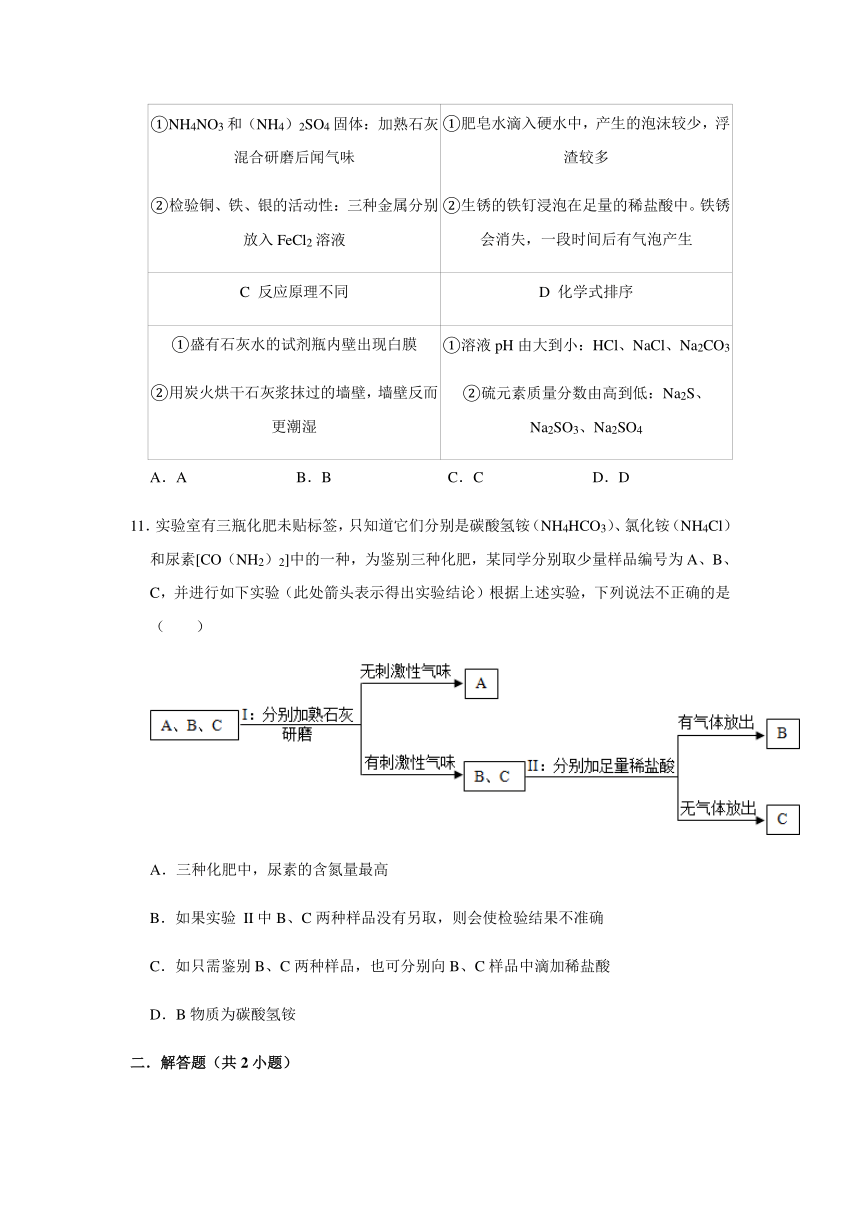
11.实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种,为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论)根据上述实验,下列说法不正确的是( )
A.三种化肥中,尿素的含氮量最高
B.如果实验 II中B、C两种样品没有另取,则会使检验结果不准确
C.如只需鉴别B、C两种样品,也可分别向B、C样品中滴加稀盐酸
D.B物质为碳酸氢铵
二.解答题(共2小题)
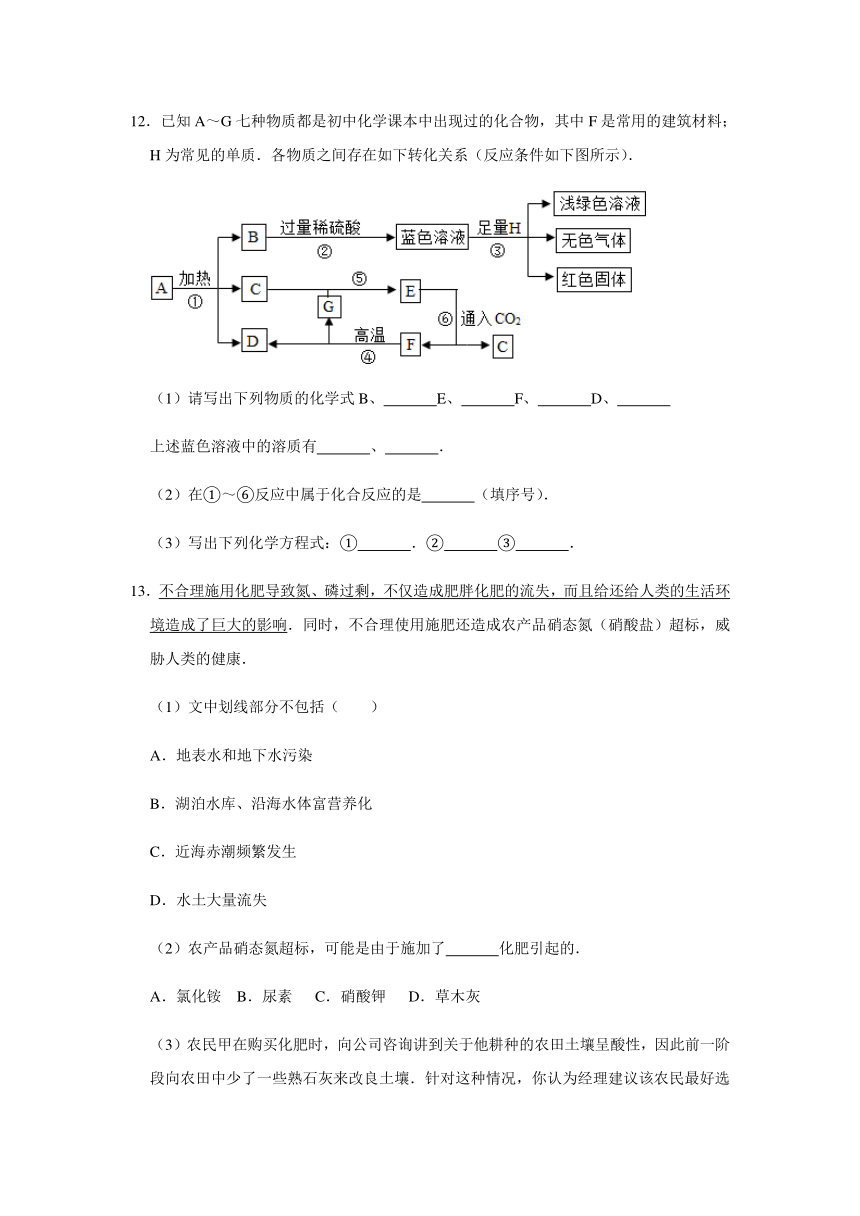
12.已知A~G七种物质都是初中化学课本中出现过的化合物,其中F是常用的建筑材料;H为常见的单质.各物质之间存在如下转化关系(反应条件如下图所示).
(1)请写出下列物质的化学式B、 E、 F、 D、
上述蓝色溶液中的溶质有 、 .
(2)在①~⑥反应中属于化合反应的是 (填序号).
(3)写出下列化学方程式:① .② ③ .
13.不合理施用化肥导致氮、磷过剩,不仅造成肥胖化肥的流失,而且给还给人类的生活环境造成了巨大的影响.同时,不合理使用施肥还造成农产品硝态氮(硝酸盐)超标,威胁人类的健康.
(1)文中划线部分不包括( )
A.地表水和地下水污染
B.湖泊水库、沿海水体富营养化
C.近海赤潮频繁发生
D.水土大量流失
(2)农产品硝态氮超标,可能是由于施加了 化肥引起的.
A.氯化铵 B.尿素 C.硝酸钾 D.草木灰
(3)农民甲在购买化肥时,向公司咨询讲到关于他耕种的农田土壤呈酸性,因此前一阶段向农田中少了一些熟石灰来改良土壤.针对这种情况,你认为经理建议该农民最好选购(2)中谈及的哪一种化肥? (填化学式)
(4)目前,“用肥越多,收成越好”的想法在农民中广泛存在,针对农民的这种想法,你的建议是 .
三.填空题(共3小题)
14.请你参加某中学初三学生识别化肥的探究活动.他们从家中拿来了四种化肥,分别是硫酸钾、氯化钾、碳酸铵和硝酸铵.
第一步:称取化肥各10g,进行研细.
第二步:取上述化肥各少量于研钵中,分别加入少量熟石灰粉末,混合研磨,能嗅到剌激性气味的是两种铵盐.请将下列硝酸铵与熟石灰反应的化学方程式填写完整:
2NH4NO3+ ═ +2NH3↑+2H2O.
第三步:另取两种铵盐各少量于试管中,都滴入少量稀盐酸,无明显现象的是氯化铵和硝酸铵,有气泡产生的是碳酸铵,写出反应的化学方程式: .
第四步:另取两种钾盐,分别在试管中配成溶液,各滴入几滴氯化钡溶液,根据盐的溶解情况判断:有白色沉淀产生的是 ,无明显现象的是 .写出生成白色沉淀时发生反应的化学方程式: .
15.某钾肥溶液可能是氯化钾、碳酸钾、硫酸钾、硝酸钾中一种或几种,现要检验成分,进行如下鉴别实验:
①写出无色气体与石灰水反应的化学方程式: ;
②通过以上实验可知,此钾肥溶液中一定含有 ,可能含有 ;
③鉴别该钾肥溶液中含有钾元素的方法是: .
16.根据下表中左栏所列的化肥的性质,从下列使用注意事项中选择合适的项(可选多项),将其序号填入表中的右栏中.
(1)储存和运输时要密封,不要受潮或暴晒;施用后要盖土或立即灌溉.
(2)不要与碱性物质混放或混用.
(3)不能与易燃物质混在一起:结块时不要用铁锤砸碎.
(4)不宜长期施用.
化肥种类 性质 使用注意事项
碳酸氢铵 易溶于水,受潮时在常温下即能分解,温度越高分解越快,遇碱时放出氨气.在土壤中不残留有害物质.
碳酸铵 易溶于水,受热易分解,遇碱时放出氨气,在高温或受猛烈撞击时易爆炸.
硫酸铵 易溶于水,吸湿性小,常温下稳定,遇碱时放出氨气,长期施用,会使土壤酸化、板结.
硫酸钾 易溶于水,长期施用,会使土壤酸化、板结.
请你从上表提供的信息中分析,使用化肥对环境的影响之一是 ;
相应的解决问题的方法是 .
参考答案
一.选择题(共11小题)
1.
C。
2.
B。
3.
B。
4.
B。
5.
C。
6.
C。
7.
D。
8.
C。
9.
A。
10.
B。
11.
B。
二.解答题(共2小题)
12.解:题中反应②加入过量稀硫酸后得到蓝色溶液,根据硫酸和蓝色以及过量的特征,可发现蓝色溶液中含有2种溶质:硫酸铜和硫酸,推出B为氧化铜;然后根据③反应后物质“浅绿色”、“无色气体”、“红色固体”的性质特点推出H为铁;
最后突破口在⑥信息是通入二氧化碳,所以C、F中有一为碳酸盐,根据④中的高温推出F为碳酸钙、E为氢氧化钙、C为水,根据信息逆推得出G为氧化钙、D为二氧化碳.这一过程中充分的应用氧化钙、氢氧化钙、碳酸钙的一系列性质而进行推断.所以此题A中含有的元素符号为Cu、H、O、C,为碱式碳酸铜,即铜绿.
综上所述:
A 为Cu2(OH)2CO3; B 为CuO; C 为H2O; D 为CO2;E 为Ca(OH)2;F 为CaCO3;G 为CaO; H 为Fe;
(1)故答案为:B:CuO; E:Ca(OH)2;F:CaCO3; E:CO2; CuSO4;H2SO4;
(2)在①~⑥反应中属于化合反应的是:⑤;
(3)①Cu2(OH)2CO32CuO+H2O+CO2↑
②H2SO4+CuO═CuSO4+H2O
③Fe+CuSO4=Cu+FeSO4 Fe+H2SO4=FeSO4+H2↑
13.解:(1)A、过多的化肥会造成地表水和地下水污染;
B、过多的化肥会会使湖泊水库、沿海水体富营养化;
C、化肥中的营养元素,会使近海赤潮频繁发生;
D、过多的施用化肥与水土流失无关.
故选D.
(2)含有“硝态氮”的物质有“硝酸钾、硝酸铵、硝酸钠钙、硝酸钙”等等硝酸类化工原料内.所以农产品硝态氮超标,可能是由于施加了硝酸钾化肥引起的.
故选C.
(3)土壤呈酸性,而且向农田中少了一些熟石灰来改良土壤,所以要用呈碱性的草木灰;
故答案为:K2CO3;
(4)根据农作物的需要,测土配方,合理施肥.
故答案为:根据农作物的需要,测土配方,合理施肥.
三.填空题(共3小题)
14.解:第二步:NH4+的检验:取样品加入碱溶液,有刺激性气味的气体放出,用湿润的红色石蕊试纸检验产生的气体,试纸变蓝色.
因此,硝酸铵能与熟石灰反应:2NH4NO3+Ca(OH)2═Ca(NO3)2+2NH3↑+2H2O.
第三步:CO32﹣的检验:常用盐酸和澄清石灰水检验.去样品加入盐酸,生成的气体通入澄清石灰水中,放出的气体能使澄清石灰水变浑浊.碳酸铵能与盐酸发生反应:(NH4)2CO3+2HCl═2NH4Cl+H2O+CO2↑
第四步:往硫酸钾和氯化钾中加入氯化钡溶液,有白色沉淀产生的原溶液是硫酸钾溶液,生成了BaSO4白色沉淀.K2SO4+BaCl2═BaSO4↓+2KCl
故答案是:
第二步:Ca(OH)2、Ca(NO3)2
第三步:(NH4)2CO3+2HCl═2NH4Cl+H2O+CO2↑
第四步:硫酸钾(K2SO4)、氯化钾(KCl)、K2SO4+BaCl2═BaSO4↓+2KCl
15.解:①加入盐酸生成无色气体则该气体是二氧化碳,原混合物中一定会有碳酸钾.
故答案为:CO2+Ca(OH)2═CaCO3↓+H2O
②因为碳酸钾在第一步中已完全反应,则加入氯化钡有白色沉淀则是说明存在硫酸根,化肥中一定含有硫酸钾,则此化肥一定含有K2CO3、K2SO4,可能含有KNO3、KCl.
故答案为:K2CO3、K2SO4;KNO3、KCl
③钾元素的鉴定只能采用焰色反应进行检验,进行焰色反应的实验完成.
故答案为:用焰色反应,若火焰透过蓝色钴玻璃呈紫色,则说明含有钾元素
16.解:碳酸氢铵易溶于水,受潮时在常温下即能分解,温度越高分解越快,所以储存和运输时要密封,不要受潮或暴晒;施用后要盖土或立即灌溉;遇碱时放出氨气,所以不要与碱性物质混放或混用;
碳酸铵易溶于水,受热易分解,高温或受猛烈撞击时易爆炸,所以储存和运输时要密封,不要受潮或暴晒,遇碱时放出氨气,所以不要与碱性物质混放或混用;在高温或受猛烈撞击时易爆炸,所以不能与易燃物质混在一起:结块时不要用铁锤砸碎;
硫酸铵遇碱时放出氨气,所以不要与碱性物质混放或混用;长期施用,会使土壤酸化、板结,所以不宜长期施用;
硫酸钾长期施用,会使土壤酸化、板结,所以不宜长期施用;
使用化肥对环境的影响之一是使土壤酸化、板结,所以可以通过酸碱中和反应原理,利用氢氧化钙来中和土壤中的酸.
故答案为:(1)(2);(1)(2)(3); (2)(4); (4);使土壤酸化、板结; 用熟石灰中和.
同课章节目录
