【化学】3.3-硫的转化课件(鲁科版必修1)第二课时(共17张PPT)
文档属性
| 名称 | 【化学】3.3-硫的转化课件(鲁科版必修1)第二课时(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 720.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-23 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
第3节 硫的转化
第3章 自然界中的元素
第二课时
二、实验室里研究不同价态硫元素间的转化
含有硫元素的物质在自然界中依靠大自然的作用进行相互转化。那么,在实验室中怎样实现这些物质间的转化呢?
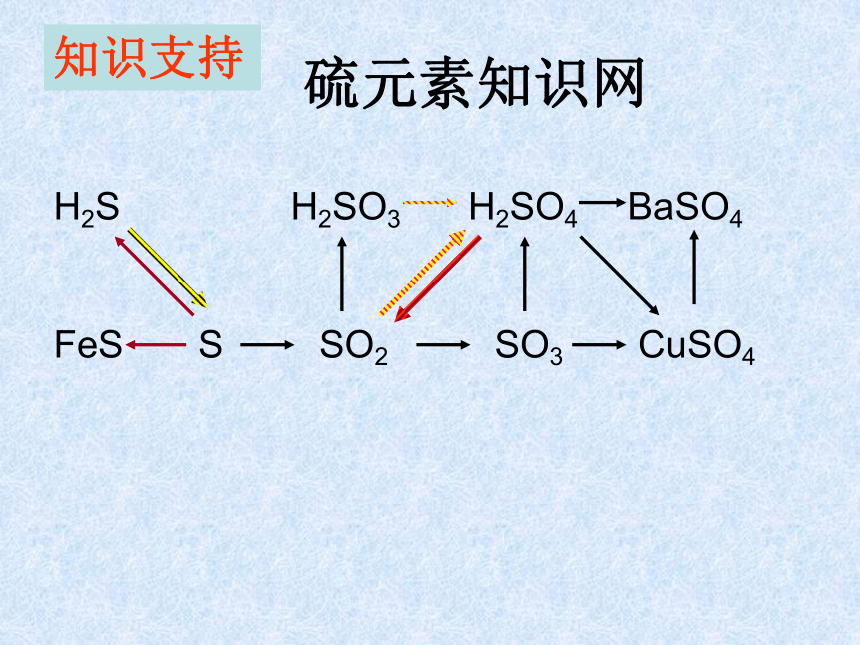
H2S H2SO3 H2SO4 BaSO4
FeS S SO2 SO3 CuSO4
硫元素知识网
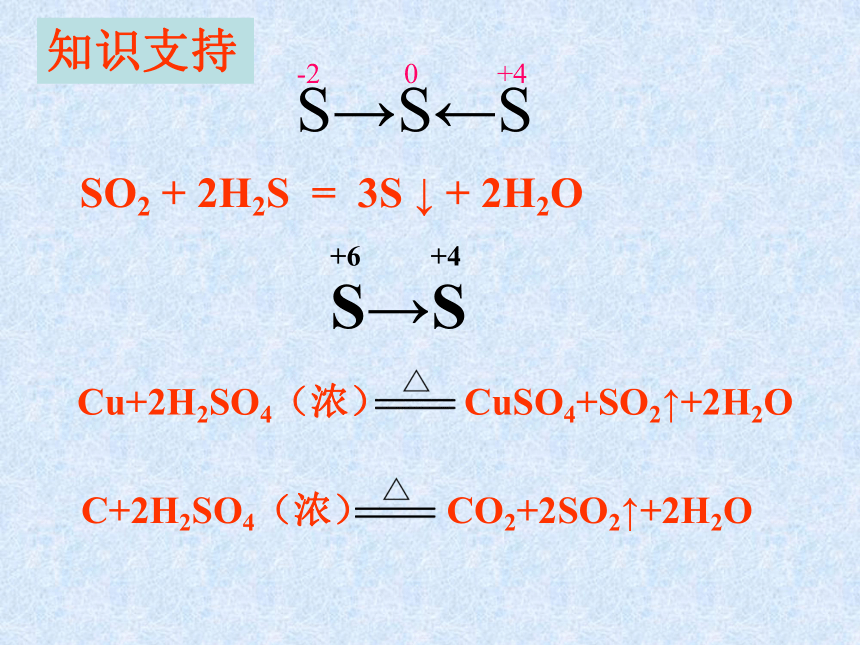
知识支持
SO2 + 2H2S = 3S ↓ + 2H2O
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
C+2H2SO4(浓) CO2+2SO2↑+2H2O
知识支持
知识支持
活动探究
(1)实验内容:探究不同价态(0,+4,+6)硫元素之间的转化。
(2)实验目的:探究不同价态(0,+4,+6)硫元素之间的转化;归纳总结SO2、浓硫酸的化学性质。
(3)实验用品:试管,试管夹,玻璃棒,胶头滴管,单孔橡皮塞,酒精灯,铁架台(带铁圈),药匙,烧杯,圆底烧瓶,止水夹,橡皮管,硫粉,亚硫酸钠,氢氧化钠稀溶液,品红溶液,酸性KMnO4溶液,氯水,浓硝酸,稀硝酸,碘化钾溶液,碘水,酚酞,氢硫酸,浓硫酸,BaCl2溶液,锌粒,铜片,火柴。
实验设计要求
(1)设计的方案尽量减少环境污染(SO2,H2S均有毒),认真对待尾气的处理。
(2)实验方案要能判断是否实现了转化。
(3)画出实验装置图。
问题讨论
(1)根据实验结果,用图示的方法,表示不同价态硫元素之间的相互转化关系。能写出方程式的请完成化学反应方程式。
(2)通过实验,总结二氧化硫,浓硫酸的化学性质。
(3)在实验过程中,你遇到了哪些问题?是如何解决的?
概括·整合
0 氧化剂 +4 氧化剂 +6
S 还原剂 S 还原剂 S
1、相互转化关系
2、二氧化硫的性质
②与水反应
SO2+H2O H2SO3
(1)物理性质:
无色,有刺激性气味的有毒气体,易溶于水。
(2)化学性质
①酸性氧化物的通性:
SO2+2NaOH=Na2SO3+H2O
③氧化性 SO2+H2S=3S↓+2H2O
⑤能使品红溶液褪色
(该性质用来检验SO2)
(2)化学性质
3.浓硫酸的特性
(1)吸水性——干燥剂。
(2)脱水性
(3)强氧化性
巩固练习
1、下列气体都能用浓硫酸干燥的是
A、SO2、H2S、O2
B、CO、O2、Cl2
C、HBr、H2、Cl2
D、HCl、CO2、NH3
答案: B 。
2、在一定条件下,SO2跟下列物质起反应时,仅显酸性的是
A.O2 B.H2S
C.溴水 D.Na2CO3
答案: D 。
巩固练习
链接高考
1、下列叙述正确的是( )
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均
能生成碱
C.Li、C、P分别在足量氧气中燃烧均生成一种
相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后
均能生成气体
答案:D。
链接高考
2、铜在自然界存在于多种矿石中,如:
请回答下列问题:
(1)上表所列铜化合物中,铜的质量百分含量最高
的是 。
(2)工业上以黄铜矿为原料。采用火法溶炼工艺生产铜。
该工艺的中间过程会发生反应:
(3)SO2尾气直接排放到大气中造成环境污染的后果
是 ;处理该尾气可得到有价值的化学品,
写出其中1种酸和1种盐的名称 。
Cu2S
Cu2O,Cu2S
形成酸雨
硫酸、硫酸铵
矿石名称 黄铜矿 斑铜矿 辉铜矿 孔雀石
主要成分 CuFeS2 Cu5FeS4 Cu2S CuCO3·Cu(OH)2
第3节 硫的转化
第3章 自然界中的元素
第二课时
二、实验室里研究不同价态硫元素间的转化
含有硫元素的物质在自然界中依靠大自然的作用进行相互转化。那么,在实验室中怎样实现这些物质间的转化呢?
H2S H2SO3 H2SO4 BaSO4
FeS S SO2 SO3 CuSO4
硫元素知识网
知识支持
SO2 + 2H2S = 3S ↓ + 2H2O
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
C+2H2SO4(浓) CO2+2SO2↑+2H2O
知识支持
知识支持
活动探究
(1)实验内容:探究不同价态(0,+4,+6)硫元素之间的转化。
(2)实验目的:探究不同价态(0,+4,+6)硫元素之间的转化;归纳总结SO2、浓硫酸的化学性质。
(3)实验用品:试管,试管夹,玻璃棒,胶头滴管,单孔橡皮塞,酒精灯,铁架台(带铁圈),药匙,烧杯,圆底烧瓶,止水夹,橡皮管,硫粉,亚硫酸钠,氢氧化钠稀溶液,品红溶液,酸性KMnO4溶液,氯水,浓硝酸,稀硝酸,碘化钾溶液,碘水,酚酞,氢硫酸,浓硫酸,BaCl2溶液,锌粒,铜片,火柴。
实验设计要求
(1)设计的方案尽量减少环境污染(SO2,H2S均有毒),认真对待尾气的处理。
(2)实验方案要能判断是否实现了转化。
(3)画出实验装置图。
问题讨论
(1)根据实验结果,用图示的方法,表示不同价态硫元素之间的相互转化关系。能写出方程式的请完成化学反应方程式。
(2)通过实验,总结二氧化硫,浓硫酸的化学性质。
(3)在实验过程中,你遇到了哪些问题?是如何解决的?
概括·整合
0 氧化剂 +4 氧化剂 +6
S 还原剂 S 还原剂 S
1、相互转化关系
2、二氧化硫的性质
②与水反应
SO2+H2O H2SO3
(1)物理性质:
无色,有刺激性气味的有毒气体,易溶于水。
(2)化学性质
①酸性氧化物的通性:
SO2+2NaOH=Na2SO3+H2O
③氧化性 SO2+H2S=3S↓+2H2O
⑤能使品红溶液褪色
(该性质用来检验SO2)
(2)化学性质
3.浓硫酸的特性
(1)吸水性——干燥剂。
(2)脱水性
(3)强氧化性
巩固练习
1、下列气体都能用浓硫酸干燥的是
A、SO2、H2S、O2
B、CO、O2、Cl2
C、HBr、H2、Cl2
D、HCl、CO2、NH3
答案: B 。
2、在一定条件下,SO2跟下列物质起反应时,仅显酸性的是
A.O2 B.H2S
C.溴水 D.Na2CO3
答案: D 。
巩固练习
链接高考
1、下列叙述正确的是( )
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均
能生成碱
C.Li、C、P分别在足量氧气中燃烧均生成一种
相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后
均能生成气体
答案:D。
链接高考
2、铜在自然界存在于多种矿石中,如:
请回答下列问题:
(1)上表所列铜化合物中,铜的质量百分含量最高
的是 。
(2)工业上以黄铜矿为原料。采用火法溶炼工艺生产铜。
该工艺的中间过程会发生反应:
(3)SO2尾气直接排放到大气中造成环境污染的后果
是 ;处理该尾气可得到有价值的化学品,
写出其中1种酸和1种盐的名称 。
Cu2S
Cu2O,Cu2S
形成酸雨
硫酸、硫酸铵
矿石名称 黄铜矿 斑铜矿 辉铜矿 孔雀石
主要成分 CuFeS2 Cu5FeS4 Cu2S CuCO3·Cu(OH)2
