人教版高二物理选修3-3第9章第1节固体(共21张PPT)
文档属性
| 名称 | 人教版高二物理选修3-3第9章第1节固体(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-04-28 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
第一节《固体》
(1)
1、生活中常见的固体:
(2)
玻璃
蜂蜡
塑料
石英
白糖
食盐
食盐
硫酸铜
明矾
雪花
白糖
石英
云母
钻石
玻璃
橡胶
蜂蜡
石蜡
塑料
沥青
松香
1.晶体:具有规则的几何形状。
常见的晶体有:石英、云母、明矾、食盐、硫酸铜、糖、味精等。
2.非晶体:没有规则的几何形状。
常见的非晶体有:玻璃、蜂蜡、塑料、沥青、橡胶、松香等。
(一)、固体分为两类:
(二)、晶体和非晶体的区别:
1、熔点:晶体具有一定的熔点,非晶体没有一定的熔点。
(二)、晶体和非晶体的区别:
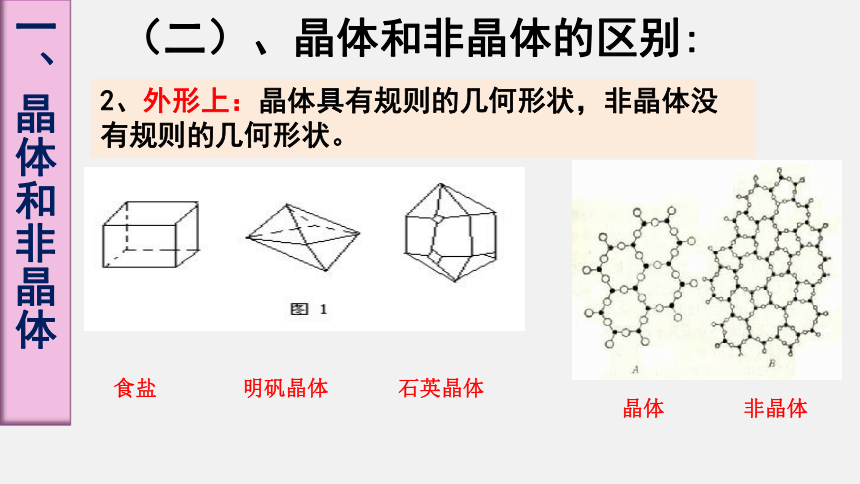
2、外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状。
食盐
石英晶体
明矾晶体
晶体
非晶体
(二)、晶体和非晶体的区别:
3、物理性质上:
晶体的物理性质与方向有关(这种特性叫各向异性)
非晶体的物理性质在各个方向是相同的(这种特性叫各向同性)
云母:导热性上表现出显著的各向异性
方铝矿:导电性上表现出显著的各向异性
方解石:光的折射上表现出显著的各向异性,
(二)、晶体和非晶体的区别:
3、物理性质上:
晶体的物理性质与方向有关(这种特性叫各向异性)
非晶体的物理性质在各个方向是相同的(这种特性叫各向同性)
1、熔点:晶体具有一定的熔点,非晶体没有一定的熔点。
2、外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状。
天然水晶和石英玻璃的成分都是sio2 思考你能想到什么?
(1)一种物质可能以晶体和非晶体两种不同的形态出现,一种物质是晶体还是非晶体并不是绝对的.
(2)许多非晶体在一定的条件下可以转化为晶体.
(3)在冷却得足够快和冷却到足够低的温度时,几乎所有的材料都能成为非晶体.
1.单晶体:一个物体就是一个完整的晶体.
例如:雪花、食盐小颗粒、单晶硅、单晶锗等.
2.多晶体:整个物体是由许多杂乱无章地排列着的小晶体组成。其中的小晶体叫做晶粒.
(1)多晶体没有规则的几何形状.
(2)不显示各向异性.(每一晶粒内部都是各向异性的).
(3) 有确定的熔点.
(一)单晶体和多晶体的区别:
(二)如何区分多晶体和非晶体?
晶体微观结构:
组成晶体的物质微粒(分子或原子、离子)依照一定的规律在空间中整齐地排列,具有空间上的周期性.
食盐的晶体结构
(一)晶体外形的规则性可以用物质微粒的规则
排列来解释
(二)晶体的各向异性也是由晶体的内部结构
决定的.
各向异性的微观解释
(三)晶体具有固定熔点.
晶体溶化时,吸收的 热量全部用来破坏规则的排列,温度不发生变化.
非晶体熔化时,先变软,然后变成粘滞性很大的液体,温度不断升高.
(三)有的物质在不同条件下能够生成不同的晶体。
因为组成它们的微粒能够按照不同规则在空
间分布.
石墨质地松软,粉状润滑剂,制作铅笔心.
金刚石有很大的硬度,可以用来切割玻璃
同一种化学成分的物质,为什么有不同的物理性质?
1.固体可分为晶体和非晶体两大类 .
2 .晶体和非晶体的差别.
熔点:晶体具有固定的熔点,非晶体没有
外形:晶体具有规则的几何形状,非晶体则没有规则的几何形状
物理性质:晶体各向异性,非晶体各向同性
3.多晶体和非晶体的差别
多晶体和非晶体都没有规则的几何形状
多晶体有一定的熔点,非晶体没有一定的熔点
多晶体和非晶体的一些物理性质都表现为各向同性
4.固体材料在生活,生产,科学,研究等方面的应用
1、
1. 关于晶体和非晶体,下列说法中正确的是( )
A.单晶体具有各向异性
B.多晶体也具有各向异性
C.非晶体的各种物理性质,在各个方向上都是相同的
D.晶体的各种物理性质,在各个方向上都是不同的
2、下列固体中全是由晶体组成的是( ).
(A)石英、云母、明矾、食盐、雪花、铜
(B)石英、玻璃、云母、铜
(C)食盐、雪花、云母、硫酸铜、松香
(D)蜂蜡、松香、橡胶、沥青
3.某物体表现出各向异性是由于组成物体的物质微粒( ).
(A)在空间的排列不规则
(B)在空间按一定的规则排列
(C)数目较多的缘故
(D)数目较少的缘故
4.晶体在熔解过程中吸收的热量,主要用于( )
(A)破坏空间点阵结构,增加分子动能
(B)破坏空间点阵结构,增加分子势能
(C)破坏空间点阵结构,增加分子的势能和动能
(D)破坏空间点阵结构,但不增加分子的势能和动能
第一节《固体》
(1)
1、生活中常见的固体:
(2)
玻璃
蜂蜡
塑料
石英
白糖
食盐
食盐
硫酸铜
明矾
雪花
白糖
石英
云母
钻石
玻璃
橡胶
蜂蜡
石蜡
塑料
沥青
松香
1.晶体:具有规则的几何形状。
常见的晶体有:石英、云母、明矾、食盐、硫酸铜、糖、味精等。
2.非晶体:没有规则的几何形状。
常见的非晶体有:玻璃、蜂蜡、塑料、沥青、橡胶、松香等。
(一)、固体分为两类:
(二)、晶体和非晶体的区别:
1、熔点:晶体具有一定的熔点,非晶体没有一定的熔点。
(二)、晶体和非晶体的区别:
2、外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状。
食盐
石英晶体
明矾晶体
晶体
非晶体
(二)、晶体和非晶体的区别:
3、物理性质上:
晶体的物理性质与方向有关(这种特性叫各向异性)
非晶体的物理性质在各个方向是相同的(这种特性叫各向同性)
云母:导热性上表现出显著的各向异性
方铝矿:导电性上表现出显著的各向异性
方解石:光的折射上表现出显著的各向异性,
(二)、晶体和非晶体的区别:
3、物理性质上:
晶体的物理性质与方向有关(这种特性叫各向异性)
非晶体的物理性质在各个方向是相同的(这种特性叫各向同性)
1、熔点:晶体具有一定的熔点,非晶体没有一定的熔点。
2、外形上:晶体具有规则的几何形状,非晶体没有规则的几何形状。
天然水晶和石英玻璃的成分都是sio2 思考你能想到什么?
(1)一种物质可能以晶体和非晶体两种不同的形态出现,一种物质是晶体还是非晶体并不是绝对的.
(2)许多非晶体在一定的条件下可以转化为晶体.
(3)在冷却得足够快和冷却到足够低的温度时,几乎所有的材料都能成为非晶体.
1.单晶体:一个物体就是一个完整的晶体.
例如:雪花、食盐小颗粒、单晶硅、单晶锗等.
2.多晶体:整个物体是由许多杂乱无章地排列着的小晶体组成。其中的小晶体叫做晶粒.
(1)多晶体没有规则的几何形状.
(2)不显示各向异性.(每一晶粒内部都是各向异性的).
(3) 有确定的熔点.
(一)单晶体和多晶体的区别:
(二)如何区分多晶体和非晶体?
晶体微观结构:
组成晶体的物质微粒(分子或原子、离子)依照一定的规律在空间中整齐地排列,具有空间上的周期性.
食盐的晶体结构
(一)晶体外形的规则性可以用物质微粒的规则
排列来解释
(二)晶体的各向异性也是由晶体的内部结构
决定的.
各向异性的微观解释
(三)晶体具有固定熔点.
晶体溶化时,吸收的 热量全部用来破坏规则的排列,温度不发生变化.
非晶体熔化时,先变软,然后变成粘滞性很大的液体,温度不断升高.
(三)有的物质在不同条件下能够生成不同的晶体。
因为组成它们的微粒能够按照不同规则在空
间分布.
石墨质地松软,粉状润滑剂,制作铅笔心.
金刚石有很大的硬度,可以用来切割玻璃
同一种化学成分的物质,为什么有不同的物理性质?
1.固体可分为晶体和非晶体两大类 .
2 .晶体和非晶体的差别.
熔点:晶体具有固定的熔点,非晶体没有
外形:晶体具有规则的几何形状,非晶体则没有规则的几何形状
物理性质:晶体各向异性,非晶体各向同性
3.多晶体和非晶体的差别
多晶体和非晶体都没有规则的几何形状
多晶体有一定的熔点,非晶体没有一定的熔点
多晶体和非晶体的一些物理性质都表现为各向同性
4.固体材料在生活,生产,科学,研究等方面的应用
1、
1. 关于晶体和非晶体,下列说法中正确的是( )
A.单晶体具有各向异性
B.多晶体也具有各向异性
C.非晶体的各种物理性质,在各个方向上都是相同的
D.晶体的各种物理性质,在各个方向上都是不同的
2、下列固体中全是由晶体组成的是( ).
(A)石英、云母、明矾、食盐、雪花、铜
(B)石英、玻璃、云母、铜
(C)食盐、雪花、云母、硫酸铜、松香
(D)蜂蜡、松香、橡胶、沥青
3.某物体表现出各向异性是由于组成物体的物质微粒( ).
(A)在空间的排列不规则
(B)在空间按一定的规则排列
(C)数目较多的缘故
(D)数目较少的缘故
4.晶体在熔解过程中吸收的热量,主要用于( )
(A)破坏空间点阵结构,增加分子动能
(B)破坏空间点阵结构,增加分子势能
(C)破坏空间点阵结构,增加分子的势能和动能
(D)破坏空间点阵结构,但不增加分子的势能和动能
