科粤版九年级下册化学:8.5 化学肥料——物质 ( 离子 ) 的共存(共22张PPT)
文档属性
| 名称 | 科粤版九年级下册化学:8.5 化学肥料——物质 ( 离子 ) 的共存(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-04-29 00:00:00 | ||
图片预览




文档简介
(共22张PPT)
科粤版九年级下册第八章
常见的酸、碱、盐
8.5化学肥料
——物质 ( 离子 ) 的共存
1、通过复习,会判断物质间是否反应,并准确说出或写出化学方程式。
2、通过分组实验,探寻并说出酸碱盐溶液能发生反应的原因。
3、通过游戏,熟练找出离子不能共存的组合。
4、通过针对训练,准确完成有关物质(离子)共存的习题,总结出解题关键。
学习目标
前置研究汇报一
1、如果物质间在一定条件下能发生反应,那么你认为它们在该条件下能同时存在吗?请举例谈谈你对物质能或不能共存的理解。
物质共存是指物质间相互不能发生化学反应。
不发生反应
共存
发生反应
不共存
目标检测
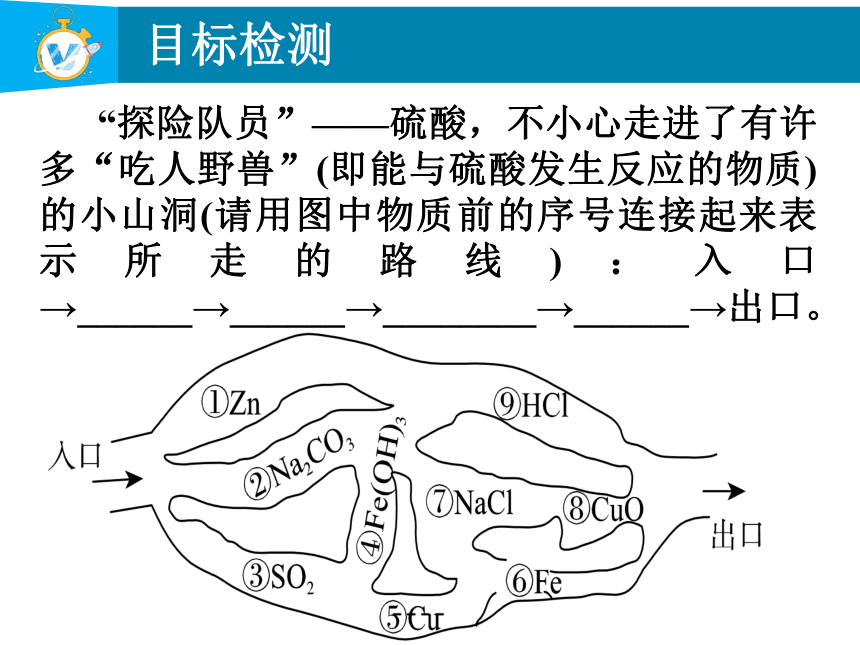
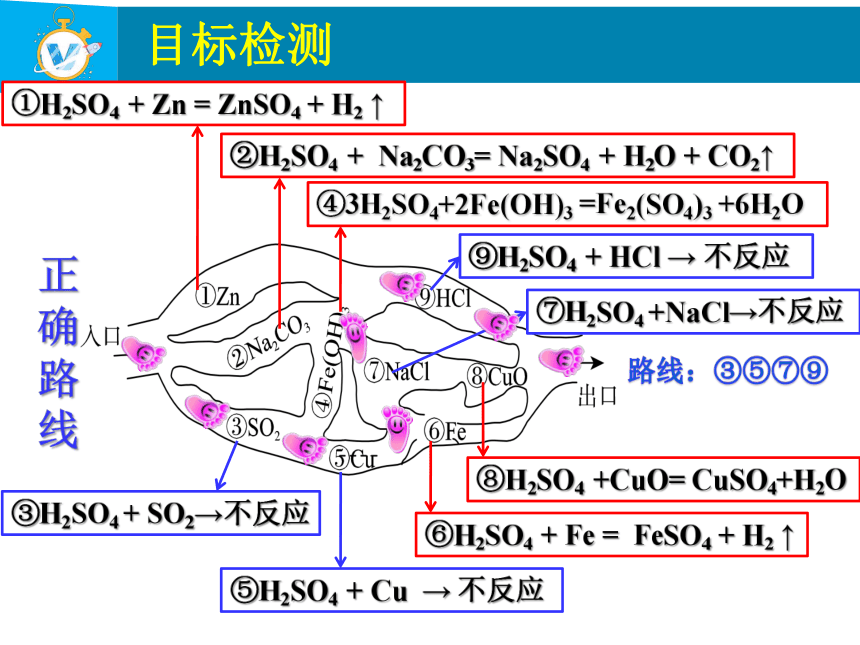
“探险队员”——硫酸,不小心走进了有许多“吃人野兽”(即能与硫酸发生反应的物质)的小山洞(请用图中物质前的序号连接起来表示所走的路线):入口→______→______→________→______→出口。
①H2SO4 + Zn = ZnSO4 + H2 ↑
②H2SO4 + Na2CO3= Na2SO4 + H2O + CO2↑
③H2SO4 + SO2→不反应
④3H2SO4+2Fe(OH)3 =Fe2(SO4)3 +6H2O
⑤H2SO4 + Cu → 不反应
⑥H2SO4 + Fe = FeSO4 + H2 ↑
⑦H2SO4 +NaCl→不反应
⑧H2SO4 +CuO= CuSO4+H2O
⑨H2SO4 + HCl → 不反应
正确路线
目标检测
前置研究汇报二
钾、钠、硝酸、铵盐溶,( K+ 、Na+ 、NO3--、NH4+ )
氯化物中银不溶, ( AgCl↓)
硫酸盐中钡不溶, ( BaSO4 ↓)
碳酸盐中都不溶。 (除K+、Na+、NH4+ )
说明:“溶”表示可溶于水,“不”表示不溶于水,“微”表示微溶于水,“空格”表示水。
2、《酸碱盐溶解性表》中“溶”“微”“不”“空格”是什么意思?你能熟练说出中表中各物质的溶解情况吗?请与大家分享一下你记忆的方法。
目标检测
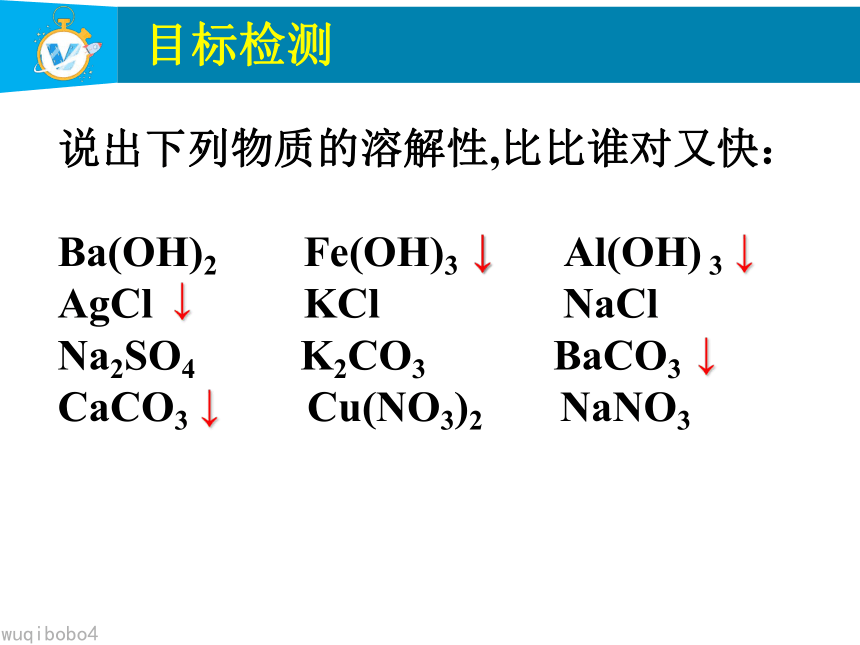
说出下列物质的溶解性,比比谁对又快:
Ba(OH)2 Fe(OH)3 Al(OH) 3?
AgCl KCl NaCl?
Na2SO4 K2CO3 ? BaCO3 CaCO3 Cu(NO3)2 NaNO3
↓
↓
↓
↓
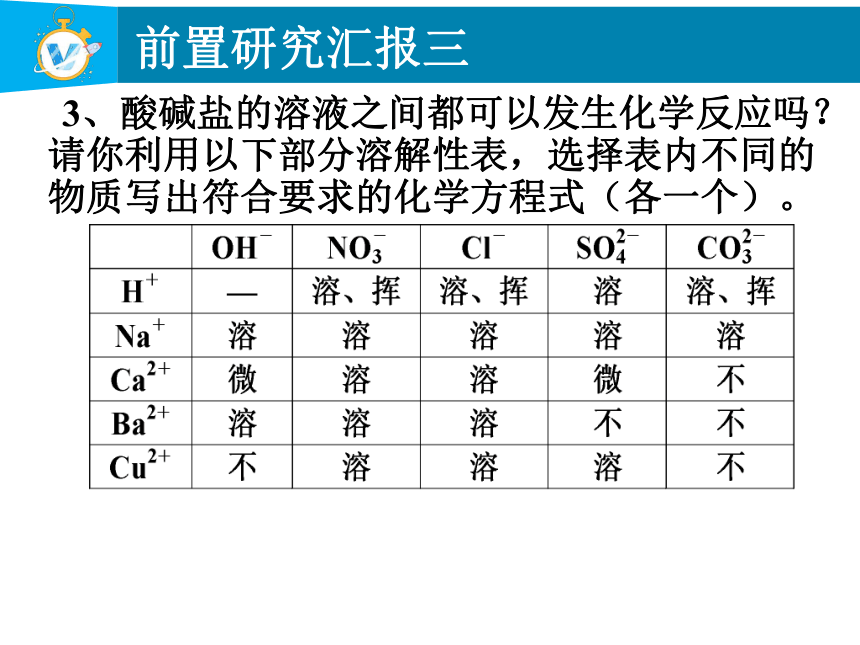
3、酸碱盐的溶液之间都可以发生化学反应吗?请你利用以下部分溶解性表,选择表内不同的物质写出符合要求的化学方程式(各一个)。
前置研究汇报三
(1)一种酸和一种碱:
______________________________。
(2)一种酸和一种盐:
____________________________________。
(3)一种碱和一种盐:
_____________________________________。
(4)一种盐和另一种盐:
_____________________________________。
HCl+NaOH===NaCl+H2O
2HCl+Na2CO3===2NaCl+H2O+CO2↑
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
BaCl2+Na2SO4===2NaCl+BaSO4↓
这些反应属于哪种基本反应类型?反应发生时生成物需要满足什么条件?
前置研究汇报四
4、如何从离子的角度解释复分解反应发生的条件呢?请你根据酸碱中和反应的实质试推其他反应产生沉淀、气体的原因,并举例说明。
中和反应的实质:
H+ 和 OH- 结合成H2O
Na+ 和Cl- 不变
H+ + OH- →H2O
在溶液中,离子共存是指阴阳离子之间不会结合成沉淀或气体或水。
不结合成↓或↑或水
共存
发生反应
不共存
实验探究:我选择的两种物质间会发生反应吗?如果反应,它们的反应实质是什么呢?
★实验仪器和药品:试管、试管架、稀HCl、
Na2CO3溶液、CuSO4溶液、 NaOH溶液、
BaCl2溶液、H2SO4溶液。
活动与探究:
酸碱盐溶液发生反应的实质是什么?
★实验要求:
1、每种试剂取用一滴管;
2、操作规范、安全实验;
3、分工合作,看、记、思;
观察并说出实验现象
写出反应方程式
找出反应实质
常见不能共存的离子组合
HCO3-
CO32-
Ba2+
SO42-
Ag+
Cl -
Cu2+
NH4+
Fe3+
Zn2+
Mg2+
Ca2+
H2O
Al3+
CO2↑
NH3 ↑
CaCO3↓
BaCO3↓
BaSO4↓
AgCl↓
Cu(OH) 2 ↓
Fe(OH) 3 ↓
Al (OH) 3↓
Mg(OH) 2 ↓
Zn (OH) 2 ↓
游戏规则
1、小组成员合作完成;
2、其中一人任意选一种离子符号,其他人找出与之不能共存的离子符号,并准确说出这两种离子结合而成的物质;
3、比一比在一分钟之内哪一组找到的组合对又多。
离子
1、下列各组中的离子,能在溶液中大量共存的是( ) A、K+、Ag+、NO3-、Cl- B、Mg 2+、Ba 2+、OH-、NO3- C、Al 3+、Fe 3+、SO42-、Cl- D、K+、H+、NH 4+、OH -
针对训练
C
AgCl ↓
Mg(OH)2 ↓
NH3 ↑
H2O
2.分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( )
A.NaNO3 Ba(OH)2 Cu(NO3)2
B.H2SO4 NaNO3 Na2SO4
C.H2SO4 KNO3 FeSO4
D.CaCl2 Na2SO4 BaCl2
B
Cu(OH)2 ↓
浅绿色
BaSO4↓
针对训练
3、下列各组离子,在pH=13的溶液中可以大量共存的是( ) A、K+、Al3+、SO42-、Cl- B、Na+、Ba 2+、 SO42- 、NO3- C、NH4+、K+、Cl-、NO3- D、K+、Na+、CO32-、SO4 2-
D
OH-
针对训练
1.pH>7的溶液
2.使酚酞溶液变红的溶液
Al(OH)3 ↓
BaSO4↓
NH3 ↑
4、在能与镁粉反应生成H2的溶液中,能大量共存,且其溶液为无色的是( )
A、 Ca 2+、Cl-、MnO4-、Na+???
B、 K+、Cl-、SO42-、NH4+
C、 CO32-、Na+、K +、Cl-????
D、 H+、Cl-、Ag+、NO3-
B
H+
针对训练
pH<7的溶液或使石蕊溶液变红的溶液
2、附加隐含条件的应用规律︰
(1)溶液无色透明时,溶液中肯定没有
有色离子 Cu2+、Fe3+、Fe2+、MnO4-等 :
(2)酸性溶液中,一定存在 H+
(3)碱性溶液中,一定存在 OH-
物质(离子)的共存
一、 物质共存:物质间相互不能发生化学反应。
二、 离子共存:在溶液中阴阳离子之间不能结合成沉淀或气体或水。
不能共存的离子组:一水二气九沉淀
三、隐含条件:
1.无色透明,不含有色离子 :
Cu2+、Fe3+、Fe2+、MnO4-
2.酸性溶液中,一定存在H+
3.碱性溶液中,一定存在OH-
梳理课堂 盘点收获
科粤版九年级下册第八章
常见的酸、碱、盐
8.5化学肥料
——物质 ( 离子 ) 的共存
1、通过复习,会判断物质间是否反应,并准确说出或写出化学方程式。
2、通过分组实验,探寻并说出酸碱盐溶液能发生反应的原因。
3、通过游戏,熟练找出离子不能共存的组合。
4、通过针对训练,准确完成有关物质(离子)共存的习题,总结出解题关键。
学习目标
前置研究汇报一
1、如果物质间在一定条件下能发生反应,那么你认为它们在该条件下能同时存在吗?请举例谈谈你对物质能或不能共存的理解。
物质共存是指物质间相互不能发生化学反应。
不发生反应
共存
发生反应
不共存
目标检测
“探险队员”——硫酸,不小心走进了有许多“吃人野兽”(即能与硫酸发生反应的物质)的小山洞(请用图中物质前的序号连接起来表示所走的路线):入口→______→______→________→______→出口。
①H2SO4 + Zn = ZnSO4 + H2 ↑
②H2SO4 + Na2CO3= Na2SO4 + H2O + CO2↑
③H2SO4 + SO2→不反应
④3H2SO4+2Fe(OH)3 =Fe2(SO4)3 +6H2O
⑤H2SO4 + Cu → 不反应
⑥H2SO4 + Fe = FeSO4 + H2 ↑
⑦H2SO4 +NaCl→不反应
⑧H2SO4 +CuO= CuSO4+H2O
⑨H2SO4 + HCl → 不反应
正确路线
目标检测
前置研究汇报二
钾、钠、硝酸、铵盐溶,( K+ 、Na+ 、NO3--、NH4+ )
氯化物中银不溶, ( AgCl↓)
硫酸盐中钡不溶, ( BaSO4 ↓)
碳酸盐中都不溶。 (除K+、Na+、NH4+ )
说明:“溶”表示可溶于水,“不”表示不溶于水,“微”表示微溶于水,“空格”表示水。
2、《酸碱盐溶解性表》中“溶”“微”“不”“空格”是什么意思?你能熟练说出中表中各物质的溶解情况吗?请与大家分享一下你记忆的方法。
目标检测
说出下列物质的溶解性,比比谁对又快:
Ba(OH)2 Fe(OH)3 Al(OH) 3?
AgCl KCl NaCl?
Na2SO4 K2CO3 ? BaCO3 CaCO3 Cu(NO3)2 NaNO3
↓
↓
↓
↓
3、酸碱盐的溶液之间都可以发生化学反应吗?请你利用以下部分溶解性表,选择表内不同的物质写出符合要求的化学方程式(各一个)。
前置研究汇报三
(1)一种酸和一种碱:
______________________________。
(2)一种酸和一种盐:
____________________________________。
(3)一种碱和一种盐:
_____________________________________。
(4)一种盐和另一种盐:
_____________________________________。
HCl+NaOH===NaCl+H2O
2HCl+Na2CO3===2NaCl+H2O+CO2↑
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
BaCl2+Na2SO4===2NaCl+BaSO4↓
这些反应属于哪种基本反应类型?反应发生时生成物需要满足什么条件?
前置研究汇报四
4、如何从离子的角度解释复分解反应发生的条件呢?请你根据酸碱中和反应的实质试推其他反应产生沉淀、气体的原因,并举例说明。
中和反应的实质:
H+ 和 OH- 结合成H2O
Na+ 和Cl- 不变
H+ + OH- →H2O
在溶液中,离子共存是指阴阳离子之间不会结合成沉淀或气体或水。
不结合成↓或↑或水
共存
发生反应
不共存
实验探究:我选择的两种物质间会发生反应吗?如果反应,它们的反应实质是什么呢?
★实验仪器和药品:试管、试管架、稀HCl、
Na2CO3溶液、CuSO4溶液、 NaOH溶液、
BaCl2溶液、H2SO4溶液。
活动与探究:
酸碱盐溶液发生反应的实质是什么?
★实验要求:
1、每种试剂取用一滴管;
2、操作规范、安全实验;
3、分工合作,看、记、思;
观察并说出实验现象
写出反应方程式
找出反应实质
常见不能共存的离子组合
HCO3-
CO32-
Ba2+
SO42-
Ag+
Cl -
Cu2+
NH4+
Fe3+
Zn2+
Mg2+
Ca2+
H2O
Al3+
CO2↑
NH3 ↑
CaCO3↓
BaCO3↓
BaSO4↓
AgCl↓
Cu(OH) 2 ↓
Fe(OH) 3 ↓
Al (OH) 3↓
Mg(OH) 2 ↓
Zn (OH) 2 ↓
游戏规则
1、小组成员合作完成;
2、其中一人任意选一种离子符号,其他人找出与之不能共存的离子符号,并准确说出这两种离子结合而成的物质;
3、比一比在一分钟之内哪一组找到的组合对又多。
离子
1、下列各组中的离子,能在溶液中大量共存的是( ) A、K+、Ag+、NO3-、Cl- B、Mg 2+、Ba 2+、OH-、NO3- C、Al 3+、Fe 3+、SO42-、Cl- D、K+、H+、NH 4+、OH -
针对训练
C
AgCl ↓
Mg(OH)2 ↓
NH3 ↑
H2O
2.分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( )
A.NaNO3 Ba(OH)2 Cu(NO3)2
B.H2SO4 NaNO3 Na2SO4
C.H2SO4 KNO3 FeSO4
D.CaCl2 Na2SO4 BaCl2
B
Cu(OH)2 ↓
浅绿色
BaSO4↓
针对训练
3、下列各组离子,在pH=13的溶液中可以大量共存的是( ) A、K+、Al3+、SO42-、Cl- B、Na+、Ba 2+、 SO42- 、NO3- C、NH4+、K+、Cl-、NO3- D、K+、Na+、CO32-、SO4 2-
D
OH-
针对训练
1.pH>7的溶液
2.使酚酞溶液变红的溶液
Al(OH)3 ↓
BaSO4↓
NH3 ↑
4、在能与镁粉反应生成H2的溶液中,能大量共存,且其溶液为无色的是( )
A、 Ca 2+、Cl-、MnO4-、Na+???
B、 K+、Cl-、SO42-、NH4+
C、 CO32-、Na+、K +、Cl-????
D、 H+、Cl-、Ag+、NO3-
B
H+
针对训练
pH<7的溶液或使石蕊溶液变红的溶液
2、附加隐含条件的应用规律︰
(1)溶液无色透明时,溶液中肯定没有
有色离子 Cu2+、Fe3+、Fe2+、MnO4-等 :
(2)酸性溶液中,一定存在 H+
(3)碱性溶液中,一定存在 OH-
物质(离子)的共存
一、 物质共存:物质间相互不能发生化学反应。
二、 离子共存:在溶液中阴阳离子之间不能结合成沉淀或气体或水。
不能共存的离子组:一水二气九沉淀
三、隐含条件:
1.无色透明,不含有色离子 :
Cu2+、Fe3+、Fe2+、MnO4-
2.酸性溶液中,一定存在H+
3.碱性溶液中,一定存在OH-
梳理课堂 盘点收获
