北京版九年级下册第11章酸与碱第三节几种常见的碱习题(解析版)
文档属性
| 名称 | 北京版九年级下册第11章酸与碱第三节几种常见的碱习题(解析版) |
|
|
| 格式 | zip | ||
| 文件大小 | 54.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-01 00:00:00 | ||
图片预览




文档简介
第三节 几种常见的碱
一、单选题(本大题共11小题,共22.0分)
1.下列说法或做法不正确的是( )
A.使用活性炭净水时不仅可滤去其中不溶性杂质,还可以除去水中一些可溶性杂质
B.胃液中含有盐酸有助于消化,所以胃中盐酸越多越好
C.衣服上的油污除了可用洗涤剂去除外,还可以用汽油代替洗涤剂使油污溶解
D.被雨水淋湿的自行车先用抹布擦干,再用带油的抹布擦
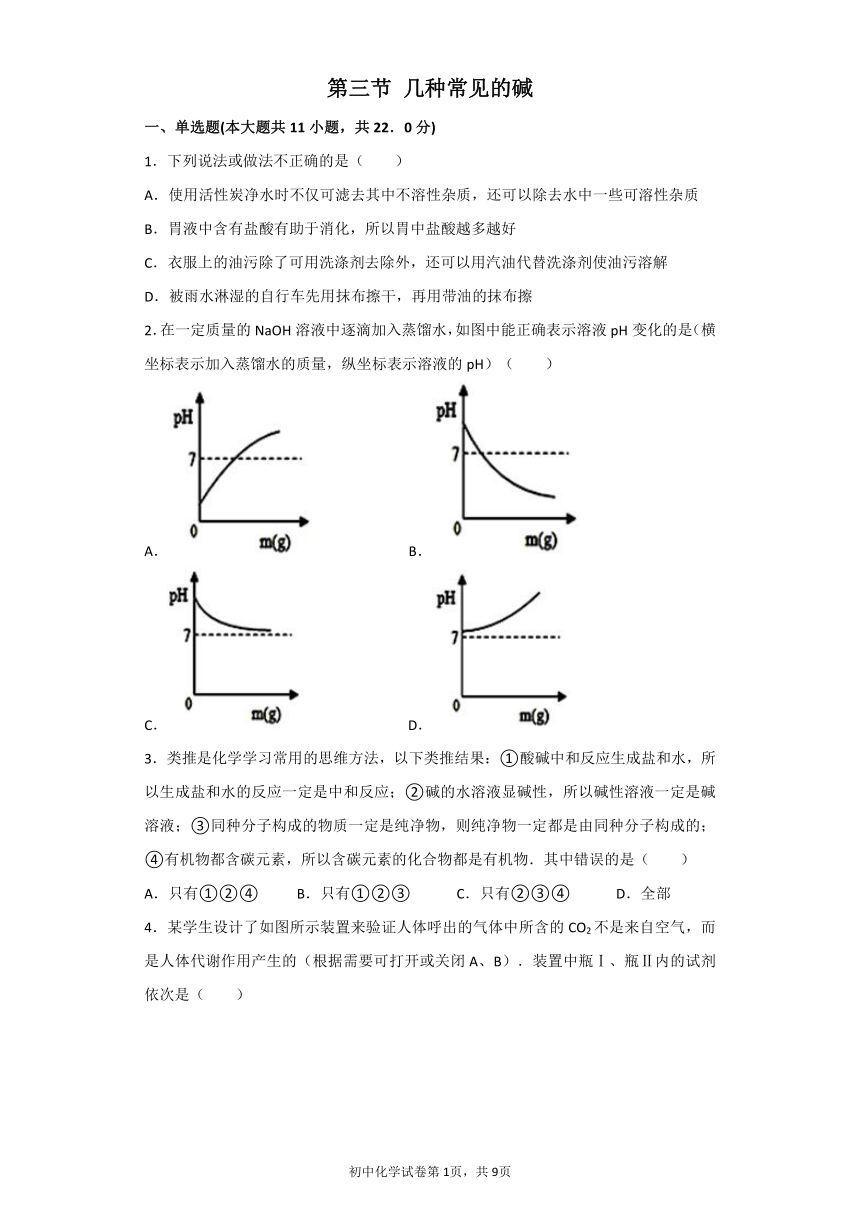
2.在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )
A. B.
C. D.
3.类推是化学学习常用的思维方法,以下类推结果:①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;③同种分子构成的物质一定是纯净物,则纯净物一定都是由同种分子构成的;④有机物都含碳元素,所以含碳元素的化合物都是有机物.其中错误的是( )
A.只有①②④ B.只有①②③ C.只有②③④ D.全部
4.某学生设计了如图所示装置来验证人体呼出的气体中所含的CO2不是来自空气,而是人体代谢作用产生的(根据需要可打开或关闭A、B).装置中瓶Ⅰ、瓶Ⅱ内的试剂依次是( )
A.Ca(OH)2、NaOH B.NaOH、Ca(OH)2
C.稀HCl、Ca(OH)2 D.NaOH、BaCl2
5.化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是( )
A.合理使用农药和化肥,既可以降低对环境的污染,又利于人体健康
B.垃圾分类放置,可以充分利用资源、保护环境
C.生活中常用的塑料、纤维、合金、玻璃都是有机合成材料
D.农作物一般适宜在pH=7或接近7的土壤中生存,常用熟石灰改良酸性土壤
6.下列关于浓盐酸和浓硫酸的叙述不正确的是( )
A.浓硫酸具有吸水性,所以常用作干燥剂
B.稀释浓硫酸时,须将水沿器壁缓慢的注入浓硫酸中,并不断用玻璃棒搅拌
C.打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现大量白雾
D.浓盐酸、浓硫酸敞口放置在空气中一段时间后,溶质的质量分数都会减小
7.下列说正确的是( )
A.石油是碳、氢元素组成的化合物 B.天然气就是甲烷
C.SO2和NO2是造成酸雨的主要物质 D.化学反应都伴有放热现象
8.化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是( )
A.合理使用农药和化肥,既可以降低对环境的污染,又利于人体健康
B.去超市购物,使用布袋代替塑料袋
C.生活中常用的塑料、纤维、合金玻璃都是有机合成材料
D.农作物一般适宜在pH=7或接近7的土壤中生存,常用熟石灰改良酸性土壤
9.下列对某一主题知识归纳有错误的一组是( )
A、物质的构成 B、性质与用途
金属铜---由铜原子构成
氧气-----由氧分子构成
氯化钠----由钠离子和氯离子构成
O2助燃-----气焊切割金属
活性炭吸附性-----作净水剂
C化学之最 D化学与生活
地壳中含量最多的元素----铝元素
空气中含量最多的元素---氮元素
减少水污染---使用无磷洗衣粉
减少酸雨发生----使用新型能源
A.A B.B C.C D.D
10.当今世界三大环境问题是:酸雨、臭氧层衰竭和温室效应.其中形成酸雨的主要原因是人们向空气中排放了大量的( )
A.SO2 B.CO2 C.CO D.水蒸气
11.下列说法中,错误的是( )
A.可用灼烧的方法鉴别羊毛、合成纤维
B.可用紫色石蕊溶液检测雨水是否为酸雨
C.人体补充铁元素可预防贫血
D.木材、棉布等着火,可用水来灭火
二、填空题(本大题共3小题,共3.0分)
12.人体的体液必须维持在一定的酸碱度范围内,如血液的pH在______之间,胃液的pH在______之间。
13.酸雨对农作物以及一下建筑等不利,酸雨的pH______。
14.从①甲烷、②干冰、③二氧化硫、④氢气、⑤一氧化碳、⑥氯酸钾等物质中选择一种物质的序号来填空(每种物质最多选一次):
(1)易形成酸雨的是______;
(2)可用来人工降雨的是______;
(3)从环境保护的角度考虑,最理想的燃料是______;
(4)造成煤气中毒的物质是______。
三、探究题(本大题共1小题,共10.0分)
15.硫酸和盐酸是两种重要的化工原料。
(1)浓硫酸常用作干燥剂因为它具有______,浓盐酸因为有______而要密封保存。
(2)写出稀硫酸与下类物质反应的化学方程式。
①和镁条的反应:______。
②和碳酸钠溶液反应:______。
③和氯化钡溶液反应:______。
上述反应中属于复分解反应的有______;属于酸的共同性质的有______;(填编号)
不同的酸性质差异的原因______。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是______。(填编号)
①金属表面除锈②制造药物氯化锌③除去氯化钠中的少量碳酸钠
第三节 几种常见的碱
【答案】
1.??B???????2.??C???????3.??D???????4.??A???????5.??C???????
6.??B???????7.??C???????8.??C???????9.??C???????10.??A???????
11.??B???????
12.??7.35~7.45 ? 0.9~1.5 ????????
13.??小于5.6???????
14.??③ ? ② ? ④ ? ⑤ ????????
15.??吸水 ? 挥发 ? Mg+H2SO4=MgSO4+H2↑; ? H2SO4+Na2CO3=Na2SO4+H2O+CO2↑; ? BaCl2+H2SO4=BaSO4↓+2HCl ? ②③ ? ①② ? 阴离子不同 ? ②③ ????????
【解析】
1.??
解:A、活性炭是固体颗粒,能起到过滤的作用除去部分不溶性固体杂质,具有的是吸附性,能吸附溶解在水中的色素和异味,正确;
B、胃液中的盐酸过多会引起病痛,错误;
C、洗涤剂对油污有乳化作用,汽油对油污具有溶解作用,故可以使用汽油代替洗涤剂使油污溶解,正确;
D、被雨水淋湿的自行车先用抹布擦干,再用带油的抹布擦,可以防止铁生锈,正确;
故选:B。
A、根据净水的方法分析解答;
B、根据胃酸的量分析解答;
C、根据油污的洗涤方法分析解答;
D、根据防锈的措施解答.
掌握常见的物质的性质和用途是正确解答本题的关键.
2.??
解:NaOH溶液的pH值大于7,随着蒸馏水的逐滴加入,pH值大会逐渐降低,但是不是低于7,观察选项,只有选项C符合题意。
故选:C。
当溶液的pH等于7时,呈中性。当溶液的pH大于7时,呈碱性。当溶液的pH小于7时,呈酸性。向碱性溶液中加水稀释时,溶液的pH降低,但是不会低于7。
注意:pH值越小,溶液的酸性越强;pH值越大,溶液的碱性越强。
3.??
解:①酸碱中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项类推错误。
②碱溶液显碱性,但碱性溶液不一定是碱溶液,如碳酸钠溶液显碱性,但属于盐,故选项说类推错误。
③同种分子构成的物质一定是纯净物,但纯净物不一定都是由同种分子构成的,也可能是由原子或离子构成的,故选项类推错误。
④有机物都含碳元素,但含碳元素的化合物不一定都是有机物,如一氧化碳、二氧化碳等虽含碳元素,但其性质与无机物类似,因此把它们看作无机物;故选项类推错误。
故①②③④类推均错误。
故选:D。
①中和反应是指酸和碱作用生成盐和水的反应,判断中和反应时一要看反应物是否是酸和碱,二是看生成物是否是盐和水,二者缺一不可.
②根据碱性溶液不一定是碱溶液,也有可能是盐溶液.
③纯净物是由同种粒子构成的,据此进行分析判断.
④含有碳元素的化合物叫有机化合物,简称有机物;不含碳元素的化合物是无机化合物;碳的氧化物、碳酸盐、碳酸虽含碳元素,但其性质与无机物类似,因此把它们看作无机物.
本题难度不大,掌握中和反应的特征、纯净物与有机物的特征、碱性溶液不一定是碱溶液等是正确解答本题的关键.
4.??
解:利用澄清的石灰水来检验产生的气体是二氧化碳;用碱液来除去空气中的二氧化碳,在除空气中的二氧化碳时应从Ⅱ端吸入空气,装置Ⅱ用来吸收空气中的二氧化碳。从I端呼出气体,装置I用来验证人呼出的二氧化碳。
故选:A。
要验证呼出的气体中的二氧化碳不是来自于空气,必须将空气中的二氧化碳吸收干净,然后,再将空气吸入体内,然后呼出,若澄清石灰水变浑浊,那么说明二氧化碳是人体产生的.
本题考查性质实验的设计,侧重于学生的分析能力和实验能力的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意把握物质的性质以及实验的原理,难道不大.
5.??
解:A、合理使用农药和化肥,既可以降低对环境的污染,又能防止农药和化肥残留,利于人体健康,故选项说法正确。
B、垃圾分类放置,可以充分利用资源、保护环境,故选项说法正确。
C、生活中常用的塑料属于有机合成材料,纤维可能是合成纤维,也可能是天然纤维,合金属于金属材料,玻璃属于无机非金属材料,故选项说法错误。
D、农作物一般适宜在pH=7或接近7的土壤中生存,熟石灰显碱性,常用熟石灰改良酸性土壤,故选项说法正确。
故选:C。
A、根据合理使用农药和化肥的意义,进行分析判断。
B、根据防治环境污染的措施,进行分析判断。
C、有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物分析判断。
D、根据中和反应应用,进行分析判断。
本题难度不大,掌握农药和化肥的使用、合成材料的特征、中和反应应用等是正确解答本题的关键。
6.??
解:A、浓硫酸具有吸水性,所以常用作干燥剂,故选项说法正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故选项说法错误。
C、浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶,瓶口会产生白雾,故选项说法正确。
D、浓硫酸露置于空气中,溶质质量不变,溶剂质量增加,则溶质的质量分数变小;浓盐酸露置于空气中,溶质质量变小,溶剂质量不变,则溶质的质量分数变小,故选项说法正确。
故选:B。
A、根据浓硫酸具有吸水性,进行分析判断;
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断;
C、根据浓盐酸具有挥发性,进行分析判断;
D、根据浓盐酸的挥发性、浓硫酸的吸水性以及溶质质量分数的概念进行分析。
本题难度不大,掌握浓盐酸具有挥发性、浓硫酸具有吸水性、浓硫酸的稀释方法是正确解答本题的关键。
7.??
解:A.石油中主要含碳、氢两种元素,但不是化合物,是混合物,故A说法错误;
B.天然气主要成分是甲烷,还含有其它杂质,属于混合物,故B说法错误;
C、SO2和NO2是造成酸雨的主要物质,故C正确;
D、有的化学反应放热,有的化学反应吸热,故D错误。
故选:C。
A.根据石油的组成成分进行分析判断;
B.根据天然气的主要成分进行解答;
C、根据造成酸雨的气体分析;
D、根据化学反应有的放热,有的吸热分析。
本题是一道基础知识的综合题,涉及知识点较多,但考查的较基础难度不大,平时注意对基础知识的积累。
8.??
解:A、合理使用农药和化肥,既可以降低对环境的污染,又能防止农药和化肥残留,利于人体健康,故选项说法正确。
B、去超市购物,使用布袋代替塑料袋,能减少白色污染,故选项说法正确。
C、生活中常用的塑料属于有机合成材料,纤维可能是合成纤维,也可能是天然纤维,合金属于金属材料,玻璃属于无机非金属材料,故选项说法错误。
D、农作物一般适宜在pH=7或接近7的土壤中生存,熟石灰显碱性,常用熟石灰改良酸性土壤,故选项说法正确。
故选:C。
A、根据合理使用农药和化肥的意义,进行分析判断。
B、根据防治白色污染的措施,进行分析判断。
C、有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物。
D、根据中和反应应用,进行分析判断。
本题难度不大,掌握防止白色污染的措施、合成材料的特征、中和反应应用等是正确解答本题的关键。
9.??
解:A、铜是由铜原子构成的,氧气是由氧分子构成的,氯化钠是由钠离子和氯离子构成的,故A正确;
B、氧气具有助燃性,可以用于切割或焊接金属;活性炭具有吸附性,能用于净水吸附色素和异味,故B正确;
C、地壳中含有最多的元素是氧元素,故C错误;
D、使用无磷洗衣粉能减少水污染,使用新能源能减少酸雨的发生,故D正确;
故选:C。
根据物质的微观构成、性质和用途以及元素的含量和减少污染的方法进行分析解答.
本题考查了对常见化学知识的归纳和总结,完成此题,可以依据已有的知识进行.
10.??
解:酸雨形成的罪魁祸首是酸性气体大量产生。一氧化碳、二氧化硫、二氧化碳、水蒸气四种气体中二氧化硫、二氧化碳是酸性气体,但是二氧化碳溶于水生成碳酸碳酸酸性很弱,而二氧化硫溶于水生成强酸,可形成酸雨。
故选:A。
酸雨主要是一些酸性气体升到空中与空气中的水蒸汽结合,使雨水酸化.罪魁祸首是煤、石油大量燃烧生成的酸性气体.
本题主要考查酸雨的形成原因;酸性气体的大量排放.这里的酸性气体溶于水后生成一些酸性较强的酸.
11.??
解:A、羊毛的主要成分是蛋白质,灼烧有烧焦羽毛的气味,而合成纤维灼烧没有烧焦羽毛的气味,可以使用灼烧的方法鉴别羊毛和合成纤维,正确;
B、石蕊在酸碱性溶液中显示的颜色不同,不可以使用石蕊试液检测雨水是否为酸雨,酸雨的pH小于5.6,错误;
C、人体补充铁元素可预防贫血,正确;
D、木材、棉布等着火,可用水来灭火,正确;
故选:B。
A、根据羊毛的主要成分是蛋白质,灼烧有烧焦羽毛的气味解答;
B、根据石蕊在酸碱性溶液中显示的颜色不同解答;
C、根据元素在人体中的作用解答;
D、根据灭火的原理解答;
掌握常见的物质的性质和用途是正确解答本题的关键。
12.??
解:人体的体液必须维持在一定的酸碱度范围内,如血液的pH在7.35~7.45之间,胃液的pH在0.9~1.5之间。
故填:7.35~7.45;0.9~1.5。
根据人体体液的酸碱性及其pH来分析解答。
要想解答好这类题目,要理解和熟记酸碱性对生命活动和农作物生长的影响等相关知识。
13.??
解:酸雨的pH<5.6,对农作物以及一些建筑等不利,可以腐蚀建筑物。
故填:小于5.6。
根据酸雨的成因、规定以及危害来分析。
要想解答好这类题目,首先,要理解和熟记酸雨的产生、危害及防治措施等相关知识。
14.??
解:(1)酸雨是因为人类活动排放的酸性气体如二氧化硫、氮氧化物(如二氧化氮)溶于水而形成的。
(2)干冰升华时吸热,降低周围温度,可以用作人工降雨。
(3)氢气燃烧产物为水,不污染环境,放热量高,属于高能、无污染的能源。
(4)一氧化碳是煤气的主要成分,具有毒性,易造成煤气中毒。
故答案为:(1)③;(2)②;(3)④;(4)⑤。
(1)酸雨是指pH值小于5.6的降水,主要是人类活动排放的酸性气体如二氧化硫、氮氧化物溶于水而形成。
(2)干冰是二氧化碳的固体,干冰升华时能吸收热量,所以干冰经常被用作制冷剂。
(3)根据氢能源的特点进行分析解答。
(4)根据一氧化碳的毒性分析。
题难度不大,掌握酸雨的形成、金属的性质与用途、二氧化碳的用途、常见的能源等是正确解答本题的关键。
15.??
解:(1)浓硫酸具有吸水性,在实验室常用作干燥剂,浓盐酸长期放置在空气中会逐渐变稀,因为浓盐酸有挥发性;
(2)①镁能与稀硫酸发生置换反应,生成氢气和硫酸镁,反应的化学方程式为:Mg+H2SO4=MgSO4+H2↑;
②稀硫酸与碳酸钠溶液反应生成硫酸钾、水和二氧化碳,反应的化学方程式为:H2SO4+Na2CO3=Na2SO4+H2O+CO2
③硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,化学方程式为:BaCl2+H2SO4=BaSO4↓+2HCl;
属于复分解反应的是②③;属于酸的共同性质的是①②;
不同的酸性质差异的原因阴离子不同;
(3)①盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应,都能用于金属表面除锈,故选项错误;
②制造药物氯化锌中含有氯元素,盐酸含氯元素,硫酸不含氯元素,故不能用硫酸代替盐酸,故选项正确;
③NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故不能用硫酸代替盐酸,故选项正确;
故选②③。
故填:(1)吸水;挥发;(2)Mg+H2SO4=MgSO4+H2↑;??H2SO4+Na2CO3=Na2SO4+H2O+CO2↑;BaCl2+H2SO4=BaSO4↓+2HCl;③;①②;阴离子不同;
(3)②③。
(1)根据浓硫酸具有强烈的腐蚀性进行分析解答;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(3)盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质。
题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、酸的用途等并能灵活运用是正确解答本题的关键。
初中化学试卷第2页,共2页
初中化学试卷第1页,共1页
一、单选题(本大题共11小题,共22.0分)
1.下列说法或做法不正确的是( )
A.使用活性炭净水时不仅可滤去其中不溶性杂质,还可以除去水中一些可溶性杂质
B.胃液中含有盐酸有助于消化,所以胃中盐酸越多越好
C.衣服上的油污除了可用洗涤剂去除外,还可以用汽油代替洗涤剂使油污溶解
D.被雨水淋湿的自行车先用抹布擦干,再用带油的抹布擦
2.在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )
A. B.
C. D.
3.类推是化学学习常用的思维方法,以下类推结果:①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;③同种分子构成的物质一定是纯净物,则纯净物一定都是由同种分子构成的;④有机物都含碳元素,所以含碳元素的化合物都是有机物.其中错误的是( )
A.只有①②④ B.只有①②③ C.只有②③④ D.全部
4.某学生设计了如图所示装置来验证人体呼出的气体中所含的CO2不是来自空气,而是人体代谢作用产生的(根据需要可打开或关闭A、B).装置中瓶Ⅰ、瓶Ⅱ内的试剂依次是( )
A.Ca(OH)2、NaOH B.NaOH、Ca(OH)2
C.稀HCl、Ca(OH)2 D.NaOH、BaCl2
5.化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是( )
A.合理使用农药和化肥,既可以降低对环境的污染,又利于人体健康
B.垃圾分类放置,可以充分利用资源、保护环境
C.生活中常用的塑料、纤维、合金、玻璃都是有机合成材料
D.农作物一般适宜在pH=7或接近7的土壤中生存,常用熟石灰改良酸性土壤
6.下列关于浓盐酸和浓硫酸的叙述不正确的是( )
A.浓硫酸具有吸水性,所以常用作干燥剂
B.稀释浓硫酸时,须将水沿器壁缓慢的注入浓硫酸中,并不断用玻璃棒搅拌
C.打开盛有浓盐酸的试剂瓶瓶盖,瓶口上方出现大量白雾
D.浓盐酸、浓硫酸敞口放置在空气中一段时间后,溶质的质量分数都会减小
7.下列说正确的是( )
A.石油是碳、氢元素组成的化合物 B.天然气就是甲烷
C.SO2和NO2是造成酸雨的主要物质 D.化学反应都伴有放热现象
8.化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是( )
A.合理使用农药和化肥,既可以降低对环境的污染,又利于人体健康
B.去超市购物,使用布袋代替塑料袋
C.生活中常用的塑料、纤维、合金玻璃都是有机合成材料
D.农作物一般适宜在pH=7或接近7的土壤中生存,常用熟石灰改良酸性土壤
9.下列对某一主题知识归纳有错误的一组是( )
A、物质的构成 B、性质与用途
金属铜---由铜原子构成
氧气-----由氧分子构成
氯化钠----由钠离子和氯离子构成
O2助燃-----气焊切割金属
活性炭吸附性-----作净水剂
C化学之最 D化学与生活
地壳中含量最多的元素----铝元素
空气中含量最多的元素---氮元素
减少水污染---使用无磷洗衣粉
减少酸雨发生----使用新型能源
A.A B.B C.C D.D
10.当今世界三大环境问题是:酸雨、臭氧层衰竭和温室效应.其中形成酸雨的主要原因是人们向空气中排放了大量的( )
A.SO2 B.CO2 C.CO D.水蒸气
11.下列说法中,错误的是( )
A.可用灼烧的方法鉴别羊毛、合成纤维
B.可用紫色石蕊溶液检测雨水是否为酸雨
C.人体补充铁元素可预防贫血
D.木材、棉布等着火,可用水来灭火
二、填空题(本大题共3小题,共3.0分)
12.人体的体液必须维持在一定的酸碱度范围内,如血液的pH在______之间,胃液的pH在______之间。
13.酸雨对农作物以及一下建筑等不利,酸雨的pH______。
14.从①甲烷、②干冰、③二氧化硫、④氢气、⑤一氧化碳、⑥氯酸钾等物质中选择一种物质的序号来填空(每种物质最多选一次):
(1)易形成酸雨的是______;
(2)可用来人工降雨的是______;
(3)从环境保护的角度考虑,最理想的燃料是______;
(4)造成煤气中毒的物质是______。
三、探究题(本大题共1小题,共10.0分)
15.硫酸和盐酸是两种重要的化工原料。
(1)浓硫酸常用作干燥剂因为它具有______,浓盐酸因为有______而要密封保存。
(2)写出稀硫酸与下类物质反应的化学方程式。
①和镁条的反应:______。
②和碳酸钠溶液反应:______。
③和氯化钡溶液反应:______。
上述反应中属于复分解反应的有______;属于酸的共同性质的有______;(填编号)
不同的酸性质差异的原因______。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是______。(填编号)
①金属表面除锈②制造药物氯化锌③除去氯化钠中的少量碳酸钠
第三节 几种常见的碱
【答案】
1.??B???????2.??C???????3.??D???????4.??A???????5.??C???????
6.??B???????7.??C???????8.??C???????9.??C???????10.??A???????
11.??B???????
12.??7.35~7.45 ? 0.9~1.5 ????????
13.??小于5.6???????
14.??③ ? ② ? ④ ? ⑤ ????????
15.??吸水 ? 挥发 ? Mg+H2SO4=MgSO4+H2↑; ? H2SO4+Na2CO3=Na2SO4+H2O+CO2↑; ? BaCl2+H2SO4=BaSO4↓+2HCl ? ②③ ? ①② ? 阴离子不同 ? ②③ ????????
【解析】
1.??
解:A、活性炭是固体颗粒,能起到过滤的作用除去部分不溶性固体杂质,具有的是吸附性,能吸附溶解在水中的色素和异味,正确;
B、胃液中的盐酸过多会引起病痛,错误;
C、洗涤剂对油污有乳化作用,汽油对油污具有溶解作用,故可以使用汽油代替洗涤剂使油污溶解,正确;
D、被雨水淋湿的自行车先用抹布擦干,再用带油的抹布擦,可以防止铁生锈,正确;
故选:B。
A、根据净水的方法分析解答;
B、根据胃酸的量分析解答;
C、根据油污的洗涤方法分析解答;
D、根据防锈的措施解答.
掌握常见的物质的性质和用途是正确解答本题的关键.
2.??
解:NaOH溶液的pH值大于7,随着蒸馏水的逐滴加入,pH值大会逐渐降低,但是不是低于7,观察选项,只有选项C符合题意。
故选:C。
当溶液的pH等于7时,呈中性。当溶液的pH大于7时,呈碱性。当溶液的pH小于7时,呈酸性。向碱性溶液中加水稀释时,溶液的pH降低,但是不会低于7。
注意:pH值越小,溶液的酸性越强;pH值越大,溶液的碱性越强。
3.??
解:①酸碱中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项类推错误。
②碱溶液显碱性,但碱性溶液不一定是碱溶液,如碳酸钠溶液显碱性,但属于盐,故选项说类推错误。
③同种分子构成的物质一定是纯净物,但纯净物不一定都是由同种分子构成的,也可能是由原子或离子构成的,故选项类推错误。
④有机物都含碳元素,但含碳元素的化合物不一定都是有机物,如一氧化碳、二氧化碳等虽含碳元素,但其性质与无机物类似,因此把它们看作无机物;故选项类推错误。
故①②③④类推均错误。
故选:D。
①中和反应是指酸和碱作用生成盐和水的反应,判断中和反应时一要看反应物是否是酸和碱,二是看生成物是否是盐和水,二者缺一不可.
②根据碱性溶液不一定是碱溶液,也有可能是盐溶液.
③纯净物是由同种粒子构成的,据此进行分析判断.
④含有碳元素的化合物叫有机化合物,简称有机物;不含碳元素的化合物是无机化合物;碳的氧化物、碳酸盐、碳酸虽含碳元素,但其性质与无机物类似,因此把它们看作无机物.
本题难度不大,掌握中和反应的特征、纯净物与有机物的特征、碱性溶液不一定是碱溶液等是正确解答本题的关键.
4.??
解:利用澄清的石灰水来检验产生的气体是二氧化碳;用碱液来除去空气中的二氧化碳,在除空气中的二氧化碳时应从Ⅱ端吸入空气,装置Ⅱ用来吸收空气中的二氧化碳。从I端呼出气体,装置I用来验证人呼出的二氧化碳。
故选:A。
要验证呼出的气体中的二氧化碳不是来自于空气,必须将空气中的二氧化碳吸收干净,然后,再将空气吸入体内,然后呼出,若澄清石灰水变浑浊,那么说明二氧化碳是人体产生的.
本题考查性质实验的设计,侧重于学生的分析能力和实验能力的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意把握物质的性质以及实验的原理,难道不大.
5.??
解:A、合理使用农药和化肥,既可以降低对环境的污染,又能防止农药和化肥残留,利于人体健康,故选项说法正确。
B、垃圾分类放置,可以充分利用资源、保护环境,故选项说法正确。
C、生活中常用的塑料属于有机合成材料,纤维可能是合成纤维,也可能是天然纤维,合金属于金属材料,玻璃属于无机非金属材料,故选项说法错误。
D、农作物一般适宜在pH=7或接近7的土壤中生存,熟石灰显碱性,常用熟石灰改良酸性土壤,故选项说法正确。
故选:C。
A、根据合理使用农药和化肥的意义,进行分析判断。
B、根据防治环境污染的措施,进行分析判断。
C、有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物分析判断。
D、根据中和反应应用,进行分析判断。
本题难度不大,掌握农药和化肥的使用、合成材料的特征、中和反应应用等是正确解答本题的关键。
6.??
解:A、浓硫酸具有吸水性,所以常用作干燥剂,故选项说法正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故选项说法错误。
C、浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶,瓶口会产生白雾,故选项说法正确。
D、浓硫酸露置于空气中,溶质质量不变,溶剂质量增加,则溶质的质量分数变小;浓盐酸露置于空气中,溶质质量变小,溶剂质量不变,则溶质的质量分数变小,故选项说法正确。
故选:B。
A、根据浓硫酸具有吸水性,进行分析判断;
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断;
C、根据浓盐酸具有挥发性,进行分析判断;
D、根据浓盐酸的挥发性、浓硫酸的吸水性以及溶质质量分数的概念进行分析。
本题难度不大,掌握浓盐酸具有挥发性、浓硫酸具有吸水性、浓硫酸的稀释方法是正确解答本题的关键。
7.??
解:A.石油中主要含碳、氢两种元素,但不是化合物,是混合物,故A说法错误;
B.天然气主要成分是甲烷,还含有其它杂质,属于混合物,故B说法错误;
C、SO2和NO2是造成酸雨的主要物质,故C正确;
D、有的化学反应放热,有的化学反应吸热,故D错误。
故选:C。
A.根据石油的组成成分进行分析判断;
B.根据天然气的主要成分进行解答;
C、根据造成酸雨的气体分析;
D、根据化学反应有的放热,有的吸热分析。
本题是一道基础知识的综合题,涉及知识点较多,但考查的较基础难度不大,平时注意对基础知识的积累。
8.??
解:A、合理使用农药和化肥,既可以降低对环境的污染,又能防止农药和化肥残留,利于人体健康,故选项说法正确。
B、去超市购物,使用布袋代替塑料袋,能减少白色污染,故选项说法正确。
C、生活中常用的塑料属于有机合成材料,纤维可能是合成纤维,也可能是天然纤维,合金属于金属材料,玻璃属于无机非金属材料,故选项说法错误。
D、农作物一般适宜在pH=7或接近7的土壤中生存,熟石灰显碱性,常用熟石灰改良酸性土壤,故选项说法正确。
故选:C。
A、根据合理使用农药和化肥的意义,进行分析判断。
B、根据防治白色污染的措施,进行分析判断。
C、有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物。
D、根据中和反应应用,进行分析判断。
本题难度不大,掌握防止白色污染的措施、合成材料的特征、中和反应应用等是正确解答本题的关键。
9.??
解:A、铜是由铜原子构成的,氧气是由氧分子构成的,氯化钠是由钠离子和氯离子构成的,故A正确;
B、氧气具有助燃性,可以用于切割或焊接金属;活性炭具有吸附性,能用于净水吸附色素和异味,故B正确;
C、地壳中含有最多的元素是氧元素,故C错误;
D、使用无磷洗衣粉能减少水污染,使用新能源能减少酸雨的发生,故D正确;
故选:C。
根据物质的微观构成、性质和用途以及元素的含量和减少污染的方法进行分析解答.
本题考查了对常见化学知识的归纳和总结,完成此题,可以依据已有的知识进行.
10.??
解:酸雨形成的罪魁祸首是酸性气体大量产生。一氧化碳、二氧化硫、二氧化碳、水蒸气四种气体中二氧化硫、二氧化碳是酸性气体,但是二氧化碳溶于水生成碳酸碳酸酸性很弱,而二氧化硫溶于水生成强酸,可形成酸雨。
故选:A。
酸雨主要是一些酸性气体升到空中与空气中的水蒸汽结合,使雨水酸化.罪魁祸首是煤、石油大量燃烧生成的酸性气体.
本题主要考查酸雨的形成原因;酸性气体的大量排放.这里的酸性气体溶于水后生成一些酸性较强的酸.
11.??
解:A、羊毛的主要成分是蛋白质,灼烧有烧焦羽毛的气味,而合成纤维灼烧没有烧焦羽毛的气味,可以使用灼烧的方法鉴别羊毛和合成纤维,正确;
B、石蕊在酸碱性溶液中显示的颜色不同,不可以使用石蕊试液检测雨水是否为酸雨,酸雨的pH小于5.6,错误;
C、人体补充铁元素可预防贫血,正确;
D、木材、棉布等着火,可用水来灭火,正确;
故选:B。
A、根据羊毛的主要成分是蛋白质,灼烧有烧焦羽毛的气味解答;
B、根据石蕊在酸碱性溶液中显示的颜色不同解答;
C、根据元素在人体中的作用解答;
D、根据灭火的原理解答;
掌握常见的物质的性质和用途是正确解答本题的关键。
12.??
解:人体的体液必须维持在一定的酸碱度范围内,如血液的pH在7.35~7.45之间,胃液的pH在0.9~1.5之间。
故填:7.35~7.45;0.9~1.5。
根据人体体液的酸碱性及其pH来分析解答。
要想解答好这类题目,要理解和熟记酸碱性对生命活动和农作物生长的影响等相关知识。
13.??
解:酸雨的pH<5.6,对农作物以及一些建筑等不利,可以腐蚀建筑物。
故填:小于5.6。
根据酸雨的成因、规定以及危害来分析。
要想解答好这类题目,首先,要理解和熟记酸雨的产生、危害及防治措施等相关知识。
14.??
解:(1)酸雨是因为人类活动排放的酸性气体如二氧化硫、氮氧化物(如二氧化氮)溶于水而形成的。
(2)干冰升华时吸热,降低周围温度,可以用作人工降雨。
(3)氢气燃烧产物为水,不污染环境,放热量高,属于高能、无污染的能源。
(4)一氧化碳是煤气的主要成分,具有毒性,易造成煤气中毒。
故答案为:(1)③;(2)②;(3)④;(4)⑤。
(1)酸雨是指pH值小于5.6的降水,主要是人类活动排放的酸性气体如二氧化硫、氮氧化物溶于水而形成。
(2)干冰是二氧化碳的固体,干冰升华时能吸收热量,所以干冰经常被用作制冷剂。
(3)根据氢能源的特点进行分析解答。
(4)根据一氧化碳的毒性分析。
题难度不大,掌握酸雨的形成、金属的性质与用途、二氧化碳的用途、常见的能源等是正确解答本题的关键。
15.??
解:(1)浓硫酸具有吸水性,在实验室常用作干燥剂,浓盐酸长期放置在空气中会逐渐变稀,因为浓盐酸有挥发性;
(2)①镁能与稀硫酸发生置换反应,生成氢气和硫酸镁,反应的化学方程式为:Mg+H2SO4=MgSO4+H2↑;
②稀硫酸与碳酸钠溶液反应生成硫酸钾、水和二氧化碳,反应的化学方程式为:H2SO4+Na2CO3=Na2SO4+H2O+CO2
③硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,化学方程式为:BaCl2+H2SO4=BaSO4↓+2HCl;
属于复分解反应的是②③;属于酸的共同性质的是①②;
不同的酸性质差异的原因阴离子不同;
(3)①盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应,都能用于金属表面除锈,故选项错误;
②制造药物氯化锌中含有氯元素,盐酸含氯元素,硫酸不含氯元素,故不能用硫酸代替盐酸,故选项正确;
③NaOH能与硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故不能用硫酸代替盐酸,故选项正确;
故选②③。
故填:(1)吸水;挥发;(2)Mg+H2SO4=MgSO4+H2↑;??H2SO4+Na2CO3=Na2SO4+H2O+CO2↑;BaCl2+H2SO4=BaSO4↓+2HCl;③;①②;阴离子不同;
(3)②③。
(1)根据浓硫酸具有强烈的腐蚀性进行分析解答;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(3)盐酸、硫酸都能与金属表面的锈的主要成分金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质。
题难度不大,掌握酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应)、酸的用途等并能灵活运用是正确解答本题的关键。
初中化学试卷第2页,共2页
初中化学试卷第1页,共1页
