课题3 元素第二课时元素周期表 (共15张PPT)
文档属性
| 名称 | 课题3 元素第二课时元素周期表 (共15张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-01 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
3.元素周期表简介
第三单元 课题3 元素
学习目标
1、元素:
2、原子的构成:
具有相同核电荷数(即核内质子数)的一类原子的总称。
原子
原子核
核外电子
质子:每个质子带1个单位正电荷 (相对质量为1)
中子:不带电(相对质量为1)
核电荷数=质子数=核外电子数 因此,原子呈电中性
每个电子带1个单位负电荷(相对质量为1/1836)
温故知新
质子的相对质量=
1个质子的质量
=
1.6726×10-27kg
1个中子的质量=1.6749×10-27kg
中子的相对质量=1.008
因此:原子的相对质量约等于质子数与中子数之和
温故知新
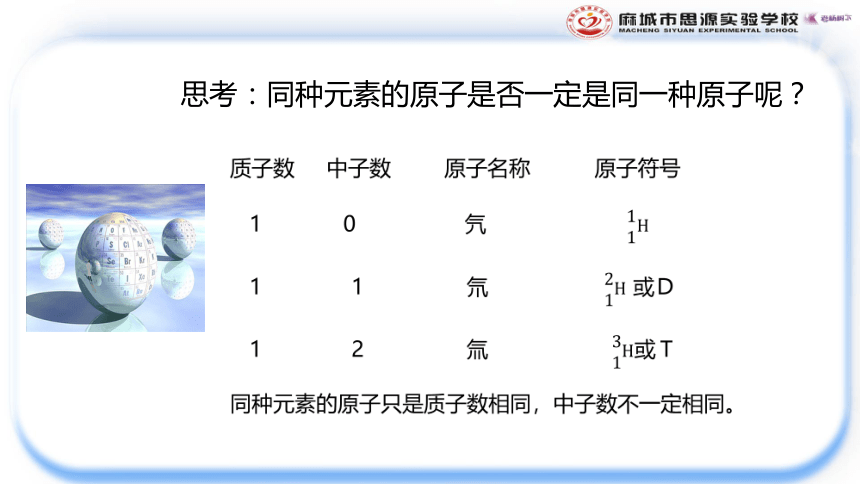
思考:同种元素的原子是否一定是同一种原子呢?
元素周期表的发展与编排原则
门捷列夫
相对原子质量
化学性质
原子核外电子层数目
原子序数
原子核外最外层电子数
电子层数
课堂练习
课堂练习
课堂练习
元素周期表的结构
电子层数
电子层数
最外层电子数
电子层数递增
最外层电子数
最外层电子数
增多
增大
增强
减弱
增强
减弱
1、元素周期表简介:
周期:每一个横行称为一个周期 ,共7个周期
族:每一个纵行称为一个族 ,共16个族
2、元素周期表按颜色分为金属元素区和非金属元素区。
金属元素 “钅”字旁
非金属“石”字旁 ,“气”字头, “氵”字旁
3、原子序数,核电荷数,核内质子数=核外电子数
4、元素周期表上标有该元素的相对原子质量。
?
3.元素周期表简介
第三单元 课题3 元素
学习目标
1、元素:
2、原子的构成:
具有相同核电荷数(即核内质子数)的一类原子的总称。
原子
原子核
核外电子
质子:每个质子带1个单位正电荷 (相对质量为1)
中子:不带电(相对质量为1)
核电荷数=质子数=核外电子数 因此,原子呈电中性
每个电子带1个单位负电荷(相对质量为1/1836)
温故知新
质子的相对质量=
1个质子的质量
=
1.6726×10-27kg
1个中子的质量=1.6749×10-27kg
中子的相对质量=1.008
因此:原子的相对质量约等于质子数与中子数之和
温故知新
思考:同种元素的原子是否一定是同一种原子呢?
元素周期表的发展与编排原则
门捷列夫
相对原子质量
化学性质
原子核外电子层数目
原子序数
原子核外最外层电子数
电子层数
课堂练习
课堂练习
课堂练习
元素周期表的结构
电子层数
电子层数
最外层电子数
电子层数递增
最外层电子数
最外层电子数
增多
增大
增强
减弱
增强
减弱
1、元素周期表简介:
周期:每一个横行称为一个周期 ,共7个周期
族:每一个纵行称为一个族 ,共16个族
2、元素周期表按颜色分为金属元素区和非金属元素区。
金属元素 “钅”字旁
非金属“石”字旁 ,“气”字头, “氵”字旁
3、原子序数,核电荷数,核内质子数=核外电子数
4、元素周期表上标有该元素的相对原子质量。
?
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
