京改版化学九年级下册第12章《盐》测试题(含答案)
文档属性
| 名称 | 京改版化学九年级下册第12章《盐》测试题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 185.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-06 00:00:00 | ||
图片预览



文档简介
第12章《盐》测试题
一、单选题(每小题只有一个正确答案)
1.在粗盐提纯实验中最后进行NaCl溶液的蒸发时,一般有如下操作:
①固定铁圈位置 ②放置蒸发皿 ③放置酒精灯 ④加热并搅拌 ⑤停止加热,借余热蒸干
正确的操作顺序是( )
A.①②③④⑤ B.①③②④⑤ C.③①②④⑤ D.③②①④⑤
2.下列物质的化学名称与俗名,对应错误的是( )
A.汞——水银 B.碳酸钠——熟石灰、消石灰
C.碳酸氢钠——小苏打 D.氢氧化钠——烧碱、火碱、苛性钠
3.下列做法中一定发生化学变化的是( )
A.用石油分馏制得汽油、柴油等 B.用柠檬酸和小苏打、白糖配置汽水
C.用钢丝球擦除灶具上的污渍 D.用汽油清洗衣服上的油污
4.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
选项 物质 操作方法
A Fe(Fe2O3) 加入过量稀盐酸,充分反应后过滤
B CaO粉末(CaCO3粉末) 加足量的水,充分搅拌后过滤
C NaOH溶液[Ca(OH)2溶液] 通入过量CO2气体,充分反应后过滤
D CuSO4溶液(硫酸) 加入过量CuO粉末,加热,充分反应后过滤
A.A B.B C.C D.D
5.下列说法正确的是
A.按溶解、过滤、蒸发的操作顺序从CuSO4和少量Fe粉的混合物中分离出CuSO4;
B.把某气体通入澄清石灰水,无浑浊出现,说明该气体中一定没有CO2;
C.用酚酞试液及溶液间的相互反应,可将Na2CO3、HCl、NaCl、NaOH四种溶液区分开来;
D.向某烧碱溶液中滴加少量稀盐酸,无气泡冒出,说明该烧碱溶液一定没有变质。
6.下列物质在水溶液中能大量共存的是
A.KNO3、NaOH、Na2CO3 B.NaCl、K2CO3、H2SO4
C.HCl、BaCl2、CuSO4 D.HCl、Ca(OH)2、NaNO3
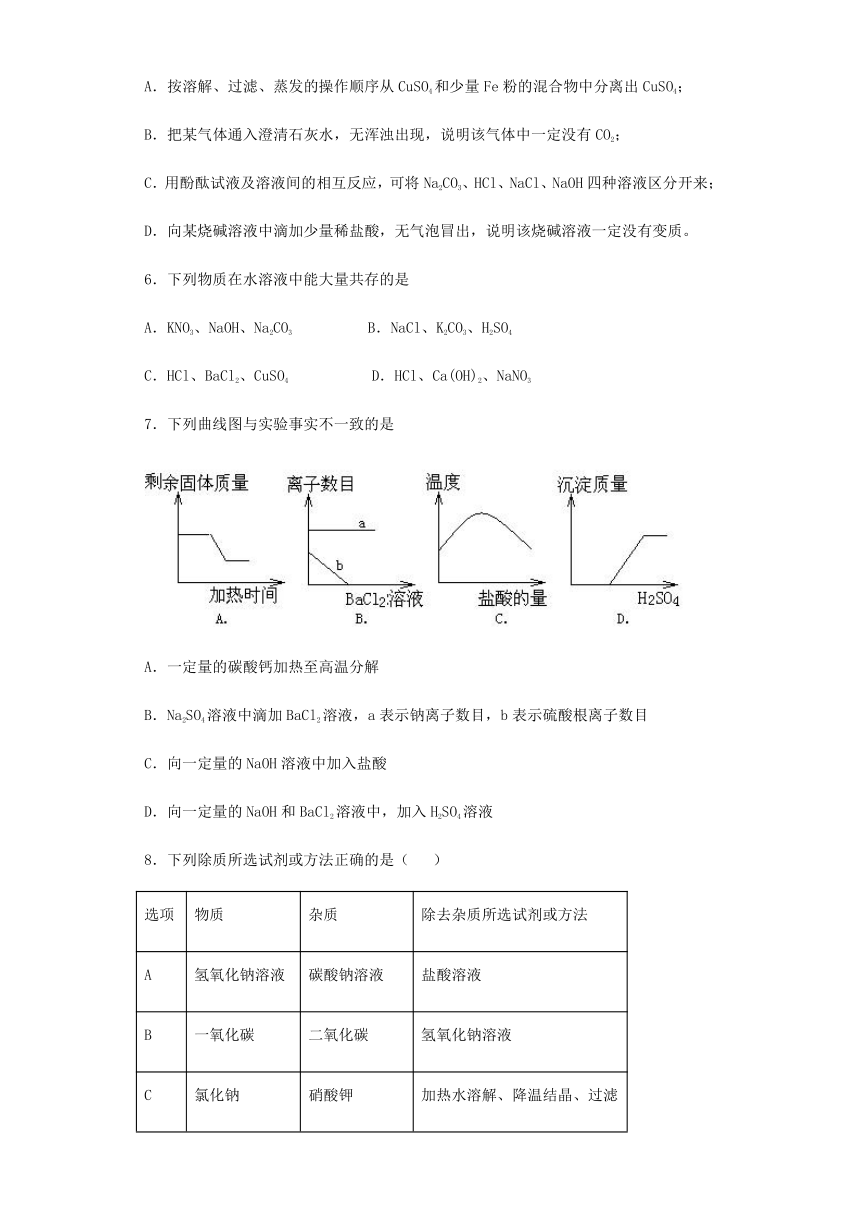
7.下列曲线图与实验事实不一致的是
A.一定量的碳酸钙加热至高温分解
B.Na2SO4溶液中滴加BaCl2溶液,a表示钠离子数目,b表示硫酸根离子数目
C.向一定量的NaOH溶液中加入盐酸
D.向一定量的NaOH和BaCl2溶液中,加入H2SO4溶液
8.下列除质所选试剂或方法正确的是( )
选项 物质 杂质 除去杂质所选试剂或方法
A 氢氧化钠溶液 碳酸钠溶液 盐酸溶液
B 一氧化碳 二氧化碳 氢氧化钠溶液
C 氯化钠 硝酸钾 加热水溶解、降温结晶、过滤
D 硝酸 盐酸 过量的硝酸银溶液
A.A B.B C.C D.D
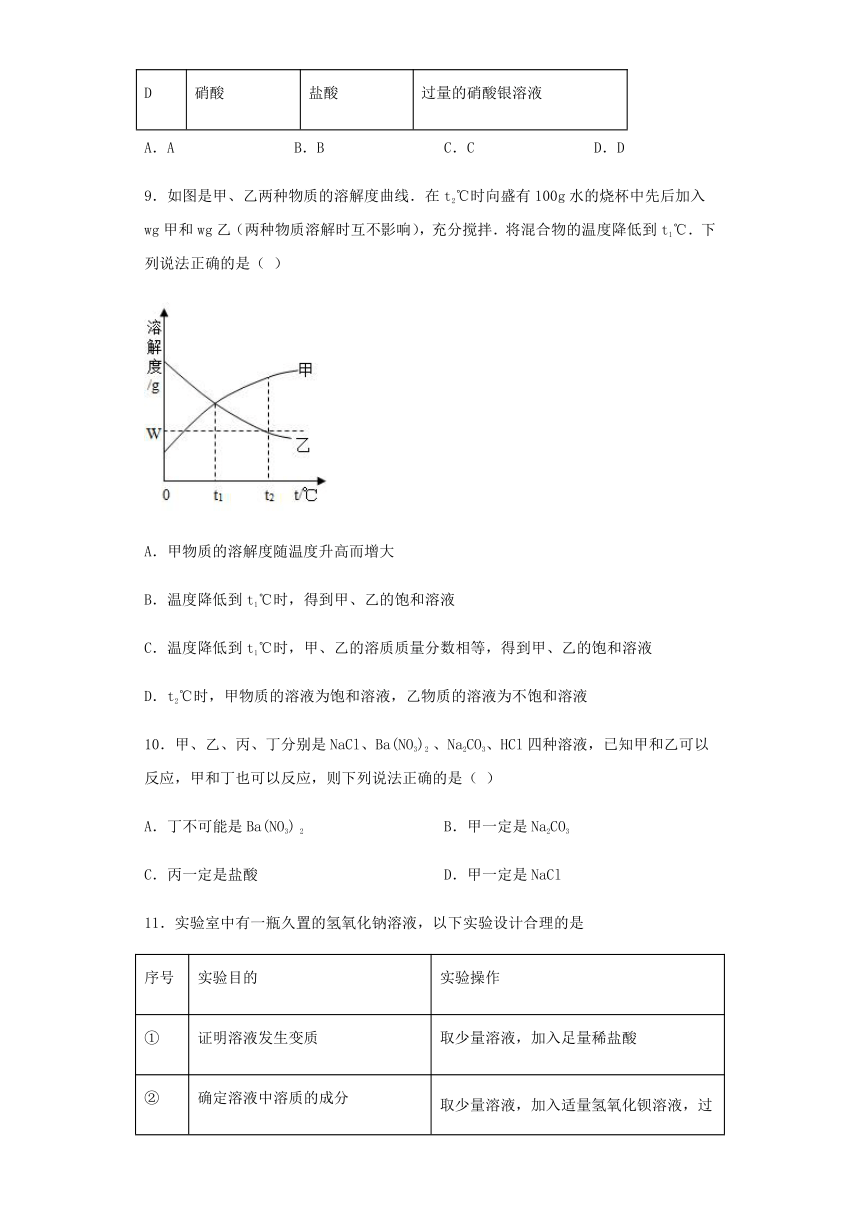
9.如图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入wg甲和wg乙(两种物质溶解时互不影响),充分搅拌.将混合物的温度降低到t1℃.下列说法正确的是( )
A.甲物质的溶解度随温度升高而增大
B.温度降低到t1℃时,得到甲、乙的饱和溶液
C.温度降低到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的饱和溶液
D.t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液
10.甲、乙、丙、丁分别是NaCl、Ba(NO3)2 、Na2CO3、HCl四种溶液,已知甲和乙可以反应,甲和丁也可以反应,则下列说法正确的是( )
A.丁不可能是Ba(NO3) 2 B.甲一定是Na2CO3
C.丙一定是盐酸 D.甲一定是NaCl
11.实验室中有一瓶久置的氢氧化钠溶液,以下实验设计合理的是
序号 实验目的 实验操作
① 证明溶液发生变质 取少量溶液,加入足量稀盐酸
② 确定溶液中溶质的成分 取少量溶液,加入适量氢氧化钡溶液,过滤,向滤液中滴加酚酞溶液
③ 测定溶液中碳酸钠的质量分数 取一定质量溶液,加入足量稀盐酸,将生成的气体通入浓硫酸,测浓硫酸的增重
④ 除去溶液中的碳酸钠 向溶液中滴加氢氧化钡溶液至恰好完全反应,过滤
A.①② B.②③ C.①④ D.②④
12.将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是( )
A.K2CO3、BaCl2、NaOH B.CaC12、HCl、KNO3
C.KOH、HCl、(NH4)2SO4 D.Fe2O3、KCl、NaNO3
13.天平两边各放质量相等的烧杯,分别装入等质量,等溶质质量分数的稀硫酸,此时天平平衡,将等质量的MgCO3和Na2CO3分别加入两烧杯中,充分反应后,下列说法错误的是
A.若天平不平衡,指针一定偏向加Na2CO3的一边
B.若天平平衡,两烧杯中的酸一定完全反应
C.若反应后Na2CO3有剩余,天平一定平衡
D.若天平不平衡,两种碳酸盐一定都没有剩余
14.下列化学推理中,正确的是
A.酸在水中都能离解出氢离子,所以能离解出氢离子的化合物都属于酸
B.湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
C.中和反应都生成盐和水, 所以有盐和水生成的反应一定是中和反应
D.某有机物燃烧生成CO2和H2O,说明该有机物含有碳、氢、氧三种元素
二、填空题
15.化学就在我们身边。从①熟石灰②金刚石③氯化钠④干冰四种物质中,选择适当的物质填空(填序号)。
(1)用于炒菜调味的是_____;
(2)用于人工降雨的是_____;
(3)用来裁玻璃的是_____;
(4)用来改良酸性土壤的是_____。
16.中国古代在认识和应用物质方面有辉煌的历史,请用恰当的化学用语填空。
(1)《本草纲目》中“灶中所烧薪柴之灰,令人以灰淋汁,取碱涴衣”中的碱为草木灰_____;
(2)《本草钢目》中“水银乃至阴之毒物,因火煅丹砂而出”水银的化学式_____;
(3)《报朴子)中记载“曾青涂铁,铁赤如铜”其曾青指硫酸铜溶液,其阳离子为_____;
(4)《天工开物》中“凡石灰,经火焚炼为用”的石灰主要成分为碳酸钙_____。
17.化学就在我们身边.请从下列物质中选择适当的物质填空.(填字母序号)
A.甲烷 B.氧气 C.生石灰 D.活性炭 E. 食盐
(1)可用作食品干燥剂的是______.
(2)能为人体提供呼吸的是______.
(3)最简单的有机物是__________.
(4)常用于冰箱内除异味的物质是______.
(5)常用作厨房调味品的是_____________.
18.如图是粗略测定粗盐中氯化钠含量的部分操作(杂质不溶于水),其中操作不规范的是( )
A.称量 B.溶解
C.过滤 D.蒸发
19.现有六种物质:A.氮气;B.氧气;C.干冰;D.碳酸钙;E.镁粉;F.红磷,选择适当的物质,将它们的字母代号填在横线上。
(1)可用于人工降雨的是_____。
(2)用于制作烟花和照明弹的是_____。
(3)可用作食品保护气的是_____。
(4)医疗上用于补钙药物的是_____。
三、推断题
20.已知A B C D E分别是初中化学常见的五种不同类别的物质,其中B是一种固体干燥剂。F是常见的一种红棕色物质,E含有两种元素,它们之间存在如图所示的关系(图中“一”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出)。
(1)写出F的化学式:_____。
(2)写出A与E反应的化学方程式:_____。
21.A~I 是初中化学常见的物质。常温下A、D、H、I为气体,E为液体,其他为固体。A、B、C、D是单质,B为红色。F与G,H与I组成元素相同。G中两元素的质量比为7:3。这些物质之间相互关系如图所示,图中“—”表示能相互反应;“→”表示转化关系;部分反应物、生成物及反应条件已略去。
(1)写出化学式:B____,G____。
(2)E→D反应的化学方程式是______。F→I反应的化学方程式是__________。
(3)反应①②的基本反应类型相同,该反应类型为__________。
四、实验题
22.氢氧化钠、氢氧化钙是两种常见的碱:
(1)它们有一些相似的化学性质,其原因是溶液中都含有_____。
(2)可作某些气体干燥剂的是_____。
(3)用氢氧化钙溶液检验二氧化碳,反应的化学方程式为_____。
(4)长期不合理使用化肥会使土壤酸化(如含有硝酸)熟石灰常用来改良酸性土壤,反应的化学方程式是_____。
(5)为了探究NaOH样品中是否存在NaCl、Na2CO3杂质,设计如下实验方案
①乙中有无色无味气体产生,证明样品中含有Na2CO3.产生气体的化学方程式为_____。
②试剂X为_____溶液;可证明NaCl存在的现象是_____。
(6)化学实验活动课上,同学们进行了如图所示的实验。
①实验一中,B试管中发生反应的化学方程式为_____。A、B两支试管中共同的实验现象是_____。
②实验二中,C试管中有白色沉淀生成,D试管中无现象。为了探究通入二氧化碳后是否发生反应,小明同学取D中少量溶液于试管中,选择合适的试剂进行实验,用化学方程式表示发生反应_____。
23.(9分)小王同学在厨房中发现一袋白色粉末状的食用物,包装袋上表示的化学成分字迹不清,于是他带到实验室探究其成分。(填空每空1分,计算3分,计9分)
(猜想与假设)猜想1.可能是淀粉(不溶)
猜想2.可能是纯碱
猜想3.可能是食盐
猜想4.可能是 (俗称小苏打)
(查阅资料)小苏打溶液显碱性,与氯化钡溶液不反应,淀粉不溶解于水中
(实验探究)
实验操作
实验现象
实验结论
(1)取样,溶于适量的水
形成无色溶液
猜想 不成立
(2)取少量品尝
有涩味
不是
(3)向(1)的溶液中滴加酚酞试液
溶液变红
是纯碱
小华认为,实验(3)结论不准确,原因是 。小华进行了如下实验:取28g所配溶液与50.2g氯化钡溶液混合,两种物质恰好完全反应。立即出现 ,由此他知道了该白色粉末是何物。过滤,所得滤液质量为58.5g,试计算:
(4)反应后生成的沉淀质量为 克。
(5)所得滤液中溶质的质量分数为多少?
五、计算题
24.为测定某纯碱样品杂质为氯化钠中碳酸钠的含量,某小组同学进行了如图所示的实验,请回答问题:
写出反应的化学方程式______;
列出求解混合物中参加反应的物质质量的比例式______;
样品中碳酸钠的含量为______最终结果保留整数;
最终所得溶液的溶质质量分数为______;
若用质量分数的浓盐酸配制实验所需稀盐酸,需要浓盐酸和水的质量比为______。
25.根据下图实验回答问题:
实验一:图1是同学们做粗盐提纯实验的操作示意图。
(1)操作④中用玻璃棒搅拌的作用是________________________________。
(2)操作⑥中的错误是________________。
(3)粗盐提纯实验的操作顺序为(填操作序号)____________、称量精盐并计算产率。
实验二:图2是验证硫酸铵的性质实验。
(4)图2实验验证了硫酸铵的物理性质:__________(答一条即可);化学性质:________________。
参考答案
1.C 2.B 3.B 4.D 5.C 6.A 7.D 8.B 9.A 10.B 11.C 12.B 13.C 14.B
15.③ ④ ② ①
16.
17. C B A D E
18.A
19.C E A D
20.Fe2O3 Na2CO3+2HCl=2NaCl+CO2↑+H2O
21.Cu Fe2O3 2H2O2H2↑+O2↑ Fe3O4+4CO4CO2+3Fe或者Fe3O4+2C2CO2↑+3Fe 置换反应
22.氢氧根离子(或OH-) 氢氧化钠固体 Ca(OH)2+CO2=CaCO3↓+H2O Ca(OH)2+2HNO3=Ca(NO3)2+2H2O Na2CO3+2HNO3=2NaNO3+H2O+CO2↑ 硝酸银(AgNO3)溶液 生成白色沉淀 2NaOH+CuSO4=Na2SO4+Cu(OH)2↓ 生成蓝色沉淀 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
23.碳酸氢钠 ,1,
(3)小苏打溶液呈碱性也能使酚酞变红,白色沉淀
(4)19.7
(5)20%
24. 1:4
25.防止局部温度过高造成液体飞溅 未用玻璃棒引流 ①⑤②③⑥④ 易溶于水(或白色固体) 能与熟石灰(碱)发生化学反应
