人教版九年级下册 第11单元 课题1 生活中常见的盐(课时2 复分解反应)(17张PPT)
文档属性
| 名称 | 人教版九年级下册 第11单元 课题1 生活中常见的盐(课时2 复分解反应)(17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-10 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
学习目标
进一步理解酸、碱、盐的基本概念;
能正确判断酸碱盐之间的反应;
理解复分解反应发生的条件。
1
2
3
下面三个反应与我们前面所学的化合、分解、置换三种反应有什么不同?这些反应有什么共同特征?
思考与交流
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
NaHCO3+HCl = NaCl+H2O+CO2↑
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH
由两种化合物互相交换成分,生成另外两种化合物的反应 叫做复分解反应。
2、复分解反应的特点
AB+CD = AD+CB
首尾两交换,各元素的化合价不变。
FeCl3+3NaOH==Fe(OH)3 ↓+3NaCl
酸和碱作用生成盐和水的中和反应是否也属于复分解反应?为什么?
思考与交流
酸+碱→盐+水
是两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应。
HCl+NaOH== NaCl+H2O
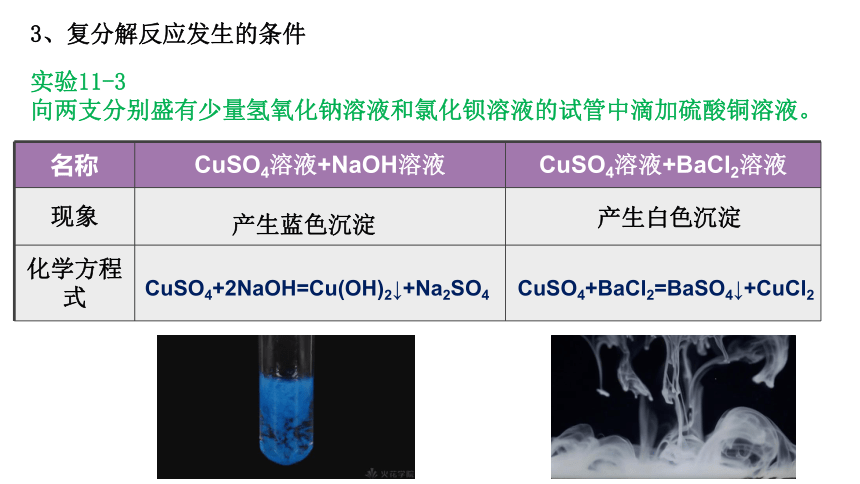
3、复分解反应发生的条件
产生蓝色沉淀
产生白色沉淀
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=BaSO4↓+CuCl2
实验11-3
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液。
名称 CuSO4溶液+NaOH溶液 CuSO4溶液+BaCl2溶液
现象
化学方程式
1、上述两个反应是否属于复分解反应?观察到的现象有什么共同之处?
思考与交流
是,都有沉淀生成
2、碳酸钠、碳酸钙等含碳酸根的盐溶液与盐酸
发生复分解反应时,可观察到的共同现象是什么?
都有气体生成
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或水(难电离的物质),复分解反应才可以发生。
生成水
生成气体
生成沉淀
部分酸碱盐的溶解性表 (课本114页)
OH- NO3- Cl- SO42- CO32-
H+ 溶 溶 溶 溶
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Ca2+ 微 溶 溶 微 不
Mg2+ 不 溶 溶 溶 微
Al3+ 不 溶 溶 溶 -----
Fe3+ 不 溶 溶 溶 -----
Cu2+ 不 溶 溶 溶 -----
Ag+ ----- 溶 不 微 不
① 常见的酸大多溶于水
② 可溶的碱有:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O
③ 钾盐、钠盐、铵盐、硝酸盐都易溶于水
④ 盐酸盐中只有AgCl不溶于水
⑤ 硫酸盐中只有BaSO4不溶于水
⑥ 碳酸盐大部分不溶于水,除钾、钠、铵盐外
常见的沉淀有八种:
Mg(OH)2、Al(OH)3、Fe(OH)3、Cu(OH)2 、AgCl 、BaSO4、BaCO3、CaCO3
白色
白色
白色
白色
白色
白色
红褐色
蓝色
背记口诀:
常见诸酸皆可溶,钾钠铵钡碱可溶;
钾钠铵盐硝酸盐,全都溶于水中间;
硫酸盐中钡不溶,氯化盐中银不溶;
碳酸除镁是微溶,其他全都不能溶。
(氢氧化钙是微溶,硫酸钙银是微溶。)
4、物质的溶解性
能
有水生成
不能
能
能
无气体、沉淀、水生成
有气体生成
有沉淀生成
1、根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液是否能发生反应。
练一练
名称 NaOH溶液 NaCl溶液 K2CO3溶液 Ba(NO3)2溶液
稀硫酸
判断依据
练一练
2、根据复分解反应发生的条件,判断下列各组物质不能发生反应的一组是( )
A、Na2CO3溶液和CaCl2溶液 B、NaOH溶液和盐酸溶液
C、CuSO4溶液和BaCl2溶液 D、K2SO4溶液和NaCl溶液
D
大部分溶液都是 色的(例如氯化钠溶液和氢氧化钠溶液等);
含亚铁离子的溶液是 色的(例如 溶液和 溶液等);
含铁离子的溶液是 色的(例如 溶液和 溶液等);
含铜离子的溶液是 色的(例如 溶液和 _________溶液等)。
无
5、溶液的颜色
浅绿
FeSO4
FeCl2
黄
Fe2(SO4)3
Fe(NO3)3
蓝
CuSO4
CuCl2
3、下列离子能在同一溶液中大量共存并且形成无色溶液的是 ( )
A.Zn2+ 、Cu2+ 、Cl?、SO42- B. K+ 、Ba2+ 、NO3- 、Cl?
C.Mg2+ 、 Cl? 、Na+ 、OH- D. K+ 、Na+ 、H+ 、OH-
B
石灰岩的主要成分是碳酸钙。碳酸钙遇到溶有二氧化碳的水时,会慢慢变成可溶于水的碳酸氢钙Ca(HCO3)2
Ca(HCO3)2=CaCO3↓+CO2↑+H2O
当受热或压强突然变小时,水中碳酸氢钙会分解,重新变成碳酸钙沉积下来。
在自然界里不断发生上述反应,石灰岩逐渐变成碳酸氢钙而溶解掉,形成溶洞;碳酸氢钙不断分解,生成的碳酸钙逐渐沉积,形成千姿百态的钟乳石、石笋和石柱。
复分解反应
学习目标
进一步理解酸、碱、盐的基本概念;
能正确判断酸碱盐之间的反应;
理解复分解反应发生的条件。
1
2
3
下面三个反应与我们前面所学的化合、分解、置换三种反应有什么不同?这些反应有什么共同特征?
思考与交流
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
NaHCO3+HCl = NaCl+H2O+CO2↑
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH
由两种化合物互相交换成分,生成另外两种化合物的反应 叫做复分解反应。
2、复分解反应的特点
AB+CD = AD+CB
首尾两交换,各元素的化合价不变。
FeCl3+3NaOH==Fe(OH)3 ↓+3NaCl
酸和碱作用生成盐和水的中和反应是否也属于复分解反应?为什么?
思考与交流
酸+碱→盐+水
是两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应。
HCl+NaOH== NaCl+H2O
3、复分解反应发生的条件
产生蓝色沉淀
产生白色沉淀
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+BaCl2=BaSO4↓+CuCl2
实验11-3
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液。
名称 CuSO4溶液+NaOH溶液 CuSO4溶液+BaCl2溶液
现象
化学方程式
1、上述两个反应是否属于复分解反应?观察到的现象有什么共同之处?
思考与交流
是,都有沉淀生成
2、碳酸钠、碳酸钙等含碳酸根的盐溶液与盐酸
发生复分解反应时,可观察到的共同现象是什么?
都有气体生成
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或水(难电离的物质),复分解反应才可以发生。
生成水
生成气体
生成沉淀
部分酸碱盐的溶解性表 (课本114页)
OH- NO3- Cl- SO42- CO32-
H+ 溶 溶 溶 溶
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 不 不
Ca2+ 微 溶 溶 微 不
Mg2+ 不 溶 溶 溶 微
Al3+ 不 溶 溶 溶 -----
Fe3+ 不 溶 溶 溶 -----
Cu2+ 不 溶 溶 溶 -----
Ag+ ----- 溶 不 微 不
① 常见的酸大多溶于水
② 可溶的碱有:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O
③ 钾盐、钠盐、铵盐、硝酸盐都易溶于水
④ 盐酸盐中只有AgCl不溶于水
⑤ 硫酸盐中只有BaSO4不溶于水
⑥ 碳酸盐大部分不溶于水,除钾、钠、铵盐外
常见的沉淀有八种:
Mg(OH)2、Al(OH)3、Fe(OH)3、Cu(OH)2 、AgCl 、BaSO4、BaCO3、CaCO3
白色
白色
白色
白色
白色
白色
红褐色
蓝色
背记口诀:
常见诸酸皆可溶,钾钠铵钡碱可溶;
钾钠铵盐硝酸盐,全都溶于水中间;
硫酸盐中钡不溶,氯化盐中银不溶;
碳酸除镁是微溶,其他全都不能溶。
(氢氧化钙是微溶,硫酸钙银是微溶。)
4、物质的溶解性
能
有水生成
不能
能
能
无气体、沉淀、水生成
有气体生成
有沉淀生成
1、根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液是否能发生反应。
练一练
名称 NaOH溶液 NaCl溶液 K2CO3溶液 Ba(NO3)2溶液
稀硫酸
判断依据
练一练
2、根据复分解反应发生的条件,判断下列各组物质不能发生反应的一组是( )
A、Na2CO3溶液和CaCl2溶液 B、NaOH溶液和盐酸溶液
C、CuSO4溶液和BaCl2溶液 D、K2SO4溶液和NaCl溶液
D
大部分溶液都是 色的(例如氯化钠溶液和氢氧化钠溶液等);
含亚铁离子的溶液是 色的(例如 溶液和 溶液等);
含铁离子的溶液是 色的(例如 溶液和 溶液等);
含铜离子的溶液是 色的(例如 溶液和 _________溶液等)。
无
5、溶液的颜色
浅绿
FeSO4
FeCl2
黄
Fe2(SO4)3
Fe(NO3)3
蓝
CuSO4
CuCl2
3、下列离子能在同一溶液中大量共存并且形成无色溶液的是 ( )
A.Zn2+ 、Cu2+ 、Cl?、SO42- B. K+ 、Ba2+ 、NO3- 、Cl?
C.Mg2+ 、 Cl? 、Na+ 、OH- D. K+ 、Na+ 、H+ 、OH-
B
石灰岩的主要成分是碳酸钙。碳酸钙遇到溶有二氧化碳的水时,会慢慢变成可溶于水的碳酸氢钙Ca(HCO3)2
Ca(HCO3)2=CaCO3↓+CO2↑+H2O
当受热或压强突然变小时,水中碳酸氢钙会分解,重新变成碳酸钙沉积下来。
在自然界里不断发生上述反应,石灰岩逐渐变成碳酸氢钙而溶解掉,形成溶洞;碳酸氢钙不断分解,生成的碳酸钙逐渐沉积,形成千姿百态的钟乳石、石笋和石柱。
复分解反应
同课章节目录
