沪教版(上海)初中化学九年级第二学期第六单元 常用的金属和盐检测题(含答案)
文档属性
| 名称 | 沪教版(上海)初中化学九年级第二学期第六单元 常用的金属和盐检测题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 144.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-10 00:00:00 | ||
图片预览

文档简介
《常用的金属和盐》检测题
一、单选题
1.下列各组溶液中,必须另加试剂才能鉴别开来的一组是
A.NaOH、FeCl3、MgSO4、NaCl B.KOH、HCl、CuSO4、KNO3
C.Na2CO3 、BaCl2、HCl、KCl D.Na2CO3、KNO3、NaCl、CaCl2
2.AlCl3溶液中逐滴加入NaOH溶液,开始时生成Al(OH)3白色沉淀,当NaOH溶液加至一定时,由于发生反应Al(OH)3+NaOH=NaAlO2+2H2O,而使白色沉淀逐渐减少,直至全部溶解。则下列图像能正确表示上述变化情况的是(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成的Al(OH)3沉淀的质量)
A.B.C.D.
3.下列实验方法错误的是
A.除去氯化银中的氯化钠,加足量的水溶解、过滤、洗涤、干燥
B.除去氯化钾中的碳酸钾,加足量的稀盐酸、蒸发结晶
C.鉴别硝酸铵和氯化钠,分别加适量的水,用手触摸容器壁
D.鉴别CO2和SO2,将气体分别通入紫色石蕊溶液中,观察颜色变化
4.下列试剂中,不能鉴别氯化钠溶液和碳酸钠溶液的是( )
A.硫酸钾溶液 B.氢氧化钡溶液 C.硝酸钙溶液 D.稀硫酸
5.某化学反应可表示为M+酸→N+盐,其中M、N的物质类别不可能是
A.碱、氧化物 B.单质、单质 C.氧化物、酸 D.盐、酸
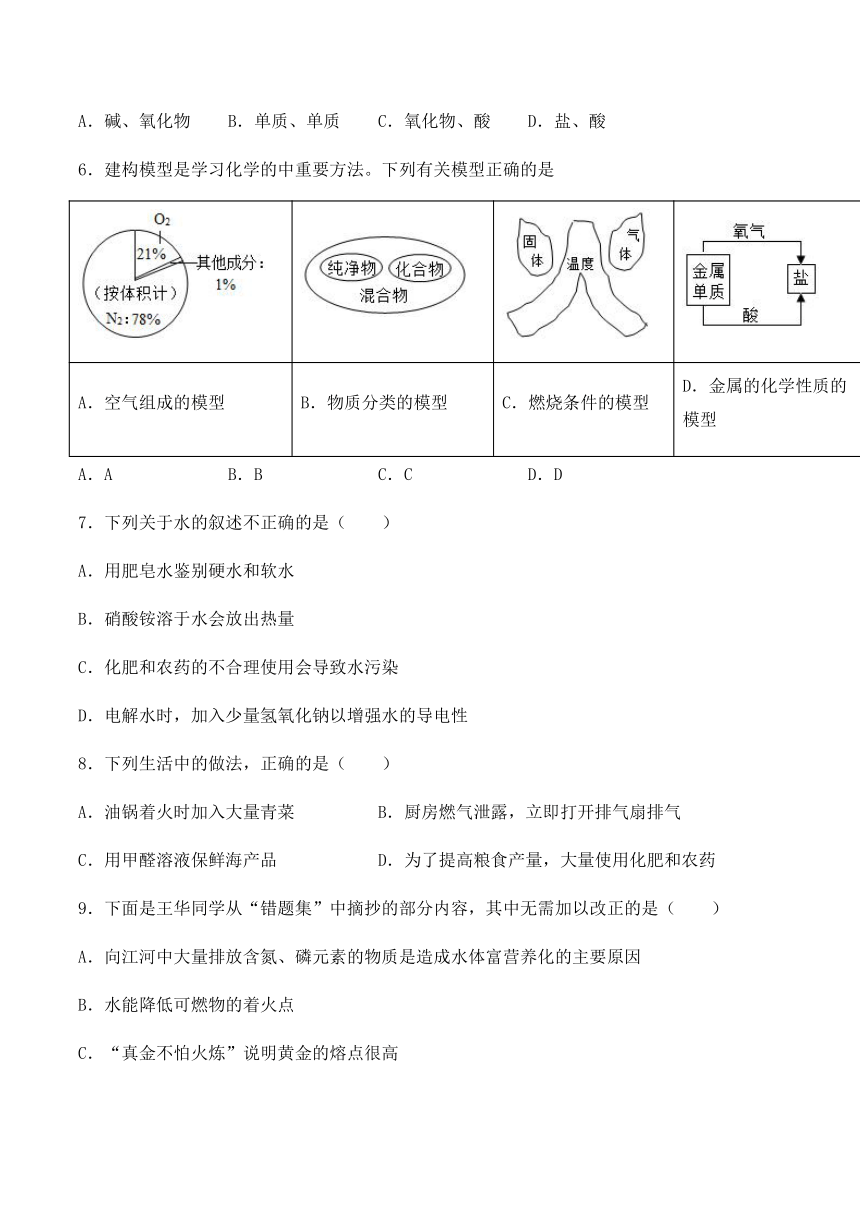
6.建构模型是学习化学的中重要方法。下列有关模型正确的是
A.空气组成的模型 B.物质分类的模型 C.燃烧条件的模型 D.金属的化学性质的模型
A.A B.B C.C D.D
7.下列关于水的叙述不正确的是( )
A.用肥皂水鉴别硬水和软水
B.硝酸铵溶于水会放出热量
C.化肥和农药的不合理使用会导致水污染
D.电解水时,加入少量氢氧化钠以增强水的导电性
8.下列生活中的做法,正确的是( )
A.油锅着火时加入大量青菜 B.厨房燃气泄露,立即打开排气扇排气
C.用甲醛溶液保鲜海产品 D.为了提高粮食产量,大量使用化肥和农药
9.下面是王华同学从“错题集”中摘抄的部分内容,其中无需加以改正的是( )
A.向江河中大量排放含氮、磷元素的物质是造成水体富营养化的主要原因
B.水能降低可燃物的着火点
C.“真金不怕火炼”说明黄金的熔点很高
D.3Fe3+表示3个亚铁离子
10.下列化肥中,属于钾肥的是
A.KCl B.NH4NO3 C.NH4Cl D.Ca(H2PO4)2
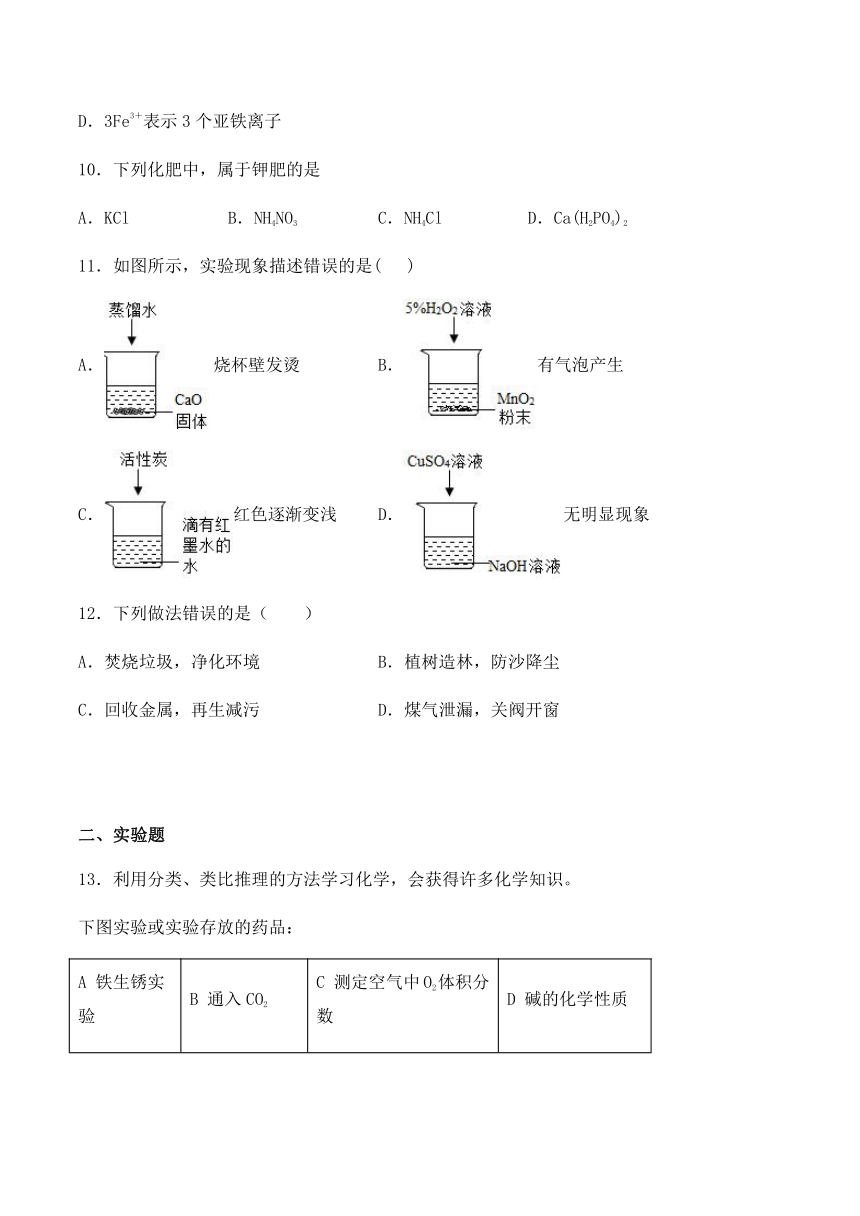
11.如图所示,实验现象描述错误的是( )
A.烧杯壁发烫 B.有气泡产生
C.红色逐渐变浅 D.无明显现象
12.下列做法错误的是( )
A.焚烧垃圾,净化环境 B.植树造林,防沙降尘
C.回收金属,再生减污 D.煤气泄漏,关阀开窗
二、实验题
13.利用分类、类比推理的方法学习化学,会获得许多化学知识。
下图实验或实验存放的药品:
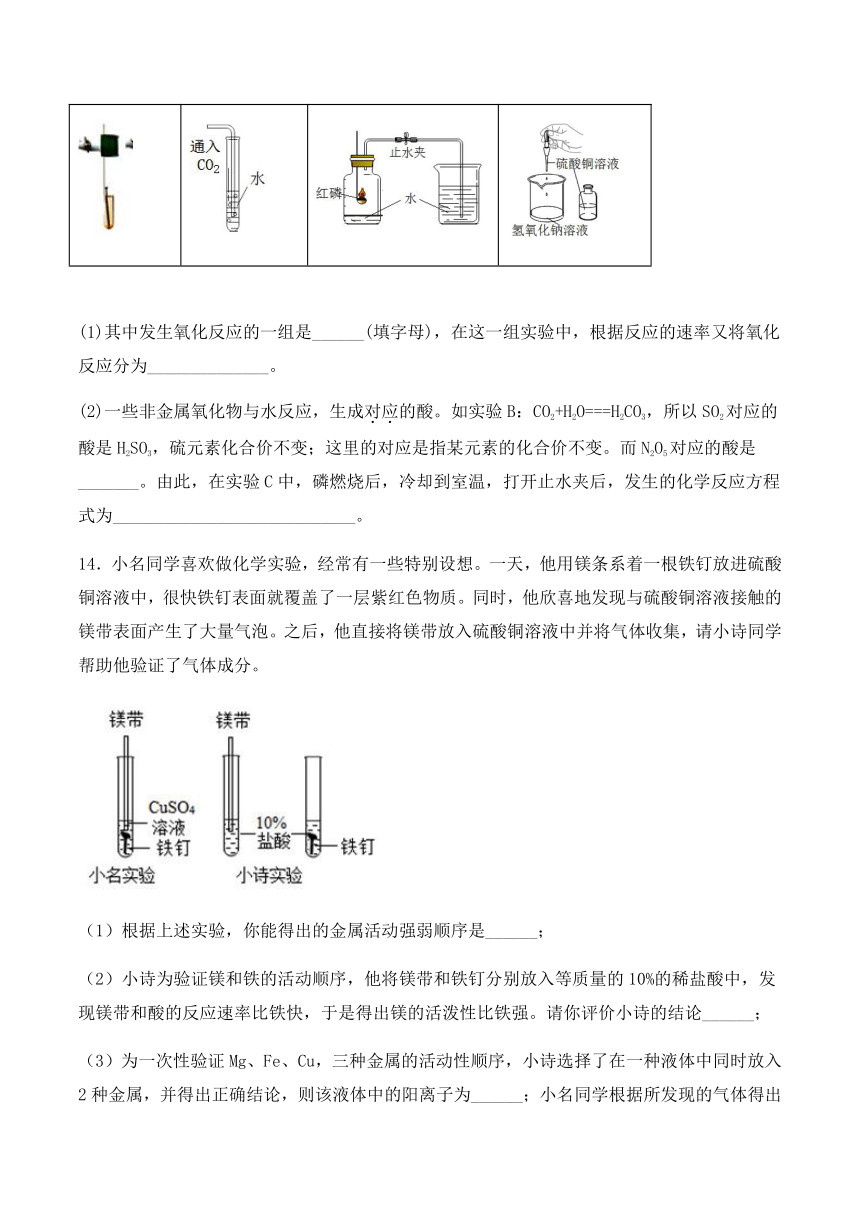
A 铁生锈实验 B 通入CO2 C 测定空气中O2体积分数 D 碱的化学性质
(1)其中发生氧化反应的一组是______(填字母),在这一组实验中,根据反应的速率又将氧化反应分为______________。
(2)一些非金属氧化物与水反应,生成对应的酸。如实验B:CO2+H2O===H2CO3,所以SO2对应的酸是H2SO3,硫元素化合价不变;这里的对应是指某元素的化合价不变。而N2O5对应的酸是_______。由此,在实验C中,磷燃烧后,冷却到室温,打开止水夹后,发生的化学反应方程式为____________________________。
14.小名同学喜欢做化学实验,经常有一些特别设想。一天,他用镁条系着一根铁钉放进硫酸铜溶液中,很快铁钉表面就覆盖了一层紫红色物质。同时,他欣喜地发现与硫酸铜溶液接触的镁带表面产生了大量气泡。之后,他直接将镁带放入硫酸铜溶液中并将气体收集,请小诗同学帮助他验证了气体成分。
(1)根据上述实验,你能得出的金属活动强弱顺序是______;
(2)小诗为验证镁和铁的活动顺序,他将镁带和铁钉分别放入等质量的10%的稀盐酸中,发现镁带和酸的反应速率比铁快,于是得出镁的活泼性比铁强。请你评价小诗的结论______;
(3)为一次性验证Mg、Fe、Cu,三种金属的活动性顺序,小诗选择了在一种液体中同时放入2种金属,并得出正确结论,则该液体中的阳离子为______;小名同学根据所发现的气体得出硫酸铜溶液显酸性的结论,则该气体名称为______;反思:验证金属活动顺序最好选用______方法,这样可以避免客观因素带来的弊端。
三、推断题
15.已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质。其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色,I是地壳中含量最高的元素所形成的常见气体单质,人体胃液中含有A,可以帮助消化。根据图所示转化关系,回答下列问题。(图中反应条件均已略去,反应物和生成物均已给出)
(1)E的名称是 ,H的化学式是 。
(2)写出反应的化学方程式: 。
(3)上图中涉及到 基本反应类型。
A.一种 B.二种 C.三种 D.四种
16.构建知识网络是一种重 要的学习方法。已知A、B、C、D、E分别是稀盐酸、碳酸钙、铁、氧化铁和二氧化碳中的一种,其中D是红棕色的固体,它们之间的关系如图所示,“一”表示两端的物质在一定条件 下可以反应,“→” 表示一种物 质生成另一种物 质(部分反应物、生成物及反应条件省略)。依据题意请回答下列问题:
(1)写出A的化学式:_____,
(2)写出物质E的一种用途_____,
(3)写出D→B的化学方程式 :_____,
(4)写出E-→C的化学方程式:_____。
17.A~G 为常见的物质,其中 B、E、G 属于单质,D、E 为红色固体,反应②是炼铁工业中的主要反应,下图是它们之间相互转化关系。请回答:
(1)F 物质的化学式是:F_____;
(2)C 物质固态时的名称是_____;
(3)G 和A 在加热时的化学方程式为______, 该反应属于_____(基本反应类型)。
四、计算题
18.某课外活动小组为测定一包碳酸钠样品的质量分数,取来了一些样品,准确称取样品10g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应),向其中加入足量的稀盐酸,根据实验测得的数据绘制出所加稀盐酸的质量和放出的CO2的质量关系图。
(1)10g样品可以产生_____克二氧化碳。
(2)该样品中碳酸钠的质量分数是_____。
(3)加入稀盐酸到恰好完全反应时,所得的溶液中溶质的质量分数是多少?_____(写出计算过程)
19.取锌、铜的混合物8g与154.7g稀硫酸恰好完全反应,称得剩余物质的总质量为162.5g。请计算:
(1)产生氢气的质量是多少?
(2)混合物中铜的质量是多少?
20.小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75g的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表。求:
实验 第一次 第二次 第三次
加入稀盐酸的量/g 25 25 25
生成气体的质量/g 2 m 0.4
(1)m的值是_______________g
(2)求该样品中碳酸钙的质量分数为_______(保留一位小数)。
参考答案
1.D 2.B 3.D 4.A 5.C 6.A 7.B 8.A 9.A 10.A 11.D 12.A
13.AC 剧烈的氧化(反应)缓慢的氧化(反应) HNO3 P2O5+3H2O==2H3PO4
14.铁比铜活泼 不正确,没有控制镁和铁与酸反应的接触面积,所以无法比较铁与镁的活动性强弱 Fe2+ 氢气 金属与盐溶液反应
15.(1)铁;H2O2(2)CuCl2+Fe=FeCl2+Cu(3)C
16.HCl 灭火(合理即可) (合理即可)
17.FeCl2 干冰 H2 + CuO=Cu+H2O 置换反应
18.2.2 53% 5.85%
19.(1)0.2g(2)1.5g
20.2 66.7%
