京改版(2013)初中化学九年级下册第10章《金属》检测题(含答案)
文档属性
| 名称 | 京改版(2013)初中化学九年级下册第10章《金属》检测题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 215.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-10 00:00:00 | ||
图片预览



文档简介
《金属》检测题
一、单选题
1.如图表示汽车尾气净化器处理尾气的过程,其主要反应原理为:2NO+2CO2CO2+N2,下列有关叙述错误的是( )
A.CO氧化为CO2所需的氧来源于NO
B.该反应是置换反应
C.Pt﹣Rh催化加在化学反应前后质量不变
D.使用该净化器能减少酸雨的发生
2.某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生下列说法正确的是( )
A.滤渣中一定含有银和铁,可能含有锌
B.滤渣中一定含有银,可能含有锌和铁
C.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
D.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
3.往200g和的混合溶液中加入铁粉。已知反应的先后顺序和化学方程式分别为: 。如图为加入铁粉的质量与反应后剩余固体质量关系。则下列说法不正确的是( )
A.B点后溶液的颜色为蓝色
B.D点对应纵坐标为6.4
C.该200g溶液中的质量分数为6.75%
D.取D、E两点间的剩余固体加入盐酸,均有气泡产生
4.下图是某化学反应的微观示意图,下列说法中错误的是
A.该反应属于置换反应 B.反应中甲、乙的质量比为17﹕32
C.反应前后原子种类、数目均不变 D.反应物中只有一种元素的化合价不变
5.在AgNO3、Zn(NO3)2和Cu(NO3)2的混合溶液中加人一定量的铁粉,充分反应后过滤.向滤渣中加入稀盐酸,有气泡产生.根据上述现象,下列结论正确的是
A.滤渣中一定有Zn B.滤渣中可能有Ag、Cu
C.滤液中﹣定有Fe(NO3)2、Zn(NO3)2 D.滤液中可能有AgNO3、Cu(NO3)2
6.下列指定反应的化学方程式正确的是
A.镁条在氧气中燃烧:2Mg+O2=2MgO
B.铁丝放入稀盐酸中:2Fe+6HCl=2FeCl3+3H2↑
C.铜丝放入硝酸银溶液中:Cu+AgNO3=Ag+Cu(NO3)2
D.高锰酸钾受热分解:2KMnO4K2MnO4+MnO2+O2↑
7.类推是学习化学的一种重要方法,下列说法中,正确的是
A.离子是带电的粒子,带电的粒子都是离子
B.点燃氢气前需要验纯,点燃任何可燃性气体前都需要验纯
C.铁在潮湿的空气中易锈蚀,金属在湖湿的空气中均易锈蚀
D.燃烧过程中伴随着发光、放热现象,有发光、放热现象的变化都是燃烧
8.将一根铁丝放入一定量的稀硫酸溶液中,恰好完全反应,反应后所得溶液中的溶质是( )
A.铁丝 B.硫酸 C.硫酸铁 D.硫酸亚铁
9.小敏同学的化学复习笔记本上有如下记录,你认为不正确的是
A.从溶解度曲线可以知道一定温度下某个物质的溶解度
B.从金属活动性顺序表可以知道金属活泼性的强弱
C.一定温度下,向溶液中加入溶质都会使其浓度增大
D.配平化学方程式的依据是质量守恒定律
10.某反应的微观示意图如图,有关说法正确的是( )
A.该反应属于置换反应 B.氧原子的结构示意图为
C.b,d两种物质均由分子构成 D.a物质中氮元素的化合价为+3价
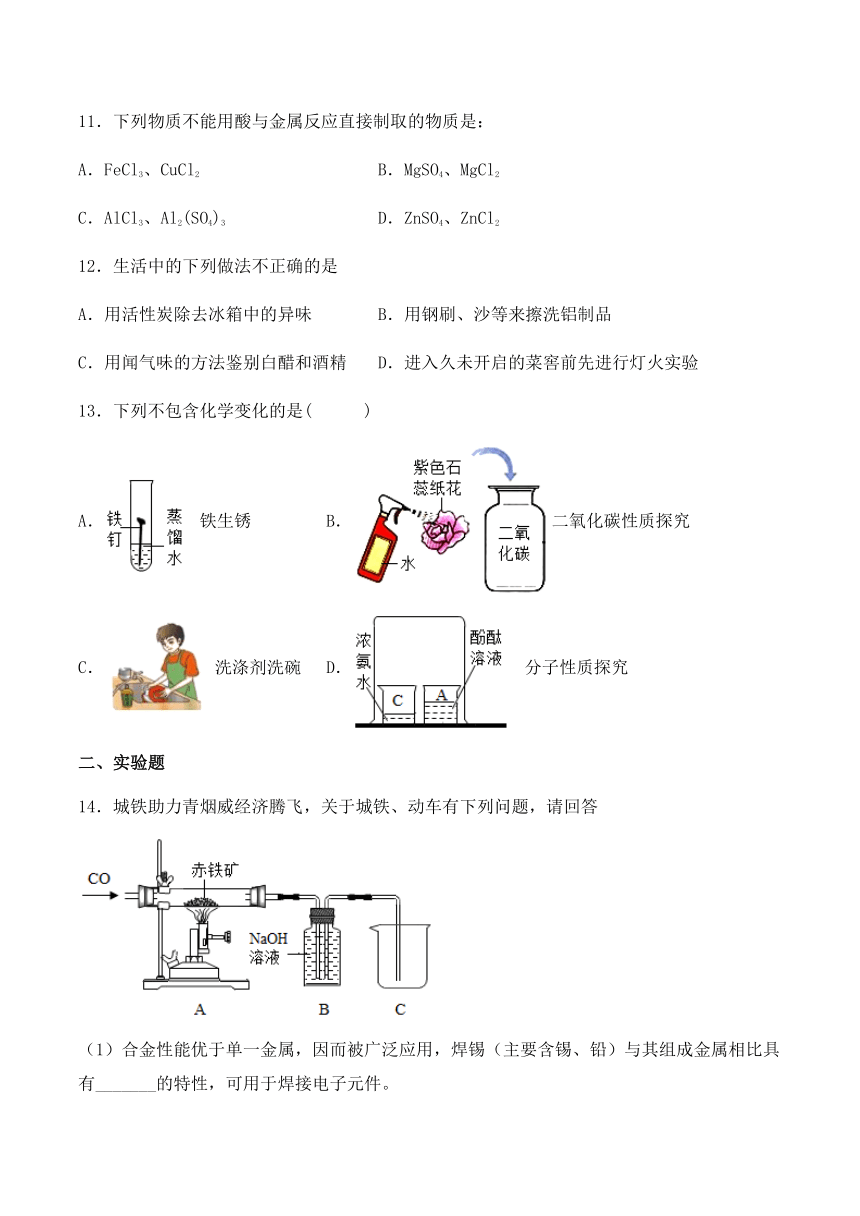
11.下列物质不能用酸与金属反应直接制取的物质是:
A.FeCl3、CuCl2 B.MgSO4、MgCl2
C.AlCl3、Al2(SO4)3 D.ZnSO4、ZnCl2
12.生活中的下列做法不正确的是
A.用活性炭除去冰箱中的异味 B.用钢刷、沙等来擦洗铝制品
C.用闻气味的方法鉴别白醋和酒精 D.进入久未开启的菜窖前先进行灯火实验
13.下列不包含化学变化的是( )
A.铁生锈 B.二氧化碳性质探究C.洗涤剂洗碗 D.分子性质探究
二、实验题
14.城铁助力青烟威经济腾飞,关于城铁、动车有下列问题,请回答
(1)合金性能优于单一金属,因而被广泛应用,焊锡(主要含锡、铅)与其组成金属相比具有_______的特性,可用于焊接电子元件。
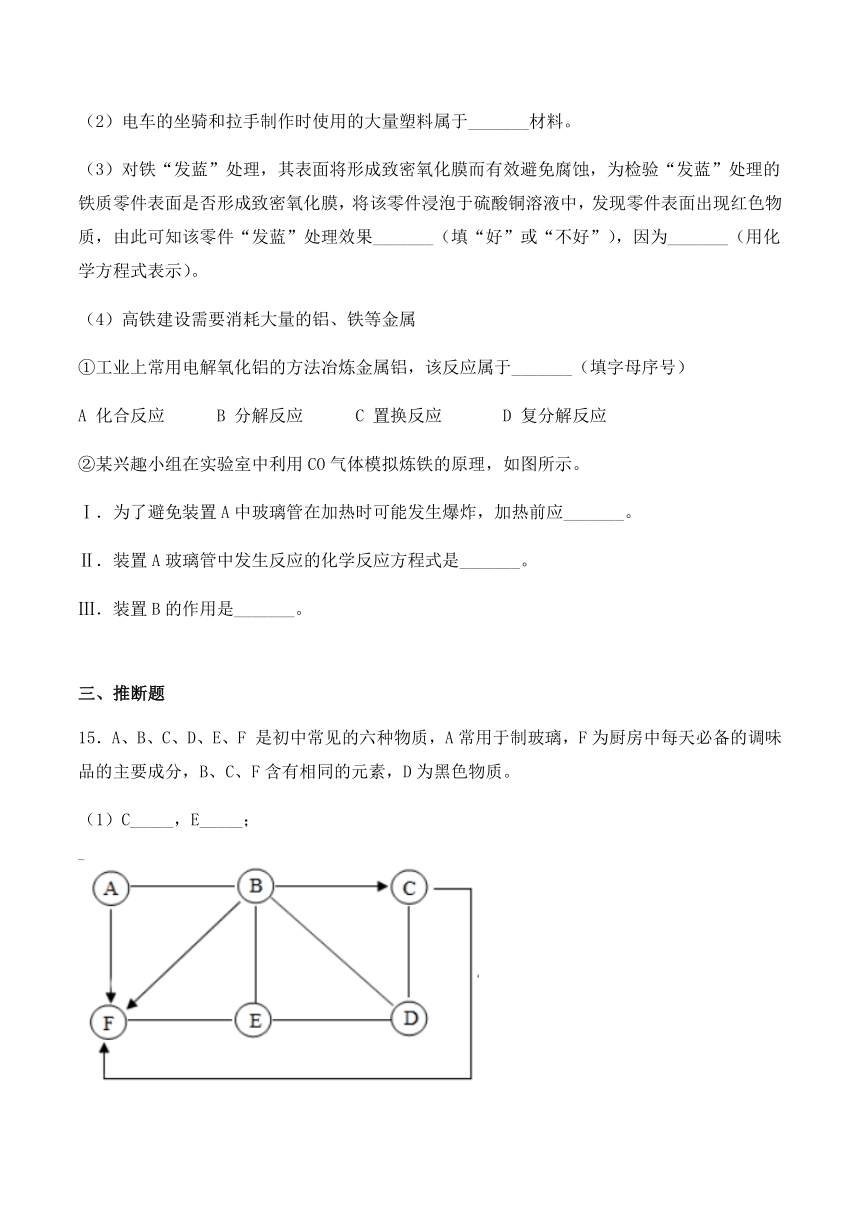
(2)电车的坐骑和拉手制作时使用的大量塑料属于_______材料。
(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀,为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知该零件“发蓝”处理效果_______(填“好”或“不好”),因为_______(用化学方程式表示)。
(4)高铁建设需要消耗大量的铝、铁等金属
①工业上常用电解氧化铝的方法冶炼金属铝,该反应属于_______(填字母序号)
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
②某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如图所示。
Ⅰ.为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应_______。
Ⅱ.装置A玻璃管中发生反应的化学反应方程式是_______。
Ⅲ.装置B的作用是_______。
三、推断题
15.A、B、C、D、E、F 是初中常见的六种物质,A常用于制玻璃,F为厨房中每天必备的调味品的主要成分,B、C、F含有相同的元素,D为黑色物质。
(1)C_____,E_____;
(2)B转化为C的实验现象:_____;
(3)E与D反应的化学方程式:_____;
(4)把两种能反应的物质用“﹣﹣”补全_____
16.已知A—— H均为初中化学常见的物质。其中A、C常温下是气体,且组成元素相同,B是赤铁矿的主要成分,E能用于改良酸性土壤,H是紫红色单质,F含有两种元素。他们的相互转化关系如图所示(图中反应条件均已略去)。请回答下列问题:
(1)写出E物质的俗称______________。
(2)反应③所属的基本类型是______________。
(3)写出反应①的化学方程式_________________。
(4)F与某物质反应可生成白色沉淀,写出该反应的化学方程式______________。
四、计算题
17.黄铜(铜锌合金)的外观与黄金极为相似、容易以假乱真。小红同学想测定黄铜中锌的含量。她称取20g黄铜样品放入烧杯中,加入足量稀硫酸充分反应后,测得生成氢气的质量为0.2g。
(1)该反应属于____________(填基本反应类型)。
(2)求黄铜样品中锌的质量分数为________(写计算过程)。
18.黄铜是铜锌合金,耐腐蚀,许多金色饰品就是用它来制作的.现称取20.0g黄铜样品置于烧杯中,慢慢加人稀硫酸使其充分反应,直至没有气泡产生为止.请结合下列图示计算.
(1)该20.0g黄铜样品中含锌的质量为_____g.
(2)完全反应时生成气体的质量为_____g.(写出计算过程)
(3)过滤后得到滤液的质量是_____克.
19.用不纯的锌片(杂质不参加反应)与稀硫酸反应,六次实验结果记录如下:(计算结果均取整数)
次数
1
2
3
4
5
6
加入锌的质量(g)
2
4
6
8
10
12
稀硫酸的质量(g)
60
60
60
60
60
60
生成的硫酸锌的质量(g)
5
15
17
17
(1)将第2次和第5次实验产生的硫酸锌的质量填在上表中;
(2)在右图中画出硫酸锌与锌的质量函数关系的曲线;
(3)若将(10+m)g这种锌片放入60g这种稀硫酸中,充分反应后剩余固体的质量为 g;
(4)该实验所使用的稀硫酸中溶质的质量分数为 .
参考答案
1.B 2.A 3.A 4.B 5.C 6.D 7.B 8.D 9.C 10.C 11.A 12.B 13.C
14.熔点低 有机合成 不好 Fe+CuSO4=FeSO4+Cu B 先通入一氧化碳 3CO+Fe2O32Fe+3CO2 吸收二氧化碳,收集未反应的一氧化碳。
15.CuCl2, AgNO3; 黑色固体逐渐溶解,溶液由无色变成蓝色; ;
16.熟石灰 置换反应 3CO+Fe2O32Fe+3CO2
17. 置换反应 32.5%
18.6.5 0.2 86.3
19.(1)10,17;(2)
;
(3)3+m;(4)l7%.
