人教版必修2高中化学3.1《最简单的有机化合物——甲烷》(61张ppt)
文档属性
| 名称 | 人教版必修2高中化学3.1《最简单的有机化合物——甲烷》(61张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-11 00:00:00 | ||
图片预览










文档简介
(共61张PPT)
欢迎进入有机物的世界
什么是有机化合物呢?
与我们过去所学化合物有什么区别?
有机化合物含有哪些元素呢?
思考
一、有机化合物
1.有机物
一般把含碳元素的化合物称为有机化合物,简称为有机物
2、组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
3、注意:
碳单质、碳的氧化物、碳酸、碳酸盐、 碳的金属化合物等看作无机物。
二、烃:
其中仅含碳和氢两种元素的有机物,或称为碳氢化合物。
碳
tàn
氢
qīng
烃
tīng
下列物质属于烃的是:H2S、C2H2、CH3Cl、C2H5OH、CH4、H2、金刚石、 CH3COOH、CO2、C2H4
小试牛刀
西气东输工程
第一节 最简单的有机化合物——甲烷
甲烷
一、在自然界存在:
沼气、油田气、煤矿坑道气、天然气、可燃冰等
甲烷是池沼底部产生的沼气和煤矿的坑道所产生的气体的主要成分。这些甲烷都是在隔绝空气的情况下,由植物残体经过微生物发酵的作用而生成的。
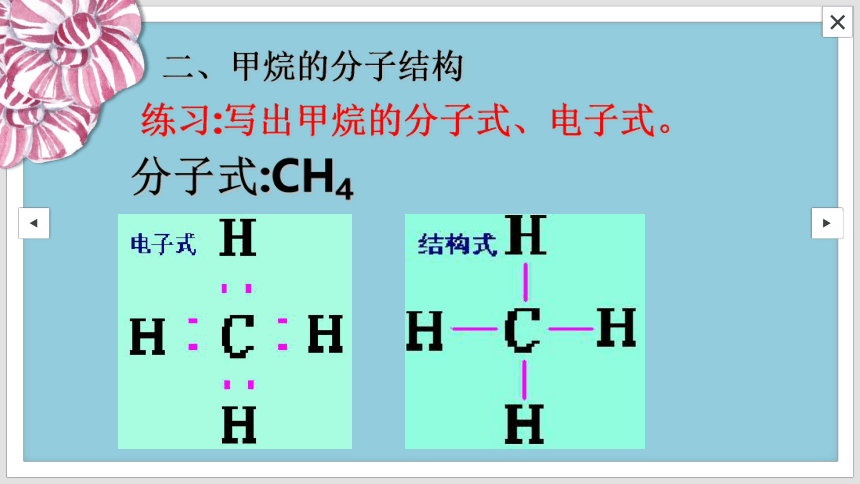
二、甲烷的分子结构
练习:写出甲烷的分子式、电子式。
分子式:CH4
实验测得,甲烷分子中4个C-H键完全相同,每两个C-H键之间的键角、键长、键能均相等,其中,键角为109028/
正四面体
球棍模型
比例模型
实际上:甲烷真实构型是正四面体
甲烷空间构型:对称的正四面结构
结构特点:4个C-H键是等价的
C原子位于中心,四个H原子位于正四面体的四个顶点。
但由于有机物的立体结构式书写起来比较费事,为方便起见,一般采用平面的结构式来表示。
三、甲烷的物理性质
无色、无味的气体
?=0.717g/L(标准状况)
极难溶于水
俗名:沼气、坑气,是天然气的主要成分
向下排空气法
排水法
四、甲烷的化学性质
1、稳定性:
通常情况下,甲烷比较稳定,与强酸、强碱、强氧化剂(三强)不发生化学反应。
不褪色
甲烷不能使酸性高锰酸钾褪色
实验视频
2、氧化反应:
强调:甲烷与空气或氧气的
混合气体点燃时,发生爆炸。
因此,在点燃甲烷气体时,
必须先进行纯度检验。
现象:
安静燃烧,淡蓝色火焰,产生使澄清石灰水变浑浊的气体,放出大量的热。
有机反应不用“ ”,而用“→”
实验视频
3、探究实验
实验视频
光照
混合气体无光照时,不发生反应;
光照时,Cl2的黄绿色变浅,试管壁上出现油状液滴,试管内的液面上升。
1、试管内Cl2的黄绿色变浅说明在光照的条件下发生了化学反应。
2、试管壁上出现液滴,说明反应中生成了新的油状物质,且不溶与水。
3、试管内液面上升,说明随着反应的进行,试管内的气压在减小,即气体总体积在减小。
现象
结论
现象与结论:
H C H
H
H
+ Cl Cl
光照
H C Cl
H
H
+ HCl
一氯甲烷(气)
有机物分子里的某些原子或原子团被其它原子或原子团所替代的反应叫做取代反应。
取代反应:
你能仿照上述化学方程式,尝试写出一氯甲烷与氯气进一步反应的化学方程式吗?
H C H
H
Cl
+ Cl Cl
光照
H C Cl
H
Cl
+ HCl
二氯甲烷(液)
Cl C H
H
Cl
+ Cl Cl
光照
Cl C Cl
H
Cl
+ HCl
三氯甲烷(液)
氯仿(有机溶剂)
Cl C H
Cl
Cl
+ Cl Cl
光照
Cl C Cl
Cl
Cl
+ HCl
四氯甲烷(液)
有机溶剂、灭火剂
*甲烷与氯气的反应,共得到五种产物,其中一氯甲烷和氯化氢为气态,其余为液态。氯化氢易溶于水,其余难溶于水。
特别提醒: 当n(CH4)∶n( Cl2)=1∶1时,反应并不只发生
CH4+Cl2 CH3Cl+HCl,其他反应仍同时发生,产物为混合物。
光照
甲烷与氯气反应的化学方程式:
(一氯甲烷,气态)
(二氯甲烷,液态)
(三氯甲烷,液态,又叫氯仿,曾用作麻醉剂)
(四氯甲烷,液态,又叫四氯化碳,常作溶剂)
取代反应与置换反应的区别?
想一想?
置换反应 取代反应
反应物
生成物
反应
条件
反应
程度
(1)反应物中一定有单质
(2)反应物一般是无机物
生成物中一定有单质
大多在溶液中进行,
一般反应较快
反应单向进行,不可逆
(1)反应物中不一定有单质
(2)反应物中至少有一种有机物
生成物中不一定有单质
受外界条件影响较大,
反应进行较慢
反应逐步进行,可逆
1、下列物质中属于有机物的是:
A、二氧化碳 B、尿素
C、蔗糖 D、碳酸氢铵
BC
练习
2、光照下,甲烷与氯气发生取代反应后,共得产物
A、5种 B、2种
C、3种 D、 4种
练习
A
3、光照下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是:
A、CH3Cl B、CH2Cl2
C、CHCl3 D、CCl4 E、HCl
E
练习
练习
C
4、将1mol甲烷和4mol的氯气发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗氯气为:
A.0.5mol B.2mol
C.2.5mol D.4mol
五、甲烷的用途:
除作燃料外,大量用于合成氨、尿素和炭黑,还可用于生产甲醇、氢气、乙炔、乙烯、甲醛、氢氰酸等。
【小结】甲烷的化学性质
1、稳定性:
2、氧化反应—
3、取代反应(特征反应)
现象:
反应条件:
特点:
不与强酸、强碱、酸性KMnO4溶液反应
燃烧
光照,与气态纯卤素反应 (与氯水、溴水不反应)
逐步取代(随机并行),产物为混合物
Thank you!
【回顾】甲烷的化学性质
1、稳定性:
2、氧化反应—
3、取代反应(特征反应)
现象:
反应条件:
特点:
不与强酸、强碱、酸性KMnO4溶液反应
燃烧
光照,与气态纯卤素反应 (与氯水、溴水不反应)
逐步取代(随机并行),产物为混合物
与甲烷结构相似的有机物还有很多,请你观察下列有机物的结构,试归纳出它们在结构上的特点。
学与问
H H H H H
| | | | |
H-C-C-H H-C-C-C-H
| | | | |
H H H H H
乙烷
丙烷
H H H H
| | | |
H-C-C-C-C-H
| | | |
H H H H
丁烷
只含C、H两种元素,每个碳以四个单键与其它原子相结合。
相同点
C、H原子数不同
不同点
一、烷烃
在烃的分子里,碳原子之间都以碳碳单键结合成链状,碳原子剩余的价键全部跟氢原子相结合,使每个碳原子的化合价都已充分利用,都达到“饱和”。这样的烃叫做饱和烃,又叫烷烃。
1、定义:
请大家用数学归纳法导出烷烃的分子式通式
思考
链状烷烃
CnH2n+2
环烷烃
CnH2n
例: H H H H H
| | | | |
H—C—C—C—C—C—H
| | | |
H H H H
H—C—H
|
H
2、结构简式:
或者:
CH3 CH(CH3)CH2 CH2 CH3
CH3—CH—CH2—CH2—CH3
CH3
CH3CHCH2CH2CH3
CH3
省略横线上C—C键
省略C—H键
把同一C上的H合并
乙烷: H H 丙烷: H H H
| | | | |
H-C-C-H H-C-C-C-H
| | | | |
H H H H H
如:下列结构式对应的结构简式
CH3CH3
CH3CH2CH3
丁烷: H H H H 异丁烷: H
| | | | |
H-C-C-C-C-H H--C--H
| | | | H H
H H H H | |
H-C——C——C-H
| | |
H H H
如:下列结构式对应的结构简式
CH3CH2CH2CH3
CH3CH(CH3 )CH3
◆以碳原子个数为基础命名
◆称“某烷”或“环某烷”
◆十个以下用“天干地支”命名:甲、乙、丙、丁、戊、己、庚、辛、壬、癸。
◆十以上用中文数字表示:十一烷、二十烷、三十五烷等。
3、烷烃的简单命名:
4、性质
(1)物理性质
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
物理性质(随分子中碳原子数增加)
规律:
状态:气(1~4)?液?固;熔沸点依次升高
密度:密度逐渐增大且均比水小
水溶性:均不溶于水
(2)化学性质(与CH4相似)
①氧化反应
具有可燃性
燃烧通式:
CnH2n+2+(3n+1)/2O2 nCO2+(n+1)H2O
②稳定性
均不能使酸性KMnO4或溴水褪色,不与强酸,强碱反应。
在光照条件下进行,产物更复杂
③取代反应
Thank you!
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
分析表3-1 相邻两个烷烃结构和分子组成上有什么联系?
表3-1几种烷烃的物理性质
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
表3-1几种烷烃的物理性质
相差一个“CH2”原子团
结构相似,在分子组成上相差一个或若干
个CH2原子团的物质互称为同系物。
同系物
碳碳原子间都以单键结合;碳原子均饱合;链状。
碳原子数不同,即碳链的长短不同。
烷烃同系物
结构相似:
分子组成:
理解
1、是否属于同类物质?
2、通式相同吗?
3、碳原子数目相同吗?
4、相对分子质量相差多少?
5、性质相同吗?
结论:属于同类物质
通式相同
碳原子数目不同
相对分子质量相差14n
物性不同,化性相似
同系物间的关系
小结
CH3CH2CH2CH3
CH3CHCH3
CH3
观察:两者结构有何异同?
同分异构现象、同分异构体:
化合物具有相同的分子式,但具有不同结构式的现象叫同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
1、定义:
同位素、同素异形体、同系物、同分异构体概念的比较
概念 内 涵 比较对象 实例
同位素
同素异形体
同系物
同分异构体
质子数等,中子数
不等,原子之间
原子
氕、氘、氚
同一元素 形成的不同单质
单质
O2、O3
结构相似,组成上差一个或n个CH2
化合物
C2H6、C4H10
相同分子式,不
同结构的化合物
化合物
CH3(CH2)3CH3
C(CH3)4
图3-6 4个碳原子相互结合的几种方式
思考与交流
参考图3-6,分析、归纳以碳为骨架的有机物种类繁多的原因。
有机物种类繁多的原因:
(1)碳原子含有4个价电子,可跟其它原子形成4个共价键
(2)碳原子易跟多种原子形成共价键;碳原子间易形成单键、双键、叁键、碳链、碳环等多种复杂的结构单元。
C
H
H
H
H
C
C
C
C
C
C
C
C
C
C
C
C
:
:
H
H
H
..
C
..
H
Thank you!
欢迎进入有机物的世界
什么是有机化合物呢?
与我们过去所学化合物有什么区别?
有机化合物含有哪些元素呢?
思考
一、有机化合物
1.有机物
一般把含碳元素的化合物称为有机化合物,简称为有机物
2、组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
3、注意:
碳单质、碳的氧化物、碳酸、碳酸盐、 碳的金属化合物等看作无机物。
二、烃:
其中仅含碳和氢两种元素的有机物,或称为碳氢化合物。
碳
tàn
氢
qīng
烃
tīng
下列物质属于烃的是:H2S、C2H2、CH3Cl、C2H5OH、CH4、H2、金刚石、 CH3COOH、CO2、C2H4
小试牛刀
西气东输工程
第一节 最简单的有机化合物——甲烷
甲烷
一、在自然界存在:
沼气、油田气、煤矿坑道气、天然气、可燃冰等
甲烷是池沼底部产生的沼气和煤矿的坑道所产生的气体的主要成分。这些甲烷都是在隔绝空气的情况下,由植物残体经过微生物发酵的作用而生成的。
二、甲烷的分子结构
练习:写出甲烷的分子式、电子式。
分子式:CH4
实验测得,甲烷分子中4个C-H键完全相同,每两个C-H键之间的键角、键长、键能均相等,其中,键角为109028/
正四面体
球棍模型
比例模型
实际上:甲烷真实构型是正四面体
甲烷空间构型:对称的正四面结构
结构特点:4个C-H键是等价的
C原子位于中心,四个H原子位于正四面体的四个顶点。
但由于有机物的立体结构式书写起来比较费事,为方便起见,一般采用平面的结构式来表示。
三、甲烷的物理性质
无色、无味的气体
?=0.717g/L(标准状况)
极难溶于水
俗名:沼气、坑气,是天然气的主要成分
向下排空气法
排水法
四、甲烷的化学性质
1、稳定性:
通常情况下,甲烷比较稳定,与强酸、强碱、强氧化剂(三强)不发生化学反应。
不褪色
甲烷不能使酸性高锰酸钾褪色
实验视频
2、氧化反应:
强调:甲烷与空气或氧气的
混合气体点燃时,发生爆炸。
因此,在点燃甲烷气体时,
必须先进行纯度检验。
现象:
安静燃烧,淡蓝色火焰,产生使澄清石灰水变浑浊的气体,放出大量的热。
有机反应不用“ ”,而用“→”
实验视频
3、探究实验
实验视频
光照
混合气体无光照时,不发生反应;
光照时,Cl2的黄绿色变浅,试管壁上出现油状液滴,试管内的液面上升。
1、试管内Cl2的黄绿色变浅说明在光照的条件下发生了化学反应。
2、试管壁上出现液滴,说明反应中生成了新的油状物质,且不溶与水。
3、试管内液面上升,说明随着反应的进行,试管内的气压在减小,即气体总体积在减小。
现象
结论
现象与结论:
H C H
H
H
+ Cl Cl
光照
H C Cl
H
H
+ HCl
一氯甲烷(气)
有机物分子里的某些原子或原子团被其它原子或原子团所替代的反应叫做取代反应。
取代反应:
你能仿照上述化学方程式,尝试写出一氯甲烷与氯气进一步反应的化学方程式吗?
H C H
H
Cl
+ Cl Cl
光照
H C Cl
H
Cl
+ HCl
二氯甲烷(液)
Cl C H
H
Cl
+ Cl Cl
光照
Cl C Cl
H
Cl
+ HCl
三氯甲烷(液)
氯仿(有机溶剂)
Cl C H
Cl
Cl
+ Cl Cl
光照
Cl C Cl
Cl
Cl
+ HCl
四氯甲烷(液)
有机溶剂、灭火剂
*甲烷与氯气的反应,共得到五种产物,其中一氯甲烷和氯化氢为气态,其余为液态。氯化氢易溶于水,其余难溶于水。
特别提醒: 当n(CH4)∶n( Cl2)=1∶1时,反应并不只发生
CH4+Cl2 CH3Cl+HCl,其他反应仍同时发生,产物为混合物。
光照
甲烷与氯气反应的化学方程式:
(一氯甲烷,气态)
(二氯甲烷,液态)
(三氯甲烷,液态,又叫氯仿,曾用作麻醉剂)
(四氯甲烷,液态,又叫四氯化碳,常作溶剂)
取代反应与置换反应的区别?
想一想?
置换反应 取代反应
反应物
生成物
反应
条件
反应
程度
(1)反应物中一定有单质
(2)反应物一般是无机物
生成物中一定有单质
大多在溶液中进行,
一般反应较快
反应单向进行,不可逆
(1)反应物中不一定有单质
(2)反应物中至少有一种有机物
生成物中不一定有单质
受外界条件影响较大,
反应进行较慢
反应逐步进行,可逆
1、下列物质中属于有机物的是:
A、二氧化碳 B、尿素
C、蔗糖 D、碳酸氢铵
BC
练习
2、光照下,甲烷与氯气发生取代反应后,共得产物
A、5种 B、2种
C、3种 D、 4种
练习
A
3、光照下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是:
A、CH3Cl B、CH2Cl2
C、CHCl3 D、CCl4 E、HCl
E
练习
练习
C
4、将1mol甲烷和4mol的氯气发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗氯气为:
A.0.5mol B.2mol
C.2.5mol D.4mol
五、甲烷的用途:
除作燃料外,大量用于合成氨、尿素和炭黑,还可用于生产甲醇、氢气、乙炔、乙烯、甲醛、氢氰酸等。
【小结】甲烷的化学性质
1、稳定性:
2、氧化反应—
3、取代反应(特征反应)
现象:
反应条件:
特点:
不与强酸、强碱、酸性KMnO4溶液反应
燃烧
光照,与气态纯卤素反应 (与氯水、溴水不反应)
逐步取代(随机并行),产物为混合物
Thank you!
【回顾】甲烷的化学性质
1、稳定性:
2、氧化反应—
3、取代反应(特征反应)
现象:
反应条件:
特点:
不与强酸、强碱、酸性KMnO4溶液反应
燃烧
光照,与气态纯卤素反应 (与氯水、溴水不反应)
逐步取代(随机并行),产物为混合物
与甲烷结构相似的有机物还有很多,请你观察下列有机物的结构,试归纳出它们在结构上的特点。
学与问
H H H H H
| | | | |
H-C-C-H H-C-C-C-H
| | | | |
H H H H H
乙烷
丙烷
H H H H
| | | |
H-C-C-C-C-H
| | | |
H H H H
丁烷
只含C、H两种元素,每个碳以四个单键与其它原子相结合。
相同点
C、H原子数不同
不同点
一、烷烃
在烃的分子里,碳原子之间都以碳碳单键结合成链状,碳原子剩余的价键全部跟氢原子相结合,使每个碳原子的化合价都已充分利用,都达到“饱和”。这样的烃叫做饱和烃,又叫烷烃。
1、定义:
请大家用数学归纳法导出烷烃的分子式通式
思考
链状烷烃
CnH2n+2
环烷烃
CnH2n
例: H H H H H
| | | | |
H—C—C—C—C—C—H
| | | |
H H H H
H—C—H
|
H
2、结构简式:
或者:
CH3 CH(CH3)CH2 CH2 CH3
CH3—CH—CH2—CH2—CH3
CH3
CH3CHCH2CH2CH3
CH3
省略横线上C—C键
省略C—H键
把同一C上的H合并
乙烷: H H 丙烷: H H H
| | | | |
H-C-C-H H-C-C-C-H
| | | | |
H H H H H
如:下列结构式对应的结构简式
CH3CH3
CH3CH2CH3
丁烷: H H H H 异丁烷: H
| | | | |
H-C-C-C-C-H H--C--H
| | | | H H
H H H H | |
H-C——C——C-H
| | |
H H H
如:下列结构式对应的结构简式
CH3CH2CH2CH3
CH3CH(CH3 )CH3
◆以碳原子个数为基础命名
◆称“某烷”或“环某烷”
◆十个以下用“天干地支”命名:甲、乙、丙、丁、戊、己、庚、辛、壬、癸。
◆十以上用中文数字表示:十一烷、二十烷、三十五烷等。
3、烷烃的简单命名:
4、性质
(1)物理性质
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
物理性质(随分子中碳原子数增加)
规律:
状态:气(1~4)?液?固;熔沸点依次升高
密度:密度逐渐增大且均比水小
水溶性:均不溶于水
(2)化学性质(与CH4相似)
①氧化反应
具有可燃性
燃烧通式:
CnH2n+2+(3n+1)/2O2 nCO2+(n+1)H2O
②稳定性
均不能使酸性KMnO4或溴水褪色,不与强酸,强碱反应。
在光照条件下进行,产物更复杂
③取代反应
Thank you!
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
分析表3-1 相邻两个烷烃结构和分子组成上有什么联系?
表3-1几种烷烃的物理性质
名称 结构简式 常温时的状态 熔点/℃ 沸点/ ℃ 相对
密度 水溶性
甲烷 CH4 气 -182 -164 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -189.7 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
表3-1几种烷烃的物理性质
相差一个“CH2”原子团
结构相似,在分子组成上相差一个或若干
个CH2原子团的物质互称为同系物。
同系物
碳碳原子间都以单键结合;碳原子均饱合;链状。
碳原子数不同,即碳链的长短不同。
烷烃同系物
结构相似:
分子组成:
理解
1、是否属于同类物质?
2、通式相同吗?
3、碳原子数目相同吗?
4、相对分子质量相差多少?
5、性质相同吗?
结论:属于同类物质
通式相同
碳原子数目不同
相对分子质量相差14n
物性不同,化性相似
同系物间的关系
小结
CH3CH2CH2CH3
CH3CHCH3
CH3
观察:两者结构有何异同?
同分异构现象、同分异构体:
化合物具有相同的分子式,但具有不同结构式的现象叫同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
1、定义:
同位素、同素异形体、同系物、同分异构体概念的比较
概念 内 涵 比较对象 实例
同位素
同素异形体
同系物
同分异构体
质子数等,中子数
不等,原子之间
原子
氕、氘、氚
同一元素 形成的不同单质
单质
O2、O3
结构相似,组成上差一个或n个CH2
化合物
C2H6、C4H10
相同分子式,不
同结构的化合物
化合物
CH3(CH2)3CH3
C(CH3)4
图3-6 4个碳原子相互结合的几种方式
思考与交流
参考图3-6,分析、归纳以碳为骨架的有机物种类繁多的原因。
有机物种类繁多的原因:
(1)碳原子含有4个价电子,可跟其它原子形成4个共价键
(2)碳原子易跟多种原子形成共价键;碳原子间易形成单键、双键、叁键、碳链、碳环等多种复杂的结构单元。
C
H
H
H
H
C
C
C
C
C
C
C
C
C
C
C
C
:
:
H
H
H
..
C
..
H
Thank you!
