人教版化学九年级下册 第十二单元课题1 人类重要的营养物质同步测试
文档属性
| 名称 | 人教版化学九年级下册 第十二单元课题1 人类重要的营养物质同步测试 |

|
|
| 格式 | zip | ||
| 文件大小 | 86.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-12 00:00:00 | ||
图片预览


文档简介
【中考题原创】
天然甜味剂蔗糖
湖北省石首市文峰中学 刘涛
【背景资料】蔗糖是食糖的主要成分,蔗糖有甜味,无气味,无毒,极易溶于水,其溶解度随温度的升高而增大,溶于水后不导电。蔗糖几乎普遍存在于植物界的叶、花、茎、种子及果实中。在甘蔗、甜菜及槭树汁中含量尤为丰富。蔗糖味甜,是重要的食品和甜味调味品。分为白砂糖、赤砂糖、绵白糖、冰糖、粗糖(黄糖)。
【知识链接】蔗糖可作为食品添加剂,糖的甜味给人以愉悦的感觉,而且它的甜味纯正、稳定、回味良好。蔗糖是一种天然有机物,人食用后分解的最终产物是二氧化碳和水。经过几百年人类的食用证明,蔗糖是安全的食品。
【中考题原创】
1.下列物质中,属于混合物的是( )
A.蔗糖 B.氧气 C.铜 D.生理盐水
2.下列变化中属于化学变化的是( )
A.金块抽成金线 B.干冰升华 C.可燃冰燃烧 D.蔗糖溶解于水
3.蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是( )
A.蔗糖是由碳、氢、氧三种元素组成 B.蔗糖中含有45个原子
C.蔗糖中氢元素的质量分数最高 D.蔗糖的相对分子质量为342g
4.蔗糖是储藏在某些植物中的糖,它的化学式为C12H22O11,它是食品中常用的甜味剂。下列有关蔗糖的说法正确的是( )
A.蔗糖属于无机化合物
B.一个蔗糖分子由45个原子构成
C.蔗糖中氢元素的质量分数最大
D.蔗糖中碳、氢、氧三种元素的质量比为12:22:11
5.下列事实能证明分子在化学反应中可分的是( )
A.白糖溶于水 B.水通电可以得到氢气和氧气
C.水蒸气冷凝成成水 D.碘的升华
6.调味品是重要的食品添加剂,将下面调味品加入水中,不能形成溶液的是( )
A.食盐 B.蔗糖 C.味精 D.芝麻油
7.下列饮品属于溶液的是( )
A.果粒橙 B.牛奶 C. 豆浆 D.蔗糖水
8.要配制100g5%的蔗糖溶液,以下操作会导致所配溶液的浓度偏低的是( )
A.称取5g含杂质的蔗糖 B.用量筒量取90mL水
C.搅拌后玻璃棒上有液体残留 D.量筒中的水未完全倒入烧杯中
9.下列实验方案的设计中合理的是( )
实验目的 实验方案
A 量取9ml水 用50ml量筒量取,仰视读数
B 验证某瓶气体是二氧化碳 用燃着的木条入集气瓶内,若木条熄灭,证明是二氧化碳
C 鉴别蔗糖和硝酸铵两种固体 取样,分别放入盛有适量蒸馏水的小烧杯中,用温度计测量两种溶液的温度
D 除去NaCl溶液中少量的Na2SO4 加入适量Ba(NO3)2溶液,充分反应后过滤
参
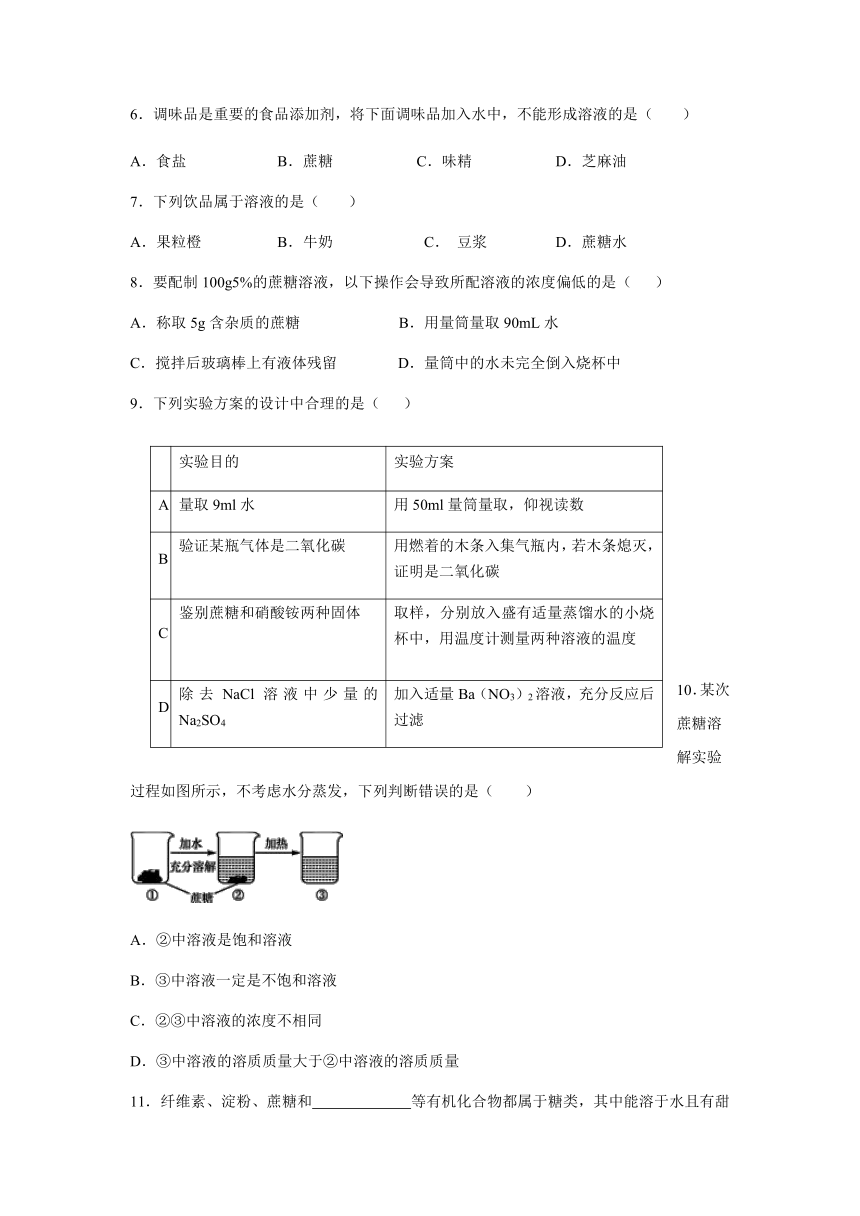
10.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的浓度不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
11.纤维素、淀粉、蔗糖和 等有机化合物都属于糖类,其中能溶于水且有甜味的是 ,不易溶于水又无甜味的是 。绿色植物光合作用的产物是 ,所以大规模植树造林可以提高空气质量。
12.日常生活中食用的白糖、冰糖和红糖的主要成分都是蔗糖(C12H22O11),则:
⑴一个蔗糖分子中含有的原子总数为 ;
⑵蔗糖中氢元素和氧元素的质量比为 。
13.酸奶是日常生活中常见的一种食品,下表是某酸奶外包装上标识的营养成分表。
项 目 能 量 蛋白质 脂 肪 糖 类 钠
每100 g 329kJ 2.6g 3.1g 10.0g 60mg
请填写下列空格:
⑴酸奶中的 在消化道内会逐渐被分解成可被人体吸收的多种氨基酸。
⑵脂肪在人体内分解、氧化释放出能量的过程,是将 能转化为热能。
⑶蔗糖(C12H22O11)是酸奶中的一种糖类物质,蔗糖的组成中碳、氢元素的质量比为(最简整数比) 。
⑷在选择制作酸奶包装盒的材料时,从化学性质的角度分析该材料应具备 的特点(填写一条即可)。
14.蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
【作出猜想】小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气,葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
【实验探究】方案一:小明将蔗糖在氧气中燃烧,检验生成物中有水和二氧化碳,得出结论“蔗糖是由碳、氢、氧三种元素组成的”。你认为小明的方案______(填“合理”或“不合理”),理由是________________________________。
方案二:小刚用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热。
⑴观察到小烧杯中 ,说明蔗糖中含有氢元素和氧元素。
⑵观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图装置,另选试剂进行了验证单质碳的实验。实验过程和现象如表,请你将表格补充完整:
实验过程 实验现象
向小烧杯中加入适量__________(填试剂名称),往硬质玻璃管通入氧气,点燃酒精灯 ①硬质玻璃管中的黑色固体剧烈燃烧,发出_______________,放热;②烧杯中_____________________。
写出上述黑色固体燃烧的化学方程式_______________________________________。
【实验结论】蔗糖是由碳、氢、氧三种元素组成的。
【拓展交流】⑴方案二中,先通入一会儿氮气的原因是 。
⑵查阅资料得知蔗糖的化学式为C12H22O11,小红发现:蔗糖分子中氢原子数目是氧原子数目的倍,但是,蔗糖中氧元素质量却是氢元素质量的8倍,导致出现这种情况的原因是 。
15.下图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。
【提出问题】改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
【进行实验】分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分,记录如下:
表1实验记录
实验 糖 浓硫酸体积/mL 水的滴数 温度/℃ 效果得分
1 蔗糖 4 5 22 65
2 蔗糖 5 10 30 81
3 蔗糖 6 15 50 93
4 冰糖 4 10 50 91
5 冰糖 5 15 22 88
6 冰糖 a 5 30 75
7 葡萄糖 4 15 30 0
8 葡萄糖 5 5 50 0
9 葡萄糖 6 10 22 0
【处理数据】分析表1,计算效果得分均值,结果如下:
表2效果得分均值
因素 糖 浓硫酸体积/mL 水的滴数 温度/℃
蔗糖 冰糖 葡萄糖 4 5 6 5 10 15 22 30 50
均值 79.7 84.7 0 52.0 56.3 56.0 46.7 57.3 60.3 51.0 52.0 61.3
依据均值推断最佳实验方案,均值越高,效果越好。
【解释与结论】
⑴蔗糖变成黑色的炭,发生了 (填“物理”或“化学”)变化。
⑵推测放出的气体含SO2,从元素守恒角度说明理由: 。
⑶实验6中,a为 mL。
⑷根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、 滴水和50℃
【反思与评价】
⑸表2中,22℃对应的均值为51.0,计算该值所依据的3个数据分别是 。
⑹综合分析,使实验3的效果得分高于实验4的因素有 。
参考答案
1~10.D、C、A、B、B;D、D、A、C、B。
11.葡萄糖(麦芽糖、果糖等);蔗糖(葡萄糖等);纤维素(淀粉);氧气和葡萄糖;
12. ⑴45;⑵1:8;
13. ⑴蛋白质;⑵化学; ⑶72:11;⑷无毒(合理即可)
14.【实验探究】不合理;蔗糖燃烧有氧气参与,氧气中含有氧元素;⑴有水雾;⑵澄清石灰水;白光;澄清石灰水变浑浊;C+O2CO2;【拓展交流】⑴排尽装置内的空气,以防干扰实验;⑵氢、氧的相对原子质量不同。
15.⑴化学;⑵浓硫酸中有硫元素和氧元素,蔗糖中含有氧元素,则生成物中也会有硫元素和氧元素;⑶6;⑷15 ;⑸65、88、0;⑹浓硫酸的体积和水的滴数
同课章节目录
