人教版九年级下册第九单元《溶液》单元复习测试题
文档属性
| 名称 | 人教版九年级下册第九单元《溶液》单元复习测试题 |
|
|
| 格式 | zip | ||
| 文件大小 | 204.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-13 00:00:00 | ||
图片预览



文档简介
【单元复习】
人教版第九单元《溶液》单元复习测试题
注意事项:
1.本卷共20小题,完成时间48分钟。
2.可能用到的相对原子质量:H-1、C-12、O-16、Cl-35.5、Ca-40。
一、我会选择(每小题只有一个选项符合题意,每题2分,共24分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
1.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.牛奶 B.食醋 C.生理盐水 D.碘酒
2.下列有关溶液的说法正确的是( )
A.长期放置不分层的液体一定是溶液
B.降低饱和溶液的温度,一定有晶体析出
C.溶质可以是固体,也可以是液体或气体
D.配制好的6%的NaCl溶液,装入试剂瓶中时不慎撒漏一部分,浓度减小
3.下列与洗涤有关的做法不合理的是( )
A.用洗洁精洗去餐具上的油污
B.用汽油洗去沾在衣服上的油渍
C.用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)
D.用纯碱溶液洗去铁制品表面的铁锈
4.下列物质溶解或稀释过程中,溶液温度没有明显改变的是( )
A.NaOH B.NH4NO3 C.浓硫酸 D.NaCl
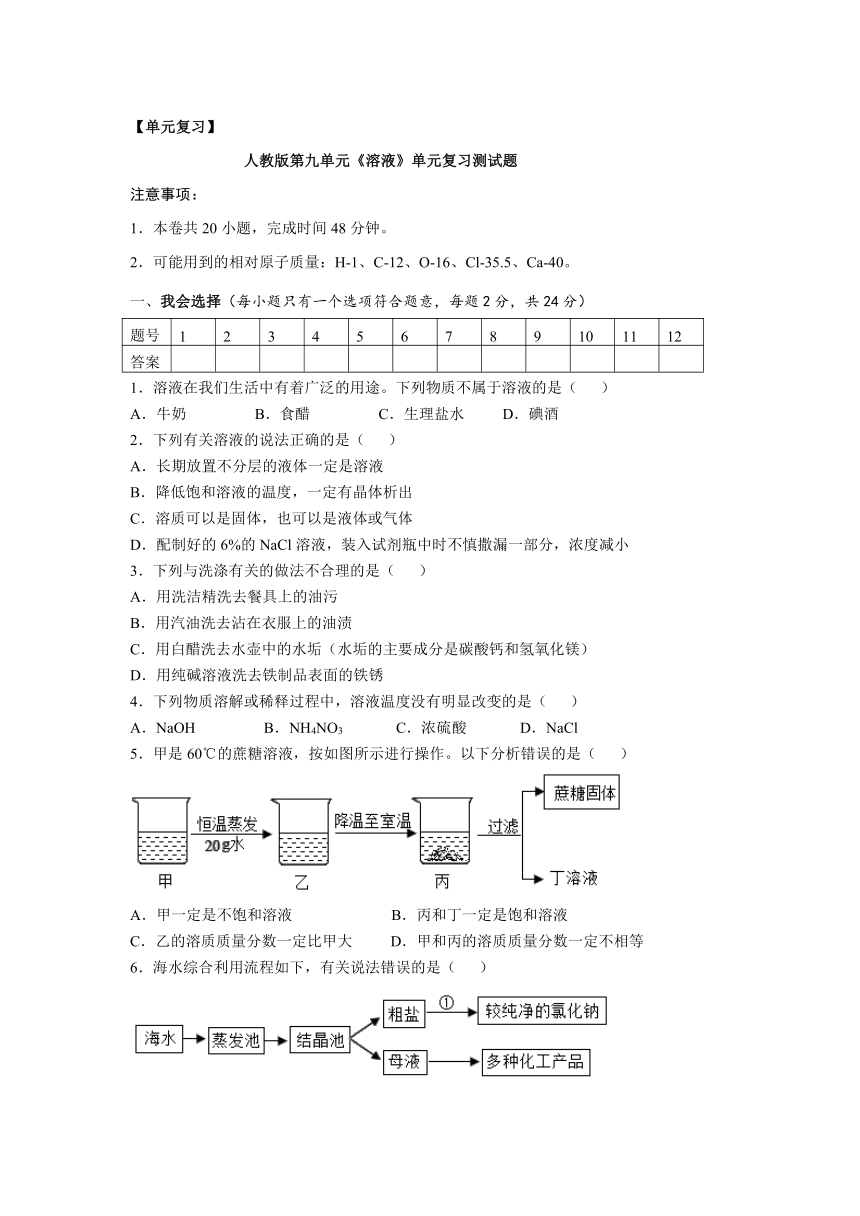
5.甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )
A.甲一定是不饱和溶液 B.丙和丁一定是饱和溶液
C.乙的溶质质量分数一定比甲大 D.甲和丙的溶质质量分数一定不相等
6.海水综合利用流程如下,有关说法错误的是( )
A.从母液中可进一步制得金属镁
B.①处操作是溶解、过滤、蒸发结晶
C.海水“晒盐”得到的粗盐还含有杂质
D.析出粗盐后的母液是氯化钠的不饱和溶液
7.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的?NaHCO3会部分析出
8.如图为甲、乙两种固体在水中的溶解度曲线。下列说法正确的是( )
A.甲物质的溶解度比乙物质的大
B.t2℃时,ag甲溶于100g水形成甲的不饱和溶液
C.t1℃时,甲、乙的饱和溶液溶质的质量分数都是25%
D.将t1℃时甲和乙的饱和溶液升温至t2℃,仍然都是饱和溶液
9.生石灰的主要成分是氧化钙,与水反应生成氢氧化钙并放出大量的热。室温时,将生石灰加入饱和石灰水中,生石灰对溶解影响的判断(参照如图溶解度曲线),错误的是( )
A.反应中,石灰水始终是饱和溶液
B.反应中,氧氧化钙的溶解度增大
C.反应后,溶液的质量减小
D.反应后,恢复至室温时,溶液的质量分数不变
10.夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,喷水的化学原理目的是( )
A.降低养殖池内水的温度
B.增加观赏性
C.增大与空气的接触面积,便于氧气溶解
D.便于太阳照射,杀灭水中的病菌
11.如图所示,下列判断正确的是( )
A.Y 的溶解度比X 的溶解度大
B.t1℃时,X、Y 两种饱和溶液的溶质质量分数都是 20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2℃时,若X、Y 的饱和溶液质量相等,则溶液中溶质的质量X<Y
12.用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g
B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
二、我会填空:(本题4小题,每空1分,共20分)
13.(5分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
⑴衣服上沾有的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
⑵喝了冰凉汽水以后,常常会打嗝。这种现象说明气体的溶解度与 有关。
⑶用海水晒盐:从海水中提取获得食盐氯化钠,通常采用的方法是 。
⑷固体物质溶于水,可使溶液的凝固点降低。利用这一性质,在冬天公路上的积雪中撒些盐,可用作 (填“吸附剂”“催化剂”或“融雪剂”)。
14.(4分)酒精的化学名称为乙醇(化学式为C2H5OH),在我们生产、生活以及实验中用途广泛。请回答:
⑴碘酒是一种常用的消毒剂,酒精作碘酒中的 (填“溶质”或“溶剂”)。
⑵酒精能与水以任何比率互溶,这是酒精的 (填“物理”或“化学”)性质,形成酒精溶液。
⑶医用酒精中乙醇的体积分数为75%,配制时将75mL乙醇与25mL蒸馏水充分混合,所得溶液体积<100mL,这一现象从微观解释原理为 。
⑷酒精灯是实验室常用的加热仪器,燃料酒精在完全燃烧时的化学方程式为 。
15.(4分)列表法是一种常用数据处理和分析方法。下表是硝酸钾在不同温度下的溶解度(单位:g/100g水)。根据下表回答回答问题:
温度/℃ 0 20 40 60 80
溶解度/g 13.3 31.6 63.9 110 169
⑴20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是 g。
⑵80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是 g。
⑶0℃时,硝酸钾饱和溶液中溶质的质量分数是 (结果精确到0.1%)。
⑷将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是 。
15.(4分)甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:
⑴t1℃时,甲、乙两种物质的溶解度大小关系为甲 乙(填“>”、“=”或“<”)。
⑵t2℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是 g。
⑶欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法是 。
⑷如果甲物质中含有少量乙物质,若要提纯甲,一般采用______________的方法。
17.t2℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
⑴固体甲对应的溶解度曲线是 (填“a”或“b”)。
⑵向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。此时(t2℃)溶液的溶质质量分数是 (结果精确到0.1%)。你认为“全部溶解”的原因是 。
⑶将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法不正确的是 (填序号)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
e.两溶液溶质质量分数甲=乙 f.两溶质溶解度甲>乙
三、我会探究(每空1分,共10分)
18.(4分)根据下列图示,回答相关问题:
⑴实验一:实验中红色铜片逐渐变黑,该反应的化学方程式是 。
⑵实验二:自制简易净水器中小卵石,石英砂和蓬松棉的作用是 。
⑶实验三:X、Y分别是水和汽油中的一种,加入X、Y后,观察到a中固体消失并得到棕色溶液,b中固体不消失,则物质X是 ,由实验可知,物质的溶解性与 有关。
19.(6分)某同学配制50g溶质质量分数为9%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
⑴配制溶液的正确操作顺序为 (填序号),其中操作错误的是 (填序号)。
⑵图②中盛放氯化钠固体的仪器名称是_____,需称取氧化钠_____ g。
⑶图④中玻璃棒作用是 。
⑷有同学发现图示实验操作步骤不完整,应补充的是 。
四、我会计算(本题1小题,共6分)
20.我市石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 剩余固体的质量
第一次加入10g 3.0g
第二次加入10g 2.0g
第三次加入10g 1.0g
第四次加入10g 0.6g
请计算:
⑴4.0g石灰石样品中碳酸钙的质量是 g。
⑵10g稀盐酸能与 g碳酸钙正好完全反应。
⑶求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
参考答案
一、我会选择(每本大题共12小题,每题2分,共24分,每小题只有一个正确答案。)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 A C D D B D B B B C D C
二、我会填空(本题包括5个小题,每空1分,共20分)
13.⑴溶解;⑵温度;⑶蒸发结晶;⑷融雪剂。
14.⑴溶剂;⑵物理;⑶分子间有一定的间隔;⑷C2H5OH+3O23H2O+2CO2。
15.⑴65.8;⑵59;⑶11.7%;⑷加水或升温。
16.⑴<;⑵62.5;⑶增加溶质或恒温蒸发溶剂;⑷降温结晶。
17.⑴a;⑵47.4%;甲物质溶于水放热,使温度升高,溶解度变大;⑶abd。
三、我会探究(每空1分,共10分)
18.⑴2Cu+O22CuO;⑵过滤;⑶汽油;溶剂的性质。
19.⑴②①⑤③④;①;⑵药匙;4.5;汽油;⑶搅拌,加速溶解;⑷装瓶贴标签。
四、我会计算(本题1小题,共6分)
20.⑴3.4(g);
⑵1.0g(g);
⑶设10g稀盐酸中HCl的质量为x:
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
1.0g x
100/1.0g80=73/x 则:x=0.73gg
稀盐酸的溶质质量分数=0.73g/10g×100%=7.3%
答:稀盐酸的溶质质量分数为7.3%。
人教版第九单元《溶液》单元复习测试题
注意事项:
1.本卷共20小题,完成时间48分钟。
2.可能用到的相对原子质量:H-1、C-12、O-16、Cl-35.5、Ca-40。
一、我会选择(每小题只有一个选项符合题意,每题2分,共24分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
1.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )
A.牛奶 B.食醋 C.生理盐水 D.碘酒
2.下列有关溶液的说法正确的是( )
A.长期放置不分层的液体一定是溶液
B.降低饱和溶液的温度,一定有晶体析出
C.溶质可以是固体,也可以是液体或气体
D.配制好的6%的NaCl溶液,装入试剂瓶中时不慎撒漏一部分,浓度减小
3.下列与洗涤有关的做法不合理的是( )
A.用洗洁精洗去餐具上的油污
B.用汽油洗去沾在衣服上的油渍
C.用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)
D.用纯碱溶液洗去铁制品表面的铁锈
4.下列物质溶解或稀释过程中,溶液温度没有明显改变的是( )
A.NaOH B.NH4NO3 C.浓硫酸 D.NaCl
5.甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )
A.甲一定是不饱和溶液 B.丙和丁一定是饱和溶液
C.乙的溶质质量分数一定比甲大 D.甲和丙的溶质质量分数一定不相等
6.海水综合利用流程如下,有关说法错误的是( )
A.从母液中可进一步制得金属镁
B.①处操作是溶解、过滤、蒸发结晶
C.海水“晒盐”得到的粗盐还含有杂质
D.析出粗盐后的母液是氯化钠的不饱和溶液
7.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的?NaHCO3会部分析出
8.如图为甲、乙两种固体在水中的溶解度曲线。下列说法正确的是( )
A.甲物质的溶解度比乙物质的大
B.t2℃时,ag甲溶于100g水形成甲的不饱和溶液
C.t1℃时,甲、乙的饱和溶液溶质的质量分数都是25%
D.将t1℃时甲和乙的饱和溶液升温至t2℃,仍然都是饱和溶液
9.生石灰的主要成分是氧化钙,与水反应生成氢氧化钙并放出大量的热。室温时,将生石灰加入饱和石灰水中,生石灰对溶解影响的判断(参照如图溶解度曲线),错误的是( )
A.反应中,石灰水始终是饱和溶液
B.反应中,氧氧化钙的溶解度增大
C.反应后,溶液的质量减小
D.反应后,恢复至室温时,溶液的质量分数不变
10.夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,喷水的化学原理目的是( )
A.降低养殖池内水的温度
B.增加观赏性
C.增大与空气的接触面积,便于氧气溶解
D.便于太阳照射,杀灭水中的病菌
11.如图所示,下列判断正确的是( )
A.Y 的溶解度比X 的溶解度大
B.t1℃时,X、Y 两种饱和溶液的溶质质量分数都是 20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2℃时,若X、Y 的饱和溶液质量相等,则溶液中溶质的质量X<Y
12.用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g
B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
二、我会填空:(本题4小题,每空1分,共20分)
13.(5分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
⑴衣服上沾有的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
⑵喝了冰凉汽水以后,常常会打嗝。这种现象说明气体的溶解度与 有关。
⑶用海水晒盐:从海水中提取获得食盐氯化钠,通常采用的方法是 。
⑷固体物质溶于水,可使溶液的凝固点降低。利用这一性质,在冬天公路上的积雪中撒些盐,可用作 (填“吸附剂”“催化剂”或“融雪剂”)。
14.(4分)酒精的化学名称为乙醇(化学式为C2H5OH),在我们生产、生活以及实验中用途广泛。请回答:
⑴碘酒是一种常用的消毒剂,酒精作碘酒中的 (填“溶质”或“溶剂”)。
⑵酒精能与水以任何比率互溶,这是酒精的 (填“物理”或“化学”)性质,形成酒精溶液。
⑶医用酒精中乙醇的体积分数为75%,配制时将75mL乙醇与25mL蒸馏水充分混合,所得溶液体积<100mL,这一现象从微观解释原理为 。
⑷酒精灯是实验室常用的加热仪器,燃料酒精在完全燃烧时的化学方程式为 。
15.(4分)列表法是一种常用数据处理和分析方法。下表是硝酸钾在不同温度下的溶解度(单位:g/100g水)。根据下表回答回答问题:
温度/℃ 0 20 40 60 80
溶解度/g 13.3 31.6 63.9 110 169
⑴20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是 g。
⑵80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是 g。
⑶0℃时,硝酸钾饱和溶液中溶质的质量分数是 (结果精确到0.1%)。
⑷将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是 。
15.(4分)甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:
⑴t1℃时,甲、乙两种物质的溶解度大小关系为甲 乙(填“>”、“=”或“<”)。
⑵t2℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是 g。
⑶欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法是 。
⑷如果甲物质中含有少量乙物质,若要提纯甲,一般采用______________的方法。
17.t2℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
⑴固体甲对应的溶解度曲线是 (填“a”或“b”)。
⑵向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。此时(t2℃)溶液的溶质质量分数是 (结果精确到0.1%)。你认为“全部溶解”的原因是 。
⑶将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法不正确的是 (填序号)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
e.两溶液溶质质量分数甲=乙 f.两溶质溶解度甲>乙
三、我会探究(每空1分,共10分)
18.(4分)根据下列图示,回答相关问题:
⑴实验一:实验中红色铜片逐渐变黑,该反应的化学方程式是 。
⑵实验二:自制简易净水器中小卵石,石英砂和蓬松棉的作用是 。
⑶实验三:X、Y分别是水和汽油中的一种,加入X、Y后,观察到a中固体消失并得到棕色溶液,b中固体不消失,则物质X是 ,由实验可知,物质的溶解性与 有关。
19.(6分)某同学配制50g溶质质量分数为9%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
⑴配制溶液的正确操作顺序为 (填序号),其中操作错误的是 (填序号)。
⑵图②中盛放氯化钠固体的仪器名称是_____,需称取氧化钠_____ g。
⑶图④中玻璃棒作用是 。
⑷有同学发现图示实验操作步骤不完整,应补充的是 。
四、我会计算(本题1小题,共6分)
20.我市石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 剩余固体的质量
第一次加入10g 3.0g
第二次加入10g 2.0g
第三次加入10g 1.0g
第四次加入10g 0.6g
请计算:
⑴4.0g石灰石样品中碳酸钙的质量是 g。
⑵10g稀盐酸能与 g碳酸钙正好完全反应。
⑶求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
参考答案
一、我会选择(每本大题共12小题,每题2分,共24分,每小题只有一个正确答案。)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 A C D D B D B B B C D C
二、我会填空(本题包括5个小题,每空1分,共20分)
13.⑴溶解;⑵温度;⑶蒸发结晶;⑷融雪剂。
14.⑴溶剂;⑵物理;⑶分子间有一定的间隔;⑷C2H5OH+3O23H2O+2CO2。
15.⑴65.8;⑵59;⑶11.7%;⑷加水或升温。
16.⑴<;⑵62.5;⑶增加溶质或恒温蒸发溶剂;⑷降温结晶。
17.⑴a;⑵47.4%;甲物质溶于水放热,使温度升高,溶解度变大;⑶abd。
三、我会探究(每空1分,共10分)
18.⑴2Cu+O22CuO;⑵过滤;⑶汽油;溶剂的性质。
19.⑴②①⑤③④;①;⑵药匙;4.5;汽油;⑶搅拌,加速溶解;⑷装瓶贴标签。
四、我会计算(本题1小题,共6分)
20.⑴3.4(g);
⑵1.0g(g);
⑶设10g稀盐酸中HCl的质量为x:
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
1.0g x
100/1.0g80=73/x 则:x=0.73gg
稀盐酸的溶质质量分数=0.73g/10g×100%=7.3%
答:稀盐酸的溶质质量分数为7.3%。
同课章节目录
