2020年春季九年级新鲁教版化学下册课后同步练习卷:第七单元常见的酸和碱第一节酸及其性质
文档属性
| 名称 | 2020年春季九年级新鲁教版化学下册课后同步练习卷:第七单元常见的酸和碱第一节酸及其性质 |

|
|
| 格式 | zip | ||
| 文件大小 | 64.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-17 00:00:00 | ||
图片预览

文档简介
第一节 酸及其性质
一、单选题(共8题;共16分)
1.在某无色水溶液中,加入少量氯化钡溶液时,生成白色沉淀,此沉淀在酸溶液中也不溶解,则原溶液中(? ?)
A.一定有SO42﹣离子?????????????????????????????
B.一定有Ag+离子
C.既无SO42﹣离子,也无Ag+离子??????????????????
D.含有SO42﹣离子或Ag+离子中的一种
2.实验时不小心打翻酒精灯着火了,最简便合理的灭火方法是(? ?)
A.用水浇灭???????????????B.用嘴吹灭
C.用灭火器朴灭?????????????D.用湿抹布盖灭
3.下列物质敞口放置在空气中一段时间后,因发生化学反应质量增加的是(? ?)
A.碳酸钙????????????B.浓硫酸???????????????
C.浓盐酸????????????D.氢氧化钠
4.下列物质敞口放置一段时间,质量减少的是(? ?)
A.浓盐酸????? ?B.浓硫酸???????????
C.氢氧化钠???????????D.食盐
5.下列物质必须密封保存的是(? )
A.木炭?????????????????????????????????
B.浓盐酸
C.石灰石???????????????????????????????
D.氯化钠
6.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减小的是(? ?)
A.石灰水????????????????B.饱和食盐水
C.苛性钠溶液??????????????D.浓硫酸
7.下列各组离子在水中能大量共存的是(? ?)
A.H+、Na+、Cl﹣、NO3﹣?????????????????????????????
B.H+、K+、Cl﹣、HCO3﹣
C.Fe3+、Ba2+、Cl﹣、SO42﹣??????????????????????????
D.K+、NH4+、Cl﹣、OH﹣
8.酸和碱混合后的溶液可能呈酸性,以下证明酸过量的操作及现象的叙述中正确的是(? )
A.加入金属铜片,产生气泡??????????????????
B.滴加石蕊溶液,溶液变红色
C.加入蒸馏水,溶液颜色不变???????????????
D.滴加酚酞溶液,溶液为无色
二、填空题(共4题;共14分)
9.现有失去标签的相同体积的两瓶液体,一瓶是98%的浓硫酸,另一瓶是10%的稀硫酸,请你根据所学的知识,例举几种方法来鉴别它们:_____________________________。
10.打开浓盐酸的瓶盖时,会看到瓶口出现________,这是由于浓盐酸有________性。
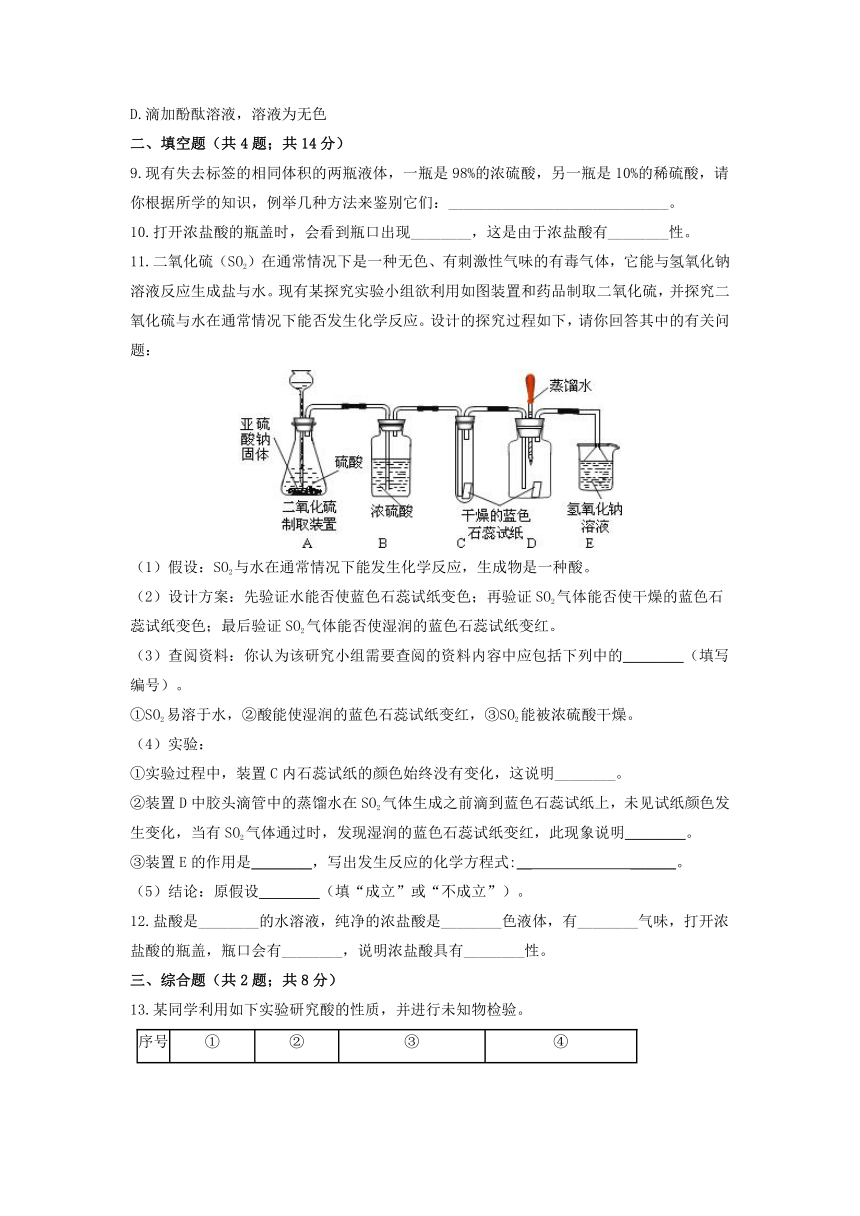
11.二氧化硫(SO2)在通常情况下是一种无色、有刺激性气味的有毒气体,它能与氢氧化钠溶液反应生成盐与水。现有某探究实验小组欲利用如图装置和药品制取二氧化硫,并探究二氧化硫与水在通常情况下能否发生化学反应。设计的探究过程如下,请你回答其中的有关问题:
(1)假设:SO2与水在通常情况下能发生化学反应,生成物是一种酸。
(2)设计方案:先验证水能否使蓝色石蕊试纸变色;再验证SO2气体能否使干燥的蓝色石蕊试纸变色;最后验证SO2气体能否使湿润的蓝色石蕊试纸变红。
(3)查阅资料:你认为该研究小组需要查阅的资料内容中应包括下列中的________(填写编号)。
①SO2易溶于水,②酸能使湿润的蓝色石蕊试纸变红,③SO2能被浓硫酸干燥。
(4)实验:
①实验过程中,装置C内石蕊试纸的颜色始终没有变化,这说明________。
②装置D中胶头滴管中的蒸馏水在SO2气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有SO2气体通过时,发现湿润的蓝色石蕊试纸变红,此现象说明________。
③装置E的作用是________,写出发生反应的化学方程式:__ ______。
(5)结论:原假设________(填“成立”或“不成立”)。
12.盐酸是________的水溶液,纯净的浓盐酸是________色液体,有________气味,打开浓盐酸的瓶盖,瓶口会有________,说明浓盐酸具有________性。
三、综合题(共2题;共8分)
13.某同学利用如下实验研究酸的性质,并进行未知物检验。
序号 ① ② ③ ④
实验
现象 红色固体消失,溶液变黄 固体表面有气泡产生,澄清石灰水变浑浊
(1)进行实验①、②的目的是________。
(2)依据实验③、④的现象,可得出关于方解石和云白石成分的结论是_______________。
14.镁是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,主要步骤是从海水中得到金属镁。下图是从海水中提取镁的简单流程:
(1)为了使 MgCl2转化为沉淀,试剂A可以用________,加入试剂A过量的目的是________,验证MgCl2已完全沉淀的方法是________;试剂C可选用________。
(2)无水MgCl2在熔融状态下通电后会产生Mg和Cl2,写出该反应的化学方程式:________。
(3)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:______________________________________________________________________________。
参考答案
一、单选题
1.D 2.D 3.D 4.A 5.B 6.A 7.A 8.B
二、填空题
9.①观察呈油状粘稠的为浓硫酸 ②用玻璃棒蘸取在纸上写字,字迹变黑的为浓硫酸
③称其质量,质量大的为浓硫酸等
10.白雾;挥发
11.①②③ SO2不能使干燥的蓝色石蕊试纸变红色 水不能使蓝色石蕊试纸变色,SO2溶于水生成酸能使蓝色石蕊试纸变色 吸收多余SO2气体,避免污染空气SO2+2NaOH=Na2SO3+H2O 成立
12.氯化氢 无 刺激性 白雾 挥发性
三、综合题
13.(1)探究酸能否与氧化铁反应 (2)含有碳酸盐
14.(1)NaOH 或 Ca(OH)2或 CaO(合理即可) 确保Mg2+完全沉淀 静置,往上层清液中继续加试剂A,不再产生沉淀 盐酸
(2)MgCl2Mg + Cl2↑
(3)海水中MgCl2含量太低
一、单选题(共8题;共16分)
1.在某无色水溶液中,加入少量氯化钡溶液时,生成白色沉淀,此沉淀在酸溶液中也不溶解,则原溶液中(? ?)
A.一定有SO42﹣离子?????????????????????????????
B.一定有Ag+离子
C.既无SO42﹣离子,也无Ag+离子??????????????????
D.含有SO42﹣离子或Ag+离子中的一种
2.实验时不小心打翻酒精灯着火了,最简便合理的灭火方法是(? ?)
A.用水浇灭???????????????B.用嘴吹灭
C.用灭火器朴灭?????????????D.用湿抹布盖灭
3.下列物质敞口放置在空气中一段时间后,因发生化学反应质量增加的是(? ?)
A.碳酸钙????????????B.浓硫酸???????????????
C.浓盐酸????????????D.氢氧化钠
4.下列物质敞口放置一段时间,质量减少的是(? ?)
A.浓盐酸????? ?B.浓硫酸???????????
C.氢氧化钠???????????D.食盐
5.下列物质必须密封保存的是(? )
A.木炭?????????????????????????????????
B.浓盐酸
C.石灰石???????????????????????????????
D.氯化钠
6.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减小的是(? ?)
A.石灰水????????????????B.饱和食盐水
C.苛性钠溶液??????????????D.浓硫酸
7.下列各组离子在水中能大量共存的是(? ?)
A.H+、Na+、Cl﹣、NO3﹣?????????????????????????????
B.H+、K+、Cl﹣、HCO3﹣
C.Fe3+、Ba2+、Cl﹣、SO42﹣??????????????????????????
D.K+、NH4+、Cl﹣、OH﹣
8.酸和碱混合后的溶液可能呈酸性,以下证明酸过量的操作及现象的叙述中正确的是(? )
A.加入金属铜片,产生气泡??????????????????
B.滴加石蕊溶液,溶液变红色
C.加入蒸馏水,溶液颜色不变???????????????
D.滴加酚酞溶液,溶液为无色
二、填空题(共4题;共14分)
9.现有失去标签的相同体积的两瓶液体,一瓶是98%的浓硫酸,另一瓶是10%的稀硫酸,请你根据所学的知识,例举几种方法来鉴别它们:_____________________________。
10.打开浓盐酸的瓶盖时,会看到瓶口出现________,这是由于浓盐酸有________性。
11.二氧化硫(SO2)在通常情况下是一种无色、有刺激性气味的有毒气体,它能与氢氧化钠溶液反应生成盐与水。现有某探究实验小组欲利用如图装置和药品制取二氧化硫,并探究二氧化硫与水在通常情况下能否发生化学反应。设计的探究过程如下,请你回答其中的有关问题:
(1)假设:SO2与水在通常情况下能发生化学反应,生成物是一种酸。
(2)设计方案:先验证水能否使蓝色石蕊试纸变色;再验证SO2气体能否使干燥的蓝色石蕊试纸变色;最后验证SO2气体能否使湿润的蓝色石蕊试纸变红。
(3)查阅资料:你认为该研究小组需要查阅的资料内容中应包括下列中的________(填写编号)。
①SO2易溶于水,②酸能使湿润的蓝色石蕊试纸变红,③SO2能被浓硫酸干燥。
(4)实验:
①实验过程中,装置C内石蕊试纸的颜色始终没有变化,这说明________。
②装置D中胶头滴管中的蒸馏水在SO2气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有SO2气体通过时,发现湿润的蓝色石蕊试纸变红,此现象说明________。
③装置E的作用是________,写出发生反应的化学方程式:__ ______。
(5)结论:原假设________(填“成立”或“不成立”)。
12.盐酸是________的水溶液,纯净的浓盐酸是________色液体,有________气味,打开浓盐酸的瓶盖,瓶口会有________,说明浓盐酸具有________性。
三、综合题(共2题;共8分)
13.某同学利用如下实验研究酸的性质,并进行未知物检验。
序号 ① ② ③ ④
实验
现象 红色固体消失,溶液变黄 固体表面有气泡产生,澄清石灰水变浑浊
(1)进行实验①、②的目的是________。
(2)依据实验③、④的现象,可得出关于方解石和云白石成分的结论是_______________。
14.镁是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,主要步骤是从海水中得到金属镁。下图是从海水中提取镁的简单流程:
(1)为了使 MgCl2转化为沉淀,试剂A可以用________,加入试剂A过量的目的是________,验证MgCl2已完全沉淀的方法是________;试剂C可选用________。
(2)无水MgCl2在熔融状态下通电后会产生Mg和Cl2,写出该反应的化学方程式:________。
(3)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:______________________________________________________________________________。
参考答案
一、单选题
1.D 2.D 3.D 4.A 5.B 6.A 7.A 8.B
二、填空题
9.①观察呈油状粘稠的为浓硫酸 ②用玻璃棒蘸取在纸上写字,字迹变黑的为浓硫酸
③称其质量,质量大的为浓硫酸等
10.白雾;挥发
11.①②③ SO2不能使干燥的蓝色石蕊试纸变红色 水不能使蓝色石蕊试纸变色,SO2溶于水生成酸能使蓝色石蕊试纸变色 吸收多余SO2气体,避免污染空气SO2+2NaOH=Na2SO3+H2O 成立
12.氯化氢 无 刺激性 白雾 挥发性
三、综合题
13.(1)探究酸能否与氧化铁反应 (2)含有碳酸盐
14.(1)NaOH 或 Ca(OH)2或 CaO(合理即可) 确保Mg2+完全沉淀 静置,往上层清液中继续加试剂A,不再产生沉淀 盐酸
(2)MgCl2Mg + Cl2↑
(3)海水中MgCl2含量太低
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
