2.1 烷烃、烯烃-天津市2020年空中课堂人教版高中化学选修五课件(共57张PPT)
文档属性
| 名称 | 2.1 烷烃、烯烃-天津市2020年空中课堂人教版高中化学选修五课件(共57张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-19 00:00:00 | ||
图片预览







文档简介
(共57张PPT)
第二章 第一节 脂肪烃
——烷烃 烯烃
高二年级 化学
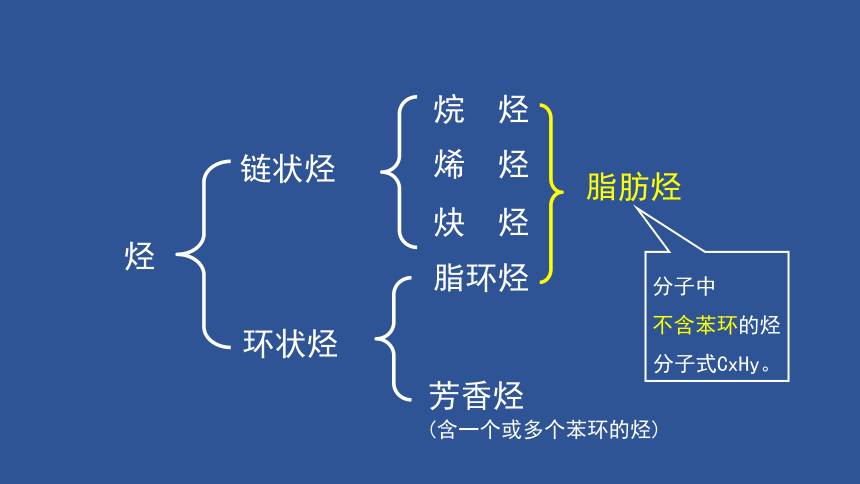
链状烃
环状烃
脂环烃
芳香烃
烃
烷 烃
烯 烃
炔 烃
脂肪烃
分子中
不含苯环的烃
分子式CxHy。
(含一个或多个苯环的烃)
一、烷烃
CH4
C
H
?
H
?
H
?
H
?
分子式
电子式
C
H
H
H
H
结构式
109o28?
正四面体
比例模型
球棍
模型
——甲烷
1.烷烃的结构
(1)烷烃碳原子间都以可旋转的单键相连接;
(2)直链烷烃碳原子不在一条直线上,空间结构是折线型或锯齿状;
(3)烷烃分子的通式:CnH2n+2(n≥1,正整数),又称为饱和烃。
乙烷
丙烷
正丁烷
1.烷烃的结构
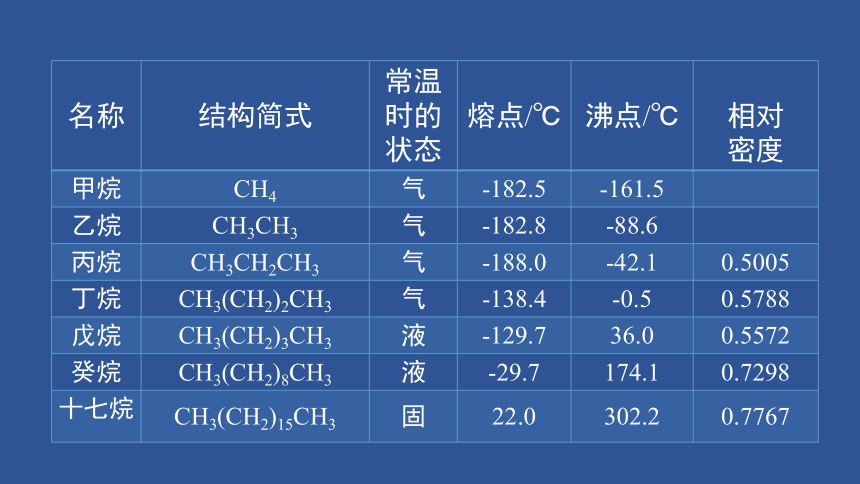
名称 结构简式 常温时的状态 熔点/℃ 沸点/℃ 相对
密度
甲烷 CH4 气 -182.5 -161.5
乙烷 CH3CH3 气 -182.8 -88.6
丙烷 CH3CH2CH3 气 -188.0 -42.1 0.5005
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788
戊烷 CH3(CH2)3CH3 液 -129.7 36.0 0.5572
癸烷 CH3(CH2)8CH3 液 -29.7 174.1 0.7298
十七烷 CH3(CH2)15CH3 固 22.0 302.2 0.7767
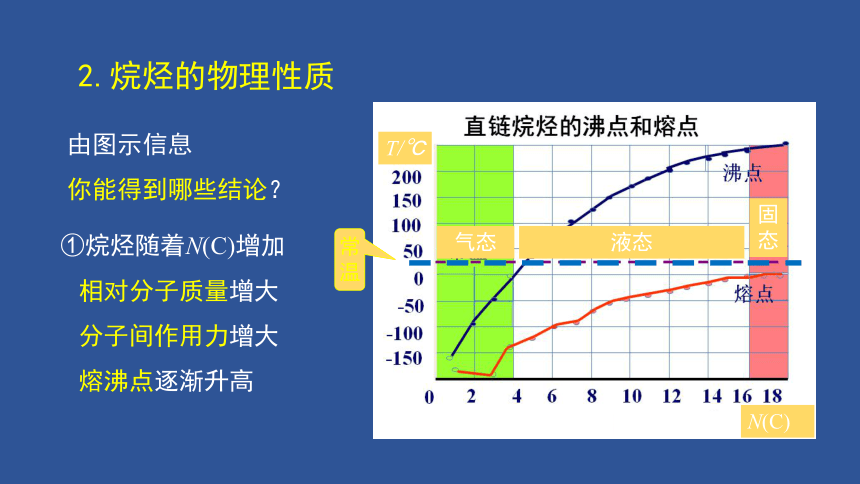
①烷烃随着N(C)增加
相对分子质量增大
分子间作用力增大
熔沸点逐渐升高
2.烷烃的物理性质
气态
常温
液态
固态
由图示信息
你能得到哪些结论?
N(C)
T/℃
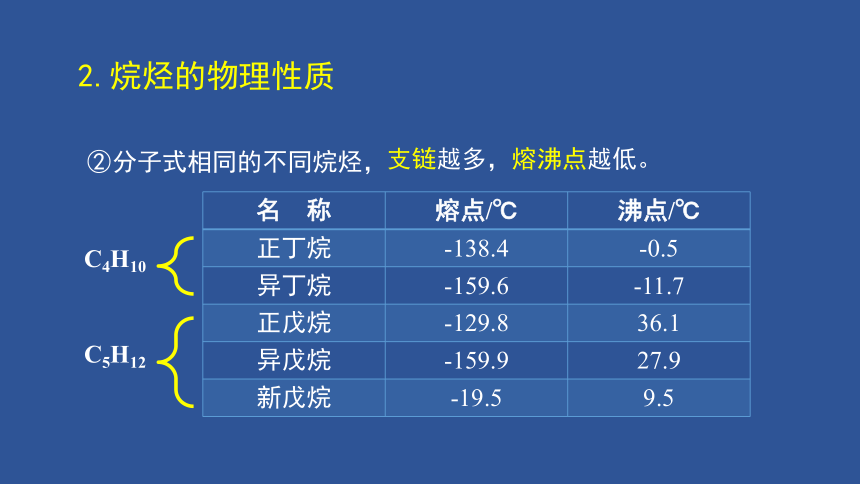
②分子式相同的不同烷烃,
名 称 熔点/℃ 沸点/℃
正丁烷 -138.4 -0.5
异丁烷 -159.6 -11.7
正戊烷 -129.8 36.1
异戊烷 -159.9 27.9
新戊烷 -19.5 9.5
C4H10
C5H12
2.烷烃的物理性质
支链越多,熔沸点越低。
③直链烷烃碳原子数的增加,
其密度增大。
烷烃都不溶于水,
且烷烃的密度比水的密度小。
2.烷烃的物理性质
(1)稳定性: 在通常状况下,性质很稳定,与酸、碱及其氧化物都不发生反应。
(2)可燃性:
——甲烷
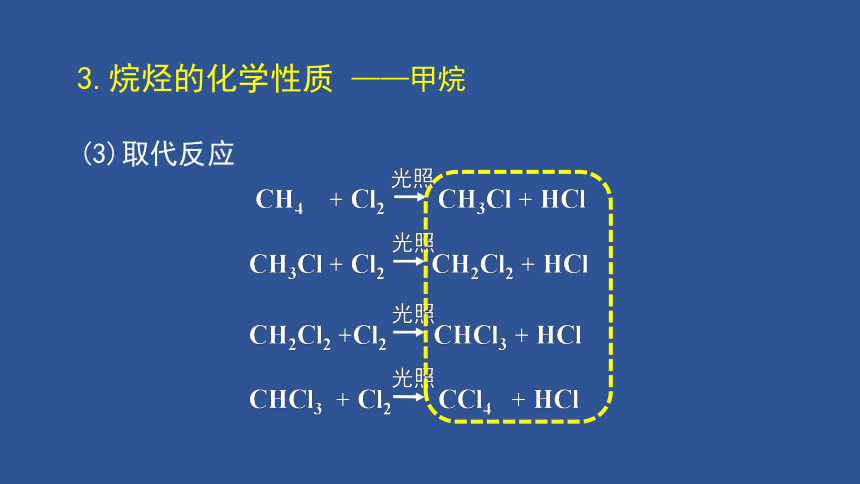
3.烷烃的化学性质
(3)取代反应
——甲烷
3.烷烃的化学性质
(3)取代反应
——甲烷
3.烷烃的化学性质
(1)稳定性: 烷烃的化学性质与甲烷类似,通常较稳定,不能使KMnO4溶液褪色,不能跟强酸、强碱反应。
烷烃的物理性质呈规律性变化:
(2)可燃性:
3.烷烃的化学性质
(3)取代反应
烷烃是有机物的基础,是烃的衍生物的母体。所以掌握了烃的性质是学好有机化学的关键。
烷烃的物理性质呈规律性变化:
CH2ClCH2Cl 、 CH3CHCl2 二氯乙烷
CHCl2CH2Cl 、 CCl3CH3 三氯乙烷
CHCl2CHCl2、 CCl3CH2Cl 四氯乙烷
CCl3CHCl 2 和 CCl3CCl 3 五氯乙烷和六氯乙烷
3.烷烃的化学性质
CH3CH3 + Cl2 CH3CH2Cl + HCl
光照
下列烷烃的一氯代物中没有同分异构的是( )
A.2-甲基丙烷
B. 丙烷
C.正 丁烷
D. 乙烷
D
C
C—C—C
C—C—C
C—C—C—C
C—C
?
o
o
o
?
o
o
?
?
o
o
?
?
反馈练习
(4)裂化和裂解
催化裂化
催化裂解
3.烷烃的化学性质
二、烯烃
名称 乙烯
分子式 C2H4
电子式
结构式
结构简式
CH2=CH2
C = C
H
H
H
H
C C
H
H
H
H
乙烯分子中的碳原子发生sp2杂化与2个氢原子形成2个碳氢δ共价键。2个碳原子之间又各以一个sp2杂化轨道形成1个碳碳δ共价键,未参加杂化的p轨道形成1个π键, π键易断裂。
——乙烯
1.烯烃的结构
名称 乙烯
分子式 C2H4
电子式
结构式
结构简式
球棍模型
比例模型
乙烯的结构
CH2=CH2
C = C
H
H
H
H
C C
H
H
H
H
(1)烯烃分子中都含有碳碳双键,比相同碳数的烷烃少两个氢原子;
(2)烯烃分子的通式:CnH2n(n≥2,正整数)。
(3)烯烃中的碳碳双键是平面结构,决定至少6个原子共平面;
1.烯烃的结构
C=C
H
H
H
H
C=C
H
H
CH3
H
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
1
2 3 4
1 4
2 3
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
——顺反异构
1.烯烃的结构
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
——顺反异构
1.烯烃的结构
顺式结构:两个相同的原子或原子团排列在双键的同一侧;
反式结构:两个相同的原子或原子团分别排列在双键的两侧。
顺?2?丁烯
反?2?丁烯
——顺反异构
1.烯烃的结构
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
顺反异构的形成条件:
(1)具有碳碳双键;
(2)组成双键的每个碳原子上必须连接
两个不同的原子或原子团。
顺反异构体:
化学性质基本相同,物理性质有一定的差异。
——顺反异构
1.烯烃的结构
√顺
√反
典型例题
顺-2-戊烯
反-3-己烯
1 2
3 2
2 3
3 4
1 4 5
1 2
5 6
首先找双键,
竖切查看碳。横切看上下,
准确定顺反。
下列有机分子中,可形成顺反异构的是( )
A.CH2=CHCH3 B.CH2=CHCH2CH2
C.CH3CH=C(CH3)2 D.CH3CH=CHCl
D
反馈练习
①烯烃随着碳原子数的增加,
相对分子质量增大,
分子间作用力增大,
沸点(熔点)逐渐升高。
②分子式相同的不同烯烃,支链越多,熔沸点越低。
2.烯烃的物理性质
烷烃的物质性质具有递变性,
烯烃的物理性质也一样吗?
2.烯烃的物理性质
烷烃的物质性质具有递变性,
烯烃的物理性质也一样吗?
③烯烃碳原子数的增加,
烯烃的密度增大。
烯烃都不溶于水,
且烯烃的密度比水的密度小。
直链烯烃相对密度
(1)可燃性:
火焰明亮,少量黒烟
——乙烯
3.烯烃的化学性质
2CO2 +2H2O
C2H4
+ 3O2
点燃
甲烷
乙烯
物质 乙烷 乙烯
碳碳键型 碳碳单键 碳碳双键
键 角 109?28ˊ 120°
键长(10-10m) 1.54 1.33
键能(kJ/mol) 348 615
(2)氧化反应:
紫红色褪去
乙烯被酸性KMnO4溶液氧化
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
将乙烯通入溴的四氯化碳溶液
溶液褪色
(3)加成反应:
——乙烯
3.烯烃的化学性质
CH2BrCH2Br
CH2 CH2
+ Br2
(3)加成反应:
——乙烯
3.烯烃的化学性质
CH3CH3
CH2 CH2
+ H2
Ni
?
CH3CH2OH
CH2 CH2
+ H2O
催化剂
?
CH3CH2Cl
CH2 CH2
+ HCl
催化剂
?
(4)加成聚合反应:
双键中的π键发生了断裂,相互间通过碳碳单键结合,形成了具有很长碳链的高分子化合物。
——乙烯
3.烯烃的化学性质
CH2 CH2
n CH2 CH2
催化剂
n
(4)加成聚合反应:
——乙烯
3.烯烃的化学性质
CH2 CH2
n CH2 CH2
催化剂
聚合度
单体
链节
n
i.烯烃能使酸性KMnO4溶液褪色。
ii.可燃性:?
含碳量高,燃烧时有黑烟。
在通常状况下,烯烃中的碳碳双键不稳定,易发生反应。
(1)氧化反应:
3.烯烃的化学性质
CnH2n + O2 n CO2 + nH2O
3n
2
点燃
(2)加成反应:
在一定条件下,烯烃能与H2 、 X2等发生加成反应。
3.烯烃的化学性质
R-CHBr-CH2Br
R-CH CH2
+ Br2
R-CH2-CH3
R-CH CH2
+ H2
Ni
?
实验证明:
顺-2-丁烯和反-2-丁烯都能和H2发生
加成反应,你认为生成的产物会有区别吗?
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
CH3CH2CH2CH3
+ H2
Ni
?
(2)加成反应:
注意:
不对称烯烃(或炔烃)与HX、H2O、HCN加成时,氢原子主要加在含氢较多的不饱和碳原子上;
在一定条件下,烯烃能与HX、 H2O等发生加成反应。
2 1
2 1
3.烯烃的化学性质
R-CH CH2
+ HCl
催化剂
?
或 R-CHCH3
Cl
R-CH CH2
+ H2O
催化剂
?
或 R-CHCH3
OH
Cl
R-CH2CH2
OH
R-CH2CH2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
1,2-加成
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
1,4-加成
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
Cl Cl
1,2-加成
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
Cl Cl
1,4-加成
1 mol 1, 3-丁二烯和
2 mol Cl2如何反应?
1,3-丁二烯
CH2 CH CH CH2
+2Cl2
CH2 CH CH CH2
Cl Cl
Cl Cl
1 mol 1, 3-丁二烯和
2 mol Cl2如何反应?
(3)加聚反应:
在一定条件下,烯烃可以发生加聚反应,生成高分子化合物。
3.烯烃的化学性质
C C
n
催化剂
C=C
R1
R2
R3
R4
R1
R3
R2
R4
n
氧化反应
加成反应
加聚反应
氧气
酸性高锰酸钾溶液
H2、X2、HX、H2O等
一定条件
归纳总结
取代反应
氯气,光照
烷烃
烯烃
下列既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的乙烯的方法是( )
A.通入溴的四氯化碳溶液
B.在导管口处点燃
C.通入酸性KMnO4溶液中
D.在一定条件下与氢气反应
A
反馈练习
下列物质中,不能使溴的四氯化碳溶液和高锰酸钾溶液褪色的是( )
A.C2H4 B. C3H6 C. C5H12 D. C4H8
C
符合CnH2n通式,Ω=1
存在碳碳双键的可能性
反馈练习
某单烯烃氢化后得到的饱和烃:
该单烯烃可能的结构有( )
A.1种 B.2种
C.3种 D.4种
C
●
●
●
●
▲
▲
★
想一想,哪种烯烃可以存在顺反异构呢?
拓展训练
基础作业
以原油为原料生产聚烯烃的几个步骤如下:
(1)第①步得到的烃类混合物中,只含有7种不同的物质吗?请举例。
(2)第②步反应中得到的丙烯,具有顺反异构现象吗?
(3)第③步发生了什么反应?请写出方程式。
原
油
C4 ~C10的
烃类混合物
烯烃
(如乙烯、
丙烯)
聚烯烃
(如聚乙烯、聚丙烯)
①
②
③
第二章 第一节 脂肪烃
——烷烃 烯烃
高二年级 化学
链状烃
环状烃
脂环烃
芳香烃
烃
烷 烃
烯 烃
炔 烃
脂肪烃
分子中
不含苯环的烃
分子式CxHy。
(含一个或多个苯环的烃)
一、烷烃
CH4
C
H
?
H
?
H
?
H
?
分子式
电子式
C
H
H
H
H
结构式
109o28?
正四面体
比例模型
球棍
模型
——甲烷
1.烷烃的结构
(1)烷烃碳原子间都以可旋转的单键相连接;
(2)直链烷烃碳原子不在一条直线上,空间结构是折线型或锯齿状;
(3)烷烃分子的通式:CnH2n+2(n≥1,正整数),又称为饱和烃。
乙烷
丙烷
正丁烷
1.烷烃的结构
名称 结构简式 常温时的状态 熔点/℃ 沸点/℃ 相对
密度
甲烷 CH4 气 -182.5 -161.5
乙烷 CH3CH3 气 -182.8 -88.6
丙烷 CH3CH2CH3 气 -188.0 -42.1 0.5005
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788
戊烷 CH3(CH2)3CH3 液 -129.7 36.0 0.5572
癸烷 CH3(CH2)8CH3 液 -29.7 174.1 0.7298
十七烷 CH3(CH2)15CH3 固 22.0 302.2 0.7767
①烷烃随着N(C)增加
相对分子质量增大
分子间作用力增大
熔沸点逐渐升高
2.烷烃的物理性质
气态
常温
液态
固态
由图示信息
你能得到哪些结论?
N(C)
T/℃
②分子式相同的不同烷烃,
名 称 熔点/℃ 沸点/℃
正丁烷 -138.4 -0.5
异丁烷 -159.6 -11.7
正戊烷 -129.8 36.1
异戊烷 -159.9 27.9
新戊烷 -19.5 9.5
C4H10
C5H12
2.烷烃的物理性质
支链越多,熔沸点越低。
③直链烷烃碳原子数的增加,
其密度增大。
烷烃都不溶于水,
且烷烃的密度比水的密度小。
2.烷烃的物理性质
(1)稳定性: 在通常状况下,性质很稳定,与酸、碱及其氧化物都不发生反应。
(2)可燃性:
——甲烷
3.烷烃的化学性质
(3)取代反应
——甲烷
3.烷烃的化学性质
(3)取代反应
——甲烷
3.烷烃的化学性质
(1)稳定性: 烷烃的化学性质与甲烷类似,通常较稳定,不能使KMnO4溶液褪色,不能跟强酸、强碱反应。
烷烃的物理性质呈规律性变化:
(2)可燃性:
3.烷烃的化学性质
(3)取代反应
烷烃是有机物的基础,是烃的衍生物的母体。所以掌握了烃的性质是学好有机化学的关键。
烷烃的物理性质呈规律性变化:
CH2ClCH2Cl 、 CH3CHCl2 二氯乙烷
CHCl2CH2Cl 、 CCl3CH3 三氯乙烷
CHCl2CHCl2、 CCl3CH2Cl 四氯乙烷
CCl3CHCl 2 和 CCl3CCl 3 五氯乙烷和六氯乙烷
3.烷烃的化学性质
CH3CH3 + Cl2 CH3CH2Cl + HCl
光照
下列烷烃的一氯代物中没有同分异构的是( )
A.2-甲基丙烷
B. 丙烷
C.正 丁烷
D. 乙烷
D
C
C—C—C
C—C—C
C—C—C—C
C—C
?
o
o
o
?
o
o
?
?
o
o
?
?
反馈练习
(4)裂化和裂解
催化裂化
催化裂解
3.烷烃的化学性质
二、烯烃
名称 乙烯
分子式 C2H4
电子式
结构式
结构简式
CH2=CH2
C = C
H
H
H
H
C C
H
H
H
H
乙烯分子中的碳原子发生sp2杂化与2个氢原子形成2个碳氢δ共价键。2个碳原子之间又各以一个sp2杂化轨道形成1个碳碳δ共价键,未参加杂化的p轨道形成1个π键, π键易断裂。
——乙烯
1.烯烃的结构
名称 乙烯
分子式 C2H4
电子式
结构式
结构简式
球棍模型
比例模型
乙烯的结构
CH2=CH2
C = C
H
H
H
H
C C
H
H
H
H
(1)烯烃分子中都含有碳碳双键,比相同碳数的烷烃少两个氢原子;
(2)烯烃分子的通式:CnH2n(n≥2,正整数)。
(3)烯烃中的碳碳双键是平面结构,决定至少6个原子共平面;
1.烯烃的结构
C=C
H
H
H
H
C=C
H
H
CH3
H
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
1
2 3 4
1 4
2 3
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
——顺反异构
1.烯烃的结构
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
——顺反异构
1.烯烃的结构
顺式结构:两个相同的原子或原子团排列在双键的同一侧;
反式结构:两个相同的原子或原子团分别排列在双键的两侧。
顺?2?丁烯
反?2?丁烯
——顺反异构
1.烯烃的结构
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
顺反异构的形成条件:
(1)具有碳碳双键;
(2)组成双键的每个碳原子上必须连接
两个不同的原子或原子团。
顺反异构体:
化学性质基本相同,物理性质有一定的差异。
——顺反异构
1.烯烃的结构
√顺
√反
典型例题
顺-2-戊烯
反-3-己烯
1 2
3 2
2 3
3 4
1 4 5
1 2
5 6
首先找双键,
竖切查看碳。横切看上下,
准确定顺反。
下列有机分子中,可形成顺反异构的是( )
A.CH2=CHCH3 B.CH2=CHCH2CH2
C.CH3CH=C(CH3)2 D.CH3CH=CHCl
D
反馈练习
①烯烃随着碳原子数的增加,
相对分子质量增大,
分子间作用力增大,
沸点(熔点)逐渐升高。
②分子式相同的不同烯烃,支链越多,熔沸点越低。
2.烯烃的物理性质
烷烃的物质性质具有递变性,
烯烃的物理性质也一样吗?
2.烯烃的物理性质
烷烃的物质性质具有递变性,
烯烃的物理性质也一样吗?
③烯烃碳原子数的增加,
烯烃的密度增大。
烯烃都不溶于水,
且烯烃的密度比水的密度小。
直链烯烃相对密度
(1)可燃性:
火焰明亮,少量黒烟
——乙烯
3.烯烃的化学性质
2CO2 +2H2O
C2H4
+ 3O2
点燃
甲烷
乙烯
物质 乙烷 乙烯
碳碳键型 碳碳单键 碳碳双键
键 角 109?28ˊ 120°
键长(10-10m) 1.54 1.33
键能(kJ/mol) 348 615
(2)氧化反应:
紫红色褪去
乙烯被酸性KMnO4溶液氧化
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
(3)加成反应:
——乙烯
3.烯烃的化学性质
将乙烯通入溴的四氯化碳溶液
溶液褪色
(3)加成反应:
——乙烯
3.烯烃的化学性质
CH2BrCH2Br
CH2 CH2
+ Br2
(3)加成反应:
——乙烯
3.烯烃的化学性质
CH3CH3
CH2 CH2
+ H2
Ni
?
CH3CH2OH
CH2 CH2
+ H2O
催化剂
?
CH3CH2Cl
CH2 CH2
+ HCl
催化剂
?
(4)加成聚合反应:
双键中的π键发生了断裂,相互间通过碳碳单键结合,形成了具有很长碳链的高分子化合物。
——乙烯
3.烯烃的化学性质
CH2 CH2
n CH2 CH2
催化剂
n
(4)加成聚合反应:
——乙烯
3.烯烃的化学性质
CH2 CH2
n CH2 CH2
催化剂
聚合度
单体
链节
n
i.烯烃能使酸性KMnO4溶液褪色。
ii.可燃性:?
含碳量高,燃烧时有黑烟。
在通常状况下,烯烃中的碳碳双键不稳定,易发生反应。
(1)氧化反应:
3.烯烃的化学性质
CnH2n + O2 n CO2 + nH2O
3n
2
点燃
(2)加成反应:
在一定条件下,烯烃能与H2 、 X2等发生加成反应。
3.烯烃的化学性质
R-CHBr-CH2Br
R-CH CH2
+ Br2
R-CH2-CH3
R-CH CH2
+ H2
Ni
?
实验证明:
顺-2-丁烯和反-2-丁烯都能和H2发生
加成反应,你认为生成的产物会有区别吗?
C=C
H3C
H
CH3
H
C=C
H3C
H
H
CH3
CH3CH2CH2CH3
+ H2
Ni
?
(2)加成反应:
注意:
不对称烯烃(或炔烃)与HX、H2O、HCN加成时,氢原子主要加在含氢较多的不饱和碳原子上;
在一定条件下,烯烃能与HX、 H2O等发生加成反应。
2 1
2 1
3.烯烃的化学性质
R-CH CH2
+ HCl
催化剂
?
或 R-CHCH3
Cl
R-CH CH2
+ H2O
催化剂
?
或 R-CHCH3
OH
Cl
R-CH2CH2
OH
R-CH2CH2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
1,2-加成
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
CH2 CH CH CH2
1 2 3 4
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
Cl Cl
1,4-加成
1,3-丁二烯
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
Cl Cl
1,2-加成
CH2 CH CH CH2
+ Cl2
CH2 CH CH CH2
Cl Cl
1,4-加成
1 mol 1, 3-丁二烯和
2 mol Cl2如何反应?
1,3-丁二烯
CH2 CH CH CH2
+2Cl2
CH2 CH CH CH2
Cl Cl
Cl Cl
1 mol 1, 3-丁二烯和
2 mol Cl2如何反应?
(3)加聚反应:
在一定条件下,烯烃可以发生加聚反应,生成高分子化合物。
3.烯烃的化学性质
C C
n
催化剂
C=C
R1
R2
R3
R4
R1
R3
R2
R4
n
氧化反应
加成反应
加聚反应
氧气
酸性高锰酸钾溶液
H2、X2、HX、H2O等
一定条件
归纳总结
取代反应
氯气,光照
烷烃
烯烃
下列既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的乙烯的方法是( )
A.通入溴的四氯化碳溶液
B.在导管口处点燃
C.通入酸性KMnO4溶液中
D.在一定条件下与氢气反应
A
反馈练习
下列物质中,不能使溴的四氯化碳溶液和高锰酸钾溶液褪色的是( )
A.C2H4 B. C3H6 C. C5H12 D. C4H8
C
符合CnH2n通式,Ω=1
存在碳碳双键的可能性
反馈练习
某单烯烃氢化后得到的饱和烃:
该单烯烃可能的结构有( )
A.1种 B.2种
C.3种 D.4种
C
●
●
●
●
▲
▲
★
想一想,哪种烯烃可以存在顺反异构呢?
拓展训练
基础作业
以原油为原料生产聚烯烃的几个步骤如下:
(1)第①步得到的烃类混合物中,只含有7种不同的物质吗?请举例。
(2)第②步反应中得到的丙烯,具有顺反异构现象吗?
(3)第③步发生了什么反应?请写出方程式。
原
油
C4 ~C10的
烃类混合物
烯烃
(如乙烯、
丙烯)
聚烯烃
(如聚乙烯、聚丙烯)
①
②
③
