2.2 芳香烃-天津市2020年空中课堂人教版高中化学选修五课件(共24张PPT)
文档属性
| 名称 | 2.2 芳香烃-天津市2020年空中课堂人教版高中化学选修五课件(共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 18.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-19 00:00:00 | ||
图片预览



文档简介
(共24张PPT)
芳 香 烃
高二年级 化学
第 二 章 第 二 节
《芳香烃》学习目标
①能清晰区分苯的同系物、芳香烃、芳香族化合物
②能掌握苯和苯的同系物的结构及其化学性质
③能分析苯的同系物的结构对化学性质的影响
④能简单了解芳香烃的来源及其应用
含有一个或多个苯环的碳氢化合物
芳香 烃
最简单 最基本的芳香烃-----苯
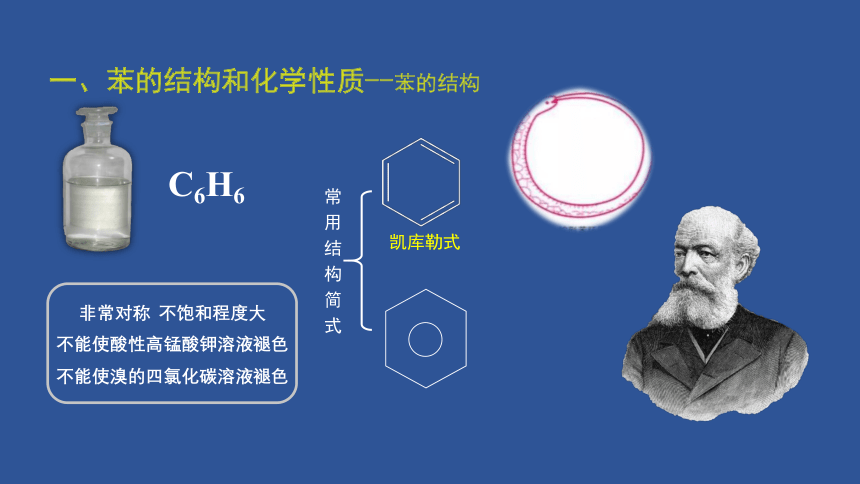
一、苯的结构和化学性质--苯的结构
C6H6
凯库勒式
常用结构简式
非常对称 不饱和程度大
不能使酸性高锰酸钾溶液褪色
不能使溴的四氯化碳溶液褪色
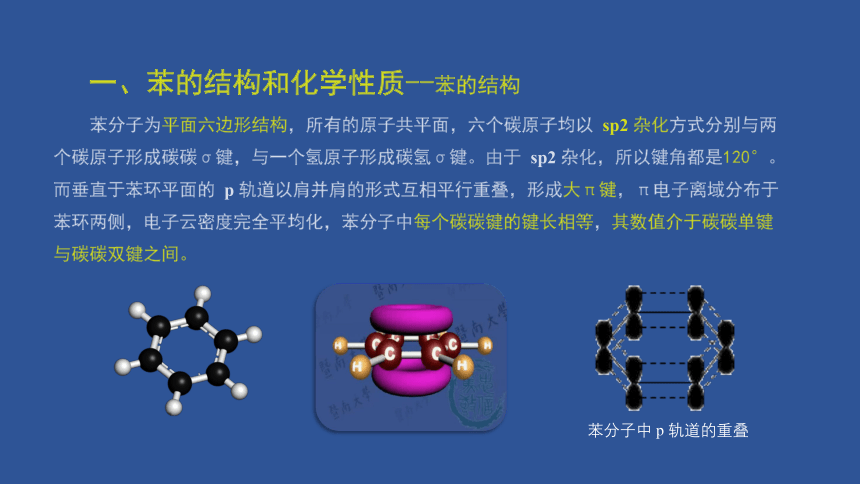
苯分子为平面六边形结构,所有的原子共平面,六个碳原子均以 sp2 杂化方式分别与两个碳原子形成碳碳σ键,与一个氢原子形成碳氢σ键。由于 sp2 杂化,所以键角都是120°。而垂直于苯环平面的 p 轨道以肩并肩的形式互相平行重叠,形成大π键,π电子离域分布于苯环两侧,电子云密度完全平均化,苯分子中每个碳碳键的键长相等,其数值介于碳碳单键与碳碳双键之间。
一、苯的结构和化学性质--苯的结构
苯分子中 p 轨道的重叠
催化剂
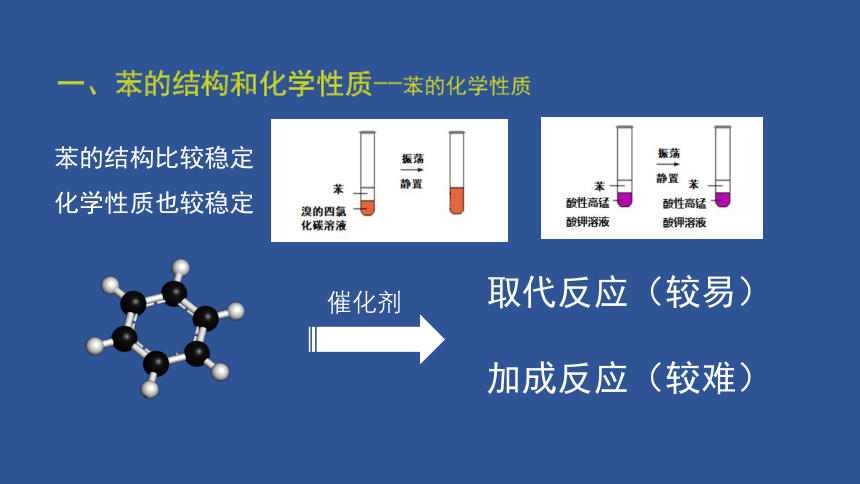
取代反应(较易)
加成反应(较难)
苯的结构比较稳定化学性质也较稳定
一、苯的结构和化学性质--苯的化学性质
苯的氧化反应:在空气中燃烧
2C6H6+15O2 12CO2+ 6H2O
点燃
一、苯的结构和化学性质--苯的化学性质
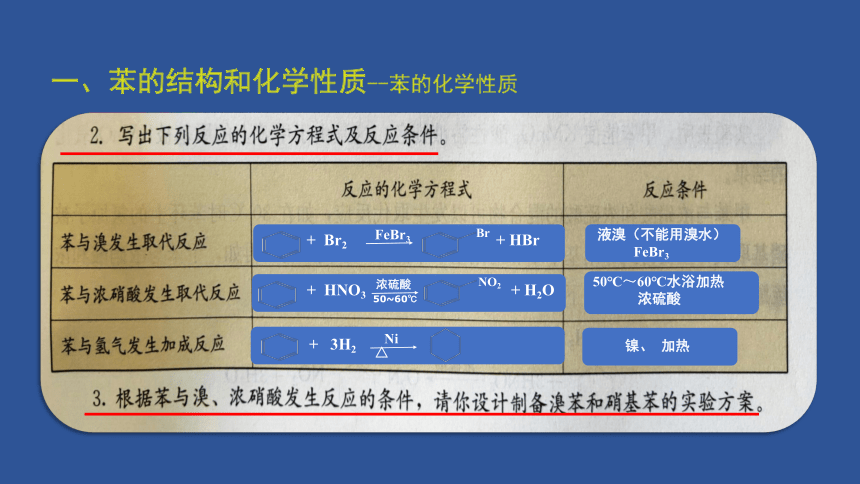
一、苯的结构和化学性质--苯的化学性质
+ Br2 + HBr
FeBr3
Br
+ HNO3 + H2O
浓硫酸
NO2
50~60℃
+ 3H2
Ni
△
液溴(不能用溴水)
FeBr3
50℃~60℃水浴加热
浓硫酸
镍、 加热
+ Br2
Br
+ HBr
FeBr3
反应物状态
反应的条件
产物的性质
苯 液溴 溴化铁
溴苯
硝酸银溶液
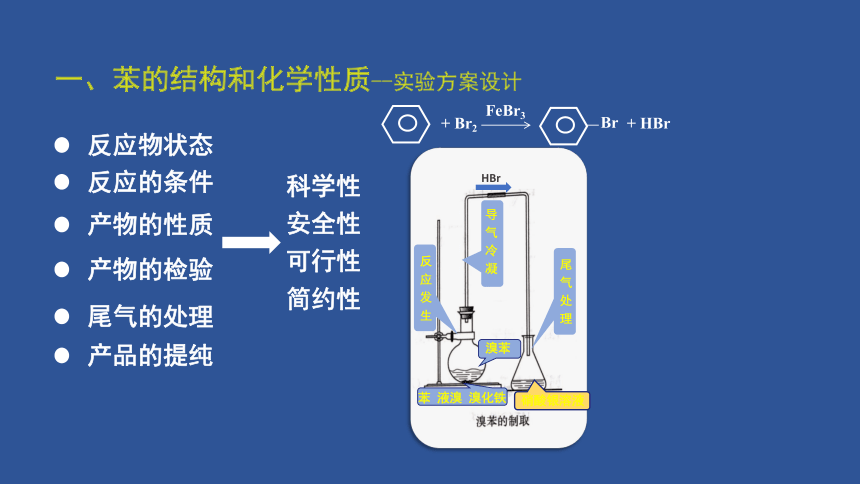
一、苯的结构和化学性质--实验方案设计
产物的检验
尾气的处理
科学性
安全性
可行性
简约性
HBr
反应发生
尾气处理
导气冷凝
产品的提纯
一、苯的结构和化学性质--实验方案设计
实验现象
反应中,导管口附近出现白雾,由溴化氢遇水蒸气所形成。反应完毕后,向锥形瓶内的液体里滴入硝酸银溶液,有浅黄色溴化银沉淀生成。所产生的溴苯是密度比水大的无色液体,实验中由于溶解了溴而显褐色。
溴
化
铁
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
50~60℃
温度计
水浴
苯和混酸
一、苯的结构和化学性质--实验方案设计
反应物状态
反应条件
产物的性质
性质的检验
尾气的处理
科学性
安全性
可行性
简约性
产品的分离
一、苯的结构和化学性质--实验方案设计
实验现象
试管中有黄色油状物质生成,硝基苯密度比水的大在下层,纯硝基苯无色、具有苦杏仁味,实验中由于溶解了 NO2而呈黄色。
一、苯的结构和化学性质--实验方案设计
产品提纯
粗产品依次用蒸馏水和5%的氢氧化钠溶液洗涤,然后再用蒸馏水洗涤,用无水氯化钙干燥后再蒸馏,可得纯硝基苯。
1.下列物质中,在一定条件下既能发生加成反应,又能发生取代反
应,但不能使酸性 KMnO4 溶液褪色的是
A . 甲烷 B . 乙烯 C . 乙炔 D . 苯
一、苯的结构和化学性质--练一练
2. 苯可发生如图所示的变化,下列说法不正确的是
A.现象①:液体分层,下层紫红色
B.现象②:火焰明亮,冒浓烟
C.溴苯的密度比水的大
D.间二硝基苯只有一种,说明苯分子中
不存在碳碳单键和碳碳双键交替出现的结构
D
D
×
Br
NO2
NO2
浓硫酸,浓硝酸
△
点燃
液溴
催化剂
KMnO4/H+
现象①
现象②
苯的同系物 CnH2n-6(n≥6):
只含一个苯环且苯环上的氢原子被烷烃基取代的产物
甲苯
乙苯
二、苯的同系物--苯的同系物定义
间二甲苯
苯乙烯
(芳香烃)
CH3
|
CH2CH3
|
CH3
|
CH3
二、苯的同系物--苯的同系物定义
Br
|
COOH
|
CH=CH2
|
CH3
|
CH3
|
CH3
苯的同系物
芳香烃
芳香族化合物
crystal:
二、苯的同系物--化学性质
②
三硝基甲苯是一种淡黄色的晶体,不溶于水,不稳定,易爆炸。它是一种烈性炸药,广泛应用于国防、开矿、筑路、兴修水利等。
③
CH3
|
NO2
|
NO2
CH3
|
O2N
+ 3HO-NO2
+ 3H2O
浓硫酸
Δ
2,4,6—三硝基甲苯
(TNT)
与溴、硝酸取代
与氢气加成
与卤素取代
①
甲基的存在活化了苯环上的氢
+3 H2
△
Ni
CH3
|
CH3
|
卤素单质
FeBr3
取代烷烃基上的氢
取代苯环上的氢
+
CH3
|
光照
CH3
|
二、苯的同系物--化学性质
CH3
|
—C—CH3
|
CH3
×
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
二、苯的同系物--化学性质
④
说 明
①无论烷烃基的碳数为多少,最后均被氧化成羧基
②苯环相邻碳上没有α氢的则不能被氧化,即不能使高锰酸钾溶液褪色。
COOH
|
CH3
|
KMnO4/H+
CH2CH3
|
COOH
|
KMnO4/H+
KMnO4/H+
KMnO4/H+
2.选择什么试剂鉴别己烯和甲苯?
1.下列化合物为苯的同系物的是??????????????????
A.①② B.③④ C.①④ D.②④
B
溴的四氯化碳溶液
二、苯的同系物--练一练
CH3
①
②
CH=CH2
③
CH2CHCH3
|
CH3
④
CH3
CH2CH3
煤的干馏
石油的催化重整
三、芳香烃的来源及其应用
很长时间里煤是一切芳香烃的主要来源,至20世纪40年代以来,随着石油化学工业的发展,通过石油化学工业中的催化重整等工艺可以获得芳香烃。一些简单的芳香烃,如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等。
来源
炸药
染料
药品
农药
应用
小 结
一、苯的结构与化学性质
二、苯的同系物
苯与溴的取代
苯与硝酸的取代
苯与氢气的加成
甲苯与溴的取代
甲苯与硝酸的取代
甲苯与氢气的加成
甲苯被酸性高锰酸钾氧化
三、芳香烃的来源
及其应用
①阅读教材 P39,了解“稠环芳香烃”
②查阅资料,了解苯及其同系物对人体健康的危害,
提出使用苯时如何防止苯中毒的注意事项
③完成教材 P40习题
作 业
爱化学,爱生活
在生活中找寻化学,用化学美化生活
同 学 们 再 见
芳 香 烃
高二年级 化学
第 二 章 第 二 节
《芳香烃》学习目标
①能清晰区分苯的同系物、芳香烃、芳香族化合物
②能掌握苯和苯的同系物的结构及其化学性质
③能分析苯的同系物的结构对化学性质的影响
④能简单了解芳香烃的来源及其应用
含有一个或多个苯环的碳氢化合物
芳香 烃
最简单 最基本的芳香烃-----苯
一、苯的结构和化学性质--苯的结构
C6H6
凯库勒式
常用结构简式
非常对称 不饱和程度大
不能使酸性高锰酸钾溶液褪色
不能使溴的四氯化碳溶液褪色
苯分子为平面六边形结构,所有的原子共平面,六个碳原子均以 sp2 杂化方式分别与两个碳原子形成碳碳σ键,与一个氢原子形成碳氢σ键。由于 sp2 杂化,所以键角都是120°。而垂直于苯环平面的 p 轨道以肩并肩的形式互相平行重叠,形成大π键,π电子离域分布于苯环两侧,电子云密度完全平均化,苯分子中每个碳碳键的键长相等,其数值介于碳碳单键与碳碳双键之间。
一、苯的结构和化学性质--苯的结构
苯分子中 p 轨道的重叠
催化剂
取代反应(较易)
加成反应(较难)
苯的结构比较稳定化学性质也较稳定
一、苯的结构和化学性质--苯的化学性质
苯的氧化反应:在空气中燃烧
2C6H6+15O2 12CO2+ 6H2O
点燃
一、苯的结构和化学性质--苯的化学性质
一、苯的结构和化学性质--苯的化学性质
+ Br2 + HBr
FeBr3
Br
+ HNO3 + H2O
浓硫酸
NO2
50~60℃
+ 3H2
Ni
△
液溴(不能用溴水)
FeBr3
50℃~60℃水浴加热
浓硫酸
镍、 加热
+ Br2
Br
+ HBr
FeBr3
反应物状态
反应的条件
产物的性质
苯 液溴 溴化铁
溴苯
硝酸银溶液
一、苯的结构和化学性质--实验方案设计
产物的检验
尾气的处理
科学性
安全性
可行性
简约性
HBr
反应发生
尾气处理
导气冷凝
产品的提纯
一、苯的结构和化学性质--实验方案设计
实验现象
反应中,导管口附近出现白雾,由溴化氢遇水蒸气所形成。反应完毕后,向锥形瓶内的液体里滴入硝酸银溶液,有浅黄色溴化银沉淀生成。所产生的溴苯是密度比水大的无色液体,实验中由于溶解了溴而显褐色。
溴
化
铁
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
50~60℃
温度计
水浴
苯和混酸
一、苯的结构和化学性质--实验方案设计
反应物状态
反应条件
产物的性质
性质的检验
尾气的处理
科学性
安全性
可行性
简约性
产品的分离
一、苯的结构和化学性质--实验方案设计
实验现象
试管中有黄色油状物质生成,硝基苯密度比水的大在下层,纯硝基苯无色、具有苦杏仁味,实验中由于溶解了 NO2而呈黄色。
一、苯的结构和化学性质--实验方案设计
产品提纯
粗产品依次用蒸馏水和5%的氢氧化钠溶液洗涤,然后再用蒸馏水洗涤,用无水氯化钙干燥后再蒸馏,可得纯硝基苯。
1.下列物质中,在一定条件下既能发生加成反应,又能发生取代反
应,但不能使酸性 KMnO4 溶液褪色的是
A . 甲烷 B . 乙烯 C . 乙炔 D . 苯
一、苯的结构和化学性质--练一练
2. 苯可发生如图所示的变化,下列说法不正确的是
A.现象①:液体分层,下层紫红色
B.现象②:火焰明亮,冒浓烟
C.溴苯的密度比水的大
D.间二硝基苯只有一种,说明苯分子中
不存在碳碳单键和碳碳双键交替出现的结构
D
D
×
Br
NO2
NO2
浓硫酸,浓硝酸
△
点燃
液溴
催化剂
KMnO4/H+
现象①
现象②
苯的同系物 CnH2n-6(n≥6):
只含一个苯环且苯环上的氢原子被烷烃基取代的产物
甲苯
乙苯
二、苯的同系物--苯的同系物定义
间二甲苯
苯乙烯
(芳香烃)
CH3
|
CH2CH3
|
CH3
|
CH3
二、苯的同系物--苯的同系物定义
Br
|
COOH
|
CH=CH2
|
CH3
|
CH3
|
CH3
苯的同系物
芳香烃
芳香族化合物
crystal:
二、苯的同系物--化学性质
②
三硝基甲苯是一种淡黄色的晶体,不溶于水,不稳定,易爆炸。它是一种烈性炸药,广泛应用于国防、开矿、筑路、兴修水利等。
③
CH3
|
NO2
|
NO2
CH3
|
O2N
+ 3HO-NO2
+ 3H2O
浓硫酸
Δ
2,4,6—三硝基甲苯
(TNT)
与溴、硝酸取代
与氢气加成
与卤素取代
①
甲基的存在活化了苯环上的氢
+3 H2
△
Ni
CH3
|
CH3
|
卤素单质
FeBr3
取代烷烃基上的氢
取代苯环上的氢
+
CH3
|
光照
CH3
|
二、苯的同系物--化学性质
CH3
|
—C—CH3
|
CH3
×
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
二、苯的同系物--化学性质
④
说 明
①无论烷烃基的碳数为多少,最后均被氧化成羧基
②苯环相邻碳上没有α氢的则不能被氧化,即不能使高锰酸钾溶液褪色。
COOH
|
CH3
|
KMnO4/H+
CH2CH3
|
COOH
|
KMnO4/H+
KMnO4/H+
KMnO4/H+
2.选择什么试剂鉴别己烯和甲苯?
1.下列化合物为苯的同系物的是??????????????????
A.①② B.③④ C.①④ D.②④
B
溴的四氯化碳溶液
二、苯的同系物--练一练
CH3
①
②
CH=CH2
③
CH2CHCH3
|
CH3
④
CH3
CH2CH3
煤的干馏
石油的催化重整
三、芳香烃的来源及其应用
很长时间里煤是一切芳香烃的主要来源,至20世纪40年代以来,随着石油化学工业的发展,通过石油化学工业中的催化重整等工艺可以获得芳香烃。一些简单的芳香烃,如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等。
来源
炸药
染料
药品
农药
应用
小 结
一、苯的结构与化学性质
二、苯的同系物
苯与溴的取代
苯与硝酸的取代
苯与氢气的加成
甲苯与溴的取代
甲苯与硝酸的取代
甲苯与氢气的加成
甲苯被酸性高锰酸钾氧化
三、芳香烃的来源
及其应用
①阅读教材 P39,了解“稠环芳香烃”
②查阅资料,了解苯及其同系物对人体健康的危害,
提出使用苯时如何防止苯中毒的注意事项
③完成教材 P40习题
作 业
爱化学,爱生活
在生活中找寻化学,用化学美化生活
同 学 们 再 见
