3.2醛-天津市2020年空中课堂人教版高中化学选修五课件(共35张PPT)
文档属性
| 名称 | 3.2醛-天津市2020年空中课堂人教版高中化学选修五课件(共35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-19 00:00:00 | ||
图片预览






文档简介
(共35张PPT)
第三章 烃的含氧衍生物
醛
高二年级 化学
学习目标:
能写出醛的官能团、乙醛的结构简式和名称;能够列举醛的典型代表物—乙醛的主要物理性质、重要反应,书写相应的反应式。
能基于官能团、化学键的特点与反应规律分析和推断含有醛基官能团的有机化合物的化学性质。根据信息书写相应的反应式。
用甲醛等合成的黏合剂制作的压层板
甲醛的水溶液(又称福尔马林)具有杀菌、防腐性能等
C
O
H
CH=CH
C
O
H
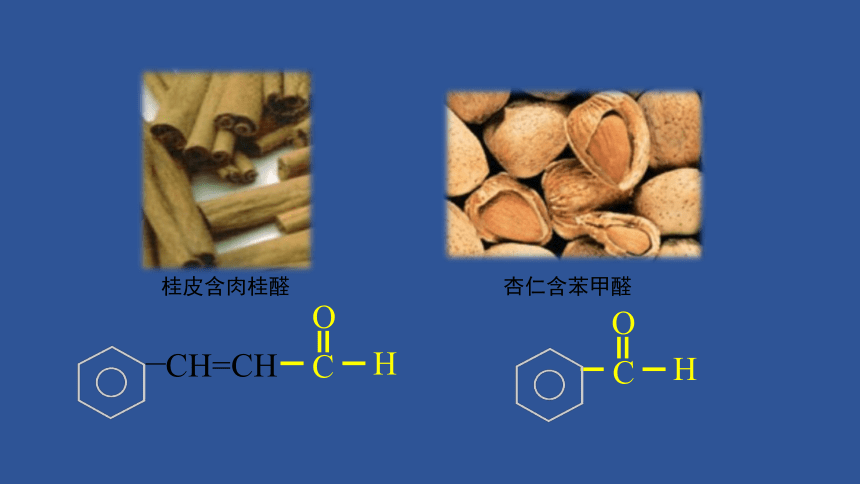
桂皮含肉桂醛
杏仁含苯甲醛
醛是由烃基(或氢原子)与醛基(-CHO)相连而构成的化合物。
简写为R—CHO
一、乙醛的物理性质
乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点是20.8℃ ,易挥发,易燃烧,能跟水、乙醇等互溶。
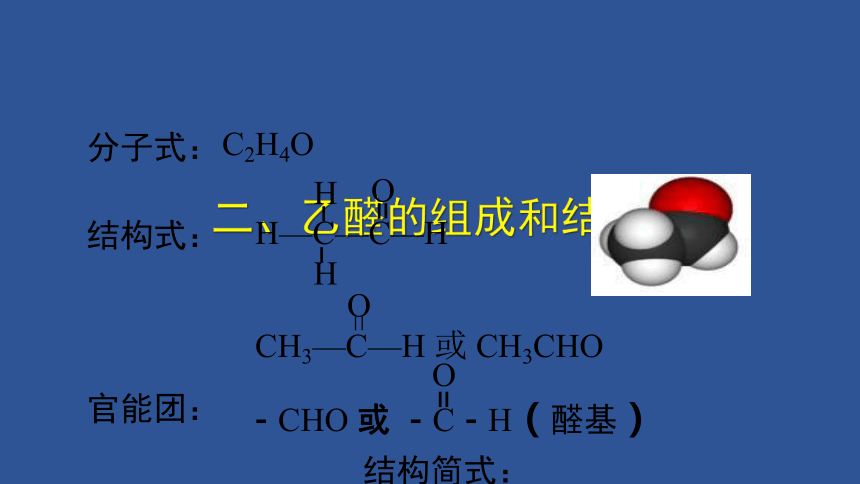
二、乙醛的组成和结构
结构简式:
C2H4O
H
H—C—C—H
H
-CHO 或 -C-H(醛基)
官能团:
O
CH3—C—H 或 CH3CHO
分子式:
结构式:
O
O
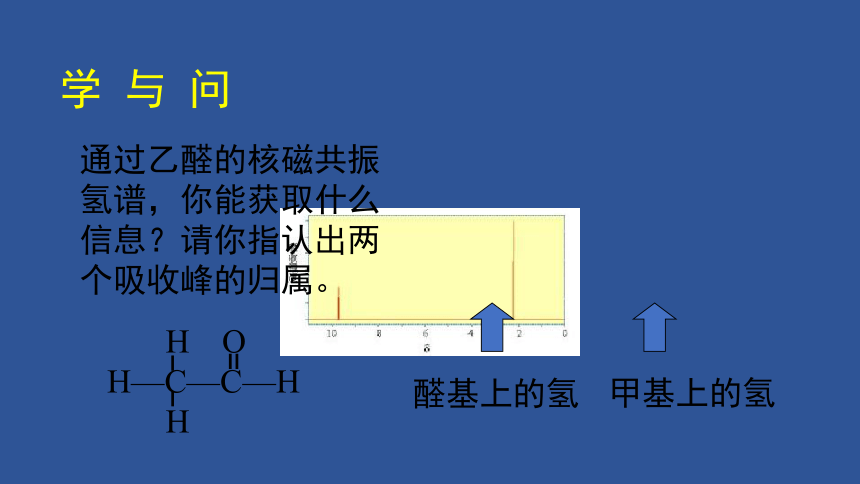
醛基上的氢
甲基上的氢
学 与 问
通过乙醛的核磁共振氢谱,你能获取什么信息?请你指认出两个吸收峰的归属。
H
H—C—C—H
H
O
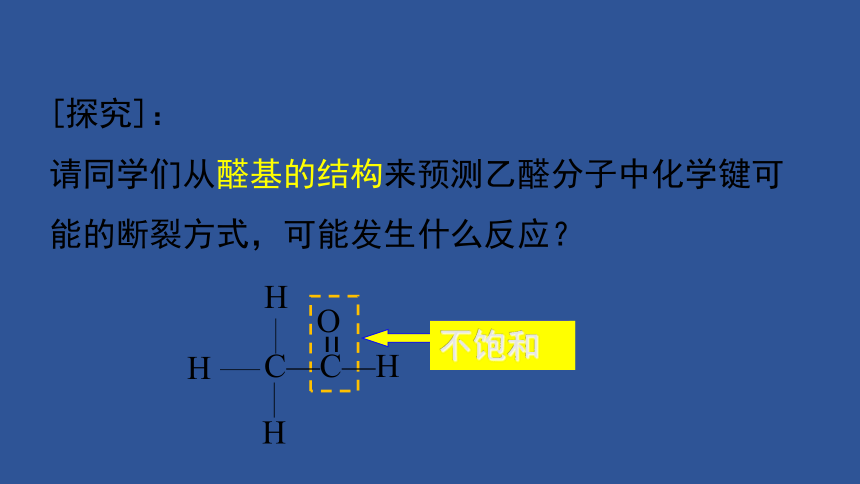
[探究]:
请同学们从醛基的结构来预测乙醛分子中化学键可能的断裂方式,可能发生什么反应?
C—C—H
不饱和
O
H
H
H
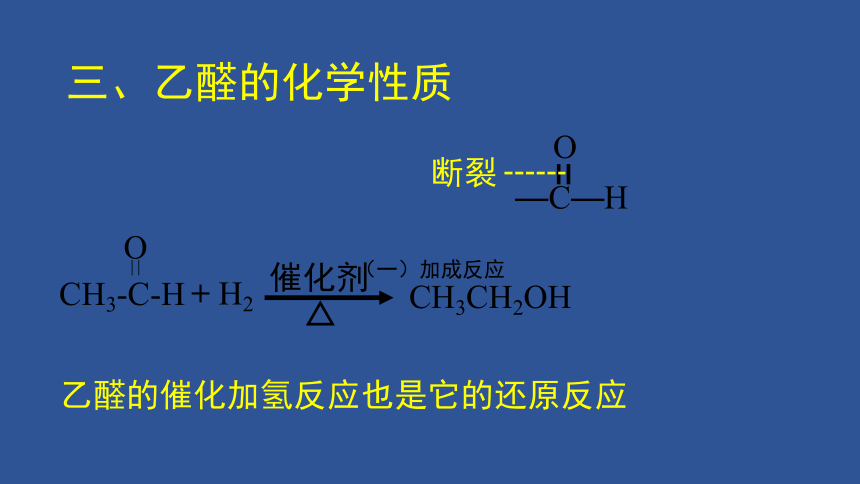
(一)加成反应
催化剂
CH3CH2OH
CH3-C-H
+ H2
断裂
乙醛的催化加氢反应也是它的还原反应
O
—C—H
O
三、乙醛的化学性质
[探究]:
请同学们从醛基的结构来预测乙醛分子中化学键的其他断裂方式,可能发生什么反应?
CH3—C—H
O
H C O
H C OH
H C OH
H C OH
H C OH
H C OH
H
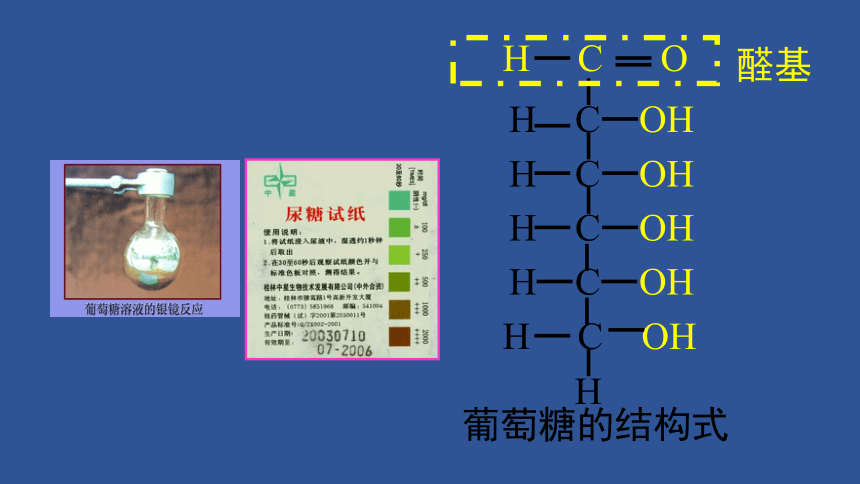
葡萄糖的结构式
醛基
(二)氧化反应
1. 与银氨溶液反应
(实验3一5)
观看实验视频
(银镜反应)
AgNO3 + NH3·H2O = AgOH↓+ NH4NO3
AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O
氢氧化二氨合银
白色沉淀
(1)配制银氨溶液
(2)银镜反应
CH3CHO + Ag(NH3)2OH
弱氧化剂
还原剂
+ Ag↓
+ H2O
+
CH3COOH
+1
0
2
2
CH3COONH4
3
NH3
H3C—C—OH
氧化反应
O
H3C—C—H
O
O
(3)实验注意事项
①实验前:清洗试管——热NaOH溶液洗,再水洗
②银氨溶液现配,因为久置会产生爆炸物质
③滴加稀氨水至沉淀刚好溶解为止,不能过量
④水浴加热,不能直接加热煮沸,加热时不能振
荡或摇动试管
⑤实验后,试管内壁附着的银如何清除及回收?
请同学们结合你所学习的知识,找出既科学又环保的方法。
(4)应用
①检验醛基的存在
③工业上用来制瓶胆和镜子
②测定醛基的数目
R-CHO~2Ag
2.与新制氢氧化铜反应: (实验3一6)
观看实验视频
蓝色絮状沉淀
红色沉淀
Cu2O↓
(1)实验
2 mL
4滴
现象:
试管内有红色沉淀产生
CH3CHO+ Cu(OH)2 →
弱氧化剂
还原剂
碱过量
(2)原理分析
+1
+2
+ NaOH
CH3COOH
+ H2O
+ Cu2O↓
CH3COONa
2
3
(3)注意事项
氢氧化铜一定要新制;呈絮状;碱一定要过量
②加热不能太久,否则会有黑色(CuO)沉淀生成
Cu(OH)2 = CuO + H2O
①
①检验醛基的存在
③医学上测定患者血液或尿液中的葡萄糖含量,
诊断患者的病情
(4)应用
RCHO~2Cu(OH)2~Cu2O
②测定醛基的数目
3. 催化氧化
+ O2 2CH3COOH
催化剂
△
2CH3CHO
H3C—C—OH
氧化反应
乙醛在氧化剂的作用下加入了氧原子被氧化为乙酸,发生的是氧化反应。
O
H3C—C—H
O
【思考】乙醛和高锰酸钾酸性溶液反应吗?
可能观察到哪些现象?
使KMnO4酸性溶液褪色
4.与强氧化剂的反应
能
四、甲醛
1. 分子结构
(1)分子式:CH2O
(2)结构式:
H一C一H
(3)结构简式:HCHO
O
甲醛分子中相当于含有两个醛基
2. 物理性质:
无色、有刺激性气味的气体,易溶于水。
甲醛的水溶液又称福尔马林,具有杀菌、防腐性能等。
反馈练习
HCHO发生银镜反应的化学方程式
HCHO +4Ag(NH3)2OH
+ 4 Ag↓
2H2O
+6NH3
+(NH4)2CO3
H一C一H
O
H—O—C—O—H
O
即:H2CO3
CH3CH2CHO和新制Cu(OH)2反应的化学方程式
CH3CH2CHO+2Cu(OH)2+NaOH → CH3CH2COONa
+Cu2O↓+3H2O
反馈练习
反馈练习
CH3CH(CH3)CH2OH是某有机化合物M的加氢
还原产物,该有机化合物M可能是( )
A. 乙醛的同系物 B. 丙醛的同分异构体
C. CH3CH(CH3)CCH3 D. CH3CH2CH2CHO
A
—CHO
O
反馈练习
从甜橙的芳香油中分离得如图结构的化合物:
现有试剂:①KMnO4酸性溶液 ②H2/Ni
③Ag(NH3)2OH溶液 ④新制Cu(OH)2悬浊液
能与该化合物中所有官能团都发生反应的试剂有( )
A.①② B.②③
C.③④ D.①④
A
思考与交流
某有机物的结构简式为CH2=CHCHCHO,
CH3
A. 该有机物与甲醛互为同系物
B. 在加热和催化剂作用下加氢,每摩尔该有机物最多能消耗3 mol H2
C. 一定条件下,该有机物能发生氧化、还原、酯化等反应
D.从理论上说,84 g该有机物能从足量银氨溶液中还原出216 g的银
D
R—CHO 2Ag
~
84 g
216 g
下列对其化学性质的判断中,正确的是( )。
2
本节课你学到了什么?
乙醛的
物理性质
乙醛的结构
乙醛的
化学性质
氧化反应和还原反应
无色、有刺激性气味的液体
密度比水的小
能与水、乙醇等互溶
醛基 :
C
H
O
CH3
2.乙醛的氧化反应
b.催化氧化
a.被弱氧化剂氧化
Ⅱ.被新制Cu(OH)2氧化反应
Ⅰ.被银氨溶液氧化
c.被强氧化剂氧化:
能使KMnO4酸性溶液褪色
小结:乙醛的化学性质
1.加成反应(还原反应) 与H2发生加成反应
1.书后习题P59 —1、2、3、4
课 后 作 业
2.甲醛是一种重要的化工原料,用途十分广泛。但是使用不当会有害于人体健康。请以“甲醛”为关键词,在Internet网上搜索资料,根据资料写一篇如何安全使用甲醛的短文。
第三章 烃的含氧衍生物
醛
高二年级 化学
学习目标:
能写出醛的官能团、乙醛的结构简式和名称;能够列举醛的典型代表物—乙醛的主要物理性质、重要反应,书写相应的反应式。
能基于官能团、化学键的特点与反应规律分析和推断含有醛基官能团的有机化合物的化学性质。根据信息书写相应的反应式。
用甲醛等合成的黏合剂制作的压层板
甲醛的水溶液(又称福尔马林)具有杀菌、防腐性能等
C
O
H
CH=CH
C
O
H
桂皮含肉桂醛
杏仁含苯甲醛
醛是由烃基(或氢原子)与醛基(-CHO)相连而构成的化合物。
简写为R—CHO
一、乙醛的物理性质
乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点是20.8℃ ,易挥发,易燃烧,能跟水、乙醇等互溶。
二、乙醛的组成和结构
结构简式:
C2H4O
H
H—C—C—H
H
-CHO 或 -C-H(醛基)
官能团:
O
CH3—C—H 或 CH3CHO
分子式:
结构式:
O
O
醛基上的氢
甲基上的氢
学 与 问
通过乙醛的核磁共振氢谱,你能获取什么信息?请你指认出两个吸收峰的归属。
H
H—C—C—H
H
O
[探究]:
请同学们从醛基的结构来预测乙醛分子中化学键可能的断裂方式,可能发生什么反应?
C—C—H
不饱和
O
H
H
H
(一)加成反应
催化剂
CH3CH2OH
CH3-C-H
+ H2
断裂
乙醛的催化加氢反应也是它的还原反应
O
—C—H
O
三、乙醛的化学性质
[探究]:
请同学们从醛基的结构来预测乙醛分子中化学键的其他断裂方式,可能发生什么反应?
CH3—C—H
O
H C O
H C OH
H C OH
H C OH
H C OH
H C OH
H
葡萄糖的结构式
醛基
(二)氧化反应
1. 与银氨溶液反应
(实验3一5)
观看实验视频
(银镜反应)
AgNO3 + NH3·H2O = AgOH↓+ NH4NO3
AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O
氢氧化二氨合银
白色沉淀
(1)配制银氨溶液
(2)银镜反应
CH3CHO + Ag(NH3)2OH
弱氧化剂
还原剂
+ Ag↓
+ H2O
+
CH3COOH
+1
0
2
2
CH3COONH4
3
NH3
H3C—C—OH
氧化反应
O
H3C—C—H
O
O
(3)实验注意事项
①实验前:清洗试管——热NaOH溶液洗,再水洗
②银氨溶液现配,因为久置会产生爆炸物质
③滴加稀氨水至沉淀刚好溶解为止,不能过量
④水浴加热,不能直接加热煮沸,加热时不能振
荡或摇动试管
⑤实验后,试管内壁附着的银如何清除及回收?
请同学们结合你所学习的知识,找出既科学又环保的方法。
(4)应用
①检验醛基的存在
③工业上用来制瓶胆和镜子
②测定醛基的数目
R-CHO~2Ag
2.与新制氢氧化铜反应: (实验3一6)
观看实验视频
蓝色絮状沉淀
红色沉淀
Cu2O↓
(1)实验
2 mL
4滴
现象:
试管内有红色沉淀产生
CH3CHO+ Cu(OH)2 →
弱氧化剂
还原剂
碱过量
(2)原理分析
+1
+2
+ NaOH
CH3COOH
+ H2O
+ Cu2O↓
CH3COONa
2
3
(3)注意事项
氢氧化铜一定要新制;呈絮状;碱一定要过量
②加热不能太久,否则会有黑色(CuO)沉淀生成
Cu(OH)2 = CuO + H2O
①
①检验醛基的存在
③医学上测定患者血液或尿液中的葡萄糖含量,
诊断患者的病情
(4)应用
RCHO~2Cu(OH)2~Cu2O
②测定醛基的数目
3. 催化氧化
+ O2 2CH3COOH
催化剂
△
2CH3CHO
H3C—C—OH
氧化反应
乙醛在氧化剂的作用下加入了氧原子被氧化为乙酸,发生的是氧化反应。
O
H3C—C—H
O
【思考】乙醛和高锰酸钾酸性溶液反应吗?
可能观察到哪些现象?
使KMnO4酸性溶液褪色
4.与强氧化剂的反应
能
四、甲醛
1. 分子结构
(1)分子式:CH2O
(2)结构式:
H一C一H
(3)结构简式:HCHO
O
甲醛分子中相当于含有两个醛基
2. 物理性质:
无色、有刺激性气味的气体,易溶于水。
甲醛的水溶液又称福尔马林,具有杀菌、防腐性能等。
反馈练习
HCHO发生银镜反应的化学方程式
HCHO +4Ag(NH3)2OH
+ 4 Ag↓
2H2O
+6NH3
+(NH4)2CO3
H一C一H
O
H—O—C—O—H
O
即:H2CO3
CH3CH2CHO和新制Cu(OH)2反应的化学方程式
CH3CH2CHO+2Cu(OH)2+NaOH → CH3CH2COONa
+Cu2O↓+3H2O
反馈练习
反馈练习
CH3CH(CH3)CH2OH是某有机化合物M的加氢
还原产物,该有机化合物M可能是( )
A. 乙醛的同系物 B. 丙醛的同分异构体
C. CH3CH(CH3)CCH3 D. CH3CH2CH2CHO
A
—CHO
O
反馈练习
从甜橙的芳香油中分离得如图结构的化合物:
现有试剂:①KMnO4酸性溶液 ②H2/Ni
③Ag(NH3)2OH溶液 ④新制Cu(OH)2悬浊液
能与该化合物中所有官能团都发生反应的试剂有( )
A.①② B.②③
C.③④ D.①④
A
思考与交流
某有机物的结构简式为CH2=CHCHCHO,
CH3
A. 该有机物与甲醛互为同系物
B. 在加热和催化剂作用下加氢,每摩尔该有机物最多能消耗3 mol H2
C. 一定条件下,该有机物能发生氧化、还原、酯化等反应
D.从理论上说,84 g该有机物能从足量银氨溶液中还原出216 g的银
D
R—CHO 2Ag
~
84 g
216 g
下列对其化学性质的判断中,正确的是( )。
2
本节课你学到了什么?
乙醛的
物理性质
乙醛的结构
乙醛的
化学性质
氧化反应和还原反应
无色、有刺激性气味的液体
密度比水的小
能与水、乙醇等互溶
醛基 :
C
H
O
CH3
2.乙醛的氧化反应
b.催化氧化
a.被弱氧化剂氧化
Ⅱ.被新制Cu(OH)2氧化反应
Ⅰ.被银氨溶液氧化
c.被强氧化剂氧化:
能使KMnO4酸性溶液褪色
小结:乙醛的化学性质
1.加成反应(还原反应) 与H2发生加成反应
1.书后习题P59 —1、2、3、4
课 后 作 业
2.甲醛是一种重要的化工原料,用途十分广泛。但是使用不当会有害于人体健康。请以“甲醛”为关键词,在Internet网上搜索资料,根据资料写一篇如何安全使用甲醛的短文。
