3.3 羧酸、酯-天津市2020年空中课堂人教版高中化学选修五课件(共37张PPT)
文档属性
| 名称 | 3.3 羧酸、酯-天津市2020年空中课堂人教版高中化学选修五课件(共37张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-19 00:00:00 | ||
图片预览






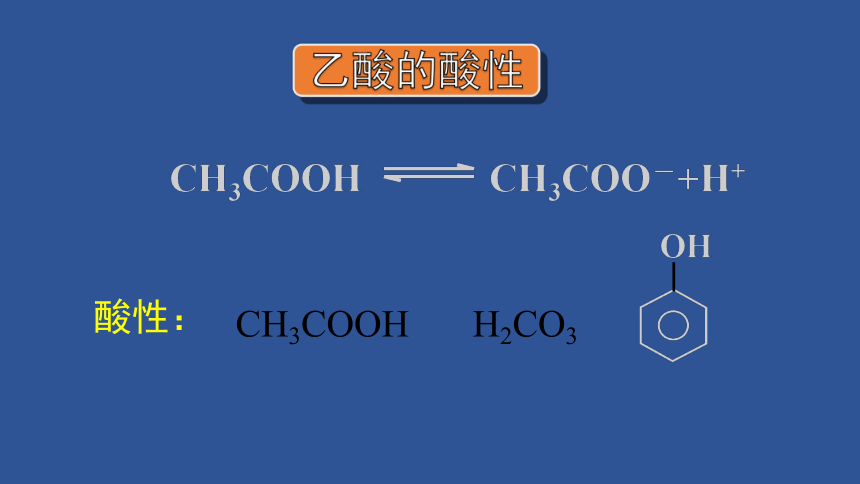



文档简介
(共37张PPT)
第三章 烃的含氧衍生物 羧酸 酯
高二年级 化学
1. 能写出羧酸和酯的官能团、乙酸的结构简式和名称
能够列举乙酸和乙酸乙酯的主要物理性质。
2.能描述和分析乙酸、乙酸乙酯的重要反应,
书写相应的反应式。
3.能基于官能团、化学键的特点与反应规律分析和
推断含有羧基、酯基官能团的有机化合物的化学
性质。根据信息书写相应的反应式。
金刀利,锦鲤肥,更那堪玉葱纤细。
添得____来风韵美,试尝道甚生滋味。
醋
柴
米
油
盐
酱
醋
茶
酒
饭
柴米油盐酱___茶
琴棋书画诗酒花
醋
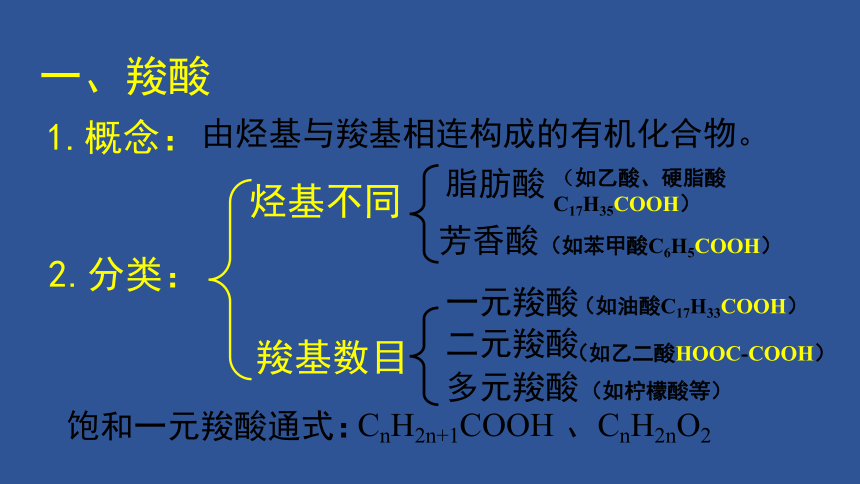
一、羧酸
1.概念:
由烃基与羧基相连构成的有机化合物。
2.分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
饱和一元羧酸通式:
CnH2n+1COOH 、CnH2nO2
(如乙酸、硬脂酸C17H35COOH)
(如苯甲酸C6H5COOH)
(如油酸C17H33COOH)
(如乙二酸HOOC-COOH)
(如柠檬酸等)
3. 自然界和日常生活中的有机酸
4.乙酸
(1)物理性质:
常温下为无色有强烈刺激性气味的液体
熔点:16.6 ℃ 沸点:117.9 ℃
低于熔点时易结成冰一样的晶体
(纯净的乙酸又称为冰醋酸)
与水、酒精以任意比互溶。
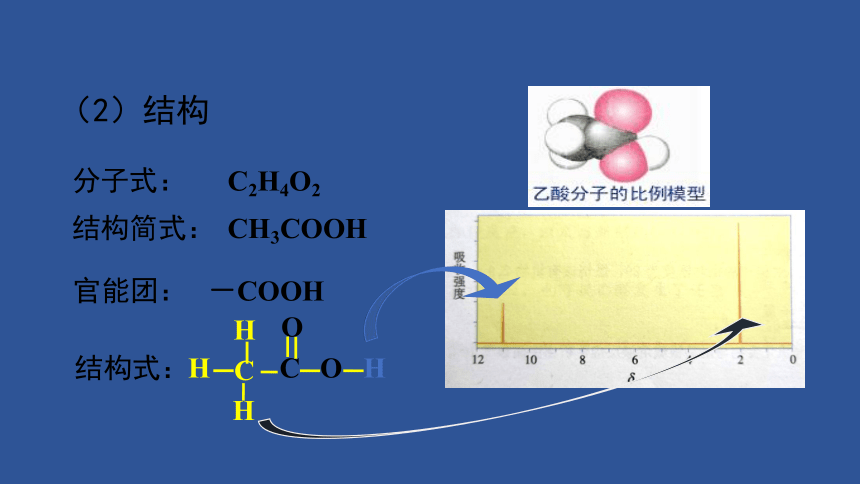
(2)结构
结构式:
分子式:
C2H4O2
结构简式:
CH3COOH
官能团:
-COOH
CH3COOH
H2CO3
酸性:
利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱
科学探究1
C6H5ONa + H2O + CO2 C6H5OH + NaHCO3
A D E B C F G H I J
仪器连接顺序:
产生气泡
除去挥发出的乙酸气体
变浑浊
书写化学反应方程式:
18
18
同位素示踪法
科学探究2
酸性
酯化反应
1.加药品顺序:
2.加碎瓷片
3.导管通到饱和Na2CO3溶液的液面上方
——防暴沸
——防倒吸
乙醇→浓硫酸→乙酸
4.浓H2SO4的作用:
5.饱和的Na2CO3溶液的作用
除去混杂在乙酸乙酯中的醋酸,溶解其中的乙醇,同时有利于降低乙酸乙酯在水中的溶解度。
催化剂、吸水剂
实验室制取乙酸乙酯的装置
乙醇、乙酸和浓硫酸
饱和Na2CO3溶液
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
酯化反应
①使用过量乙醇
②蒸出乙酸乙酯
依据化学平衡移动原理:
在一定条件下,当可逆反应达到平衡后,如果改变影响平衡的条件(如温度、浓度、压强),平衡就向能够减弱这种改变的方向移动。
水果中含低级酯
酯是羧酸分子羧基中的—OH被—OR′取代后的产物
二、酯
1. 概念:
2. 通式:
(饱和一元羧酸和饱和一元醇生成的酯)
(R可以是烃基或H原子, 而R′只能是烃基,可与R相同也可不同)
(或RCOOR′)
(1)
CnH2nO2(n≥2)
(2)
与碳原子数相同饱和一元羧酸互为同分异构体
例:C4H8O2属于羧酸和酯的同分异构体各有多少种?
羧酸:
R -COOH
C3H7-
{
CH3CH2CH2-
CH3 CH-
CH3
酯:
H 3C
2种
C 2C
2C C
1种
2种
1种
4种
3.物理性质:
①低级酯是具有芳香气味的液体。
②密度比水的小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
4. 化学性质:水解反应(或取代反应)
+H2O CH3COOH+C2H5OH
(以乙酸乙酯为例)
‖
那么如何加快乙酸乙酯的水解速率,应采取哪些措施呢?
科学探究:请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液中的水解速率
6滴乙酸乙酯
蒸馏水5.5 mL
同时70℃水浴,5 min,记录各试管中乙酸乙酯层高度的变化
酯层无明显变化
酯层明显减少
酯层消失
基本未水解
部分水解
完全水解
结论:水解速率-碱性条件>酸性条件
乙酸乙酯的水解反应
6滴乙酸乙酯
蒸馏水5.0 mL
稀硫酸0.5 mL
6滴乙酸乙酯
蒸馏水5.0 mL
NaOH溶液0.5 mL
编号 试管① 试管② 试管③
步骤I
振荡
均匀
步骤II
现象
结论
注意:酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
4. 化学性质:水解反应(或取代反应)
反馈练习
乙酸乙酯在KOH溶液中加热水解,得到的产物
是( )
A. 乙酸钾 B. 甲醇 C. 乙醇 D. 乙酸
A C
反馈练习
写出下列变化的化学方程式:
CH3CH2CH2OH CH3CH2CHO CH3CH2COOH
CH3CH2Br CH2=CH2 CH3CH2OH
CH3CH2COOC2H5
(1)
(2)
(3)
(4)
(5)
反馈练习
2CH3CH2CH2OH+O2
CH3CH2CHO+2H2O
催化剂
2CH3CH2CHO+O2
2CH3CH2COOH
催化剂
CH3CH2Br+NaOH
乙醇
CH2=CH2
+NaBr+H2O
CH2=CH2
催化剂
CH3CH2OH
CH3CH2COOH+
CH3CH2OH
稀H2SO4
CH3CH2
COOC2H5
(1)
(2)
(3)
(4)
(5)
+H2O
+H2O
有机物A的分子式C3H6O2,它与NaOH溶液共热蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C。B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的Cu(OH)2悬浊液加热煮沸,有红色沉淀和E生成。写出下述变化的反应方程式。
(1)A B (2)B C (3)B D(4)D E
反馈练习
C为乙烯
有醛基
+ NaOH HCOONa + C2H5OH
HC-OC2H5
‖
O
(1)
2CH3CH2OH + O2
催化剂
2CH3CHO + 2H2O
(3)
CH3CHO+2Cu(OH)2+NaOH CH3COONa
+Cu2O↓+3H2O
(2)
(4)
CH3CH2OH
浓硫酸
170℃
CH2=CH2
+ H2O
反馈练习
B
反馈提升
2 mol
1 mol
1 mol
一、乙酸
断键方式:
弱酸性:
乙酸>碳酸>苯酚
二、酯
物理性质
密度比水的小
难溶于水的液体等
化学性质
水解反应等
酸性
酯化反应
1、完成书P63习题 1、2、3
课后作业
2、几种衍生物之间的关系
乙烷
溴乙烷
乙烯
乙醇
乙醛
乙酸
乙酸乙酯
卤代
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
用化学方程式表示上述变化过程
第三章 烃的含氧衍生物 羧酸 酯
高二年级 化学
1. 能写出羧酸和酯的官能团、乙酸的结构简式和名称
能够列举乙酸和乙酸乙酯的主要物理性质。
2.能描述和分析乙酸、乙酸乙酯的重要反应,
书写相应的反应式。
3.能基于官能团、化学键的特点与反应规律分析和
推断含有羧基、酯基官能团的有机化合物的化学
性质。根据信息书写相应的反应式。
金刀利,锦鲤肥,更那堪玉葱纤细。
添得____来风韵美,试尝道甚生滋味。
醋
柴
米
油
盐
酱
醋
茶
酒
饭
柴米油盐酱___茶
琴棋书画诗酒花
醋
一、羧酸
1.概念:
由烃基与羧基相连构成的有机化合物。
2.分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
饱和一元羧酸通式:
CnH2n+1COOH 、CnH2nO2
(如乙酸、硬脂酸C17H35COOH)
(如苯甲酸C6H5COOH)
(如油酸C17H33COOH)
(如乙二酸HOOC-COOH)
(如柠檬酸等)
3. 自然界和日常生活中的有机酸
4.乙酸
(1)物理性质:
常温下为无色有强烈刺激性气味的液体
熔点:16.6 ℃ 沸点:117.9 ℃
低于熔点时易结成冰一样的晶体
(纯净的乙酸又称为冰醋酸)
与水、酒精以任意比互溶。
(2)结构
结构式:
分子式:
C2H4O2
结构简式:
CH3COOH
官能团:
-COOH
CH3COOH
H2CO3
酸性:
利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱
科学探究1
C6H5ONa + H2O + CO2 C6H5OH + NaHCO3
A D E B C F G H I J
仪器连接顺序:
产生气泡
除去挥发出的乙酸气体
变浑浊
书写化学反应方程式:
18
18
同位素示踪法
科学探究2
酸性
酯化反应
1.加药品顺序:
2.加碎瓷片
3.导管通到饱和Na2CO3溶液的液面上方
——防暴沸
——防倒吸
乙醇→浓硫酸→乙酸
4.浓H2SO4的作用:
5.饱和的Na2CO3溶液的作用
除去混杂在乙酸乙酯中的醋酸,溶解其中的乙醇,同时有利于降低乙酸乙酯在水中的溶解度。
催化剂、吸水剂
实验室制取乙酸乙酯的装置
乙醇、乙酸和浓硫酸
饱和Na2CO3溶液
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
酯化反应
①使用过量乙醇
②蒸出乙酸乙酯
依据化学平衡移动原理:
在一定条件下,当可逆反应达到平衡后,如果改变影响平衡的条件(如温度、浓度、压强),平衡就向能够减弱这种改变的方向移动。
水果中含低级酯
酯是羧酸分子羧基中的—OH被—OR′取代后的产物
二、酯
1. 概念:
2. 通式:
(饱和一元羧酸和饱和一元醇生成的酯)
(R可以是烃基或H原子, 而R′只能是烃基,可与R相同也可不同)
(或RCOOR′)
(1)
CnH2nO2(n≥2)
(2)
与碳原子数相同饱和一元羧酸互为同分异构体
例:C4H8O2属于羧酸和酯的同分异构体各有多少种?
羧酸:
R -COOH
C3H7-
{
CH3CH2CH2-
CH3 CH-
CH3
酯:
H 3C
2种
C 2C
2C C
1种
2种
1种
4种
3.物理性质:
①低级酯是具有芳香气味的液体。
②密度比水的小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
4. 化学性质:水解反应(或取代反应)
+H2O CH3COOH+C2H5OH
(以乙酸乙酯为例)
‖
那么如何加快乙酸乙酯的水解速率,应采取哪些措施呢?
科学探究:请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液中的水解速率
6滴乙酸乙酯
蒸馏水5.5 mL
同时70℃水浴,5 min,记录各试管中乙酸乙酯层高度的变化
酯层无明显变化
酯层明显减少
酯层消失
基本未水解
部分水解
完全水解
结论:水解速率-碱性条件>酸性条件
乙酸乙酯的水解反应
6滴乙酸乙酯
蒸馏水5.0 mL
稀硫酸0.5 mL
6滴乙酸乙酯
蒸馏水5.0 mL
NaOH溶液0.5 mL
编号 试管① 试管② 试管③
步骤I
振荡
均匀
步骤II
现象
结论
注意:酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
4. 化学性质:水解反应(或取代反应)
反馈练习
乙酸乙酯在KOH溶液中加热水解,得到的产物
是( )
A. 乙酸钾 B. 甲醇 C. 乙醇 D. 乙酸
A C
反馈练习
写出下列变化的化学方程式:
CH3CH2CH2OH CH3CH2CHO CH3CH2COOH
CH3CH2Br CH2=CH2 CH3CH2OH
CH3CH2COOC2H5
(1)
(2)
(3)
(4)
(5)
反馈练习
2CH3CH2CH2OH+O2
CH3CH2CHO+2H2O
催化剂
2CH3CH2CHO+O2
2CH3CH2COOH
催化剂
CH3CH2Br+NaOH
乙醇
CH2=CH2
+NaBr+H2O
CH2=CH2
催化剂
CH3CH2OH
CH3CH2COOH+
CH3CH2OH
稀H2SO4
CH3CH2
COOC2H5
(1)
(2)
(3)
(4)
(5)
+H2O
+H2O
有机物A的分子式C3H6O2,它与NaOH溶液共热蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C。B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的Cu(OH)2悬浊液加热煮沸,有红色沉淀和E生成。写出下述变化的反应方程式。
(1)A B (2)B C (3)B D(4)D E
反馈练习
C为乙烯
有醛基
+ NaOH HCOONa + C2H5OH
HC-OC2H5
‖
O
(1)
2CH3CH2OH + O2
催化剂
2CH3CHO + 2H2O
(3)
CH3CHO+2Cu(OH)2+NaOH CH3COONa
+Cu2O↓+3H2O
(2)
(4)
CH3CH2OH
浓硫酸
170℃
CH2=CH2
+ H2O
反馈练习
B
反馈提升
2 mol
1 mol
1 mol
一、乙酸
断键方式:
弱酸性:
乙酸>碳酸>苯酚
二、酯
物理性质
密度比水的小
难溶于水的液体等
化学性质
水解反应等
酸性
酯化反应
1、完成书P63习题 1、2、3
课后作业
2、几种衍生物之间的关系
乙烷
溴乙烷
乙烯
乙醇
乙醛
乙酸
乙酸乙酯
卤代
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
用化学方程式表示上述变化过程
