第二章 烃和卤代烃 复习课-天津市2020年空中课堂人教版高中化学选修五课件(共23张PPT)
文档属性
| 名称 | 第二章 烃和卤代烃 复习课-天津市2020年空中课堂人教版高中化学选修五课件(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-19 00:00:00 | ||
图片预览




文档简介
(共23张PPT)
第二章 烃和卤代烃 复习课
高二年级 化学
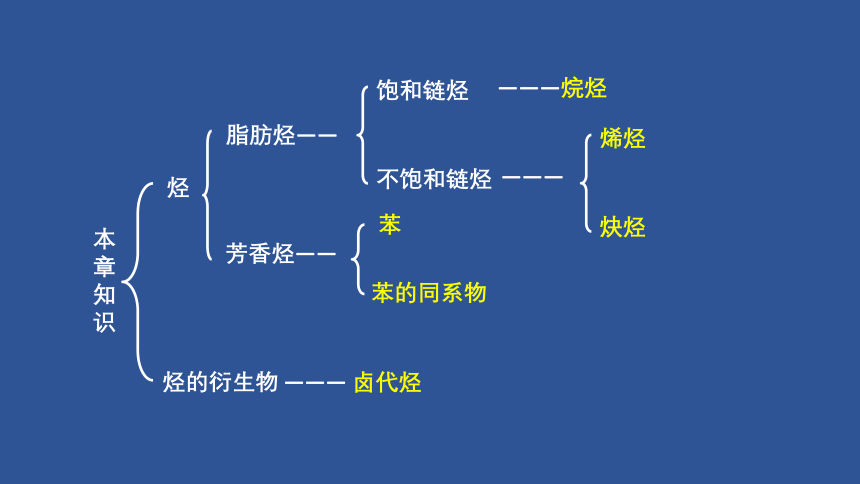
本章知识
烃
饱和链烃
不饱和链烃
脂肪烃——
芳香烃——
———烷烃
——— 卤代烃
烃的衍生物
———
烯烃
炔烃
苯
苯的同系物
复习目标
1.能写出烃及卤代烃的官能团、简单代表物的结构简式和名称;能够列举它们的典型代表物的主要物理性质。
2.能描述和分析烃及卤代烃的典型代表物的重要反应,能书写相应的化学方程式。并能基于官能团、化学键的特点与反应规律分析和推断含有典型官能团的有机化合物的化学性质,根据有关信息书写相应的化学方程式。
3.能以本章典型实验为例进行有关有机实验的设计、评价、优化等问题
4.能关注烃及卤代烃在日常生活、生产中的正确使用;为能参与环境保护等与有机化合物性质应用相关的社会性议题的讨论、科学的判断、评价等做好铺垫。
①密度:大多数烃的密度比水的小 ;大多数卤代烃的密度比水的大
②状态:C1-C4气态 C5-C16液态 C16-以上固态
③熔沸点:碳原子数越多,熔、沸点越高 ;同碳数,支链越多,熔沸点越低
含碳量规律:
烷烃<烯烃<炔烃<苯的同系物
烷烃(CnH2n+2 n≥1):随n值增大,含碳量增大
烯烃(CnH2n n ≥ 2 ):随n值增大,含碳量为定值
炔烃(CnH2n-2 n ≥ 2):随n值增大,含碳量减小
苯及其同系物(CnH2n-6 ≥ 6 ):随n值增大含碳量减小
一、物理性质
甲烷 乙烯 乙炔
苯 甲苯 溴乙烷
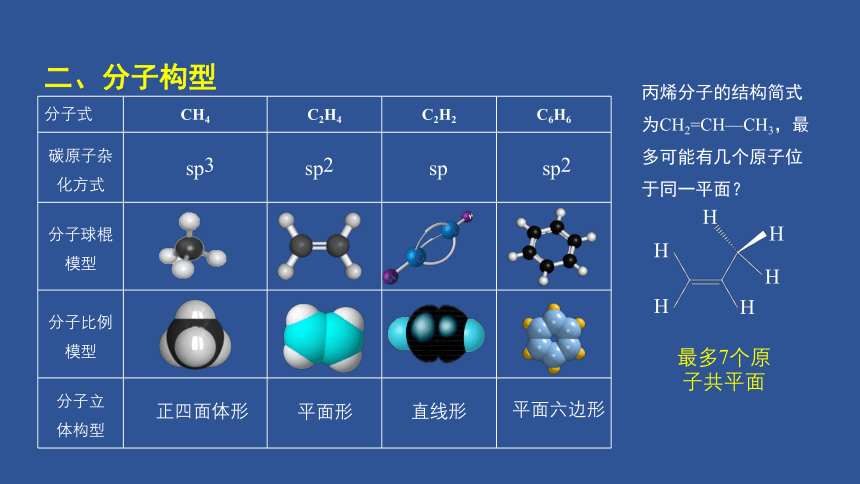
二、分子构型
丙烯分子的结构简式为CH2=CH—CH3,最多可能有几个原子位于同一平面?
分子式 CH4 C2H4 C2H2 C6H6
碳原子杂化方式
分子球棍模型
分子比例模型
分子立
体构型
sp
sp2
sp3
sp2
平面六边形
平面形
直线形
正四面体形
最多7个原子共平面
H
H
H
H
H
H
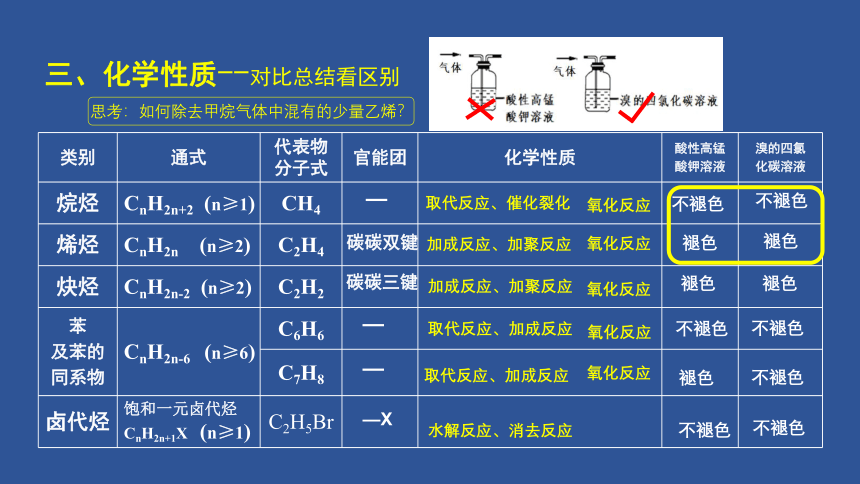
类别 通式 代表物分子式 官能团 化学性质 酸性高锰
酸钾溶液 溴的四氯
化碳溶液
烷烃 CnH2n+2 (n≥1) CH4
烯烃 CnH2n (n≥2) C2H4
炔烃 CnH2n-2 (n≥2) C2H2
苯
及苯的
同系物 CnH2n-6 (n≥6) C6H6
C7H8
卤代烃 饱和一元卤代烃CnH2n+1X (n≥1) C2H5Br
取代反应、催化裂化
加成反应、加聚反应
加成反应、加聚反应
取代反应、加成反应
水解反应、消去反应
三、化学性质--对比总结看区别
不褪色
不褪色
不褪色
不褪色
褪色
褪色
褪色
褪色
褪色
不褪色
不褪色
不褪色
碳碳双键
碳碳三键
—X
—
—
—
取代反应、加成反应
思考:如何除去甲烷气体中混有的少量乙烯?
氧化反应
氧化反应
氧化反应
氧化反应
氧化反应
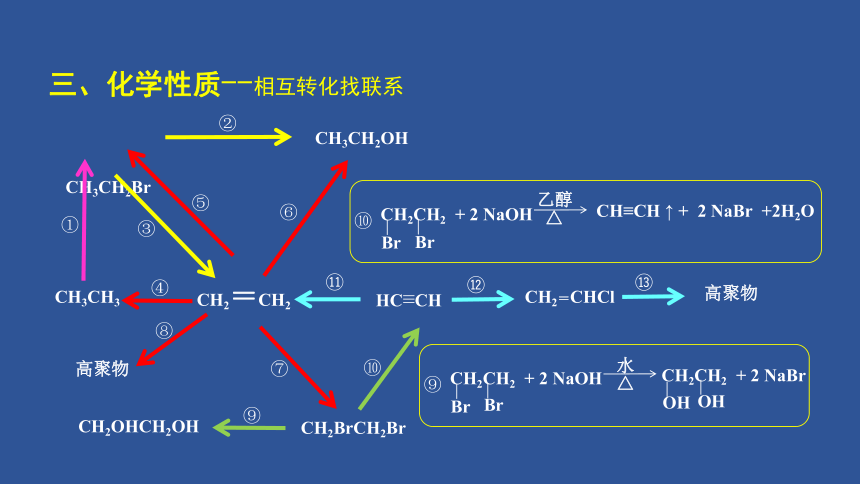
CH3CH2Br
CH3CH2OH
CH3CH3
HC≡CH
CH2=CH2
CH2BrCH2Br
CH2OHCH2OH
三、化学性质--相互转化找联系
①
②
③
④
⑤
⑥
⑦
⑧
高聚物
⑨
⑩
高聚物
?
CH2=CHCl
?
?
⑨
CH2CH2 + 2 NaOH
水
△
CH2CH2 + 2 NaBr
OH
OH
Br
Br
⑩
CH2CH2 + 2 NaOH
乙醇
△
CH≡CH ↑ + 2 NaBr +2H2O
Br
Br
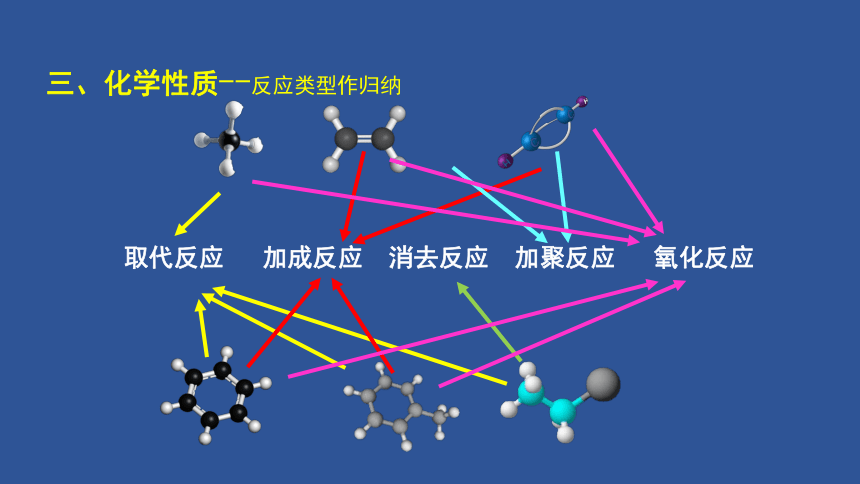
取代反应 加成反应 消去反应 加聚反应 氧化反应
三、化学性质--反应类型作归纳
下列化合物中,既能发生消去反应,又能发生水解反应的是( )
A. 氯仿 B.氯甲烷 C.乙醇 D.氯乙烷
D
三、化学性质--反应类型作归纳
CH3-C≡CH
CH3-CH=CH2或
CH3-CCl=CHCl
在 CH3CH2=CH2 、CH3CCl=CHCl 、 CH3C≡CH 、 CH2=CHCHCl2 四种物质之间,_____________________是_____________ 发生加成的产物。
三、化学性质--反应类型作归纳
四、本章实验
实验2-2
苯、甲苯分别与
酸性高锰酸钾溶液反应
关注实验过程的设计细节、评价、优选等实际问题
从而提高对实验的理解
科学探究
溴乙烷的性质
实验2-1
乙炔的制取及性质检验
四、本章实验
实验2-1 乙炔的制取及性质检验
饱和食盐水代替水减缓过快的反应速率
为什么选用饱和食盐水?
CuSO4+H2S = CuS↓+H2SO4
吸收反应中产生的硫化氢等还原性的杂质气体
避免对乙炔气体的性质验证造成干扰
CaC2 + 2H2O = C2H2↑ + Ca(OH)2
硫酸铜溶液起什么作用?
四、本章实验
科学探究 溴乙烷的性质
为什么采用水浴加热?
如何证明溴乙烷发生了消去反应还是取代反应?
试管 b 中如果放置酸性高锰酸钾溶液可以说明上面的问题吗?
水浴加热可以使试管受热均匀,更好地控制反应温度,温度不会过高,可以减少溴乙烷和乙醇的挥发。
如果产物中检验到不饱和烃,则溴乙烷发生的是消去反应,否则说明溴乙烷发生了取代反应。
不可以。因为反应器中挥发出的乙醇也能使酸性高锰酸钾溶液褪色。
五、来源与应用
脂肪烃
芳香烃
卤代烃
石油天然气和煤
煤、石油
烃、醇等物质的取代
正确使用烃和卤代烃
防止污染 爱护环境
AC
汽油燃烧产生的尾气中,所含的大气污染物主要是( )
A. 碳的氧化物 B.硫的氧化物
C. 氮的氧化物 D.磷的氧化物
五、来源与应用
关注生活中的有机物
A
家庭使用的天然气(主要成分为CH4)、液化石油气(主要成分为C3H8),
燃烧反应的主要化学方程式分别为:
CH4 + 2 O2 → CO2 + 2H2O ;C3H8 + 5 O2 → 3CO2 + 4H2O ;
现有一套以液化石油气为原料的灶具,欲改为天然气,应采取的措施是( )
A.减小空气进量,增大天然气进量 B.减小空气进量,减小天然气进量
C.增大空气进量,增大天然气进量 D.增大空气进量,减小天然气进量
点燃
点燃
关注生活中的有机物
五、来源与应用
C
1 mol 某烃完全燃烧可得到 2 mol CO2;在一定条件下, 1 mol 该烃能与 2 mol H2发生反应,这种烃是( )
A. CH4 B.C2H4 C.C2H2 D.C3H4
六、习题巩固
饱和卤代烃
C
C
C
-
-
Cl
Cl
C
C
C
-
-
Cl
Cl
C
C
C
-
-
C
C
C
-
-
Cl
Cl
Cl
Cl
C
C
C
-
-
Cl
B
组成为 C3H6Cl2 的卤代烃,可能存在的同分异构体有( )
A. 3种 B.4种 C.5种 D.6种
六、习题巩固
CxHy + (x+y/4)O2 → xCO2 + y/2 H2O
点燃
C2H6
C2H2
CO2
分别完全燃烧 1 mol C2H6、 1 mol C2H4、 1 mol C2H2,需要的氧气最多的是______;生成水最少的是______ ;生成_____质量相等。
六、习题巩固
含有1 mol 碳碳双键
CH3
∣
Cl
∣
C
CH3
C
CH
CH2
-
H3-
Cl
∣
2-甲基-2-戊烯
1 mol 某不饱和烃可以和 1 mol Cl2 发生加成反应,生成 2-甲基-2,3-二氯戊烷,则该不饱和烃是____________________________
六、习题巩固
2 C2H6 + 7 O2 → 4 CO2 + 6 H2O
点燃
2
7
4
△V
5
4 L
10 L
反应后气体 20 L + 4 L - 10 L = 14 L
通入足量石灰水后剩余气体 14 L - 8 L = 6 L
8 L
在 20 L 氧气中充分燃烧 4.0 L 乙烷,反应后气体的体积为多少?如将生成的气体通入足量的石灰水中,剩余气体的体积是多少?(气体体积均为常温时的体积)
六、习题巩固
小 结
作 业
①完成本节课思维导图中的所有化学方程式②完成教材P45中未讲解的习题
③用自己的方法归纳整理第二章的知识
脂肪烃
芳香烃
卤代烃
列表对比
思维导图
习题巩固
物理性质
物质结构
化学性质
相关实验
来源应用
复习方法
复习物质
复习内容
用正确的方法学习能事半功倍
常做总结和复习能助你基础扎实概念清晰
同 学 们 再 见
第二章 烃和卤代烃 复习课
高二年级 化学
本章知识
烃
饱和链烃
不饱和链烃
脂肪烃——
芳香烃——
———烷烃
——— 卤代烃
烃的衍生物
———
烯烃
炔烃
苯
苯的同系物
复习目标
1.能写出烃及卤代烃的官能团、简单代表物的结构简式和名称;能够列举它们的典型代表物的主要物理性质。
2.能描述和分析烃及卤代烃的典型代表物的重要反应,能书写相应的化学方程式。并能基于官能团、化学键的特点与反应规律分析和推断含有典型官能团的有机化合物的化学性质,根据有关信息书写相应的化学方程式。
3.能以本章典型实验为例进行有关有机实验的设计、评价、优化等问题
4.能关注烃及卤代烃在日常生活、生产中的正确使用;为能参与环境保护等与有机化合物性质应用相关的社会性议题的讨论、科学的判断、评价等做好铺垫。
①密度:大多数烃的密度比水的小 ;大多数卤代烃的密度比水的大
②状态:C1-C4气态 C5-C16液态 C16-以上固态
③熔沸点:碳原子数越多,熔、沸点越高 ;同碳数,支链越多,熔沸点越低
含碳量规律:
烷烃<烯烃<炔烃<苯的同系物
烷烃(CnH2n+2 n≥1):随n值增大,含碳量增大
烯烃(CnH2n n ≥ 2 ):随n值增大,含碳量为定值
炔烃(CnH2n-2 n ≥ 2):随n值增大,含碳量减小
苯及其同系物(CnH2n-6 ≥ 6 ):随n值增大含碳量减小
一、物理性质
甲烷 乙烯 乙炔
苯 甲苯 溴乙烷
二、分子构型
丙烯分子的结构简式为CH2=CH—CH3,最多可能有几个原子位于同一平面?
分子式 CH4 C2H4 C2H2 C6H6
碳原子杂化方式
分子球棍模型
分子比例模型
分子立
体构型
sp
sp2
sp3
sp2
平面六边形
平面形
直线形
正四面体形
最多7个原子共平面
H
H
H
H
H
H
类别 通式 代表物分子式 官能团 化学性质 酸性高锰
酸钾溶液 溴的四氯
化碳溶液
烷烃 CnH2n+2 (n≥1) CH4
烯烃 CnH2n (n≥2) C2H4
炔烃 CnH2n-2 (n≥2) C2H2
苯
及苯的
同系物 CnH2n-6 (n≥6) C6H6
C7H8
卤代烃 饱和一元卤代烃CnH2n+1X (n≥1) C2H5Br
取代反应、催化裂化
加成反应、加聚反应
加成反应、加聚反应
取代反应、加成反应
水解反应、消去反应
三、化学性质--对比总结看区别
不褪色
不褪色
不褪色
不褪色
褪色
褪色
褪色
褪色
褪色
不褪色
不褪色
不褪色
碳碳双键
碳碳三键
—X
—
—
—
取代反应、加成反应
思考:如何除去甲烷气体中混有的少量乙烯?
氧化反应
氧化反应
氧化反应
氧化反应
氧化反应
CH3CH2Br
CH3CH2OH
CH3CH3
HC≡CH
CH2=CH2
CH2BrCH2Br
CH2OHCH2OH
三、化学性质--相互转化找联系
①
②
③
④
⑤
⑥
⑦
⑧
高聚物
⑨
⑩
高聚物
?
CH2=CHCl
?
?
⑨
CH2CH2 + 2 NaOH
水
△
CH2CH2 + 2 NaBr
OH
OH
Br
Br
⑩
CH2CH2 + 2 NaOH
乙醇
△
CH≡CH ↑ + 2 NaBr +2H2O
Br
Br
取代反应 加成反应 消去反应 加聚反应 氧化反应
三、化学性质--反应类型作归纳
下列化合物中,既能发生消去反应,又能发生水解反应的是( )
A. 氯仿 B.氯甲烷 C.乙醇 D.氯乙烷
D
三、化学性质--反应类型作归纳
CH3-C≡CH
CH3-CH=CH2或
CH3-CCl=CHCl
在 CH3CH2=CH2 、CH3CCl=CHCl 、 CH3C≡CH 、 CH2=CHCHCl2 四种物质之间,_____________________是_____________ 发生加成的产物。
三、化学性质--反应类型作归纳
四、本章实验
实验2-2
苯、甲苯分别与
酸性高锰酸钾溶液反应
关注实验过程的设计细节、评价、优选等实际问题
从而提高对实验的理解
科学探究
溴乙烷的性质
实验2-1
乙炔的制取及性质检验
四、本章实验
实验2-1 乙炔的制取及性质检验
饱和食盐水代替水减缓过快的反应速率
为什么选用饱和食盐水?
CuSO4+H2S = CuS↓+H2SO4
吸收反应中产生的硫化氢等还原性的杂质气体
避免对乙炔气体的性质验证造成干扰
CaC2 + 2H2O = C2H2↑ + Ca(OH)2
硫酸铜溶液起什么作用?
四、本章实验
科学探究 溴乙烷的性质
为什么采用水浴加热?
如何证明溴乙烷发生了消去反应还是取代反应?
试管 b 中如果放置酸性高锰酸钾溶液可以说明上面的问题吗?
水浴加热可以使试管受热均匀,更好地控制反应温度,温度不会过高,可以减少溴乙烷和乙醇的挥发。
如果产物中检验到不饱和烃,则溴乙烷发生的是消去反应,否则说明溴乙烷发生了取代反应。
不可以。因为反应器中挥发出的乙醇也能使酸性高锰酸钾溶液褪色。
五、来源与应用
脂肪烃
芳香烃
卤代烃
石油天然气和煤
煤、石油
烃、醇等物质的取代
正确使用烃和卤代烃
防止污染 爱护环境
AC
汽油燃烧产生的尾气中,所含的大气污染物主要是( )
A. 碳的氧化物 B.硫的氧化物
C. 氮的氧化物 D.磷的氧化物
五、来源与应用
关注生活中的有机物
A
家庭使用的天然气(主要成分为CH4)、液化石油气(主要成分为C3H8),
燃烧反应的主要化学方程式分别为:
CH4 + 2 O2 → CO2 + 2H2O ;C3H8 + 5 O2 → 3CO2 + 4H2O ;
现有一套以液化石油气为原料的灶具,欲改为天然气,应采取的措施是( )
A.减小空气进量,增大天然气进量 B.减小空气进量,减小天然气进量
C.增大空气进量,增大天然气进量 D.增大空气进量,减小天然气进量
点燃
点燃
关注生活中的有机物
五、来源与应用
C
1 mol 某烃完全燃烧可得到 2 mol CO2;在一定条件下, 1 mol 该烃能与 2 mol H2发生反应,这种烃是( )
A. CH4 B.C2H4 C.C2H2 D.C3H4
六、习题巩固
饱和卤代烃
C
C
C
-
-
Cl
Cl
C
C
C
-
-
Cl
Cl
C
C
C
-
-
C
C
C
-
-
Cl
Cl
Cl
Cl
C
C
C
-
-
Cl
B
组成为 C3H6Cl2 的卤代烃,可能存在的同分异构体有( )
A. 3种 B.4种 C.5种 D.6种
六、习题巩固
CxHy + (x+y/4)O2 → xCO2 + y/2 H2O
点燃
C2H6
C2H2
CO2
分别完全燃烧 1 mol C2H6、 1 mol C2H4、 1 mol C2H2,需要的氧气最多的是______;生成水最少的是______ ;生成_____质量相等。
六、习题巩固
含有1 mol 碳碳双键
CH3
∣
Cl
∣
C
CH3
C
CH
CH2
-
H3-
Cl
∣
2-甲基-2-戊烯
1 mol 某不饱和烃可以和 1 mol Cl2 发生加成反应,生成 2-甲基-2,3-二氯戊烷,则该不饱和烃是____________________________
六、习题巩固
2 C2H6 + 7 O2 → 4 CO2 + 6 H2O
点燃
2
7
4
△V
5
4 L
10 L
反应后气体 20 L + 4 L - 10 L = 14 L
通入足量石灰水后剩余气体 14 L - 8 L = 6 L
8 L
在 20 L 氧气中充分燃烧 4.0 L 乙烷,反应后气体的体积为多少?如将生成的气体通入足量的石灰水中,剩余气体的体积是多少?(气体体积均为常温时的体积)
六、习题巩固
小 结
作 业
①完成本节课思维导图中的所有化学方程式②完成教材P45中未讲解的习题
③用自己的方法归纳整理第二章的知识
脂肪烃
芳香烃
卤代烃
列表对比
思维导图
习题巩固
物理性质
物质结构
化学性质
相关实验
来源应用
复习方法
复习物质
复习内容
用正确的方法学习能事半功倍
常做总结和复习能助你基础扎实概念清晰
同 学 们 再 见
