苏教版高二化学选修5 有机化学基础专题5第一单元 糖类 油脂 (共29张PPT)
文档属性
| 名称 | 苏教版高二化学选修5 有机化学基础专题5第一单元 糖类 油脂 (共29张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-20 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
专题5 生命活动的物质基础
第一单元 糖类 油脂
糖 类
zxxkw
学.科.网
学科网
1.有甜味的不一定是糖。如
2.没有甜味的也可能是糖。如
甘油
淀粉、纤维素
1.符合Cn(H2O)m的不一定是糖类化合物。如
2.不符合此通式的不一定不是糖类化合物。如
3.在分子中,氢原子和氧原子并不是以结合成水的形式存在
CH2O 、C2H4O2
C6H12O5
鼠李糖
糖类的定义
糖类(carbohydrate):是指多羟基醛或
多羟基酮以及能水解生成它们的物质。
糖类的划分
阅读思考:
糖类物质可分为那些类别?
分类的依据是什么?
1、根据能否水解及水解产物多少分:
单糖、低聚糖、多糖
2、按照分子中所含碳原子数的多少:
单糖中碳原子数为3:丙糖
4:丁糖
5:戊糖
6:己糖
3、按照与羰基连接的原子或原子团的
情况不同:
单糖又可分为醛糖和酮糖
归
纳
一、单糖 — 葡萄糖和果糖
1.葡萄糖:C6H12O6
(1)葡萄糖的结构与化学性质
活动与探究——葡萄糖分子式与结构式推算
实验式:CH2O
分子式: (CH2O)6
每个分子中含
5个 -OH
分子中含醛基
6个碳排成直链
该有机物(C6H12O6),一个分子中含
一个—CHO,5个—OH, 6个碳排成直链
实验事实 结论
(1) 1.80g葡萄糖完全燃烧,只得到2.64gCO2和1.08gH2O
(2) 葡萄糖的相对分子质量为180
(3) 在一定条件下, 1.80g葡萄糖与乙酸完全酯化,生成的乙酸酯的质量为3.90g
(4) 葡萄糖可以发生银镜反应
(5) 葡萄糖可以被还原为直链己六醇
关于葡萄糖分子结构的结论:
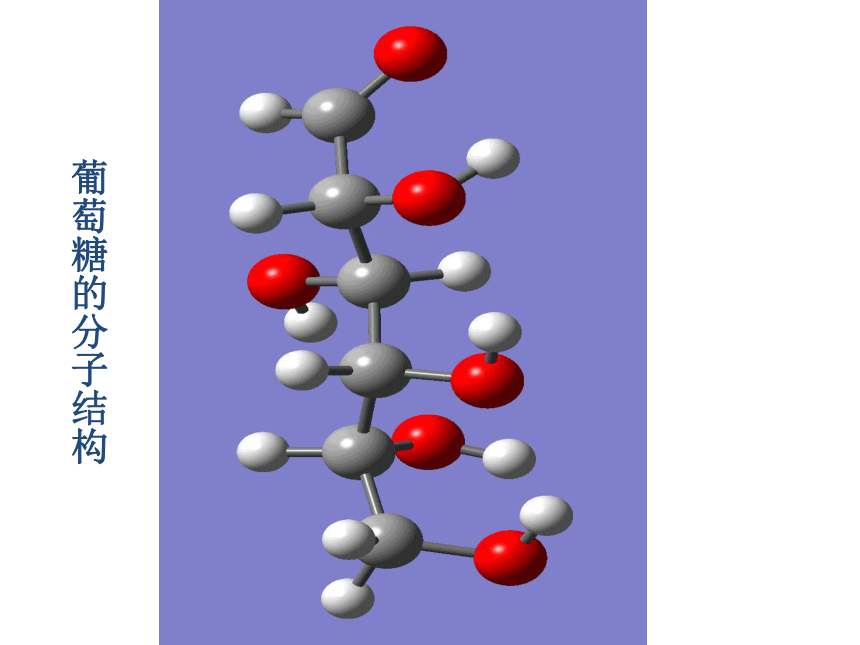
葡萄糖的分子结构
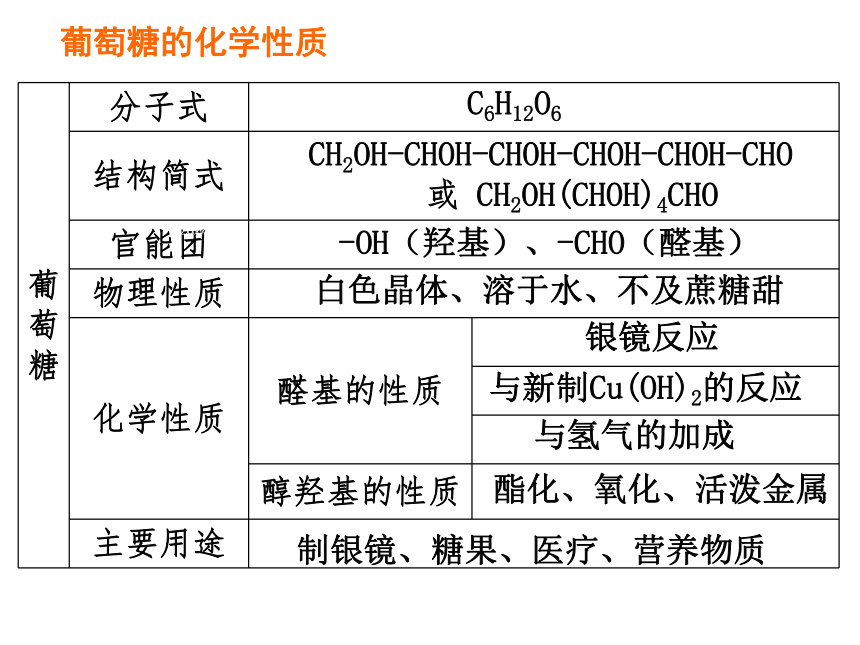
C6H12O6
CH2OH-CHOH-CHOH-CHOH-CHOH-CHO
或 CH2OH(CHOH)4CHO
-OH(羟基)、-CHO(醛基)
白色晶体、溶于水、不及蔗糖甜
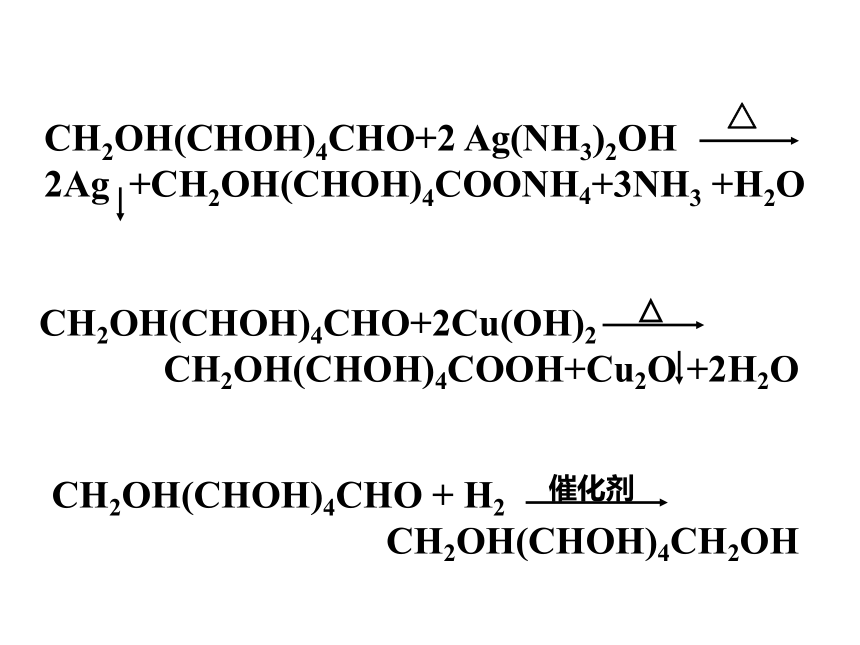
银镜反应
与新制Cu(OH)2的反应
制银镜、糖果、医疗、营养物质
葡萄糖的化学性质
与氢气的加成
酯化、氧化、活泼金属
zxxkw
葡 萄 糖 分子式
结构简式
官能团
物理性质
化学性质 醛基的性质
醇羟基的性质
主要用途
分子式:
结构简式:
所含官能团:
葡萄糖
化学性质
葡萄糖的结构与化学性质
用途
葡萄糖的用途和工业制法
生活上
●用途 工业上
医药上
——糖类
——制镜
——迅速补充营养
●果糖简介:
1. 分子式:C6H12O6
2. 结构简式:
CH2OH(CHOH) 3COCH2OH
多羟基酮,是葡萄糖的同分异构体。
3. 存在:
蜂蜜、水果中。天然存在的糖中最甜的一种。代谢不需胰岛素的调节,对糖尿病患者无害。
(五羟基己酮)
二、二糖 — 蔗糖和麦芽糖
(C12H22O11)
1、蔗糖的存在 和物理性质
蔗糖(冰糖、白砂糖)
.物理性质:无色晶体,溶于水,有甜味
蔗糖
麦芽糖
相似点
不 同 点
官能团
化学性质
水解产物
来源
1.组成相同,同分异构体 2.都属于二糖 3.水解产物都能发生银镜、与新制氢氧化铜反应 4.都有甜味
不含-CHO
水解
含-CHO
水解、银镜、与新制氢氧化铜反应
葡萄糖+果糖
2分子葡萄糖
甘蔗、甜菜
主要由淀粉的水解而来
活动与探究——蔗糖及其水解产物的性质
有砖红色沉淀出现
无砖红色沉淀出现
存在与物理性质
淀粉的化学性质(不与银氨溶液和新制氢氧化铜反应,不显还原性,在稀酸作用下在人体中均能水解,最终产物为葡萄糖,淀粉溶液遇碘单质变蓝色)
1、淀粉(是由几百到几千个葡萄糖单元构成的高分子化合物)
白色、无气味、无味道的粉末状物质。不溶于冷水, 在热水中能膨胀, 部分溶于热水, 部分悬浮在水里,形成胶状淀粉糊。
三、多糖 — 淀粉和纤维素
(C6H10O5)n
注意:淀粉胶体微粒不带电荷
淀粉的水解:
① 0.5g淀粉+ 5mL水
① 0.5g淀粉+ 稀硫酸
②加热煮沸5min
③加入NaOH溶液中和稀硫酸
④加入新制的氢氧化铜加热
不产生砖红色沉淀
蓝色沉淀→砖红色沉淀
无醛基
产物中含有醛基
活动与探究
P93
分组编号 Ⅰ Ⅱ
实验步骤
实验现象
实验结论
检验淀粉水解进行程度的方法:
未水解: ,
完全水解 ,
部分水解 。
检葡萄糖
检淀粉
均检
注意:
多糖水解后的溶液中有硫酸,须加碱中和后才能进行银镜实验或 氢氧化铜实验。
多糖的水解 活动与探究P93
●淀粉的水解:
(C6H10O5)n+nH2O nC6H12O6
稀硫酸
加热
淀粉水解方程式:
淀粉
葡萄糖
淀粉的用途:淀粉是人类生活中的三大营养物质之一,同时也是一种工业原料,可用于制酒,主要存在于植物的种子、块茎或块根里,谷类含量较高。
1、存在
2、物理性质
2、纤维素(是由几千个葡萄糖单元构成的高分子化合物)
3、纤维素的结构与化学性质(无醛基)
白色、无气味、无味道的具有纤维结构的物质。不溶于水, 也不溶于有机溶剂.
纤维素存在于一切植物中。是构成植物细胞壁的基础物质。其中:棉花含纤维素92%~95%;
亚麻含纤维素约80%;
木材含纤维素约50%。
(C6H10O5)n + nH2O
(纤维素)
催化剂
△
nC6H12O6(葡萄糖)
水解反应
纤维素的结构与化学性质
结构
“C6H10O5”称为单糖单元,纤维素的“C6H10O5”又称为葡萄糖单元。每个单糖单元含有3个—OH,故纤维素可写成
因此,能显示出醇的性质。发生酯化反应,生成酯。
纤维素的硝化反应方程式:
(C6H7O2)
OH
OH
OH
n
3n HO—NO2
3nH2O
+
+
纤维素硝酸酯
俗称:(硝酸纤维)
浓硫酸
a. 制造纤维素硝酸酯(硝酸纤维)。根据含N 量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐珞和喷漆)
b. 制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
c. 制造黏胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)、铜氨纤维等
纤维素的用途
纯棉上衣
麻布
法国棉麻
d. 棉麻纤维大量用于纺织工业
e. 木材、稻草、麦秸、蔗渣等用于造纸
f. 食物中的纤维素有利于人的消化。
糖的分类
单糖 二糖 二糖 多糖 多糖
溶于水 溶于水 溶于水 不溶于水 不溶于水
甜 甜 甜 不甜 不甜
多羟基醛 多羟基醛 多羟基酮 n个葡萄糖单元
同分异构 不是同分异构
物质 葡萄糖 麦芽糖 蔗糖 淀粉 纤维素
分子式
类别
溶解性
甜味
结构
关系
专题5 生命活动的物质基础
第一单元 糖类 油脂
糖 类
zxxkw
学.科.网
学科网
1.有甜味的不一定是糖。如
2.没有甜味的也可能是糖。如
甘油
淀粉、纤维素
1.符合Cn(H2O)m的不一定是糖类化合物。如
2.不符合此通式的不一定不是糖类化合物。如
3.在分子中,氢原子和氧原子并不是以结合成水的形式存在
CH2O 、C2H4O2
C6H12O5
鼠李糖
糖类的定义
糖类(carbohydrate):是指多羟基醛或
多羟基酮以及能水解生成它们的物质。
糖类的划分
阅读思考:
糖类物质可分为那些类别?
分类的依据是什么?
1、根据能否水解及水解产物多少分:
单糖、低聚糖、多糖
2、按照分子中所含碳原子数的多少:
单糖中碳原子数为3:丙糖
4:丁糖
5:戊糖
6:己糖
3、按照与羰基连接的原子或原子团的
情况不同:
单糖又可分为醛糖和酮糖
归
纳
一、单糖 — 葡萄糖和果糖
1.葡萄糖:C6H12O6
(1)葡萄糖的结构与化学性质
活动与探究——葡萄糖分子式与结构式推算
实验式:CH2O
分子式: (CH2O)6
每个分子中含
5个 -OH
分子中含醛基
6个碳排成直链
该有机物(C6H12O6),一个分子中含
一个—CHO,5个—OH, 6个碳排成直链
实验事实 结论
(1) 1.80g葡萄糖完全燃烧,只得到2.64gCO2和1.08gH2O
(2) 葡萄糖的相对分子质量为180
(3) 在一定条件下, 1.80g葡萄糖与乙酸完全酯化,生成的乙酸酯的质量为3.90g
(4) 葡萄糖可以发生银镜反应
(5) 葡萄糖可以被还原为直链己六醇
关于葡萄糖分子结构的结论:
葡萄糖的分子结构
C6H12O6
CH2OH-CHOH-CHOH-CHOH-CHOH-CHO
或 CH2OH(CHOH)4CHO
-OH(羟基)、-CHO(醛基)
白色晶体、溶于水、不及蔗糖甜
银镜反应
与新制Cu(OH)2的反应
制银镜、糖果、医疗、营养物质
葡萄糖的化学性质
与氢气的加成
酯化、氧化、活泼金属
zxxkw
葡 萄 糖 分子式
结构简式
官能团
物理性质
化学性质 醛基的性质
醇羟基的性质
主要用途
分子式:
结构简式:
所含官能团:
葡萄糖
化学性质
葡萄糖的结构与化学性质
用途
葡萄糖的用途和工业制法
生活上
●用途 工业上
医药上
——糖类
——制镜
——迅速补充营养
●果糖简介:
1. 分子式:C6H12O6
2. 结构简式:
CH2OH(CHOH) 3COCH2OH
多羟基酮,是葡萄糖的同分异构体。
3. 存在:
蜂蜜、水果中。天然存在的糖中最甜的一种。代谢不需胰岛素的调节,对糖尿病患者无害。
(五羟基己酮)
二、二糖 — 蔗糖和麦芽糖
(C12H22O11)
1、蔗糖的存在 和物理性质
蔗糖(冰糖、白砂糖)
.物理性质:无色晶体,溶于水,有甜味
蔗糖
麦芽糖
相似点
不 同 点
官能团
化学性质
水解产物
来源
1.组成相同,同分异构体 2.都属于二糖 3.水解产物都能发生银镜、与新制氢氧化铜反应 4.都有甜味
不含-CHO
水解
含-CHO
水解、银镜、与新制氢氧化铜反应
葡萄糖+果糖
2分子葡萄糖
甘蔗、甜菜
主要由淀粉的水解而来
活动与探究——蔗糖及其水解产物的性质
有砖红色沉淀出现
无砖红色沉淀出现
存在与物理性质
淀粉的化学性质(不与银氨溶液和新制氢氧化铜反应,不显还原性,在稀酸作用下在人体中均能水解,最终产物为葡萄糖,淀粉溶液遇碘单质变蓝色)
1、淀粉(是由几百到几千个葡萄糖单元构成的高分子化合物)
白色、无气味、无味道的粉末状物质。不溶于冷水, 在热水中能膨胀, 部分溶于热水, 部分悬浮在水里,形成胶状淀粉糊。
三、多糖 — 淀粉和纤维素
(C6H10O5)n
注意:淀粉胶体微粒不带电荷
淀粉的水解:
① 0.5g淀粉+ 5mL水
① 0.5g淀粉+ 稀硫酸
②加热煮沸5min
③加入NaOH溶液中和稀硫酸
④加入新制的氢氧化铜加热
不产生砖红色沉淀
蓝色沉淀→砖红色沉淀
无醛基
产物中含有醛基
活动与探究
P93
分组编号 Ⅰ Ⅱ
实验步骤
实验现象
实验结论
检验淀粉水解进行程度的方法:
未水解: ,
完全水解 ,
部分水解 。
检葡萄糖
检淀粉
均检
注意:
多糖水解后的溶液中有硫酸,须加碱中和后才能进行银镜实验或 氢氧化铜实验。
多糖的水解 活动与探究P93
●淀粉的水解:
(C6H10O5)n+nH2O nC6H12O6
稀硫酸
加热
淀粉水解方程式:
淀粉
葡萄糖
淀粉的用途:淀粉是人类生活中的三大营养物质之一,同时也是一种工业原料,可用于制酒,主要存在于植物的种子、块茎或块根里,谷类含量较高。
1、存在
2、物理性质
2、纤维素(是由几千个葡萄糖单元构成的高分子化合物)
3、纤维素的结构与化学性质(无醛基)
白色、无气味、无味道的具有纤维结构的物质。不溶于水, 也不溶于有机溶剂.
纤维素存在于一切植物中。是构成植物细胞壁的基础物质。其中:棉花含纤维素92%~95%;
亚麻含纤维素约80%;
木材含纤维素约50%。
(C6H10O5)n + nH2O
(纤维素)
催化剂
△
nC6H12O6(葡萄糖)
水解反应
纤维素的结构与化学性质
结构
“C6H10O5”称为单糖单元,纤维素的“C6H10O5”又称为葡萄糖单元。每个单糖单元含有3个—OH,故纤维素可写成
因此,能显示出醇的性质。发生酯化反应,生成酯。
纤维素的硝化反应方程式:
(C6H7O2)
OH
OH
OH
n
3n HO—NO2
3nH2O
+
+
纤维素硝酸酯
俗称:(硝酸纤维)
浓硫酸
a. 制造纤维素硝酸酯(硝酸纤维)。根据含N 量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐珞和喷漆)
b. 制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
c. 制造黏胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)、铜氨纤维等
纤维素的用途
纯棉上衣
麻布
法国棉麻
d. 棉麻纤维大量用于纺织工业
e. 木材、稻草、麦秸、蔗渣等用于造纸
f. 食物中的纤维素有利于人的消化。
糖的分类
单糖 二糖 二糖 多糖 多糖
溶于水 溶于水 溶于水 不溶于水 不溶于水
甜 甜 甜 不甜 不甜
多羟基醛 多羟基醛 多羟基酮 n个葡萄糖单元
同分异构 不是同分异构
物质 葡萄糖 麦芽糖 蔗糖 淀粉 纤维素
分子式
类别
溶解性
甜味
结构
关系
