人教版高二化学必修二第三章第二节第二课时:苯(共24张PPT)
文档属性
| 名称 | 人教版高二化学必修二第三章第二节第二课时:苯(共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 888.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-21 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
学习目标
第二节 来自石油和煤的两种基本化工原料
第2课时 苯
1.了解苯的物理性质及其来源和应用。
2.掌握苯的分子结构特点。
3.知道苯能够发生氧化反应、加成反应、取代反应。
1825年,英国科学家法拉第在煤气灯中首先发现油状液体苯,并测得其含碳量,确定其最简式为CH,法拉第将这种液体称为“氢的重碳化合物” ;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,分子式为C6H6。
一、苯的结构和性质
现代苯来源于石油的催化重整和煤的干馏产品煤焦油中分馏而得
(1)苯是无色带有特殊气味的液体,有毒
(2)密度比水小,不溶于水
(4)苯的熔沸点低:沸点 80.1℃, 易挥发
熔点 5.5℃(用冰冷却,可得无色晶体)
(3)是一种重要溶剂
1. 苯的物理性质
苯的可能结构:
CH≡C—CH2—CH2—C≡CH CH2=C=CH—CH=C=CH2
CH2=CH—CH=CH—C≡CH ……
讨论:若苯分子为上述结构之一,则其应具有什么重要化学性质?可设计怎样的实验来证明?
根据苯的分子式(C6H6)推测其结构
现象
注:苯不能与Br2水反应,但能萃取溴水中的Br2而使溴水褪色
液体分层,上层橙红色,下层几乎无色
实验3—1: 验证苯的分子结构
结论:苯分子的结构中不存在碳碳双键或碳碳三键。
实验: 分别往酸性KMnO4和Br2水加入苯,振荡
液体分层,上层无色,下层为紫红色
KMnO4溶液:
Br2水:
那么苯分子到底是怎么的结构呢? 阅读课本71页的科学史话:法拉第的对苯发现和凯库勒发现苯环结构的传奇----- “梦的启示”。
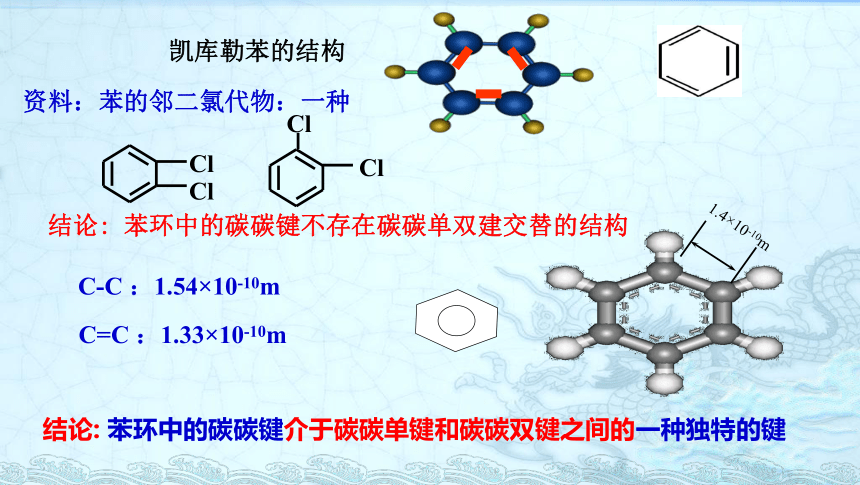
凯库勒苯的结构
资料:苯的邻二氯代物:一种
Cl
Cl
Cl
Cl
结论: 苯环中的碳碳键不存在碳碳单双建交替的结构
C-C :1.54×10-10m
C=C :1.33×10-10m
结论: 苯环中的碳碳键介于碳碳单键和碳碳双键之间的一种独特的键
1.4×10-10m
结构式:
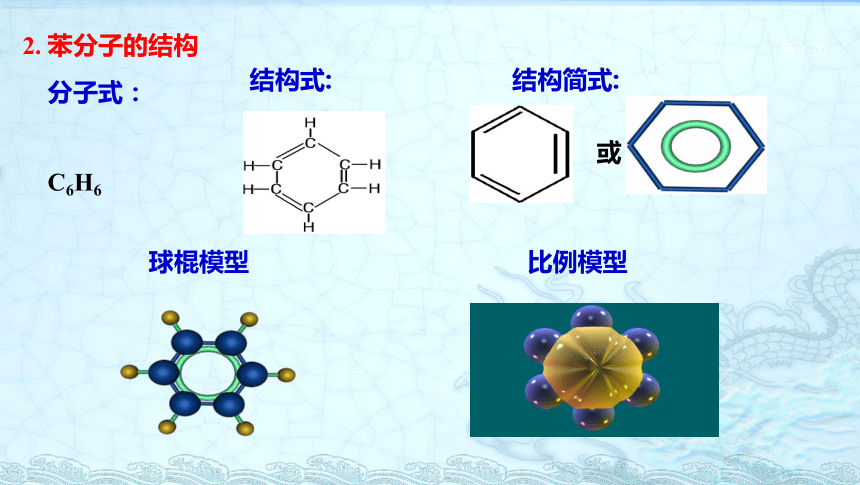
2. 苯分子的结构
分子式:
C6H6
结构简式:
或
球棍模型
比例模型
结构特点:
1.具有平面正六边形结构,所有原子(十二原子)均在同一平面上
2.苯环中所有碳碳键等同,是一种介于单键和双键之间的独特的键,
键角是120°
3.共一条直线的原子最多有四个
4.苯的邻二氯代物只有一种,即 是同种物质
Cl
Cl
Cl
Cl
例1.按要求回答下列问题:
①. 最多有多少个原子共面?
13个
解析:与苯环直接相连原子和苯环上原子共面,共有12个,单键可以旋转,从而—CH3上有一个H与苯环共面,最多13个共面。
②. 最多有多少个原子共面?
16个
解析:苯环和乙烯上所有原子都可以共面,所以最多16个共面。
③. 最多有多少个原子共面?最多有多少原子在一条直线上?
17个 4个
练1.下列有机分子中,所有原子不可能处于同一平面的是( )
解析:首先要熟悉常见分子的结构
甲烷(CH4)是正四面体结构,其分子中最多有3个原子共面;
乙烯(CH2===CH2)是平面形结构,其分子中所有原子共面;
苯(C6H6)是平面正六边形结构,其分子中所有原子共面。
其次对于一些复杂的有机物分子结构,要解剖成若干个基本单元,由整体到局部,然后再回到整体
最后把握住单键可以旋转,双键不能旋转
D
3. 苯的化学性质
3.1 氧化反应
(1)在空气里燃烧火焰明亮且带有黑烟
(2)苯不能被酸性KMnO4溶液氧化
2C6H6 + 15O2 12CO2 + 6H2O
点燃
3.2 苯的取代反应
苯+
液溴
铁
水
现象:烧瓶中产生红棕色的蒸气;
导管口有白雾;
锥形瓶中滴入AgNO3溶液,出现浅黄色沉淀。
烧瓶中液体倒入盛有水的烧杯中,烧杯底部呈油状的褐色(溶解了溴的溴苯)液体
Br + HBr
(溴苯)
FeBr3
H + Br Br
四氯化碳
溴苯是无色油状液体,不溶于水,ρ>ρ水
先加苯,再加溴,最后加入还原铁粉
(1)与液溴的反应
反应装置中长导管作用:
①导气 ②冷凝回流,提高原料利用率
洗气瓶盛装试剂及作用:
四氯化碳等有机溶剂,吸收挥发出的Br2,避免对HBr的检验产生干扰。
锥形瓶中的导管下口位置:
紧贴液面不能浸没在溶液中,生成的HBr极易溶于水,产生倒吸
还原铁粉的作用:
催化剂,实际其催化剂作用的的FeBr3,FeBr3在实验室难以保存
粗溴苯的提纯方法:
水洗
NaOH溶液洗
干燥
蒸馏
水洗
除苯
除水,常用无水硫酸镁
除过量的碱和生成的盐
除溴
除溴化铁和溴化氢
(2)与浓硝酸的反应——硝化反应
先配置混酸:将浓硫酸慢慢倒入浓硝酸中,并不断搅拌,以减少浓硝酸的挥发与分解。
等混酸的温度冷却到50 ~60 ℃以下,再慢慢加入苯,并振荡,减少苯的挥发、浓硝酸的挥发与分解,同时避免苯与浓硫酸在50 ~60 ℃发生副反应。
反应条件: 50 ~60 ℃水浴加热,温度计置于水浴中
长导管作用: 使挥发的反应物冷凝回流,提高原料的利用率
水浴加热优点:便于控温,受热均匀
NO2 + H2O
浓硫酸
50~60℃
(硝基苯)
H + HO NO2
硝基苯是一种无色油状液体,有苦杏仁气味,有毒,密度比水大,不溶于水。
硝基:-NO2(注意与NO2、NO2- 区别)
硝基苯的提纯方法:
水洗
NaOH溶液洗
干燥
蒸馏
水洗
浓硫酸作用:
催化剂和吸水剂
(3)苯的磺化
条件:70℃-80℃共热
3.2 苯的加成反应
(环己烷)
+3H2
Ni
△
4. 苯的用途
(1)苯常用于有机溶剂;
(2)是重要的化工原料。
对比项 甲烷 乙烯 苯
空间构型 正四面体 平面型 平面正六边形
共平面原子数 3 6 12
典型化学键 碳氢键 碳碳双键 一种介于单键与双
键之间的独特的键
取代反应 易 难 催化剂
加成反应 不 易 催化剂
可燃性 易燃
溴水 不反应 加成,褪色 萃取,水层褪色
KMnO4(H+) 不反应 氧化,褪色 不反应
甲烷、乙烯、苯的比较
芳香族化合物:含有一个或多个苯环的化合物
芳香烃:含有一个或多个苯环的烃类。
苯的同系物:苯环和烷基构成的化合物。CnH2n-6
二. 苯的同系物
(1)苯的同系物必含有且仅含有一个苯环,在组成上比苯多一个或若干个CH2原子团。
(2)通式:CnH2n-6(n≥6)
因此,苯的同系物只有苯环上的取代基是烷基时,才属于苯的同系物。
乙苯
邻二甲苯
间二甲苯
对二甲苯
同分异构体
条件一:光照;
条件二:FeBr3
思考:甲苯和溴在一定条件下可以生成 种一取代物
四
苯的同系物化学性质与苯相似,但比苯活泼,多数能被酸性KMnO4溶液氧化。
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
H
|
—C—H
|
H
H
| |
—C—C—
| |
H
C
|
—C—C
|
C
×
√
√
思考: (苯乙烯)使酸性高门酸价褪色的原因可能是什么?
CH=CH2
解析:①与苯环直接相连的碳原子上有氢原子; ②乙烯基
例2.苯的二溴取代物有?????? 种同分异构体。写出它们的结构简式。
Br
Br
Br
Br
Br
Br
3
练2. 下列各组物质中可以用分液漏斗分离的( )
A. 酒精与碘 B. 溴与四氯化碳
C. 硝基苯与水 D. 苯与溴苯
C
例3.苯分子实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有( )
①苯的间位二元取代物只有一种。
②苯的邻位二元取代物只有一种。
③苯不能使酸性KMnO4溶液褪色。
④苯能在一定条件下与氢气反应生成环己烷。
⑤苯在FeBr3存在的条件下同液溴发生取代反应。
A.①③④ B.③④⑤
C.②③⑤ D.①③⑤
C
C
学习目标
第二节 来自石油和煤的两种基本化工原料
第2课时 苯
1.了解苯的物理性质及其来源和应用。
2.掌握苯的分子结构特点。
3.知道苯能够发生氧化反应、加成反应、取代反应。
1825年,英国科学家法拉第在煤气灯中首先发现油状液体苯,并测得其含碳量,确定其最简式为CH,法拉第将这种液体称为“氢的重碳化合物” ;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,分子式为C6H6。
一、苯的结构和性质
现代苯来源于石油的催化重整和煤的干馏产品煤焦油中分馏而得
(1)苯是无色带有特殊气味的液体,有毒
(2)密度比水小,不溶于水
(4)苯的熔沸点低:沸点 80.1℃, 易挥发
熔点 5.5℃(用冰冷却,可得无色晶体)
(3)是一种重要溶剂
1. 苯的物理性质
苯的可能结构:
CH≡C—CH2—CH2—C≡CH CH2=C=CH—CH=C=CH2
CH2=CH—CH=CH—C≡CH ……
讨论:若苯分子为上述结构之一,则其应具有什么重要化学性质?可设计怎样的实验来证明?
根据苯的分子式(C6H6)推测其结构
现象
注:苯不能与Br2水反应,但能萃取溴水中的Br2而使溴水褪色
液体分层,上层橙红色,下层几乎无色
实验3—1: 验证苯的分子结构
结论:苯分子的结构中不存在碳碳双键或碳碳三键。
实验: 分别往酸性KMnO4和Br2水加入苯,振荡
液体分层,上层无色,下层为紫红色
KMnO4溶液:
Br2水:
那么苯分子到底是怎么的结构呢? 阅读课本71页的科学史话:法拉第的对苯发现和凯库勒发现苯环结构的传奇----- “梦的启示”。
凯库勒苯的结构
资料:苯的邻二氯代物:一种
Cl
Cl
Cl
Cl
结论: 苯环中的碳碳键不存在碳碳单双建交替的结构
C-C :1.54×10-10m
C=C :1.33×10-10m
结论: 苯环中的碳碳键介于碳碳单键和碳碳双键之间的一种独特的键
1.4×10-10m
结构式:
2. 苯分子的结构
分子式:
C6H6
结构简式:
或
球棍模型
比例模型
结构特点:
1.具有平面正六边形结构,所有原子(十二原子)均在同一平面上
2.苯环中所有碳碳键等同,是一种介于单键和双键之间的独特的键,
键角是120°
3.共一条直线的原子最多有四个
4.苯的邻二氯代物只有一种,即 是同种物质
Cl
Cl
Cl
Cl
例1.按要求回答下列问题:
①. 最多有多少个原子共面?
13个
解析:与苯环直接相连原子和苯环上原子共面,共有12个,单键可以旋转,从而—CH3上有一个H与苯环共面,最多13个共面。
②. 最多有多少个原子共面?
16个
解析:苯环和乙烯上所有原子都可以共面,所以最多16个共面。
③. 最多有多少个原子共面?最多有多少原子在一条直线上?
17个 4个
练1.下列有机分子中,所有原子不可能处于同一平面的是( )
解析:首先要熟悉常见分子的结构
甲烷(CH4)是正四面体结构,其分子中最多有3个原子共面;
乙烯(CH2===CH2)是平面形结构,其分子中所有原子共面;
苯(C6H6)是平面正六边形结构,其分子中所有原子共面。
其次对于一些复杂的有机物分子结构,要解剖成若干个基本单元,由整体到局部,然后再回到整体
最后把握住单键可以旋转,双键不能旋转
D
3. 苯的化学性质
3.1 氧化反应
(1)在空气里燃烧火焰明亮且带有黑烟
(2)苯不能被酸性KMnO4溶液氧化
2C6H6 + 15O2 12CO2 + 6H2O
点燃
3.2 苯的取代反应
苯+
液溴
铁
水
现象:烧瓶中产生红棕色的蒸气;
导管口有白雾;
锥形瓶中滴入AgNO3溶液,出现浅黄色沉淀。
烧瓶中液体倒入盛有水的烧杯中,烧杯底部呈油状的褐色(溶解了溴的溴苯)液体
Br + HBr
(溴苯)
FeBr3
H + Br Br
四氯化碳
溴苯是无色油状液体,不溶于水,ρ>ρ水
先加苯,再加溴,最后加入还原铁粉
(1)与液溴的反应
反应装置中长导管作用:
①导气 ②冷凝回流,提高原料利用率
洗气瓶盛装试剂及作用:
四氯化碳等有机溶剂,吸收挥发出的Br2,避免对HBr的检验产生干扰。
锥形瓶中的导管下口位置:
紧贴液面不能浸没在溶液中,生成的HBr极易溶于水,产生倒吸
还原铁粉的作用:
催化剂,实际其催化剂作用的的FeBr3,FeBr3在实验室难以保存
粗溴苯的提纯方法:
水洗
NaOH溶液洗
干燥
蒸馏
水洗
除苯
除水,常用无水硫酸镁
除过量的碱和生成的盐
除溴
除溴化铁和溴化氢
(2)与浓硝酸的反应——硝化反应
先配置混酸:将浓硫酸慢慢倒入浓硝酸中,并不断搅拌,以减少浓硝酸的挥发与分解。
等混酸的温度冷却到50 ~60 ℃以下,再慢慢加入苯,并振荡,减少苯的挥发、浓硝酸的挥发与分解,同时避免苯与浓硫酸在50 ~60 ℃发生副反应。
反应条件: 50 ~60 ℃水浴加热,温度计置于水浴中
长导管作用: 使挥发的反应物冷凝回流,提高原料的利用率
水浴加热优点:便于控温,受热均匀
NO2 + H2O
浓硫酸
50~60℃
(硝基苯)
H + HO NO2
硝基苯是一种无色油状液体,有苦杏仁气味,有毒,密度比水大,不溶于水。
硝基:-NO2(注意与NO2、NO2- 区别)
硝基苯的提纯方法:
水洗
NaOH溶液洗
干燥
蒸馏
水洗
浓硫酸作用:
催化剂和吸水剂
(3)苯的磺化
条件:70℃-80℃共热
3.2 苯的加成反应
(环己烷)
+3H2
Ni
△
4. 苯的用途
(1)苯常用于有机溶剂;
(2)是重要的化工原料。
对比项 甲烷 乙烯 苯
空间构型 正四面体 平面型 平面正六边形
共平面原子数 3 6 12
典型化学键 碳氢键 碳碳双键 一种介于单键与双
键之间的独特的键
取代反应 易 难 催化剂
加成反应 不 易 催化剂
可燃性 易燃
溴水 不反应 加成,褪色 萃取,水层褪色
KMnO4(H+) 不反应 氧化,褪色 不反应
甲烷、乙烯、苯的比较
芳香族化合物:含有一个或多个苯环的化合物
芳香烃:含有一个或多个苯环的烃类。
苯的同系物:苯环和烷基构成的化合物。CnH2n-6
二. 苯的同系物
(1)苯的同系物必含有且仅含有一个苯环,在组成上比苯多一个或若干个CH2原子团。
(2)通式:CnH2n-6(n≥6)
因此,苯的同系物只有苯环上的取代基是烷基时,才属于苯的同系物。
乙苯
邻二甲苯
间二甲苯
对二甲苯
同分异构体
条件一:光照;
条件二:FeBr3
思考:甲苯和溴在一定条件下可以生成 种一取代物
四
苯的同系物化学性质与苯相似,但比苯活泼,多数能被酸性KMnO4溶液氧化。
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
H
|
—C—H
|
H
H
| |
—C—C—
| |
H
C
|
—C—C
|
C
×
√
√
思考: (苯乙烯)使酸性高门酸价褪色的原因可能是什么?
CH=CH2
解析:①与苯环直接相连的碳原子上有氢原子; ②乙烯基
例2.苯的二溴取代物有?????? 种同分异构体。写出它们的结构简式。
Br
Br
Br
Br
Br
Br
3
练2. 下列各组物质中可以用分液漏斗分离的( )
A. 酒精与碘 B. 溴与四氯化碳
C. 硝基苯与水 D. 苯与溴苯
C
例3.苯分子实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有( )
①苯的间位二元取代物只有一种。
②苯的邻位二元取代物只有一种。
③苯不能使酸性KMnO4溶液褪色。
④苯能在一定条件下与氢气反应生成环己烷。
⑤苯在FeBr3存在的条件下同液溴发生取代反应。
A.①③④ B.③④⑤
C.②③⑤ D.①③⑤
C
C
