人教版高二化学选修3第三章第一节 晶体的常识(共17张PPT)
文档属性
| 名称 | 人教版高二化学选修3第三章第一节 晶体的常识(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 569.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-23 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第三章 晶体的结构与性质
第一节 晶体的常识
一、晶体与非晶体
1、晶体与非晶体
晶体——具有规则几何外形的固体
非晶体——没有规则几何外形的固体 又称玻璃体
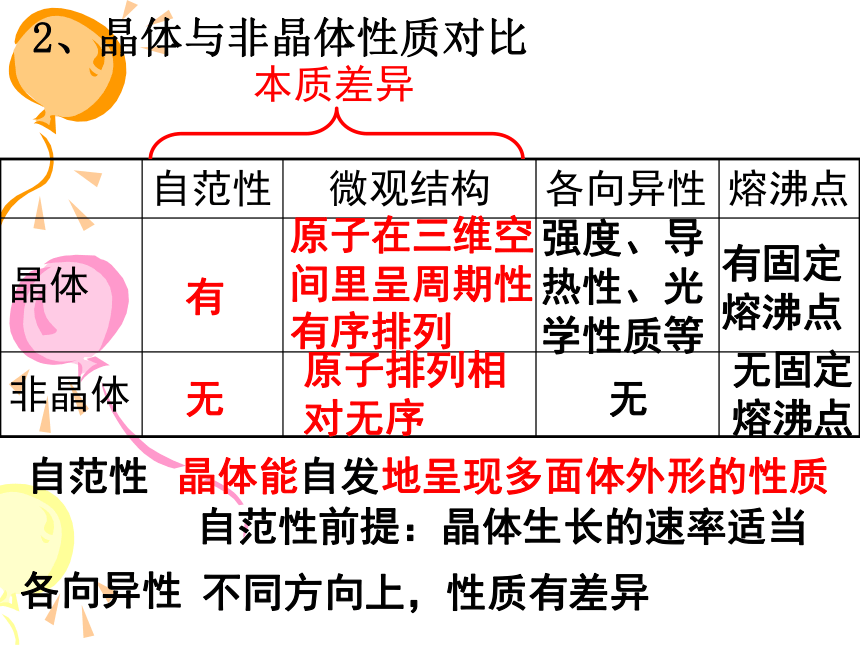
2、晶体与非晶体性质对比
有
无
原子在三维空间里呈周期性有序排列
原子排列相对无序
强度、导热性、光学性质等
无
有固定熔沸点
无固定 熔沸点
自范性
晶体能自发地呈现多面体外形的性质
自范性前提:晶体生长的速率适当
本质差异
各向异性
不同方向上,性质有差异
自范性 微观结构 各向异性 熔沸点
晶体
非晶体
3、晶体形成的途径
①熔融态物质凝固
②气态物质冷却不经液态直接凝固(凝华)
③溶质从溶液中析出
4、晶体的鉴别
①物理性质差异
如:外形、硬度、熔点、折光率
②最科学的方法是对固体进行X-射线衍射实验
1、下列关于晶体与非晶体的说法正确的是
A、晶体一定比非晶体的熔点高
B、晶体有自范性但排列无序
C、非晶体无自范性而且排列无序
D、固体SiO2一定是晶体
2、区别晶体与非晶体最可靠的科学方法是
A、熔沸点 B、硬度
C、颜色 D、x-射线衍射实验
C
D
[课堂练习]
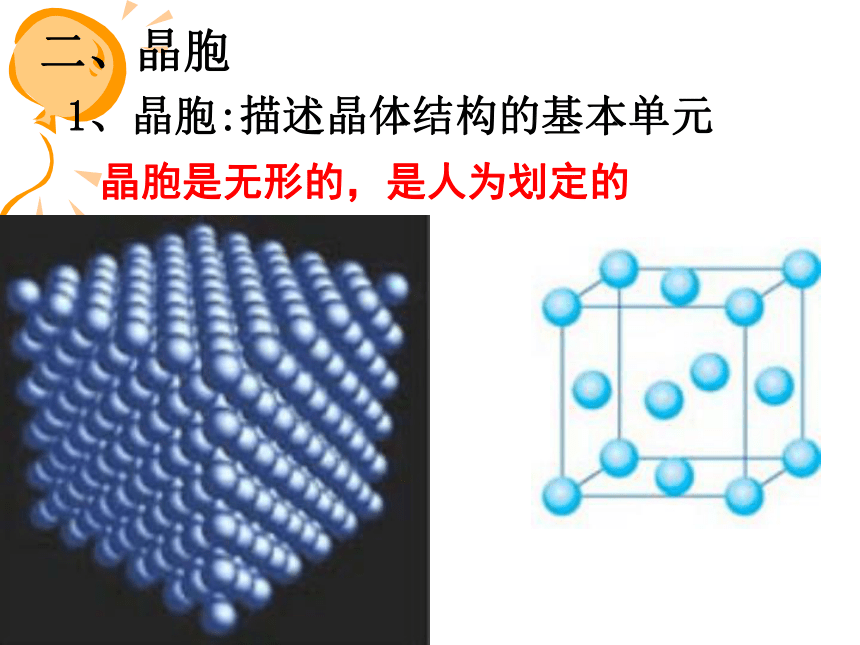
二、晶胞
1、晶胞:描述晶体结构的基本单元
晶胞是无形的,是人为划定的
2、晶胞特征
一般是平行六面体
晶体由晶胞“无隙并置”而成
平行六面体
无隙并置
3、三种典型立方晶体结构
4.晶胞中原子个数的计算
晶胞顶角原子为8个晶胞共用,每个晶胞占1/8
晶胞棱上原子为4个晶胞共用,每个晶胞占1/4
晶胞面上原子为2个晶胞共用,每个晶胞占1/2
晶胞内部的原子为1个晶胞独自占有,即为1
1、现有甲、乙、丙、丁四种晶胞,可推知:甲晶体中A与B的离子个数比为 ;乙晶体的化学式为 ;丙晶体的化学式为______;丁晶体可能的化学式为______。
1:1
C2D
EF
XY3Z
2、下图依次是金属钠(Na)、金属锌(Zn)、碘(I2)、晶胞的示意图,数一数,它们分别平均含有几个原子?
Zn
I2
分别平均含有:
2
2
8
3、钙-钛矿晶胞结构如图所示。观察钙-钛矿晶胞结构,求该晶体中,钙、钛、氧的微粒个数比为多少?
钙、钛、氧的微粒个数比=1:1:3
4、下图是CO2分子晶体的晶胞结构示意图,其中有多少个原子?
5、最近发现一种由钛原子和碳原子构成的气态团簇分子,如下图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是 。
Ti14C13
6
第三章 晶体的结构与性质
第一节 晶体的常识
一、晶体与非晶体
1、晶体与非晶体
晶体——具有规则几何外形的固体
非晶体——没有规则几何外形的固体 又称玻璃体
2、晶体与非晶体性质对比
有
无
原子在三维空间里呈周期性有序排列
原子排列相对无序
强度、导热性、光学性质等
无
有固定熔沸点
无固定 熔沸点
自范性
晶体能自发地呈现多面体外形的性质
自范性前提:晶体生长的速率适当
本质差异
各向异性
不同方向上,性质有差异
自范性 微观结构 各向异性 熔沸点
晶体
非晶体
3、晶体形成的途径
①熔融态物质凝固
②气态物质冷却不经液态直接凝固(凝华)
③溶质从溶液中析出
4、晶体的鉴别
①物理性质差异
如:外形、硬度、熔点、折光率
②最科学的方法是对固体进行X-射线衍射实验
1、下列关于晶体与非晶体的说法正确的是
A、晶体一定比非晶体的熔点高
B、晶体有自范性但排列无序
C、非晶体无自范性而且排列无序
D、固体SiO2一定是晶体
2、区别晶体与非晶体最可靠的科学方法是
A、熔沸点 B、硬度
C、颜色 D、x-射线衍射实验
C
D
[课堂练习]
二、晶胞
1、晶胞:描述晶体结构的基本单元
晶胞是无形的,是人为划定的
2、晶胞特征
一般是平行六面体
晶体由晶胞“无隙并置”而成
平行六面体
无隙并置
3、三种典型立方晶体结构
4.晶胞中原子个数的计算
晶胞顶角原子为8个晶胞共用,每个晶胞占1/8
晶胞棱上原子为4个晶胞共用,每个晶胞占1/4
晶胞面上原子为2个晶胞共用,每个晶胞占1/2
晶胞内部的原子为1个晶胞独自占有,即为1
1、现有甲、乙、丙、丁四种晶胞,可推知:甲晶体中A与B的离子个数比为 ;乙晶体的化学式为 ;丙晶体的化学式为______;丁晶体可能的化学式为______。
1:1
C2D
EF
XY3Z
2、下图依次是金属钠(Na)、金属锌(Zn)、碘(I2)、晶胞的示意图,数一数,它们分别平均含有几个原子?
Zn
I2
分别平均含有:
2
2
8
3、钙-钛矿晶胞结构如图所示。观察钙-钛矿晶胞结构,求该晶体中,钙、钛、氧的微粒个数比为多少?
钙、钛、氧的微粒个数比=1:1:3
4、下图是CO2分子晶体的晶胞结构示意图,其中有多少个原子?
5、最近发现一种由钛原子和碳原子构成的气态团簇分子,如下图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是 。
Ti14C13
6
