人教版必修一 第五章 第1节 降低化学反应活化能的酶47PPT
文档属性
| 名称 | 人教版必修一 第五章 第1节 降低化学反应活化能的酶47PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 12.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2020-05-22 00:00:00 | ||
图片预览









文档简介
(共47张PPT)
第五章 细胞的能量供应和利用
第1节 降低化学反应活化能的酶
1、为什么斯帕兰扎尼将肉块放在金属笼中?
2、对肉块起消化作用的是什么物质?
资料:1773年,意大利科学家斯帕兰札尼设计了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鹰把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内的肉块消失了。
排除了胃对肉块的物理性消化。
一定是某种物质进入到金属笼中,使肉块分解了。
后来证实该物质是胃蛋白酶。
细胞中每时每刻都进行着许多化学反应的统称。
线粒体
核糖体
是细胞生命活动的基础
细胞代谢
叶绿体
绝大多数细胞代谢,需要酶的参与
酶在细胞代谢中的作用
细胞代谢是细胞生命活动的基础,但代谢也会产生对细胞有害的物质,如过氧化氢。而细胞中含有过氧化氢酶,能将过氧化氢分解,变成氧和水
一、酶的作用和本质
不超过20℃保存
过氧化氢严禁与Fe3+等金属化合物混合存放。这是为什么呢?
加热,Fe3+等也能促使过氧化氢分解
(1)目的要求:
比较过氧化氢在不同条件下分解的快慢,了解过氧化氢的作用和意义。
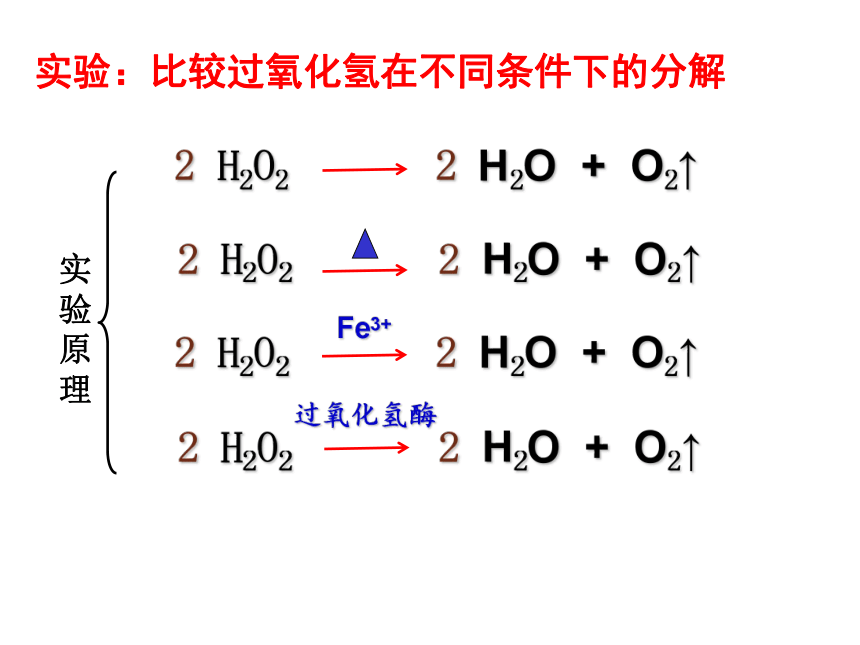
(2)实验原理:
H2O2在水浴加热、FeCl3溶液、肝脏研磨液中过氧化氢酶的作用下加速分解
2 H2O2 2 H2O + O2↑
2 H2O2 2 H2O + O2↑
2 H2O2 2 H2O + O2↑
Fe3+
过氧化氢酶
2 H2O2 2 H2O + O2↑
实验:比较过氧化氢在不同条件下的分解
实验原理
(3)实验材料:
新鲜的质量分数为20%的肝脏研磨液
质量分数为3.5%的FeCl3溶液
体积分数为3%的过氧化氢溶液
量筒、试管、滴管、试管架、卫生香、火柴、试管夹、大烧杯、三脚架、石棉网、温度计
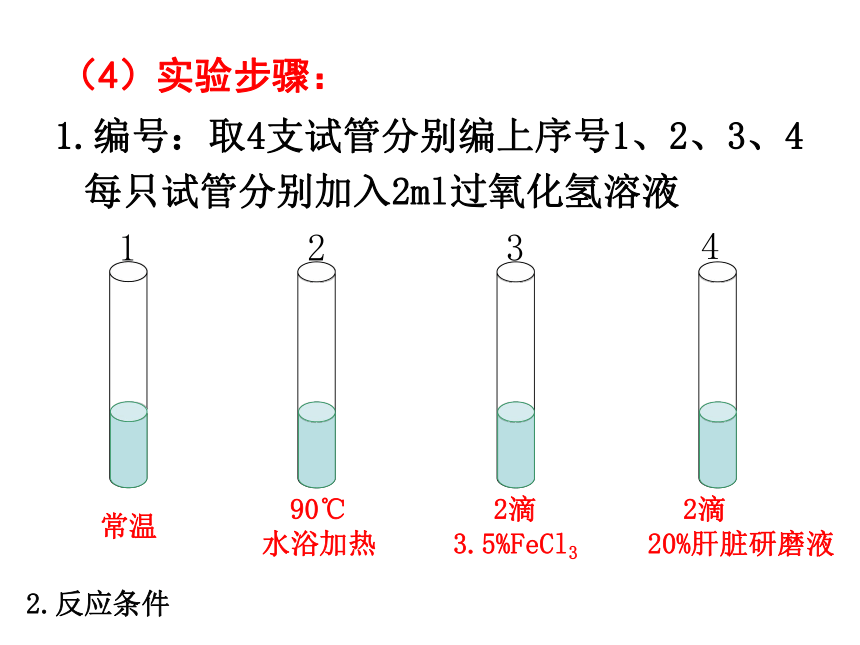
(4)实验步骤:
1.编号:取4支试管分别编上序号1、2、3、4
每只试管分别加入2ml过氧化氢溶液
1
2
3
4
2.反应条件
常温
90℃
水浴加热
2滴
3.5%FeCl3
2滴
20%肝脏研磨液
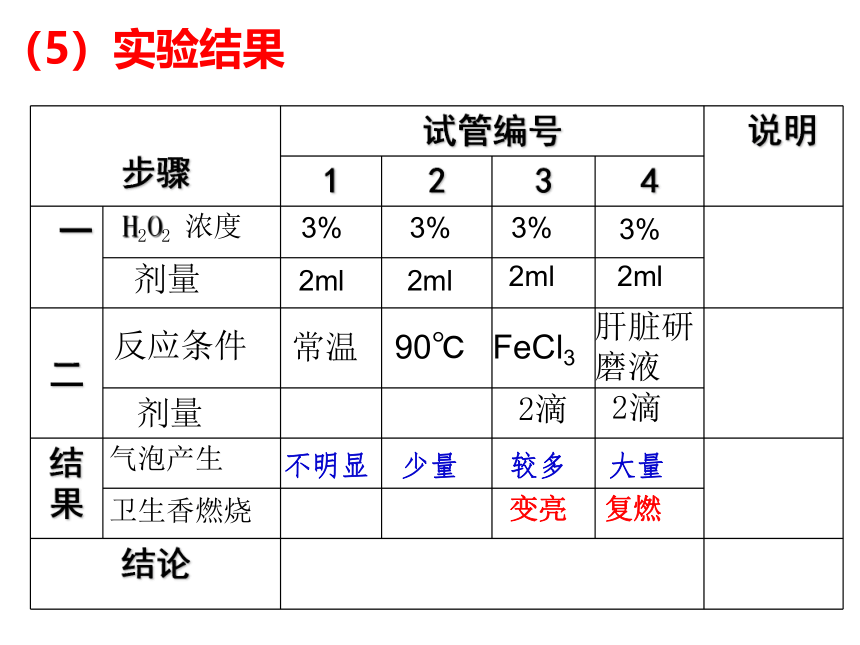
(5)实验结果
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
肝脏研磨液
2滴
不明显
少量
较多
大量
变亮
复燃
反应条件
H2O2 浓度
剂量
剂量
气泡产生
卫生香燃烧
2滴
步骤 试管编号 说明
1 2 3 4
一
二
结果
结论
1)与1号试管相比,2号试管产生的气泡多,这一现象说明了什么?
2号试管,加热能促进H2O2的分解,提高反应速率;
2) 3、4号试管未经加热,也有大量气泡产生,这说明了什么?
FeCl3中的Fe3+ 和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率,
3)3号试管和4号试管相比,4号试管中的反应速率快,这说明了什么?
过氧化氢酶比Fe3+ 的催化效率高得多,
(6)思考与讨论
实验结论:
1.酶能催化化学反应的进行
2.酶的催化效率高于无机催化剂
变量
自变量
因变量
无关变量
对照实验
实验过程中可以变化的因素。
其中人为改变的变量。
随着自变量的变化而变化的变量。
实除自变量外,实验过程中可能还会因一些可变因素,?对实验结果造成影响,?这些变量称为无关变量。
除了一个因素以外,其余因素都保持不变的实验。对照实验一般设置对照组和实验组
Y= f(x)+b
实验设计的基本原则:
1、对照性原则
2、科学性原则
3、单一变量和等量性原则
4、平行重复原则
自变量、因变量和无关变量的关系
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
新鲜肝脏研磨液
2滴清水
2滴清水
2滴
2滴
不明显
少量
较多
大量
不复燃
不复燃
变亮
复燃
过氧化氢在不同条件下的分解速率不一样
反应条件
对照组
实验组
(7)实验变量分析:
步骤 试管编号 说明
1 2 3 4
一 H2O2 浓度
剂量
二
剂量
结果 气泡产生
卫生香燃烧
结论
分子从常态转变为容易发生化学反应的活跃状态所需的能量称为活化能。
酶是如何催化生物化学反应?
能量
加热
思考:
1、与1号试管相比,为什么2号试管加热后过氧化氢就能分解?
加热使反应加快的本质:加热使过氧化氢分子得到能量,从常态转变为容易分解的活跃状态。
能量
反应过程
酶使活化能降低
没有酶催化
有酶的催化
各条件使过氧化氢分解加快的本质:
加热:
为反应物分子提供能量(活化能),使其达到活跃状态
Fe3+:
降低化学反应的活化能
酶:
更显著地降低化学反应的活化能
想一想:如何表示?
无催化剂曲线:______
酶促反应曲线:______
无酶促反应所需活化能:______
酶促反应所需活化能: ______
酶降低的活化能: ______
曲线B
曲线A
E2
E3—E2
E3
那么酶的本质是什么呢?
正是由于酶的催化作用,细胞代谢才能在温和的条件下快速进行。
二、 酶的本质
阅读教材P81-82,“关于酶本质的探索”
思考:巴斯德、李比希、毕希纳、萨姆纳、切赫和奥特曼的观点各是什么?
葡萄酒为什么变酸?
葡萄酒为什么变酸?
2. 那时人们认为酿酒过程是一个什么过程?
纯化学过程
3.如果你是巴斯德,你会从哪里入手来研究葡萄酒变酸的原因?
酵母
1. 酿酒的基本原理:
糖 酒精+CO2
关于酶本质的探索
对这一问题的争论有哪些观点?代表人物分别是谁?
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
糖 酒精+CO2
关于酶本质的探索
对这一问题的争论有哪些观点?代表人物分别是谁?
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
他们争论的焦点是什么,出现争论的原因是什么?
糖 酒精+CO2
关于酶本质的探索
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
他们争论的焦点是什么,出现争论的原因是什么?
是谁通过怎样的实验结束了这场争论?得到什么结论?
是谁最先鉴定出酶的化学本质?为什么在他之前很难鉴定?
脲酶是蛋白质
少数RNA也具有生物催化作用
巴斯德之前
发酵是纯化学反应,与生命活动无关
巴斯德
发酵与活细胞有关,发酵是整个细胞而不是细胞中某些物质起作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
毕希纳
酵母细胞中的某些物质能够在酵母细胞破碎后继续起催化作用,就像在活酵母细胞中一样
萨姆纳
用丙酮提取酶,酶是蛋白质
李比希
切赫、奥特曼
少数RNA也具有生物催化功能
总结酶的定义
阅读教材81页“资料分析”,完成练习题
PK
酶(Enzyme)的概念:
绝大多数是蛋白质,
少数的是RNA。
酶是 产生的一类具有 作用的 。
活细胞
催化
有机物
酶是一类生物催化剂
二、酶的特性
1、酶具有高效性
酶的催化效率是无机催化剂的107 ~1013 倍
酶高效性的曲线
(1)催化剂可加快化学反应速率,与无机催化剂相比,酶的催化效率更高。
(2)酶只能缩短达到化学反应平衡所需时间,不改变化学反应的平衡点。
蛋白酶只能催化蛋白质水解,但不能催化脂肪、淀粉等的水解。
由上述资料大胆的提出问题,作出你的假设。
酶具有专一性
口腔里有唾液淀粉酶,可塞进牙缝里的肉丝两天后还没被消化。
思考:
酶催化反应的机制(底物-酶结合)
2、酶具有专一性
淀粉酶只能催化淀粉水解,不能催化蔗糖水解。
验证淀粉酶的专一性
淀粉溶液 蔗糖溶液
实验步骤 一
二
三
实验现象
结论
2、感冒发烧的你为什么不想吃饭呢?
1、实验证明,用加酶洗衣粉时,温水的洗涤效果要比冷水好。
3、我们知道口腔温度和体温差不多,而当我们口腔中的唾液淀粉酶进入胃中以后,却发现,唾液不再具有催化淀粉分解的功能,你能给出合理的解释吗?
(提示:唾液的pH为6.2-7.4,胃液的pH为0.9-1.5)
继续研究:
酶具有高效性和专一性;那么它的这两个特性的发挥是不是在任何条件下都可以呢?
探究影响酶活性的条件
提出问题
作出假设
设计实验
进行实验
分析结果,得出结论
表达和交流
怎样表示酶的活性大小?
通常以单位时间内底物减少的量或产物生成的量(即反应的速度)来表示酶活性的大小。
探究1 温度对酶活性的影响
问题聚焦
1、选择淀粉还是H2O2作为实验材料?
三组,高温,低温和常温
2、设计几组实验?选择几个温度?
H2O2受温度影响会分解
3、观察指标怎么确定,选择什么样的鉴定试剂?为什么不用斐林试剂?
碘液,看是否变蓝,斐林试剂鉴定需要水浴加热,会影响实验结果。
试管各加入2mL可溶性淀粉溶液
1号试管
2号试管
3号试管
1′试管
2 ′试管
3 ′试管
试管各加入2mL淀粉酶溶液
将相应温度下的两试管溶液混合均匀,在各自温度下继续保温2min
试管中各滴加1~2滴碘液,摇匀
蓝 色
不变蓝
蓝 色
温度过高过低,都会影响酶的活性
实 验
步
骤 1
2
3
4
5
观察并记录实验现象
结论
(1)在一定温度范围内,酶促反应速率随温度的升高而_______,但当温度升高到一定限度时,酶促反应速率不仅不再加快反而随着温度的升高而________。
(3)低温影响酶的活性,但不会使酶的_________遭到破坏,温度升高后,酶________恢复活性。但高温会导致酶_________,酶会_______活性。
(2)在一定条件下,酶活性最大时的温度称为该酶的_________。
升高
降低
最适温度
空间结构
能够
变性
空间结构遭到破坏
一般地,动物体内的酶最适温度在35~40℃之间;植物体内的酶最适温度在40~50℃之间;细菌和真菌体内的酶最适温度差别较大。
探究2 pH对酶活性的影响
问题聚焦
1、选择淀粉还是H2O2作为实验材料?
三组,酸性,碱性和中性
2、设计几组实验?选择几个pH?
H2O2,因为在酸性条件下,淀粉会发生水解反应。
3、观察指标怎么确定?
气泡产生数量
探究2. pH对酶活性的影响实验
无明显气泡
无明显气泡
大量气泡
酶的作用需要适宜的pH,pH偏高或偏低都会使酶活性降低。
步骤 项 目 试 管
1 取三支试管分别编号 1 2 3
2 注入新鲜猪肝研磨液 2滴 2滴 2滴
2 各试管分别注入 2mlH2O2 2mlH2O2
2mlH2O2
3 各试管分别滴加 HCl
2ml NaOH
2ml 蒸馏水
2ml
5 观察并记录实验现象(气泡产生多少)
结论
(1)在一定条件下,酶活性最大时的pH值称为该酶的________。偏离该pH,不论升高还是降低,酶促反应速率都会________。
(2)过酸,过碱都会使酶的_________遭到破坏,使酶___________。
降低
最适pH
空间结构
永久失活
一般地,动物体内的酶最适pH在6.5~8.0之间,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶最适pH在4.5~6.5之间。
二、酶的特性
3、酶的作用条件比较温和
1)需要适宜的温度
2)需要适宜的pH值
(1)甲图中在其他条件适宜、酶浓度一定的情况下,酶促反应速率随底物浓度的改变怎样变化?
(2)甲图中:A~B段限制因素:_____________;B以后稳定阶段限制因素:___________________________
(3)乙图显示在底物足够、其他条件适宜的情况下,酶促反应速率和酶浓度之间的关系:________________________________
底物浓度
酶的数量和酶的活性
成正比
酶促反应速率随底物浓度增大而加快,但当底物达到一定浓度后,酶促反应速率不再增大。
温度
pH
酶浓度
底物浓度
酶活性
影响
影响
酶与底物的接触面积
酶促反应速率
第五章 细胞的能量供应和利用
第1节 降低化学反应活化能的酶
1、为什么斯帕兰扎尼将肉块放在金属笼中?
2、对肉块起消化作用的是什么物质?
资料:1773年,意大利科学家斯帕兰札尼设计了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鹰把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内的肉块消失了。
排除了胃对肉块的物理性消化。
一定是某种物质进入到金属笼中,使肉块分解了。
后来证实该物质是胃蛋白酶。
细胞中每时每刻都进行着许多化学反应的统称。
线粒体
核糖体
是细胞生命活动的基础
细胞代谢
叶绿体
绝大多数细胞代谢,需要酶的参与
酶在细胞代谢中的作用
细胞代谢是细胞生命活动的基础,但代谢也会产生对细胞有害的物质,如过氧化氢。而细胞中含有过氧化氢酶,能将过氧化氢分解,变成氧和水
一、酶的作用和本质
不超过20℃保存
过氧化氢严禁与Fe3+等金属化合物混合存放。这是为什么呢?
加热,Fe3+等也能促使过氧化氢分解
(1)目的要求:
比较过氧化氢在不同条件下分解的快慢,了解过氧化氢的作用和意义。
(2)实验原理:
H2O2在水浴加热、FeCl3溶液、肝脏研磨液中过氧化氢酶的作用下加速分解
2 H2O2 2 H2O + O2↑
2 H2O2 2 H2O + O2↑
2 H2O2 2 H2O + O2↑
Fe3+
过氧化氢酶
2 H2O2 2 H2O + O2↑
实验:比较过氧化氢在不同条件下的分解
实验原理
(3)实验材料:
新鲜的质量分数为20%的肝脏研磨液
质量分数为3.5%的FeCl3溶液
体积分数为3%的过氧化氢溶液
量筒、试管、滴管、试管架、卫生香、火柴、试管夹、大烧杯、三脚架、石棉网、温度计
(4)实验步骤:
1.编号:取4支试管分别编上序号1、2、3、4
每只试管分别加入2ml过氧化氢溶液
1
2
3
4
2.反应条件
常温
90℃
水浴加热
2滴
3.5%FeCl3
2滴
20%肝脏研磨液
(5)实验结果
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
肝脏研磨液
2滴
不明显
少量
较多
大量
变亮
复燃
反应条件
H2O2 浓度
剂量
剂量
气泡产生
卫生香燃烧
2滴
步骤 试管编号 说明
1 2 3 4
一
二
结果
结论
1)与1号试管相比,2号试管产生的气泡多,这一现象说明了什么?
2号试管,加热能促进H2O2的分解,提高反应速率;
2) 3、4号试管未经加热,也有大量气泡产生,这说明了什么?
FeCl3中的Fe3+ 和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率,
3)3号试管和4号试管相比,4号试管中的反应速率快,这说明了什么?
过氧化氢酶比Fe3+ 的催化效率高得多,
(6)思考与讨论
实验结论:
1.酶能催化化学反应的进行
2.酶的催化效率高于无机催化剂
变量
自变量
因变量
无关变量
对照实验
实验过程中可以变化的因素。
其中人为改变的变量。
随着自变量的变化而变化的变量。
实除自变量外,实验过程中可能还会因一些可变因素,?对实验结果造成影响,?这些变量称为无关变量。
除了一个因素以外,其余因素都保持不变的实验。对照实验一般设置对照组和实验组
Y= f(x)+b
实验设计的基本原则:
1、对照性原则
2、科学性原则
3、单一变量和等量性原则
4、平行重复原则
自变量、因变量和无关变量的关系
2ml
2ml
2ml
2ml
3%
3%
3%
3%
常温
90℃
FeCl3
新鲜肝脏研磨液
2滴清水
2滴清水
2滴
2滴
不明显
少量
较多
大量
不复燃
不复燃
变亮
复燃
过氧化氢在不同条件下的分解速率不一样
反应条件
对照组
实验组
(7)实验变量分析:
步骤 试管编号 说明
1 2 3 4
一 H2O2 浓度
剂量
二
剂量
结果 气泡产生
卫生香燃烧
结论
分子从常态转变为容易发生化学反应的活跃状态所需的能量称为活化能。
酶是如何催化生物化学反应?
能量
加热
思考:
1、与1号试管相比,为什么2号试管加热后过氧化氢就能分解?
加热使反应加快的本质:加热使过氧化氢分子得到能量,从常态转变为容易分解的活跃状态。
能量
反应过程
酶使活化能降低
没有酶催化
有酶的催化
各条件使过氧化氢分解加快的本质:
加热:
为反应物分子提供能量(活化能),使其达到活跃状态
Fe3+:
降低化学反应的活化能
酶:
更显著地降低化学反应的活化能
想一想:如何表示?
无催化剂曲线:______
酶促反应曲线:______
无酶促反应所需活化能:______
酶促反应所需活化能: ______
酶降低的活化能: ______
曲线B
曲线A
E2
E3—E2
E3
那么酶的本质是什么呢?
正是由于酶的催化作用,细胞代谢才能在温和的条件下快速进行。
二、 酶的本质
阅读教材P81-82,“关于酶本质的探索”
思考:巴斯德、李比希、毕希纳、萨姆纳、切赫和奥特曼的观点各是什么?
葡萄酒为什么变酸?
葡萄酒为什么变酸?
2. 那时人们认为酿酒过程是一个什么过程?
纯化学过程
3.如果你是巴斯德,你会从哪里入手来研究葡萄酒变酸的原因?
酵母
1. 酿酒的基本原理:
糖 酒精+CO2
关于酶本质的探索
对这一问题的争论有哪些观点?代表人物分别是谁?
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
糖 酒精+CO2
关于酶本质的探索
对这一问题的争论有哪些观点?代表人物分别是谁?
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
他们争论的焦点是什么,出现争论的原因是什么?
糖 酒精+CO2
关于酶本质的探索
巴斯德(微生物学家)
是活酵母细胞
的作用
李比希(化学家)
是某些物质在
细胞死亡裂解
后的作用
他们争论的焦点是什么,出现争论的原因是什么?
是谁通过怎样的实验结束了这场争论?得到什么结论?
是谁最先鉴定出酶的化学本质?为什么在他之前很难鉴定?
脲酶是蛋白质
少数RNA也具有生物催化作用
巴斯德之前
发酵是纯化学反应,与生命活动无关
巴斯德
发酵与活细胞有关,发酵是整个细胞而不是细胞中某些物质起作用
引起发酵的是细胞中的某些物质,但这些物质只有在酵母细胞死亡并裂解后才能发挥作用
毕希纳
酵母细胞中的某些物质能够在酵母细胞破碎后继续起催化作用,就像在活酵母细胞中一样
萨姆纳
用丙酮提取酶,酶是蛋白质
李比希
切赫、奥特曼
少数RNA也具有生物催化功能
总结酶的定义
阅读教材81页“资料分析”,完成练习题
PK
酶(Enzyme)的概念:
绝大多数是蛋白质,
少数的是RNA。
酶是 产生的一类具有 作用的 。
活细胞
催化
有机物
酶是一类生物催化剂
二、酶的特性
1、酶具有高效性
酶的催化效率是无机催化剂的107 ~1013 倍
酶高效性的曲线
(1)催化剂可加快化学反应速率,与无机催化剂相比,酶的催化效率更高。
(2)酶只能缩短达到化学反应平衡所需时间,不改变化学反应的平衡点。
蛋白酶只能催化蛋白质水解,但不能催化脂肪、淀粉等的水解。
由上述资料大胆的提出问题,作出你的假设。
酶具有专一性
口腔里有唾液淀粉酶,可塞进牙缝里的肉丝两天后还没被消化。
思考:
酶催化反应的机制(底物-酶结合)
2、酶具有专一性
淀粉酶只能催化淀粉水解,不能催化蔗糖水解。
验证淀粉酶的专一性
淀粉溶液 蔗糖溶液
实验步骤 一
二
三
实验现象
结论
2、感冒发烧的你为什么不想吃饭呢?
1、实验证明,用加酶洗衣粉时,温水的洗涤效果要比冷水好。
3、我们知道口腔温度和体温差不多,而当我们口腔中的唾液淀粉酶进入胃中以后,却发现,唾液不再具有催化淀粉分解的功能,你能给出合理的解释吗?
(提示:唾液的pH为6.2-7.4,胃液的pH为0.9-1.5)
继续研究:
酶具有高效性和专一性;那么它的这两个特性的发挥是不是在任何条件下都可以呢?
探究影响酶活性的条件
提出问题
作出假设
设计实验
进行实验
分析结果,得出结论
表达和交流
怎样表示酶的活性大小?
通常以单位时间内底物减少的量或产物生成的量(即反应的速度)来表示酶活性的大小。
探究1 温度对酶活性的影响
问题聚焦
1、选择淀粉还是H2O2作为实验材料?
三组,高温,低温和常温
2、设计几组实验?选择几个温度?
H2O2受温度影响会分解
3、观察指标怎么确定,选择什么样的鉴定试剂?为什么不用斐林试剂?
碘液,看是否变蓝,斐林试剂鉴定需要水浴加热,会影响实验结果。
试管各加入2mL可溶性淀粉溶液
1号试管
2号试管
3号试管
1′试管
2 ′试管
3 ′试管
试管各加入2mL淀粉酶溶液
将相应温度下的两试管溶液混合均匀,在各自温度下继续保温2min
试管中各滴加1~2滴碘液,摇匀
蓝 色
不变蓝
蓝 色
温度过高过低,都会影响酶的活性
实 验
步
骤 1
2
3
4
5
观察并记录实验现象
结论
(1)在一定温度范围内,酶促反应速率随温度的升高而_______,但当温度升高到一定限度时,酶促反应速率不仅不再加快反而随着温度的升高而________。
(3)低温影响酶的活性,但不会使酶的_________遭到破坏,温度升高后,酶________恢复活性。但高温会导致酶_________,酶会_______活性。
(2)在一定条件下,酶活性最大时的温度称为该酶的_________。
升高
降低
最适温度
空间结构
能够
变性
空间结构遭到破坏
一般地,动物体内的酶最适温度在35~40℃之间;植物体内的酶最适温度在40~50℃之间;细菌和真菌体内的酶最适温度差别较大。
探究2 pH对酶活性的影响
问题聚焦
1、选择淀粉还是H2O2作为实验材料?
三组,酸性,碱性和中性
2、设计几组实验?选择几个pH?
H2O2,因为在酸性条件下,淀粉会发生水解反应。
3、观察指标怎么确定?
气泡产生数量
探究2. pH对酶活性的影响实验
无明显气泡
无明显气泡
大量气泡
酶的作用需要适宜的pH,pH偏高或偏低都会使酶活性降低。
步骤 项 目 试 管
1 取三支试管分别编号 1 2 3
2 注入新鲜猪肝研磨液 2滴 2滴 2滴
2 各试管分别注入 2mlH2O2 2mlH2O2
2mlH2O2
3 各试管分别滴加 HCl
2ml NaOH
2ml 蒸馏水
2ml
5 观察并记录实验现象(气泡产生多少)
结论
(1)在一定条件下,酶活性最大时的pH值称为该酶的________。偏离该pH,不论升高还是降低,酶促反应速率都会________。
(2)过酸,过碱都会使酶的_________遭到破坏,使酶___________。
降低
最适pH
空间结构
永久失活
一般地,动物体内的酶最适pH在6.5~8.0之间,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶最适pH在4.5~6.5之间。
二、酶的特性
3、酶的作用条件比较温和
1)需要适宜的温度
2)需要适宜的pH值
(1)甲图中在其他条件适宜、酶浓度一定的情况下,酶促反应速率随底物浓度的改变怎样变化?
(2)甲图中:A~B段限制因素:_____________;B以后稳定阶段限制因素:___________________________
(3)乙图显示在底物足够、其他条件适宜的情况下,酶促反应速率和酶浓度之间的关系:________________________________
底物浓度
酶的数量和酶的活性
成正比
酶促反应速率随底物浓度增大而加快,但当底物达到一定浓度后,酶促反应速率不再增大。
温度
pH
酶浓度
底物浓度
酶活性
影响
影响
酶与底物的接触面积
酶促反应速率
同课章节目录
- 第一章 走近细胞
- 第1节 从生物圈到细胞
- 第2节 细胞的多样性和统一性
- 第二章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 生命活动的主要承担者──蛋白质
- 第3节 遗传信息的携带者──核酸
- 第4节 细胞中的糖类和脂质
- 第5节 细胞中的无机物
- 第三章 细胞的基本结构
- 第1节 细胞膜──系统的边界
- 第2节 细胞器──系统内的分工合作
- 第3节 细胞核──系统的控制中心
- 第四章 细胞的物质输入和输出
- 第1节 物质跨膜运输的实例
- 第2节 生物膜的流动镶嵌模型
- 第3节 物质跨膜运输的方式
- 第五章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“通货”──ATP
- 第3节 ATP的主要来源──细胞呼吸
- 第4节 能量之源——光与光合作用
- 第六章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和凋亡
- 第4节 细胞的癌变
