人教版高一化学必修二第三章第四节第二课时:油脂的蛋白质(共20张PPT)
文档属性
| 名称 | 人教版高一化学必修二第三章第四节第二课时:油脂的蛋白质(共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 692.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-27 00:00:00 | ||
图片预览




文档简介
(共20张PPT)
学习目标
第四节
基本营养物质
第2课时
油脂和蛋白质
1.认识油脂和蛋白质的主要性质。
2.了解油脂和蛋白质的组成。
3.知道油脂和蛋白质在日常生活、生产中的应用。
我们知道糖吃多了,人会发胖,由于能量的过剩,就会转化成一种更高能量的物质----油脂,油脂是人类主要食物之一,是人体中重要的能源物质,被称为人体的备用油箱,今天我们就共同学习油脂的性质。
一、油脂的组成和结构
1.
油脂的成分
由C、H、O元素组成的,是高级脂肪酸和甘油酯化反应生成的酯。
C17H35COOH
硬脂酸
C17H33COOH
油
酸
C15H31COOH
软脂酸
油
(oil)
脂肪
(fat)
CH2—O—C-C17H35
CH
—
O—C-C17H35
CH2—O—C-C17H35
O
O
O
非油脂
油脂
CH2—O—C-CH3
CH
—O—C-CH3
CH2—O—C-CH3
O
O
O
下列物质是油脂吗?
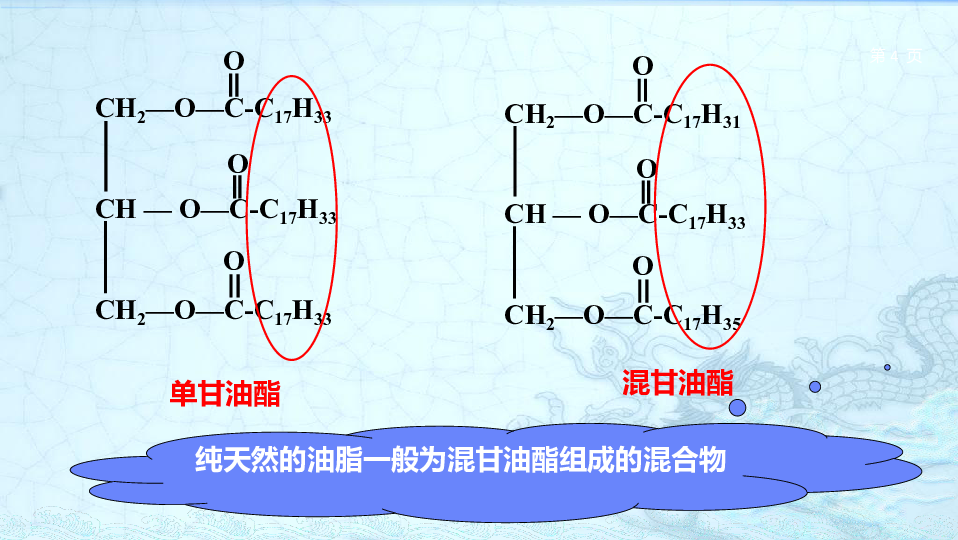
单甘油酯
混甘油酯
纯天然的油脂一般为混甘油酯组成的混合物
CH2—O—C-C17H33
CH
—
O—C-C17H33
CH2—O—C-C17H33
O
O
O
CH2—O—C-C17H31
CH
—
O—C-C17H33
CH2—O—C-C17H35
O
O
O
2.
结构
R1
C
O
O
CH2
R2
C
O
O
CH
R3
C
O
O
CH2
R1、R2、R3代表烃基,它们可以相同,也可以不同。相同时称为单甘油酯,不同时称为混甘油酯。
天然油脂大都是混甘油酯组成的混合物。
3.
分类
植物油
脂肪
如:菜籽油、花生油、豆油、棉籽油
动物油脂呈固态,称脂肪,沸点较高
如:猪油、牛油
油脂
含有不饱和键:C=C,呈液态,沸点低
只有饱和键:C-C
干油酯
4.
物理性质
密度比水的密度小,为0.9~0.95
g/cm3
有明显的油腻感
不溶于水,易溶于有机溶剂
是一种良好的有机溶剂
天然油脂都是混合物,所以没有固定的
熔点、沸点。
二、油脂的化学性质
烃基中含有碳碳双键:可以发生加成反应、
氧化反应
酯基:
可以在酸、碱溶液或脂肪酶中发生水解反应
——油脂兼有酯类和烯烃的性质
R1-C-O-CH2
R2-C-O-CH
R3-C-O-CH2
O=
O=
O=
使溴水或碘水发生加成反应而褪色
使高锰酸钾(H+)因氧化反应而褪色
久置在空气中被氧气氧化而变质
1.油脂在体内的水解
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+3H2O
HOCH2
HOCH
HOCH2
3C17H35COOH
+
脂肪酶
人类由此获得一些必须得脂肪酸。如亚油酸(9,12——十八碳二烯酸)等。
一般不饱和酸比饱和酸对人体更有益。
2.在酸性条件下水解
3.皂化反应
油脂在碱性条件下,生成高级脂肪酸盐和甘油的反应。
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+
3NaOH
3C17H35COONa
CH2OH
CHOH
CH2OH
+
硬脂酸甘油脂
硬
脂
酸
钠
甘油
工业上利用这个反应来制造肥皂。硬脂酸钠是肥皂的有效成分。
混合液
胶状液体
上层:高级
脂肪酸钠
动
植
物
油
脂
下层:甘油、
NaCl溶液
工业制皂流程:
NaOH
△
NaCl
盐析
加填充剂,压滤干燥
肥皂
蒸馏
甘油
盐析:
加入无机盐使某些有机物降低溶解度,从而析出的过程,属于物理变化。这里的盐析是指加入食盐使肥皂析出的过程。
油+H2
脂肪(固态),人造脂肪(硬化油)
一定条件下
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
+
3
H2
催化剂
加热、加压
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
4.
氢化反应(加成反应、硬化反应)
硬化油性质稳定,不易变质,便于运输,可用于制造肥皂、脂肪酸、甘油、人造奶油等。
例1.区别植物油和矿物油的正确方法是(
)
A.加酸性高锰酸钾溶液,振荡
B.加NaOH溶液,煮沸
C.加新制Cu(OH)2悬浊液,煮沸
D.加溴水,振荡
解析:植物油中含有碳碳不饱和键,能使酸性KMnO4溶液或溴水褪色,有些矿物油含有烯烃,也能使溴水或酸性KMnO4溶液褪色,A、D项无法区别;
植物油属于酯类,在NaOH溶液中煮沸时,水解后的生成物能溶于水,矿物油无此性质,故B项可区别植物油和矿物油。
B
物质
油脂
矿物油
脂肪
油
组成
多种高级脂肪酸的甘油酯
多种烃(石油及其分馏产品)
含饱和烃基多
含不饱和烃基多
性质
固态或半固态
液态
具有烃的性质,不能水解
能水解并部分兼有烯烃的性质
鉴别
加含酚酞的NaOH溶液,加热,红色变浅
加含酚酞的NaOH溶液,加热,无变化
油脂和矿物油的比较
1.蛋白质的组成和存在
(1)由C、H、O、N、S、P等元素组成,是氨基酸分子连接的高分子化合物。
(2)主要存在于生物体内,肌肉、毛发、皮肤、角、蹄、酶、激素、抗体、病毒中;在植物中也很丰富,比如大豆、花生、谷物。
2.蛋白质的水解
蛋白质也可以在酶等催化剂作用下水解生成氨基酸
蛋白质
多肽
氨基酸
水解
合成
水解
合成
三、蛋白质
蛋白质在酶等催化剂的作用下水解生成氨基酸。天然蛋白质水解的氨基酸都是α-氨基酸。
R-CH-COOH
NH2
α
CH2-COOH
NH2
甘氨酸
(α-氨基乙酸)
CH3-CH-COOH
NH2
丙氨酸(α-氨基丙酸)
苯丙氨酸(α-氨基-β-苯基丙酸)
-CH2-CH-COOH
NH2
3.
蛋白质的特征反应
实验步骤:取2
mL鸡蛋清于试管中,滴加4滴浓硝酸,在酒精灯上微热。
浓硝酸使蛋白质颜色变黄。
①颜色反应:
蛋白质被灼烧时,有烧焦羽毛的气味。
②蛋白质灼烧:
以上两个反应均可用于鉴别部分蛋白质,
多用灼烧法鉴别羊毛或蚕丝织物的真伪。
4.盐析
现象:有白色絮状物质析出,白色絮状物质放入水中,溶解。
加入某些浓的轻金属盐溶液或铵盐溶液后,降低有机物的溶解度,使之析出,即为盐析。少量的无机盐能促进蛋白质的溶解。是可逆过程,用于分离和提纯蛋白质。
5.变性
现象:加热后,鸡蛋清沉淀,凝结的鸡蛋清放入蒸馏水中不溶解。
是不可逆过程,造成蛋白质变性的因素有:高温、紫外线、X射线、强酸、强碱、重金属离子、酒精、甲醛、苯甲酸等,用此性质可消毒灭菌。
例2.为了鉴别某白色纺织物成分是蚕丝还是人造丝,可以选用的方法是(
)
A.滴加浓硝酸
B.滴加浓硫酸
C.滴加酒精
D.灼烧
AD
例3.棉花和羊毛都具有的特点是( )
A.遇浓硝酸显黄色
B.灼烧后有烧焦羽毛的气味
C.燃烧产物只有二氧化碳和水
D.在一定条件下能发生水解
D
解析:棉花的主要成分为纤维素,羊毛的主要成分为蛋白质,二者共同的性质是都能发生水解反应。“遇浓硝酸显黄色、灼烧后有烧焦羽毛的气味”是蛋白质的特征反应;蛋白质燃烧不仅生成二氧化碳和水,还生成含氮的物质、硫的氧化物等。
练1.下列关于蛋白质的叙述中正确的是( )
A.天然蛋白质的组成元素只有碳、氢、氧、氮四种
B.加热会使蛋白质变性,因此食用生鸡蛋所获得的营养价值更高
C.向鸡蛋清中加入食盐,会使蛋白质凝固变性
D.用一束光线照射蛋白质溶液,可以产生丁达尔效应
D
练2.误食重金属盐会引起中毒,下列急救方法不能用于解毒的是( )
A.立即喝大量的食盐水
B.立即喝大量牛奶
C.立即喝大量的豆浆
D.立即喝大量蛋清
解析:牛奶、豆浆、蛋清均为蛋白质,立即服用,可以减轻重金属盐对人体蛋白质的凝结作用,起到解毒的效果。
A
练3.下列关于蛋白质的叙述正确的是( )
A.鸡蛋黄的主要成分是蛋白质
B.鸡蛋生食营养价值更高
C.鸡蛋白遇碘变蓝色
D.蛋白质水解最终产物是氨基酸
D
解析:鸡蛋白的主要成分是蛋白质,遇碘不变蓝色,淀粉遇碘变蓝色。
学习目标
第四节
基本营养物质
第2课时
油脂和蛋白质
1.认识油脂和蛋白质的主要性质。
2.了解油脂和蛋白质的组成。
3.知道油脂和蛋白质在日常生活、生产中的应用。
我们知道糖吃多了,人会发胖,由于能量的过剩,就会转化成一种更高能量的物质----油脂,油脂是人类主要食物之一,是人体中重要的能源物质,被称为人体的备用油箱,今天我们就共同学习油脂的性质。
一、油脂的组成和结构
1.
油脂的成分
由C、H、O元素组成的,是高级脂肪酸和甘油酯化反应生成的酯。
C17H35COOH
硬脂酸
C17H33COOH
油
酸
C15H31COOH
软脂酸
油
(oil)
脂肪
(fat)
CH2—O—C-C17H35
CH
—
O—C-C17H35
CH2—O—C-C17H35
O
O
O
非油脂
油脂
CH2—O—C-CH3
CH
—O—C-CH3
CH2—O—C-CH3
O
O
O
下列物质是油脂吗?
单甘油酯
混甘油酯
纯天然的油脂一般为混甘油酯组成的混合物
CH2—O—C-C17H33
CH
—
O—C-C17H33
CH2—O—C-C17H33
O
O
O
CH2—O—C-C17H31
CH
—
O—C-C17H33
CH2—O—C-C17H35
O
O
O
2.
结构
R1
C
O
O
CH2
R2
C
O
O
CH
R3
C
O
O
CH2
R1、R2、R3代表烃基,它们可以相同,也可以不同。相同时称为单甘油酯,不同时称为混甘油酯。
天然油脂大都是混甘油酯组成的混合物。
3.
分类
植物油
脂肪
如:菜籽油、花生油、豆油、棉籽油
动物油脂呈固态,称脂肪,沸点较高
如:猪油、牛油
油脂
含有不饱和键:C=C,呈液态,沸点低
只有饱和键:C-C
干油酯
4.
物理性质
密度比水的密度小,为0.9~0.95
g/cm3
有明显的油腻感
不溶于水,易溶于有机溶剂
是一种良好的有机溶剂
天然油脂都是混合物,所以没有固定的
熔点、沸点。
二、油脂的化学性质
烃基中含有碳碳双键:可以发生加成反应、
氧化反应
酯基:
可以在酸、碱溶液或脂肪酶中发生水解反应
——油脂兼有酯类和烯烃的性质
R1-C-O-CH2
R2-C-O-CH
R3-C-O-CH2
O=
O=
O=
使溴水或碘水发生加成反应而褪色
使高锰酸钾(H+)因氧化反应而褪色
久置在空气中被氧气氧化而变质
1.油脂在体内的水解
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+3H2O
HOCH2
HOCH
HOCH2
3C17H35COOH
+
脂肪酶
人类由此获得一些必须得脂肪酸。如亚油酸(9,12——十八碳二烯酸)等。
一般不饱和酸比饱和酸对人体更有益。
2.在酸性条件下水解
3.皂化反应
油脂在碱性条件下,生成高级脂肪酸盐和甘油的反应。
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+
3NaOH
3C17H35COONa
CH2OH
CHOH
CH2OH
+
硬脂酸甘油脂
硬
脂
酸
钠
甘油
工业上利用这个反应来制造肥皂。硬脂酸钠是肥皂的有效成分。
混合液
胶状液体
上层:高级
脂肪酸钠
动
植
物
油
脂
下层:甘油、
NaCl溶液
工业制皂流程:
NaOH
△
NaCl
盐析
加填充剂,压滤干燥
肥皂
蒸馏
甘油
盐析:
加入无机盐使某些有机物降低溶解度,从而析出的过程,属于物理变化。这里的盐析是指加入食盐使肥皂析出的过程。
油+H2
脂肪(固态),人造脂肪(硬化油)
一定条件下
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
+
3
H2
催化剂
加热、加压
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
4.
氢化反应(加成反应、硬化反应)
硬化油性质稳定,不易变质,便于运输,可用于制造肥皂、脂肪酸、甘油、人造奶油等。
例1.区别植物油和矿物油的正确方法是(
)
A.加酸性高锰酸钾溶液,振荡
B.加NaOH溶液,煮沸
C.加新制Cu(OH)2悬浊液,煮沸
D.加溴水,振荡
解析:植物油中含有碳碳不饱和键,能使酸性KMnO4溶液或溴水褪色,有些矿物油含有烯烃,也能使溴水或酸性KMnO4溶液褪色,A、D项无法区别;
植物油属于酯类,在NaOH溶液中煮沸时,水解后的生成物能溶于水,矿物油无此性质,故B项可区别植物油和矿物油。
B
物质
油脂
矿物油
脂肪
油
组成
多种高级脂肪酸的甘油酯
多种烃(石油及其分馏产品)
含饱和烃基多
含不饱和烃基多
性质
固态或半固态
液态
具有烃的性质,不能水解
能水解并部分兼有烯烃的性质
鉴别
加含酚酞的NaOH溶液,加热,红色变浅
加含酚酞的NaOH溶液,加热,无变化
油脂和矿物油的比较
1.蛋白质的组成和存在
(1)由C、H、O、N、S、P等元素组成,是氨基酸分子连接的高分子化合物。
(2)主要存在于生物体内,肌肉、毛发、皮肤、角、蹄、酶、激素、抗体、病毒中;在植物中也很丰富,比如大豆、花生、谷物。
2.蛋白质的水解
蛋白质也可以在酶等催化剂作用下水解生成氨基酸
蛋白质
多肽
氨基酸
水解
合成
水解
合成
三、蛋白质
蛋白质在酶等催化剂的作用下水解生成氨基酸。天然蛋白质水解的氨基酸都是α-氨基酸。
R-CH-COOH
NH2
α
CH2-COOH
NH2
甘氨酸
(α-氨基乙酸)
CH3-CH-COOH
NH2
丙氨酸(α-氨基丙酸)
苯丙氨酸(α-氨基-β-苯基丙酸)
-CH2-CH-COOH
NH2
3.
蛋白质的特征反应
实验步骤:取2
mL鸡蛋清于试管中,滴加4滴浓硝酸,在酒精灯上微热。
浓硝酸使蛋白质颜色变黄。
①颜色反应:
蛋白质被灼烧时,有烧焦羽毛的气味。
②蛋白质灼烧:
以上两个反应均可用于鉴别部分蛋白质,
多用灼烧法鉴别羊毛或蚕丝织物的真伪。
4.盐析
现象:有白色絮状物质析出,白色絮状物质放入水中,溶解。
加入某些浓的轻金属盐溶液或铵盐溶液后,降低有机物的溶解度,使之析出,即为盐析。少量的无机盐能促进蛋白质的溶解。是可逆过程,用于分离和提纯蛋白质。
5.变性
现象:加热后,鸡蛋清沉淀,凝结的鸡蛋清放入蒸馏水中不溶解。
是不可逆过程,造成蛋白质变性的因素有:高温、紫外线、X射线、强酸、强碱、重金属离子、酒精、甲醛、苯甲酸等,用此性质可消毒灭菌。
例2.为了鉴别某白色纺织物成分是蚕丝还是人造丝,可以选用的方法是(
)
A.滴加浓硝酸
B.滴加浓硫酸
C.滴加酒精
D.灼烧
AD
例3.棉花和羊毛都具有的特点是( )
A.遇浓硝酸显黄色
B.灼烧后有烧焦羽毛的气味
C.燃烧产物只有二氧化碳和水
D.在一定条件下能发生水解
D
解析:棉花的主要成分为纤维素,羊毛的主要成分为蛋白质,二者共同的性质是都能发生水解反应。“遇浓硝酸显黄色、灼烧后有烧焦羽毛的气味”是蛋白质的特征反应;蛋白质燃烧不仅生成二氧化碳和水,还生成含氮的物质、硫的氧化物等。
练1.下列关于蛋白质的叙述中正确的是( )
A.天然蛋白质的组成元素只有碳、氢、氧、氮四种
B.加热会使蛋白质变性,因此食用生鸡蛋所获得的营养价值更高
C.向鸡蛋清中加入食盐,会使蛋白质凝固变性
D.用一束光线照射蛋白质溶液,可以产生丁达尔效应
D
练2.误食重金属盐会引起中毒,下列急救方法不能用于解毒的是( )
A.立即喝大量的食盐水
B.立即喝大量牛奶
C.立即喝大量的豆浆
D.立即喝大量蛋清
解析:牛奶、豆浆、蛋清均为蛋白质,立即服用,可以减轻重金属盐对人体蛋白质的凝结作用,起到解毒的效果。
A
练3.下列关于蛋白质的叙述正确的是( )
A.鸡蛋黄的主要成分是蛋白质
B.鸡蛋生食营养价值更高
C.鸡蛋白遇碘变蓝色
D.蛋白质水解最终产物是氨基酸
D
解析:鸡蛋白的主要成分是蛋白质,遇碘不变蓝色,淀粉遇碘变蓝色。
