鲁教五四学制九年级化学:第一单元 第二节 溶液组成的定量表示 (共15张PPT)
文档属性
| 名称 | 鲁教五四学制九年级化学:第一单元 第二节 溶液组成的定量表示 (共15张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 688.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-05-27 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
第一单元
溶液
第二节
溶液的配制
学习目标:
1、通过动手操作,初步学会配制一定溶质质量分数的溶液。
2、进一步熟练药品取用、托盘天平和量筒的使用等基本实验操作。并会分析错误操作对所配溶液的质量分数的影响。
3、通过完成配制一定溶质质量分数的溶液实验,培养科学严谨的实验态度。
学习重难点:
重点:溶液配制的步骤及注意事项;
难点:配制溶液的误差分析。
1、讨论与交流:
关于“15%的食盐水溶液”的解释错误的是(
)
A、100克水中溶解了15克食盐
B、30克食盐溶于170克水中所得的溶液
C、溶液中食盐与水按15:85的质量比
配成溶液
D、100克食盐水溶液中溶解了15克食盐
A
在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150
kg的这种溶液,需要氯化钠和水的质量各是多少?
2、分析与计算:
1、你知道配制一定质量分数溶液用到的仪器有哪些吗?你了解这些仪器的使用方法吗?
2、你知道配制一定溶质质量分数溶液的一般步骤吗?
活动天地:请阅读教材11页活动天地1-5,并讨论分析以下问题:
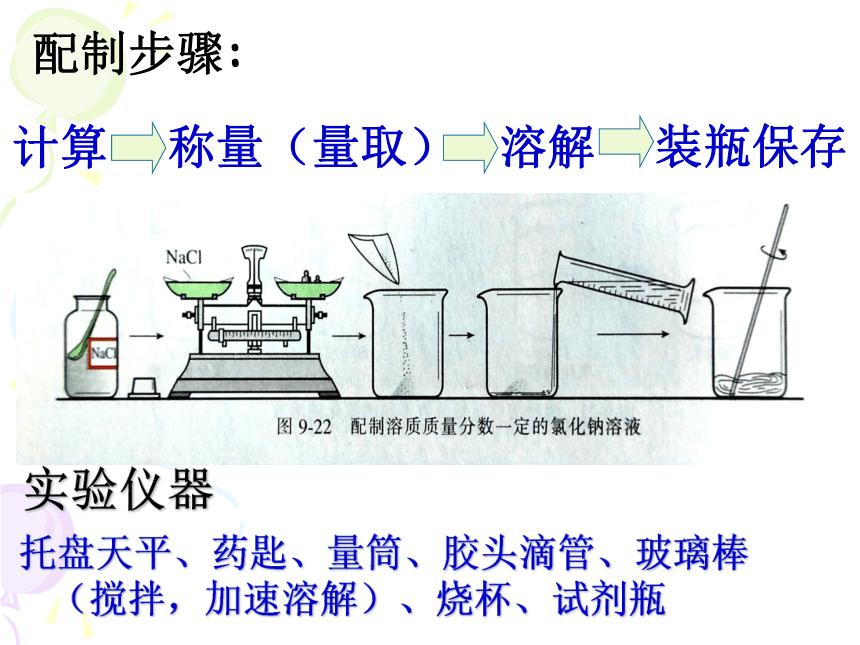
实验仪器
托盘天平、药匙、量筒、胶头滴管、玻璃棒(搅拌,加速溶解)、烧杯、试剂瓶
配制一定溶质质量分数的溶液
如何配制50g质量分数为16%的氯化钠溶液
1、计算:配制时所需NaCl质量为__________,
所需水的质量_____,
2、称量(或量取)
用托盘天平称8gNaCl固体,倒入烧杯中
用量筒量取42m
L的水,倒入盛有NaCl
的烧杯中
3、溶解:用玻璃棒搅拌烧杯中的溶液,使NaCl溶解
4、装瓶保存:把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(注明药品名称和溶质质量分数),放入试剂柜中。
8g
42g
相当于42m
L
活动天地:
用托盘天平来称量固体药品
应注意哪些?
思考:NaOH能否直接放在称量纸上称量?为什么?应如何操作?
不能,NaOH为强腐蚀性、易潮解的药品,应两边各放一小烧杯
称量
若俯视则读数偏高,液体的
实际体积<读数
若仰视,读数偏低,液体的
实际体积>读数
配制一定溶质质量分数的溶液
如何配制50g质量分数为16%的氯化钠溶液
1、计算:配制时所需NaCl质量为__________,
所需水的质量_____,
2、称量(或量取)
用托盘天平称8gNaCl固体,倒入烧杯中
用量筒量取42m
L的水,倒入盛有NaCl
的烧杯中
3、溶解:用玻璃棒搅拌烧杯中的溶液,使NaCl溶解
4、装瓶保存:把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(注明药品名称和溶质质量分数),放入试剂柜中。
8g
42g
相当于42m
L
活动天地:
反思交流:
如果所配溶液的溶质质量分数略大于或略小于16%,你认为可能的原因有哪些?
误差分析
【讨论】在上述两例配制溶液中,如下的操作,对所配制的溶液的质量分数有何影响?
1、称量氯化钠时将药品放在右盘,砝码放在左盘,所得溶液质量分数______________;
2、将所称量的氯化钠放入烧杯时有少量洒出,所得溶液质量分数__________________;
3、用湿润的烧杯来溶解氯化钠,所得溶液质量分数__________________;
4、将所量取的水注入烧杯时有少量水洒出,所得溶液质量分数__________________;
5、量取所需水时仰视凹液面最低处,所得溶液质量分数__________________;
6、量取所需水时俯视凹液面最低处,所得溶液质量分数__________________;
7、将所配的溶液装瓶时有少量溶液洒出,所得溶液质量分数____________
实验误差分析
偏大的原因:
1用量筒量取水时俯视读数
2称量时托盘天平的指针偏左
3水量好后,向烧杯中倾倒时
有水溅出
4砝码生锈
偏小的原因:
1称量时药品和砝码颠倒了
(并且用到了游码)
2称量时托盘天平的指针偏右
3在托盘天平的左盘称取药品时,
游码不在零位置就调节天平平衡,
后将游码移动得到度数。
4药品中有杂质
5药品称好后,倒入烧杯中洒落到外面
5用量筒量取水时仰视读数
6配制溶液的烧杯中有残留的水
7盛装溶液的试剂瓶用蒸馏水润湿
无影响:
配制好的溶液装瓶
时倒在细口瓶外
1、下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。
练习检测
2、现欲配制一定质量分数的NaCl溶液,以下
操作会引起所配溶液溶质质量分数降低的是
(
)
A、用托盘天平称量3.2克NaCl时,误将砝
码放在左盘,并使用游码
B、用量筒量取水时,面对刻度,俯视凹液
面最低处
C、将量筒中的水倒入盛有NaCl的烧杯时,
有水溅出
D、将配好的溶液转移到试剂瓶中时,不慎
洒落
练习检测
第一单元
溶液
第二节
溶液的配制
学习目标:
1、通过动手操作,初步学会配制一定溶质质量分数的溶液。
2、进一步熟练药品取用、托盘天平和量筒的使用等基本实验操作。并会分析错误操作对所配溶液的质量分数的影响。
3、通过完成配制一定溶质质量分数的溶液实验,培养科学严谨的实验态度。
学习重难点:
重点:溶液配制的步骤及注意事项;
难点:配制溶液的误差分析。
1、讨论与交流:
关于“15%的食盐水溶液”的解释错误的是(
)
A、100克水中溶解了15克食盐
B、30克食盐溶于170克水中所得的溶液
C、溶液中食盐与水按15:85的质量比
配成溶液
D、100克食盐水溶液中溶解了15克食盐
A
在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150
kg的这种溶液,需要氯化钠和水的质量各是多少?
2、分析与计算:
1、你知道配制一定质量分数溶液用到的仪器有哪些吗?你了解这些仪器的使用方法吗?
2、你知道配制一定溶质质量分数溶液的一般步骤吗?
活动天地:请阅读教材11页活动天地1-5,并讨论分析以下问题:
实验仪器
托盘天平、药匙、量筒、胶头滴管、玻璃棒(搅拌,加速溶解)、烧杯、试剂瓶
配制一定溶质质量分数的溶液
如何配制50g质量分数为16%的氯化钠溶液
1、计算:配制时所需NaCl质量为__________,
所需水的质量_____,
2、称量(或量取)
用托盘天平称8gNaCl固体,倒入烧杯中
用量筒量取42m
L的水,倒入盛有NaCl
的烧杯中
3、溶解:用玻璃棒搅拌烧杯中的溶液,使NaCl溶解
4、装瓶保存:把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(注明药品名称和溶质质量分数),放入试剂柜中。
8g
42g
相当于42m
L
活动天地:
用托盘天平来称量固体药品
应注意哪些?
思考:NaOH能否直接放在称量纸上称量?为什么?应如何操作?
不能,NaOH为强腐蚀性、易潮解的药品,应两边各放一小烧杯
称量
若俯视则读数偏高,液体的
实际体积<读数
若仰视,读数偏低,液体的
实际体积>读数
配制一定溶质质量分数的溶液
如何配制50g质量分数为16%的氯化钠溶液
1、计算:配制时所需NaCl质量为__________,
所需水的质量_____,
2、称量(或量取)
用托盘天平称8gNaCl固体,倒入烧杯中
用量筒量取42m
L的水,倒入盛有NaCl
的烧杯中
3、溶解:用玻璃棒搅拌烧杯中的溶液,使NaCl溶解
4、装瓶保存:把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(注明药品名称和溶质质量分数),放入试剂柜中。
8g
42g
相当于42m
L
活动天地:
反思交流:
如果所配溶液的溶质质量分数略大于或略小于16%,你认为可能的原因有哪些?
误差分析
【讨论】在上述两例配制溶液中,如下的操作,对所配制的溶液的质量分数有何影响?
1、称量氯化钠时将药品放在右盘,砝码放在左盘,所得溶液质量分数______________;
2、将所称量的氯化钠放入烧杯时有少量洒出,所得溶液质量分数__________________;
3、用湿润的烧杯来溶解氯化钠,所得溶液质量分数__________________;
4、将所量取的水注入烧杯时有少量水洒出,所得溶液质量分数__________________;
5、量取所需水时仰视凹液面最低处,所得溶液质量分数__________________;
6、量取所需水时俯视凹液面最低处,所得溶液质量分数__________________;
7、将所配的溶液装瓶时有少量溶液洒出,所得溶液质量分数____________
实验误差分析
偏大的原因:
1用量筒量取水时俯视读数
2称量时托盘天平的指针偏左
3水量好后,向烧杯中倾倒时
有水溅出
4砝码生锈
偏小的原因:
1称量时药品和砝码颠倒了
(并且用到了游码)
2称量时托盘天平的指针偏右
3在托盘天平的左盘称取药品时,
游码不在零位置就调节天平平衡,
后将游码移动得到度数。
4药品中有杂质
5药品称好后,倒入烧杯中洒落到外面
5用量筒量取水时仰视读数
6配制溶液的烧杯中有残留的水
7盛装溶液的试剂瓶用蒸馏水润湿
无影响:
配制好的溶液装瓶
时倒在细口瓶外
1、下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。
练习检测
2、现欲配制一定质量分数的NaCl溶液,以下
操作会引起所配溶液溶质质量分数降低的是
(
)
A、用托盘天平称量3.2克NaCl时,误将砝
码放在左盘,并使用游码
B、用量筒量取水时,面对刻度,俯视凹液
面最低处
C、将量筒中的水倒入盛有NaCl的烧杯时,
有水溅出
D、将配好的溶液转移到试剂瓶中时,不慎
洒落
练习检测
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
