人教版高中生物必修一2.2《蛋白质》(共41张PPT)
文档属性
| 名称 | 人教版高中生物必修一2.2《蛋白质》(共41张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2020-05-29 00:00:00 | ||
图片预览








文档简介
(共41张PPT)
第2节
生命活动的主要承担者
——蛋白质
物质名称
化学式
原子个数
相对分子质量
水
H2O
3
18
硫酸
H2SO4
7
98
牛奶乳蛋白
C1642H2652O492
N420S12
5224
36684
人血红蛋白
C3032H4816O872
N780S8Fe4
9512
64500
原子序数:是指元素在周期表中的序号。
原子序数等于核外电子数。
C原子
核外电子排布
H
H
H
H
H
H
H2
O
O
O
O
O
O
o2
电子式
结构式
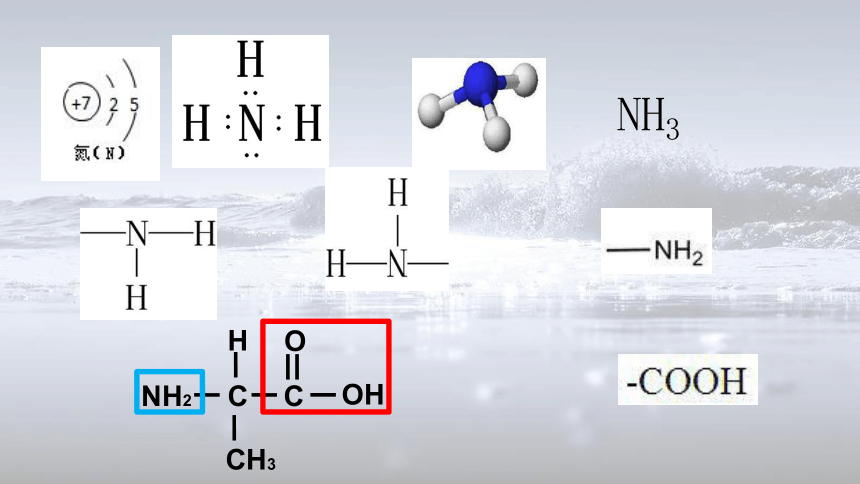
NH3
1.氨基酸分子结构通式
C
H
C
H2N
OH
O
R
氨基
羧基
侧链基团
二.
氨基酸
一个中心(C
原子)
三个支点(氨基、氢、羧基)
一个可变项(
R基团)
特点:a.
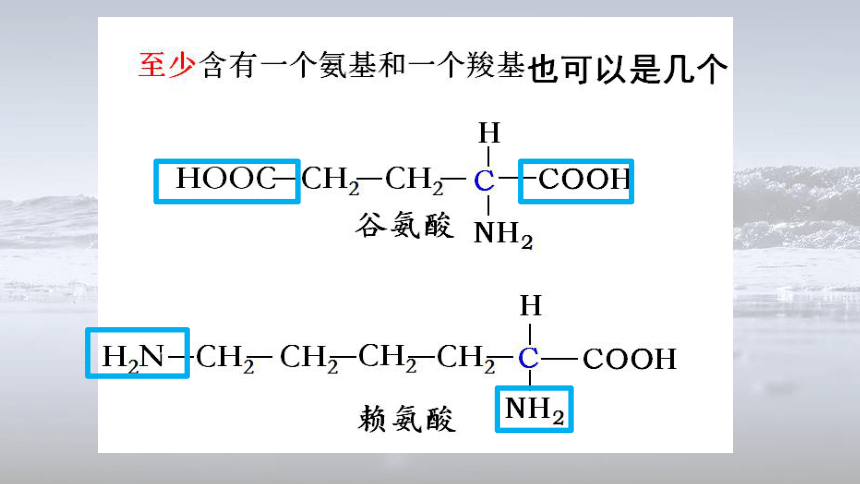
构成蛋白质的氨基酸,至少都含有一个氨基(-NH2)和一个羧基(-COOH),并连在同一个碳原子上。
b.
R基不同、氨基酸不同。
蛋白质的基本组成单位:
氨基酸
(20种)
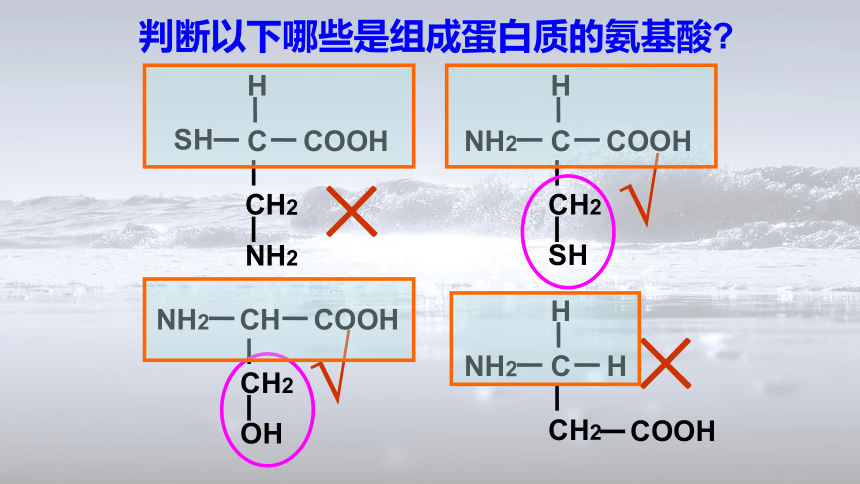
判断以下哪些是组成蛋白质的氨基酸?
√
√
×
×
二.
氨基酸
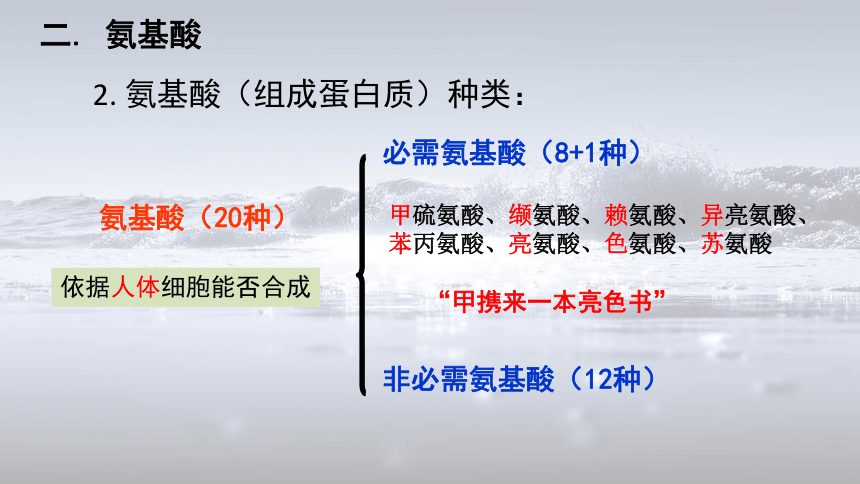
2.
氨基酸(组成蛋白质)种类:
氨基酸(20种)
必需氨基酸(8+1种)
非必需氨基酸(12种)
“甲携来一本亮色书”
甲硫氨酸、缬氨酸、赖氨酸、异亮氨酸、苯丙氨酸、亮氨酸、色氨酸、苏氨酸
依据人体细胞能否合成
氨基酸组成蛋白质的过程
氨基酸
二肽
三肽
多肽
一条多肽链折叠形成蛋白质
几条多肽链折叠形成蛋白质
脱水缩合
折叠盘曲成空间结构
三、蛋白质的结构
氨基酸
多肽
蛋白质
脱水缩合
盘曲折叠
1.氨基酸的脱水缩合
C
H
R1
NH2
OH
C
O
H2O
H
C
H
R1
NH2
C
O
H2O
二肽
肽键
1.氨基酸的脱水缩合
肽键
OH
H
二肽
H2O
H2O
1.氨基酸的脱水缩合
肽键
二肽
H2O
肽键
三肽
以此类推,由多个氨基酸分子缩合而成的含有多个肽键的化合物,叫多肽(链状)。
H2O
1.氨基酸的脱水缩合
练习:根据下面图解,回答问题:
(1)该图示_____肽化合物;含_____个肽键。(2)填写虚线框内结构的名称:A._____
B._____
C._____
(3)生成此化合物的反应叫________。
三
两
氨基
肽键
羧基
脱水缩合
蛋白质
一级结构
蛋白质
二级结构
三级
结构
四级
结构
2.多肽盘曲折叠形成蛋白质
A、6个氨基酸形成1条肽链时,形成几个肽键?
脱掉几个水分子?
B、n个氨基酸形成1条肽链时,形成几个肽键?
脱去几个水分子?
小结:在一条肽链中
脱去的水分子数
=
=
肽键数
氨基酸总数-1
1
n
n-1
n-1
6
5
5
3.有关脱水缩合的计算
1
氨基酸数目
形成肽链数
形成肽键数
脱去水分子数目
C、6个氨基酸形成2条肽链时,形成几个肽键?
脱去几个水分子?
D、n个氨基酸形成m条肽链时,形成几个肽键?
脱去几个水分子?
1
n
m
n-m
n-m
小结:在m条肽链中
脱去的水分子数
=肽键数=氨基酸总数-
m
=氨基酸-肽链的条数
6
6
2
5
4
5
4
肽链1:
氨基酸数目
形成肽链数
形成肽键数
脱去水分子数目
G.蛋白质的相对分子质量=氨基酸数×氨基酸的平均分子量-失去的水分子数×水的分子量
一个由n个氨基酸形成的含有m条肽链的蛋白质,氨基酸的平均分子质量为a,则蛋白质的相对分子质量=a·n-18(n-m)。
练习1:
组成人体的20种氨基酸的平均分子量是128,血红蛋白由4条多肽链组成,共含有574个氨基酸,则血红蛋白分子中肽键
个,形成过程中脱水
个,血红蛋白分子质量约为
。血红蛋白分子中游离的氨基有
个,游离的羧基有
个。
570
570
63212
至少4
至少4
练习2:某蛋白质由2条肽链、16个氨基酸组成。在其形成过程中,相对分子质量减少了
(
)
254
18
×(16
-
2)+2
小结归纳:
肽键
肽键
练习3:某蛋白质由m条肽链、n个氨基酸组成。该蛋白质至少有氧原子数是:(
)?
?????
n+m
四.蛋白质结构的多样性:
氨基酸种类不同,肽链的结构不同
氨基酸数目不同,肽链的结构不同
氨基酸排列顺序不同,肽链的结构不同
肽链的空间结构不同,蛋白质的结构不同
蛋白质的结构多样性
思考:二种不同的氨基酸可以组成几种二肽。
思考1:二种氨基酸各一个,可以组成几种二肽?二种氨基酸均有多个,可以组成几种二肽?
COOH
NH2
NH2
NH2
NH2
COOH
COOH
COOH
思考2:三种氨基酸各一个,可以组成几种三肽?
思考1:二种氨基酸各一个,可以组成几种二肽?二种氨基酸均有多个,可以组成几种二肽?
COOH
NH2
NH2
NH2
NH2
COOH
COOH
COOH
思考2:三种氨基酸各一个,可以组成几种三肽?
思考3:三种氨基酸均多个,可以组成几种三肽?
3
3
3
思考4:三种氨基酸均多个,可以组成几种二肽?
蛋白质的结构多样性
蛋白质功能的多样性
思考5:
20种氨基酸均多个,形成由500个氨基酸组成的蛋白质,可形成多少种?
20500种
五.蛋白质的功能
(1)构成细胞和生物体的重要物质(结构蛋白):如肌球蛋白、肌动蛋白等
(2)催化作用:如绝大多数酶
(3)运输作用:如血红蛋白、细胞膜上的载体
(4)免疫作用:如抗体
(5)调节蛋白:如胰岛素和生长激素等
六.蛋白质的理化性质
(一)盐析
(二)变性
1.蛋白质变性的因素
①重金属盐(汞盐,银盐,铜盐)
②酸、碱、乙醇、尿素等
③高温
④X射线、紫外线
2.蛋白质变性过程中发生的变化
主要发生空间结构的变化,不发生肽键的断裂
肽链由有序状态变为无序状态
溶解度降低易于形成沉淀
思考1.
蛋白质的空间结构被破坏对其功能有影响吗?
有
思考2.
请分析蛋白质与多肽的关系?
蛋白质由一至多条多肽分子组成,结构复杂
多肽没有生理功能,蛋白质才有。
无色
紫色
(创造碱性条件)
(提供Cu2+)
双缩脲试剂B
3-4滴
双缩脲试剂A
2mL
2mL组织样液
操作时,应先加A再加B,且A多B少,如果B过量,
Cu2+的蓝色就会遮盖生成的紫色。
(三)蛋白质的检测:
(1)原理:蛋白质
+
双缩脲试剂
紫色络合物
(2)选材:黄豆、鸡蛋清(稀释)、牛奶、豆浆
(3)检测过程:
在碱性条件(NaOH)下,蛋白质中的肽键(—NH—CO—)与Cu2+作用生生紫色络合物。因此,操作时,应先加A再加B,且A多B少,如果B过量,
Cu2+的蓝色就会遮盖生成的紫色。
将尿素(脲)加热,两分子尿素放出一分子氨而缩合成双缩脲。反应式为:
双缩脲在碱性环境中能和Cu2+作用生成紫色的络化物,这个反应叫做双缩脲反应。蛋白质分子中含有的肽键结构与双缩脲结构相似,因此,蛋白质也可与双缩脲试剂发生颜色反应。
双缩脲≠双缩脲试剂
斐林试剂与双缩脲试剂的比较
斐林试剂
双缩脲试剂
甲液
乙液
A液
B液
成分
0.1
g/mL
NaOH溶液
0.05
g/mL
CuSO4溶液
0.1
g/mL
NaOH溶液
0.01
g/mL
CuSO4溶液
鉴定物质
可溶性还原糖
蛋白质
添加顺序
等量混匀
现配现用
先加入A液1
mL,摇匀,再加入B液4滴(不能过量),摇匀
反应条件
50~65
℃水浴加热
不需加热,摇匀即可
反应现象
样液变砖红色沉淀
样液变紫色
相同点:都含有NaOH、CuSO4两种成分,且所用NaOH浓度都是0.1g/mL
组成元素
C、H、O、N(P、S)
导致
氨基酸
种类:20种
必需氨基酸:8种
非必需氨基酸:12种
通式:
C
H
C
H2N
OH
O
R
特点:至少有一个-NH2和一个-COOH连在同一个C原子上
脱水缩合
多肽
组成蛋白质的氨基酸不同
氨基酸的数目不同
氨基酸排列顺序不同
多肽的空间结构不同
盘曲折叠
蛋白质
结构多样性
功能多样性
构成生物体,如结构蛋白
运输作用,如血红蛋白
催化作用,如酶
调节作用,如胰岛素
免疫作用,如抗体
组成
导致
脱水数=肽键数=氨基酸数—肽链数=n—m
m条肽链构成的蛋白质,至少m个氨基,至少m个羧基
M(pro)=na—(n—m)18
课堂小结
第2节
生命活动的主要承担者
——蛋白质
物质名称
化学式
原子个数
相对分子质量
水
H2O
3
18
硫酸
H2SO4
7
98
牛奶乳蛋白
C1642H2652O492
N420S12
5224
36684
人血红蛋白
C3032H4816O872
N780S8Fe4
9512
64500
原子序数:是指元素在周期表中的序号。
原子序数等于核外电子数。
C原子
核外电子排布
H
H
H
H
H
H
H2
O
O
O
O
O
O
o2
电子式
结构式
NH3
1.氨基酸分子结构通式
C
H
C
H2N
OH
O
R
氨基
羧基
侧链基团
二.
氨基酸
一个中心(C
原子)
三个支点(氨基、氢、羧基)
一个可变项(
R基团)
特点:a.
构成蛋白质的氨基酸,至少都含有一个氨基(-NH2)和一个羧基(-COOH),并连在同一个碳原子上。
b.
R基不同、氨基酸不同。
蛋白质的基本组成单位:
氨基酸
(20种)
判断以下哪些是组成蛋白质的氨基酸?
√
√
×
×
二.
氨基酸
2.
氨基酸(组成蛋白质)种类:
氨基酸(20种)
必需氨基酸(8+1种)
非必需氨基酸(12种)
“甲携来一本亮色书”
甲硫氨酸、缬氨酸、赖氨酸、异亮氨酸、苯丙氨酸、亮氨酸、色氨酸、苏氨酸
依据人体细胞能否合成
氨基酸组成蛋白质的过程
氨基酸
二肽
三肽
多肽
一条多肽链折叠形成蛋白质
几条多肽链折叠形成蛋白质
脱水缩合
折叠盘曲成空间结构
三、蛋白质的结构
氨基酸
多肽
蛋白质
脱水缩合
盘曲折叠
1.氨基酸的脱水缩合
C
H
R1
NH2
OH
C
O
H2O
H
C
H
R1
NH2
C
O
H2O
二肽
肽键
1.氨基酸的脱水缩合
肽键
OH
H
二肽
H2O
H2O
1.氨基酸的脱水缩合
肽键
二肽
H2O
肽键
三肽
以此类推,由多个氨基酸分子缩合而成的含有多个肽键的化合物,叫多肽(链状)。
H2O
1.氨基酸的脱水缩合
练习:根据下面图解,回答问题:
(1)该图示_____肽化合物;含_____个肽键。(2)填写虚线框内结构的名称:A._____
B._____
C._____
(3)生成此化合物的反应叫________。
三
两
氨基
肽键
羧基
脱水缩合
蛋白质
一级结构
蛋白质
二级结构
三级
结构
四级
结构
2.多肽盘曲折叠形成蛋白质
A、6个氨基酸形成1条肽链时,形成几个肽键?
脱掉几个水分子?
B、n个氨基酸形成1条肽链时,形成几个肽键?
脱去几个水分子?
小结:在一条肽链中
脱去的水分子数
=
=
肽键数
氨基酸总数-1
1
n
n-1
n-1
6
5
5
3.有关脱水缩合的计算
1
氨基酸数目
形成肽链数
形成肽键数
脱去水分子数目
C、6个氨基酸形成2条肽链时,形成几个肽键?
脱去几个水分子?
D、n个氨基酸形成m条肽链时,形成几个肽键?
脱去几个水分子?
1
n
m
n-m
n-m
小结:在m条肽链中
脱去的水分子数
=肽键数=氨基酸总数-
m
=氨基酸-肽链的条数
6
6
2
5
4
5
4
肽链1:
氨基酸数目
形成肽链数
形成肽键数
脱去水分子数目
G.蛋白质的相对分子质量=氨基酸数×氨基酸的平均分子量-失去的水分子数×水的分子量
一个由n个氨基酸形成的含有m条肽链的蛋白质,氨基酸的平均分子质量为a,则蛋白质的相对分子质量=a·n-18(n-m)。
练习1:
组成人体的20种氨基酸的平均分子量是128,血红蛋白由4条多肽链组成,共含有574个氨基酸,则血红蛋白分子中肽键
个,形成过程中脱水
个,血红蛋白分子质量约为
。血红蛋白分子中游离的氨基有
个,游离的羧基有
个。
570
570
63212
至少4
至少4
练习2:某蛋白质由2条肽链、16个氨基酸组成。在其形成过程中,相对分子质量减少了
(
)
254
18
×(16
-
2)+2
小结归纳:
肽键
肽键
练习3:某蛋白质由m条肽链、n个氨基酸组成。该蛋白质至少有氧原子数是:(
)?
?????
n+m
四.蛋白质结构的多样性:
氨基酸种类不同,肽链的结构不同
氨基酸数目不同,肽链的结构不同
氨基酸排列顺序不同,肽链的结构不同
肽链的空间结构不同,蛋白质的结构不同
蛋白质的结构多样性
思考:二种不同的氨基酸可以组成几种二肽。
思考1:二种氨基酸各一个,可以组成几种二肽?二种氨基酸均有多个,可以组成几种二肽?
COOH
NH2
NH2
NH2
NH2
COOH
COOH
COOH
思考2:三种氨基酸各一个,可以组成几种三肽?
思考1:二种氨基酸各一个,可以组成几种二肽?二种氨基酸均有多个,可以组成几种二肽?
COOH
NH2
NH2
NH2
NH2
COOH
COOH
COOH
思考2:三种氨基酸各一个,可以组成几种三肽?
思考3:三种氨基酸均多个,可以组成几种三肽?
3
3
3
思考4:三种氨基酸均多个,可以组成几种二肽?
蛋白质的结构多样性
蛋白质功能的多样性
思考5:
20种氨基酸均多个,形成由500个氨基酸组成的蛋白质,可形成多少种?
20500种
五.蛋白质的功能
(1)构成细胞和生物体的重要物质(结构蛋白):如肌球蛋白、肌动蛋白等
(2)催化作用:如绝大多数酶
(3)运输作用:如血红蛋白、细胞膜上的载体
(4)免疫作用:如抗体
(5)调节蛋白:如胰岛素和生长激素等
六.蛋白质的理化性质
(一)盐析
(二)变性
1.蛋白质变性的因素
①重金属盐(汞盐,银盐,铜盐)
②酸、碱、乙醇、尿素等
③高温
④X射线、紫外线
2.蛋白质变性过程中发生的变化
主要发生空间结构的变化,不发生肽键的断裂
肽链由有序状态变为无序状态
溶解度降低易于形成沉淀
思考1.
蛋白质的空间结构被破坏对其功能有影响吗?
有
思考2.
请分析蛋白质与多肽的关系?
蛋白质由一至多条多肽分子组成,结构复杂
多肽没有生理功能,蛋白质才有。
无色
紫色
(创造碱性条件)
(提供Cu2+)
双缩脲试剂B
3-4滴
双缩脲试剂A
2mL
2mL组织样液
操作时,应先加A再加B,且A多B少,如果B过量,
Cu2+的蓝色就会遮盖生成的紫色。
(三)蛋白质的检测:
(1)原理:蛋白质
+
双缩脲试剂
紫色络合物
(2)选材:黄豆、鸡蛋清(稀释)、牛奶、豆浆
(3)检测过程:
在碱性条件(NaOH)下,蛋白质中的肽键(—NH—CO—)与Cu2+作用生生紫色络合物。因此,操作时,应先加A再加B,且A多B少,如果B过量,
Cu2+的蓝色就会遮盖生成的紫色。
将尿素(脲)加热,两分子尿素放出一分子氨而缩合成双缩脲。反应式为:
双缩脲在碱性环境中能和Cu2+作用生成紫色的络化物,这个反应叫做双缩脲反应。蛋白质分子中含有的肽键结构与双缩脲结构相似,因此,蛋白质也可与双缩脲试剂发生颜色反应。
双缩脲≠双缩脲试剂
斐林试剂与双缩脲试剂的比较
斐林试剂
双缩脲试剂
甲液
乙液
A液
B液
成分
0.1
g/mL
NaOH溶液
0.05
g/mL
CuSO4溶液
0.1
g/mL
NaOH溶液
0.01
g/mL
CuSO4溶液
鉴定物质
可溶性还原糖
蛋白质
添加顺序
等量混匀
现配现用
先加入A液1
mL,摇匀,再加入B液4滴(不能过量),摇匀
反应条件
50~65
℃水浴加热
不需加热,摇匀即可
反应现象
样液变砖红色沉淀
样液变紫色
相同点:都含有NaOH、CuSO4两种成分,且所用NaOH浓度都是0.1g/mL
组成元素
C、H、O、N(P、S)
导致
氨基酸
种类:20种
必需氨基酸:8种
非必需氨基酸:12种
通式:
C
H
C
H2N
OH
O
R
特点:至少有一个-NH2和一个-COOH连在同一个C原子上
脱水缩合
多肽
组成蛋白质的氨基酸不同
氨基酸的数目不同
氨基酸排列顺序不同
多肽的空间结构不同
盘曲折叠
蛋白质
结构多样性
功能多样性
构成生物体,如结构蛋白
运输作用,如血红蛋白
催化作用,如酶
调节作用,如胰岛素
免疫作用,如抗体
组成
导致
脱水数=肽键数=氨基酸数—肽链数=n—m
m条肽链构成的蛋白质,至少m个氨基,至少m个羧基
M(pro)=na—(n—m)18
课堂小结
同课章节目录
- 第一章 走近细胞
- 第1节 从生物圈到细胞
- 第2节 细胞的多样性和统一性
- 第二章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 生命活动的主要承担者──蛋白质
- 第3节 遗传信息的携带者──核酸
- 第4节 细胞中的糖类和脂质
- 第5节 细胞中的无机物
- 第三章 细胞的基本结构
- 第1节 细胞膜──系统的边界
- 第2节 细胞器──系统内的分工合作
- 第3节 细胞核──系统的控制中心
- 第四章 细胞的物质输入和输出
- 第1节 物质跨膜运输的实例
- 第2节 生物膜的流动镶嵌模型
- 第3节 物质跨膜运输的方式
- 第五章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“通货”──ATP
- 第3节 ATP的主要来源──细胞呼吸
- 第4节 能量之源——光与光合作用
- 第六章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和凋亡
- 第4节 细胞的癌变
