鲁教版(五四学制)九年级化学1.2.1溶液组成的定量表示课件 (共38张PPT)
文档属性
| 名称 | 鲁教版(五四学制)九年级化学1.2.1溶液组成的定量表示课件 (共38张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 508.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-01 00:00:00 | ||
图片预览











文档简介
(共38张PPT)
知识回顾
1、什么是溶液?溶质?溶剂?
2、溶质、溶剂、溶液的质量
有何关系?
溶液的质量=溶质的质量+溶剂的质量
第
1
课时
第二节
溶液组成的定量表示
溶液组成的表示方法
1、理解并记住溶质质量分数的概念及
其计算公式;
2、会利用溶质质量分数的计算式进行
简单的计算。
40ml水
50ml水
8g糖
10g糖
哪一杯更甜呢?
1、称取8克白糖加到烧杯中。再加入40mL水,搅拌,使白糖溶解。
2、称取10克白糖加到另一烧杯中。再加入50mL水,搅拌,使白糖溶解。
活动天地
问题探究:
1、实验1、2所得两种糖水,哪种更甜?你的
根据是什么?
2、如果你的结论是通过计算获得的,你列出
的算式是怎样的?
友情提示:
已知水的密度为1g/mL,
根据
m
=
ρV,则40mL和50mL的水的质量为40g和50g.
1、
8g/(40mL×1g/mL)=1:5
2、10g/(50mL×1g/mL)=1:5
1、8g/(
8g
+40mL×1g/mL)=1:6
2、10g/(10g+50mL×1g/mL)=1:6
……
议一议
溶质质量与溶剂的质量比
溶质质量与溶液的质量比
溶质质量分数
溶质质量分数
溶质的质量
=
——————
×
100﹪
溶液的质量
溶质的质量
=
———————————
×
100﹪
溶质的质量+溶剂的质量
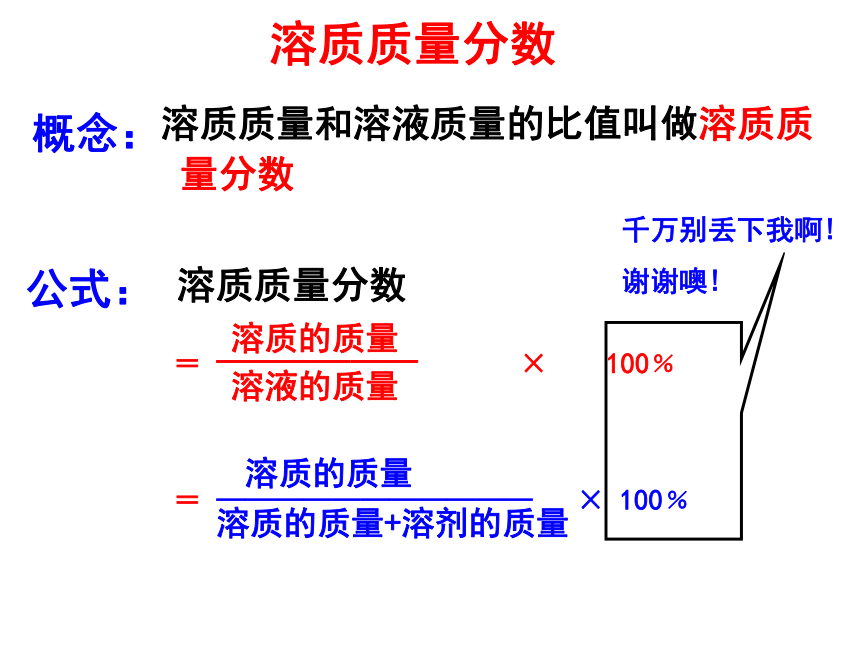
溶质质量分数
概念:
公式:
千万别丢下我啊!
谢谢噢!
溶质质量和溶液质量的比值叫做溶质质
量分数
3、溶剂的质量
=
溶液的质量
-溶质的质量
变形公式
1、溶质的质量
=
溶液的质量×溶质的质量分数
2、溶液的质量
=
溶质的质量/溶质的质量分数
应用一:溶液中溶质质量分数的计算
例1:从一瓶氯化钠溶液中取出20克溶液,蒸干后得到2.8克氯化钠固体。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为
答:这瓶溶液中氯化钠的质量分数为14%。
2.8g
20g
×100%=
14%
1、“14%”的氯化钠溶液的具体含义是什么吗?
思考
2、“14%”和“16%”的氯化钠溶液相比,哪种溶液浓?
100克氯化钠溶液含有14克氯化钠
溶质质量分数越大,溶液越浓
3、把不饱和的氯化钠溶液恰好变为饱和溶液的过程中溶质质量分数如何变化?
【例2】
在农业生产上,常用质量分数为10%~20%的食盐溶液来选种。现要配制150kg质量分数为16%的食盐溶液,需要氯化钠和水的质量各是多少?
解:需要氯化钠的质量为:
150kg×16%
=
24kg
需要水的质量为:
150kg-24kg
=
126kg
答:配制150kg质量分数为16%的氯化钠溶液需要24kg
氯化钠和126kg的水。
应用二:溶液中溶质和溶剂质量的计算
食醋中的溶质为醋酸,计算500g溶质质量分数为4%的食醋中含醋酸和水的质量分别为多少克?
跟踪练习
解:醋酸的质量为:
500g×4%
=
20g
需要水的质量为:
500g-20g
=
480g
答:含醋酸的质量为20g,水的质量为480g。
例3:把100g25%的硝酸钾溶液用水稀释成溶质质量分数为10%的溶液。求所需水的质量?
解:设稀释后溶液的质量为x。
100g×25%=10%·x
100g×25%
x=------------
=
250g
10%
需要水的质量为:250g-100g=150g
答:稀释时需要水的质量为150g。
设未知数不带单位
计算过程带单位
简明的写出答案
应用三:溶液的稀释问题
加水
100g
25%
10%
加水的质量
=加水后溶液质量-加水前溶液质量
稀释前后
溶质的质
量不变
解:设加水的质量为x。
100g×25%=
(100g+x)·10%
x=150g
答:稀释时需要水的质量为150g。
方法二:
把100g80%的氢氧化钠溶液稀释成40%的氢氧化钠溶液,需要加水多少克?
解:设稀释后溶液的质量为χ
100g×80%=40%χ
χ=200g
需水的质量为200g-100g=100g
答:需要水的质量为100g
学以致用:
若用质量分数为18%的氯化钠溶液配制500g溶质质量分数为0.9%的生理盐水,需18%的氯化钠溶液多少克?要加水多少克?
解:设18%的氯化钠溶液的质量为X
18%X=0.9%×500g
X=25g
需水的质量为500g-25g=475g
答:需18%的氯化钠溶液25g,要加水的质量为475g
学以致用
通过本节课的学习,你有什么收获?
2.溶质质量分数的概念、计算公式
3.计算公式的几种简单应用
溶质质量分数
溶质的质量
=
——————
×
100﹪
溶液的质量
1.可用溶质的质量分数定量表示溶液的组成
白酒的“度”是怎么回事?
白酒包装上面都标有“度数”,如53度(53°)的茅台酒。白酒的“度”实际上是白酒中酒精的含量,这里的含量不是质量分数,而是体积分数,即酒精和白酒的体积比为53:100。
品牌
53度茅台
卫生许可证
QS110015010349
净重
500(ml)
酒精含量
53(%)
生产厂家
贵州茅台股份有限公司
多识一点
1、判断
(1)在100g水中溶解20g食盐,所得食
盐水中溶质的质量分数为20%。
(2)从100g溶质质量分数为20%的碳酸
钠溶液中取出10g溶液,则取出的
溶液中溶质的质量分数变为2%。
课堂检测
×
×
2、把5g食盐溶解在120g水中,所得溶液
中溶质的质量分数为(
)
A. 4%
B. 4.2%
C. 4.4%
D. 5%
3、把10g溶质质量分数为20%食盐水加水
稀释到100g,则所得溶液中溶质的质
量将 ( )
A.增大9倍
B.减小10倍
C.增大10倍
D.不变
A
D
第二课时
溶质质量/g
溶剂质量/g
溶液质量/g
溶质质量分数
10
200
96
100
150
16%
20
80
190
5%
4%
24
126
100
20%
4
分组练习
计算:需食盐:50
g×1
6%
=
8
g
需
水:
50
g–
8g=
42
g
V(水)=42g/1g/ml
=42ml
配制50
g16%氯化钠溶液
二、溶液的配制
1、步骤:
用天平称量
8
g食盐,
用量筒量取42ml水(胶头滴管)
称量:
将称量出的8g氯化钠放入烧杯中,并将量取的42
ml水倒
入烧杯,用玻璃棒搅拌,使氯化钠全部溶解。
2、实验仪器:
天平(砝码)、药匙、量筒(50
ml)、胶头滴管、
烧杯、玻璃棒、细口瓶
把配好的溶液装入试剂瓶(细口瓶)中,盖好瓶塞,贴上标签(注名药品名称和溶质质量分数)
溶解:
装瓶存放:
发现问题
若所配溶液的溶质质量分数略大于16%,可能的原因有哪些?
2.称量时:
称量食盐时指针偏左
量取水时俯视读数
3.溶解时:
1.计算时:
量筒中的水没有完全倒入烧杯
食盐算多了或水算少了
发现问题
药品和砝码放颠倒
量水时仰视读数
将盐倒入烧杯时撒到桌子上
药品中有杂质
2.称量时:
3.溶解时:
1.计算时:
食盐算少了或水算多了
若所配溶液的溶质质量分数略小于16%,可能的原因有哪些?
你会了吗?
1、配制100
g溶质质量分数为6%的氢氧化钠溶液(水的密度近似看作1
g/mL),下列操作正确的是
(
)
A.将氢氧化钠固体置于滤纸上称量
B.俯视量筒刻度读出所取水的体积
C.将氢氧化钠固体置于托盘天平的右盘、砝码置于左盘称量
D.将94
mL水倒入盛有6
g氢氧化钠固体的烧杯中搅拌溶解
D
2、实验室提供了
①天平
②量筒
③烧杯
④玻璃棒
⑤酒精灯等仪器,小华同学用固体氯化钠配制10%的氯化钠溶液,小亮同学用浓盐酸配制10%的稀盐酸。
(1)当用天平称量药品时,砝码应放在天平的
盘,配制过程中用玻璃棒搅拌是为了
。
(2)上述仪器中,两位同学都不需要的仪器是
(填序号,后同)小华需要而小亮不需要的仪器是
。
加速固体溶解
①
⑤
右
1、把10克氯化钠放入40克水中,完全溶解后,溶液中氯化钠的质量分数为(
)
A.10%
B.20%
C.25%
D.33.3%
2、配制100克质量分数为19.6%的稀硫酸,需要质量分数为98%的浓硫酸
克。
B
20
在线测试
3、将5g碳酸钠粉末加到95g溶质质量分数为10%的碳酸钠
溶液中,完全溶解后溶液的溶质的质量分数为
。
4、现有100g溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应向此溶液中加入食盐
g,
或蒸发掉水
g.
14.5%
50
12.25
5、把一杯食盐水倒出一部分,没有改变的是(
)
A
溶质的质量
B
溶剂的质量
C
溶液的质量
D
溶质的质量分数
6、家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是(
)
A
100克醋酸中含醋为10克
B
100克醋酸的水溶液中含醋酸10克
C
100克水中含醋酸为10克
D
100克醋酸的水溶液中含水10克
D
B
7.实验室中要用浓硫酸配制一定质量分数的稀硫酸,先后顺序的操作步骤是(
)
A.量取、溶解、计算
B.计算、溶解、量取
C.量取、计算、溶解
D.计算、量取、溶解
8.用浓硫酸配制一定质量分数的稀硫酸,不需要用到的仪器是(
)
A.托盘天平
B.烧杯
C.量筒
D.玻璃棒
D
A
9.
要配制100g溶质质量分数为10%的氯化钠溶液,下列操作正确的是(
)
A.将10g氯化钠固体直接放在天平的托盘上称量
B.量取90mL水时,俯视读数
C.为加快固体溶解,用温度计搅拌溶液
D.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
D
10.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是
(
)
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液
B
11.欲配制50g7%的氯化钠溶液:
(1)实验步骤应为:
、
、
、
、
。
(2)需要的玻璃仪器有:________________________
________________________。
(3)在托盘天平上称取
氯化钠,用规格为_____
的量筒量取
水。
计算
称量
量取
溶解
装瓶存放
量筒、胶头滴管、烧杯、
3.5g
50mL
46.5mL
玻璃棒
(4)将称量的氯化钠和水倒入烧杯中,为加快氯化钠的溶解速率,常用的方是_____、_____、_____________。
(5)在量取水的体积时,若俯视读数,则配制的溶液的溶质质量分数会
。(填偏高、相等、或偏低)
搅拌
加热
把大颗粒盐研细
偏高
再见
知识回顾
1、什么是溶液?溶质?溶剂?
2、溶质、溶剂、溶液的质量
有何关系?
溶液的质量=溶质的质量+溶剂的质量
第
1
课时
第二节
溶液组成的定量表示
溶液组成的表示方法
1、理解并记住溶质质量分数的概念及
其计算公式;
2、会利用溶质质量分数的计算式进行
简单的计算。
40ml水
50ml水
8g糖
10g糖
哪一杯更甜呢?
1、称取8克白糖加到烧杯中。再加入40mL水,搅拌,使白糖溶解。
2、称取10克白糖加到另一烧杯中。再加入50mL水,搅拌,使白糖溶解。
活动天地
问题探究:
1、实验1、2所得两种糖水,哪种更甜?你的
根据是什么?
2、如果你的结论是通过计算获得的,你列出
的算式是怎样的?
友情提示:
已知水的密度为1g/mL,
根据
m
=
ρV,则40mL和50mL的水的质量为40g和50g.
1、
8g/(40mL×1g/mL)=1:5
2、10g/(50mL×1g/mL)=1:5
1、8g/(
8g
+40mL×1g/mL)=1:6
2、10g/(10g+50mL×1g/mL)=1:6
……
议一议
溶质质量与溶剂的质量比
溶质质量与溶液的质量比
溶质质量分数
溶质质量分数
溶质的质量
=
——————
×
100﹪
溶液的质量
溶质的质量
=
———————————
×
100﹪
溶质的质量+溶剂的质量
溶质质量分数
概念:
公式:
千万别丢下我啊!
谢谢噢!
溶质质量和溶液质量的比值叫做溶质质
量分数
3、溶剂的质量
=
溶液的质量
-溶质的质量
变形公式
1、溶质的质量
=
溶液的质量×溶质的质量分数
2、溶液的质量
=
溶质的质量/溶质的质量分数
应用一:溶液中溶质质量分数的计算
例1:从一瓶氯化钠溶液中取出20克溶液,蒸干后得到2.8克氯化钠固体。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为
答:这瓶溶液中氯化钠的质量分数为14%。
2.8g
20g
×100%=
14%
1、“14%”的氯化钠溶液的具体含义是什么吗?
思考
2、“14%”和“16%”的氯化钠溶液相比,哪种溶液浓?
100克氯化钠溶液含有14克氯化钠
溶质质量分数越大,溶液越浓
3、把不饱和的氯化钠溶液恰好变为饱和溶液的过程中溶质质量分数如何变化?
【例2】
在农业生产上,常用质量分数为10%~20%的食盐溶液来选种。现要配制150kg质量分数为16%的食盐溶液,需要氯化钠和水的质量各是多少?
解:需要氯化钠的质量为:
150kg×16%
=
24kg
需要水的质量为:
150kg-24kg
=
126kg
答:配制150kg质量分数为16%的氯化钠溶液需要24kg
氯化钠和126kg的水。
应用二:溶液中溶质和溶剂质量的计算
食醋中的溶质为醋酸,计算500g溶质质量分数为4%的食醋中含醋酸和水的质量分别为多少克?
跟踪练习
解:醋酸的质量为:
500g×4%
=
20g
需要水的质量为:
500g-20g
=
480g
答:含醋酸的质量为20g,水的质量为480g。
例3:把100g25%的硝酸钾溶液用水稀释成溶质质量分数为10%的溶液。求所需水的质量?
解:设稀释后溶液的质量为x。
100g×25%=10%·x
100g×25%
x=------------
=
250g
10%
需要水的质量为:250g-100g=150g
答:稀释时需要水的质量为150g。
设未知数不带单位
计算过程带单位
简明的写出答案
应用三:溶液的稀释问题
加水
100g
25%
10%
加水的质量
=加水后溶液质量-加水前溶液质量
稀释前后
溶质的质
量不变
解:设加水的质量为x。
100g×25%=
(100g+x)·10%
x=150g
答:稀释时需要水的质量为150g。
方法二:
把100g80%的氢氧化钠溶液稀释成40%的氢氧化钠溶液,需要加水多少克?
解:设稀释后溶液的质量为χ
100g×80%=40%χ
χ=200g
需水的质量为200g-100g=100g
答:需要水的质量为100g
学以致用:
若用质量分数为18%的氯化钠溶液配制500g溶质质量分数为0.9%的生理盐水,需18%的氯化钠溶液多少克?要加水多少克?
解:设18%的氯化钠溶液的质量为X
18%X=0.9%×500g
X=25g
需水的质量为500g-25g=475g
答:需18%的氯化钠溶液25g,要加水的质量为475g
学以致用
通过本节课的学习,你有什么收获?
2.溶质质量分数的概念、计算公式
3.计算公式的几种简单应用
溶质质量分数
溶质的质量
=
——————
×
100﹪
溶液的质量
1.可用溶质的质量分数定量表示溶液的组成
白酒的“度”是怎么回事?
白酒包装上面都标有“度数”,如53度(53°)的茅台酒。白酒的“度”实际上是白酒中酒精的含量,这里的含量不是质量分数,而是体积分数,即酒精和白酒的体积比为53:100。
品牌
53度茅台
卫生许可证
QS110015010349
净重
500(ml)
酒精含量
53(%)
生产厂家
贵州茅台股份有限公司
多识一点
1、判断
(1)在100g水中溶解20g食盐,所得食
盐水中溶质的质量分数为20%。
(2)从100g溶质质量分数为20%的碳酸
钠溶液中取出10g溶液,则取出的
溶液中溶质的质量分数变为2%。
课堂检测
×
×
2、把5g食盐溶解在120g水中,所得溶液
中溶质的质量分数为(
)
A. 4%
B. 4.2%
C. 4.4%
D. 5%
3、把10g溶质质量分数为20%食盐水加水
稀释到100g,则所得溶液中溶质的质
量将 ( )
A.增大9倍
B.减小10倍
C.增大10倍
D.不变
A
D
第二课时
溶质质量/g
溶剂质量/g
溶液质量/g
溶质质量分数
10
200
96
100
150
16%
20
80
190
5%
4%
24
126
100
20%
4
分组练习
计算:需食盐:50
g×1
6%
=
8
g
需
水:
50
g–
8g=
42
g
V(水)=42g/1g/ml
=42ml
配制50
g16%氯化钠溶液
二、溶液的配制
1、步骤:
用天平称量
8
g食盐,
用量筒量取42ml水(胶头滴管)
称量:
将称量出的8g氯化钠放入烧杯中,并将量取的42
ml水倒
入烧杯,用玻璃棒搅拌,使氯化钠全部溶解。
2、实验仪器:
天平(砝码)、药匙、量筒(50
ml)、胶头滴管、
烧杯、玻璃棒、细口瓶
把配好的溶液装入试剂瓶(细口瓶)中,盖好瓶塞,贴上标签(注名药品名称和溶质质量分数)
溶解:
装瓶存放:
发现问题
若所配溶液的溶质质量分数略大于16%,可能的原因有哪些?
2.称量时:
称量食盐时指针偏左
量取水时俯视读数
3.溶解时:
1.计算时:
量筒中的水没有完全倒入烧杯
食盐算多了或水算少了
发现问题
药品和砝码放颠倒
量水时仰视读数
将盐倒入烧杯时撒到桌子上
药品中有杂质
2.称量时:
3.溶解时:
1.计算时:
食盐算少了或水算多了
若所配溶液的溶质质量分数略小于16%,可能的原因有哪些?
你会了吗?
1、配制100
g溶质质量分数为6%的氢氧化钠溶液(水的密度近似看作1
g/mL),下列操作正确的是
(
)
A.将氢氧化钠固体置于滤纸上称量
B.俯视量筒刻度读出所取水的体积
C.将氢氧化钠固体置于托盘天平的右盘、砝码置于左盘称量
D.将94
mL水倒入盛有6
g氢氧化钠固体的烧杯中搅拌溶解
D
2、实验室提供了
①天平
②量筒
③烧杯
④玻璃棒
⑤酒精灯等仪器,小华同学用固体氯化钠配制10%的氯化钠溶液,小亮同学用浓盐酸配制10%的稀盐酸。
(1)当用天平称量药品时,砝码应放在天平的
盘,配制过程中用玻璃棒搅拌是为了
。
(2)上述仪器中,两位同学都不需要的仪器是
(填序号,后同)小华需要而小亮不需要的仪器是
。
加速固体溶解
①
⑤
右
1、把10克氯化钠放入40克水中,完全溶解后,溶液中氯化钠的质量分数为(
)
A.10%
B.20%
C.25%
D.33.3%
2、配制100克质量分数为19.6%的稀硫酸,需要质量分数为98%的浓硫酸
克。
B
20
在线测试
3、将5g碳酸钠粉末加到95g溶质质量分数为10%的碳酸钠
溶液中,完全溶解后溶液的溶质的质量分数为
。
4、现有100g溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应向此溶液中加入食盐
g,
或蒸发掉水
g.
14.5%
50
12.25
5、把一杯食盐水倒出一部分,没有改变的是(
)
A
溶质的质量
B
溶剂的质量
C
溶液的质量
D
溶质的质量分数
6、家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是(
)
A
100克醋酸中含醋为10克
B
100克醋酸的水溶液中含醋酸10克
C
100克水中含醋酸为10克
D
100克醋酸的水溶液中含水10克
D
B
7.实验室中要用浓硫酸配制一定质量分数的稀硫酸,先后顺序的操作步骤是(
)
A.量取、溶解、计算
B.计算、溶解、量取
C.量取、计算、溶解
D.计算、量取、溶解
8.用浓硫酸配制一定质量分数的稀硫酸,不需要用到的仪器是(
)
A.托盘天平
B.烧杯
C.量筒
D.玻璃棒
D
A
9.
要配制100g溶质质量分数为10%的氯化钠溶液,下列操作正确的是(
)
A.将10g氯化钠固体直接放在天平的托盘上称量
B.量取90mL水时,俯视读数
C.为加快固体溶解,用温度计搅拌溶液
D.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
D
10.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是
(
)
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液
B
11.欲配制50g7%的氯化钠溶液:
(1)实验步骤应为:
、
、
、
、
。
(2)需要的玻璃仪器有:________________________
________________________。
(3)在托盘天平上称取
氯化钠,用规格为_____
的量筒量取
水。
计算
称量
量取
溶解
装瓶存放
量筒、胶头滴管、烧杯、
3.5g
50mL
46.5mL
玻璃棒
(4)将称量的氯化钠和水倒入烧杯中,为加快氯化钠的溶解速率,常用的方是_____、_____、_____________。
(5)在量取水的体积时,若俯视读数,则配制的溶液的溶质质量分数会
。(填偏高、相等、或偏低)
搅拌
加热
把大颗粒盐研细
偏高
再见
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
