京改版九年级下册化学 第12章 盐复习 课件(30张PPT)
文档属性
| 名称 | 京改版九年级下册化学 第12章 盐复习 课件(30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-05 00:00:00 | ||
图片预览







文档简介
(共30张PPT)
温故而知新
复习内容
一、
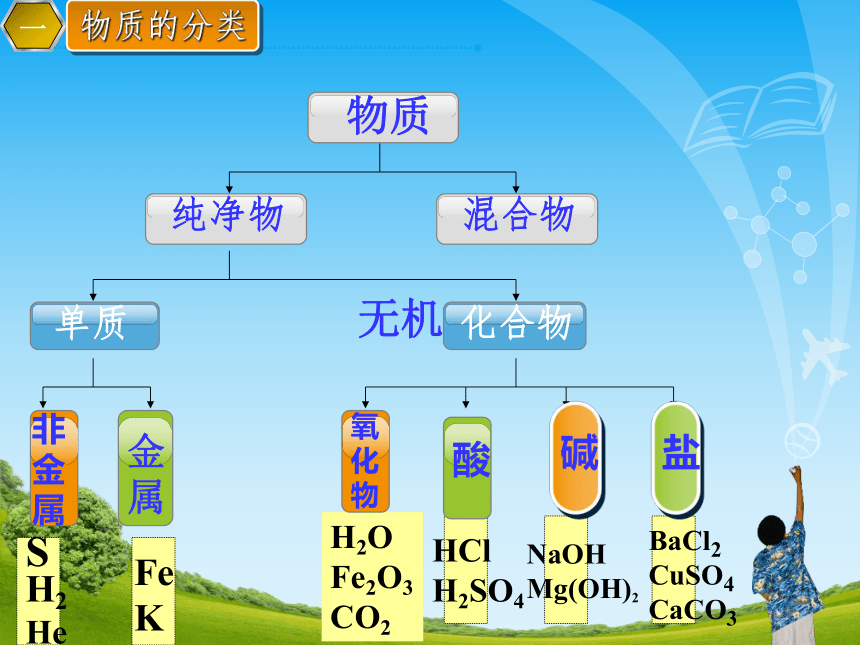
物质的分类
盐的化学性质
复分解反应发生的条件及类别
生活中常见的盐
四、
三、
二、
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
无机
1、下列物质的名称、化学式和所属的类别都正确的是(
)
A.甲烷、CH4、有机物
B.锰、MN、金属单质
C.氯酸钾、KCl03、金属氧化物
D.氧化汞、HgO、非金属氧化物
A
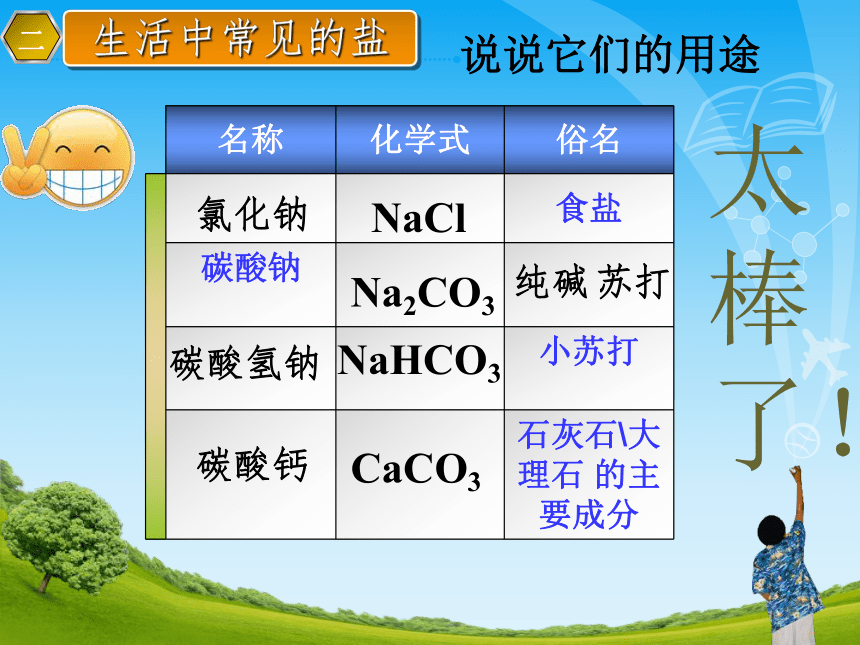
氯化钠
NaCl
Na2CO3
苏打
纯碱
碳酸氢钠
NaHCO3
碳酸钙
CaCO3
生活中常见的盐
太棒了!
说说它们的用途
名称
化学式
俗名
食盐
碳酸钠
小苏打
石灰石\大理石
的主要成分
2、下列有关物质的化学式、名称、俗名不完全对应的是
A.NaOH
氢氧化钠
烧碱
B.CaO
氢氧化钙
生石灰
C.Na2CO3
碳酸钠
纯碱
D.NaCl
氯化钠
食盐
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
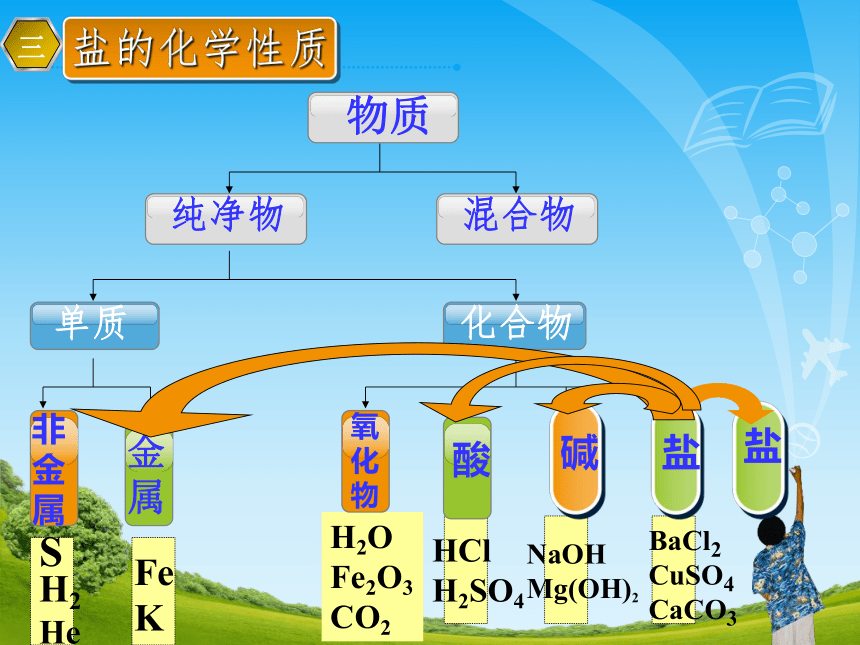
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
盐的化学性质
盐的化学性质
2、盐
+
酸
——
3、盐(溶液)+碱(溶液)——
4、盐(溶液)+盐(溶液)—
1、盐(溶液)+金属—
新盐+新金属
新盐
+
新酸
新盐+新碱
两种新盐
盐的化学性质
1盐(溶液)+金属—新盐+新金属
CuSO4+
Fe
===
FeSO4
+
Cu
CuCl2+
Ag
------
(置换反应)
Ag排在Cu的后面
?
古代炼铜,“湿法炼铜”“曾经得铁则化铜)
反应的条件:
只有排在前面的金属才能把可溶性盐中的金属置换出来
三、盐的化学性质1
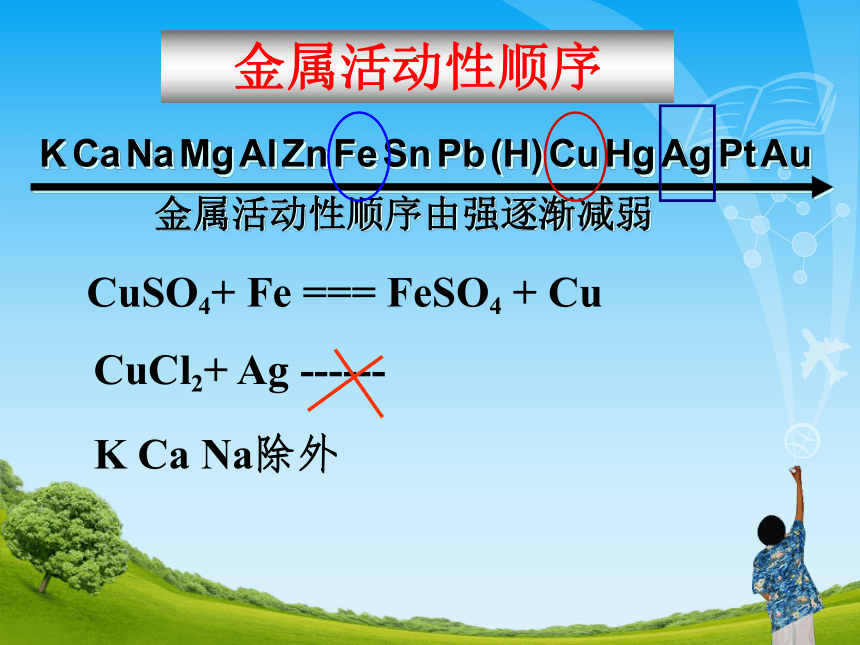
金属活动性顺序
金属活动性顺序由强逐渐减弱
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
CuSO4+
Fe
===
FeSO4
+
Cu
CuCl2+
Ag
------
K
Ca
Na除外
(2)盐+酸——新盐+新酸
BaCl2
+
HCl ------
CaCO3+2HCl
==
Na2CO3+2HCl==
(复分解反应)
无↓
符合复分解反应的条件:生成物中有气体或沉淀或水
三、盐的化学性质2
CaCl2
+
CO2↑+H2O
2NaCl+H2O+CO2↑
(3)盐(溶液)+碱(溶液)——新盐+新碱
Na2CO3+Ca(OH)
2==
BaCl2
+
NaOH -----
(复分解反应)
无↓
符合复分解反应的条件:生成物中有气体或沉淀或水.
反应物均要可溶于水。
三、盐的化学性质3
CaCO3↓
+2NaOH
(4)盐(溶液)+盐(溶液)—两种新盐
(复分解反应)
NaCl
+
AgNO3
==
符合复分解反应的条件:生成物中有气体或沉淀或水.
反应物均要可溶于水。
三、盐的化学性质4
AgCl
↓
+NaNO3
复分解反应
由两种化合物互相交换成分,生成另外两种化合物的反应。
在水溶液中互相交换离子。
元素化合价不变
1
2
3
生成物中有沉淀、气体或水
定义:
特点:
条件:
4
发生复分解反应的物质类别:
3、在以下的反应中:属于复分解反应类型的是
A、Fe+H2SO4==FeSO4+H2
↑
B、CO2+Ca(OH)2==CaCO3↓
+H2O
C
、H2CO3==H2O+CO2
↑
D、
NaCl
+
AgNO3
==
AgCl
↓
+NaNO3
(
)
4、部分酸、碱和盐的溶解性:
绝大多数的酸都___溶于水;碱中能溶于水的只有_
_____________________,
微溶于水;
四大类可溶性盐是__________________;盐酸盐
只有____不溶,其余都能溶于水;硫酸盐中______不
溶,_____________微溶,其余都能溶于水;碳酸盐
中
能溶于水的只有________________________,
微溶的是_____,其余都不能溶于水。
能
KOH、
NaOH、氨水、
Ba(OH)2
钾盐、钠盐、铵盐和硝酸盐
AgCl
BaSO4
CaSO4
、Ag2SO4
K2CO3
、Na2CO3、(NH4)2CO3.
MgCO3
Ca(OH)
2
5、给盐酸、氯化锌、硫酸钠、碳酸钠、氢氧化钡这五种物质分类。将其化学式填入空格中。酸
,碱
,盐
,这五种物质两两相互能发生化学反应的共有
种。写出反应的化学方程式。
HCl
Ba(OH)2
ZnCl2
Na2SO4
Na2CO3
6
HCl
Ba(OH)2
ZnCl2
Na2SO4
Na2CO3
1
4
3
5
6
2
1、2HCl+Ba(OH)2==BaCl2+2H2O
2、2HCl+Na2CO3==2NaCl+H2O+CO2
↑
3、Ba(OH)2+ZnCl2
==BaCl2+Zn
(OH)2
↓
4、Ba(OH)2+Na2SO4
==BaSO4
↓+2NaOH
5、Ba(OH)2+Na2CO3
==BaCO3+2NaOH
6
、
ZnCl2
+Na2CO3
==ZnCO3
↓
+2NaCl
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
复分解反应
4、发生复分解反应的物质类别:
④.酸
+
碱
—盐
+
水
①.盐
+
酸
——新盐+新酸
②.盐(溶液)+碱(溶液)
—新盐+新碱
③.盐(溶液)+
盐(溶液)----
两种新盐
复分解反应
⑤
.金属氧化物+酸——盐+水
6、以下反应中属于复分解反应类型的有
A、CuO+H2SO4
==CuSO4
+H2O
C、NaOH+HCl==H2O+NaCl
D、
Na2CO3+2HCl==2NaCl+H2O+CO2↑
E、CO2+Ca(OH)2==CaCO3
↓
+H2O
第一关
闯关拿奖
1.下列几组物质按酸、碱、盐顺序排列的是(
)
第一关
A.KNO3、NaOH、HCl
B.Ca(OH)2、HCl、NaCl
C.H2SO4、Na2CO3、Ba(OH)2
D.HNO3、KOH、CuSO4
2、下列物质中属于氧化物的是(
)
第二关
A、食盐
你拥有的奖品
C、白酒
D、干冰
B、空气
恭喜你,过关了!
第二关
奖
去第三关
你拥有的奖品
第三关
你拥有的奖品
3、下列盐的用途中,错误的是
(
)
A.用含亚硝酸钠的工业用盐烹调食物
B.用碳酸钙作补钙剂
C.用氯化钠配制生理盐水
D.用碳酸氢钠治疗胃酸过多
第四关
你拥有的奖品
4、下列各组物质能在pH=1的无色溶液中大量共存的是
(
)
K2SO4
Ba(OH)2
KCl
Cu(NO3)2
NaCl
KNO3
C.
Na2CO3
KNO3
NH4Cl
D.
MgSO4
NaNO3
KCl
第五关
你拥有的奖品
5、右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
(
)
?A.反应后溶液的pH大于7
?B.反应前的溶液均可导电,
反应后的溶液不导电
?C.反应后溶液中存在的粒子只
有Na+和Cl―
?
D.反应前后所有元素的化合价均无变化
恭喜你拥有了奖杯,请发表一下获奖感言,这节课有什么收获?
恳请批评指正
温故而知新
复习内容
一、
物质的分类
盐的化学性质
复分解反应发生的条件及类别
生活中常见的盐
四、
三、
二、
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
无机
1、下列物质的名称、化学式和所属的类别都正确的是(
)
A.甲烷、CH4、有机物
B.锰、MN、金属单质
C.氯酸钾、KCl03、金属氧化物
D.氧化汞、HgO、非金属氧化物
A
氯化钠
NaCl
Na2CO3
苏打
纯碱
碳酸氢钠
NaHCO3
碳酸钙
CaCO3
生活中常见的盐
太棒了!
说说它们的用途
名称
化学式
俗名
食盐
碳酸钠
小苏打
石灰石\大理石
的主要成分
2、下列有关物质的化学式、名称、俗名不完全对应的是
A.NaOH
氢氧化钠
烧碱
B.CaO
氢氧化钙
生石灰
C.Na2CO3
碳酸钠
纯碱
D.NaCl
氯化钠
食盐
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
盐的化学性质
盐的化学性质
2、盐
+
酸
——
3、盐(溶液)+碱(溶液)——
4、盐(溶液)+盐(溶液)—
1、盐(溶液)+金属—
新盐+新金属
新盐
+
新酸
新盐+新碱
两种新盐
盐的化学性质
1盐(溶液)+金属—新盐+新金属
CuSO4+
Fe
===
FeSO4
+
Cu
CuCl2+
Ag
------
(置换反应)
Ag排在Cu的后面
?
古代炼铜,“湿法炼铜”“曾经得铁则化铜)
反应的条件:
只有排在前面的金属才能把可溶性盐中的金属置换出来
三、盐的化学性质1
金属活动性顺序
金属活动性顺序由强逐渐减弱
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
CuSO4+
Fe
===
FeSO4
+
Cu
CuCl2+
Ag
------
K
Ca
Na除外
(2)盐+酸——新盐+新酸
BaCl2
+
HCl ------
CaCO3+2HCl
==
Na2CO3+2HCl==
(复分解反应)
无↓
符合复分解反应的条件:生成物中有气体或沉淀或水
三、盐的化学性质2
CaCl2
+
CO2↑+H2O
2NaCl+H2O+CO2↑
(3)盐(溶液)+碱(溶液)——新盐+新碱
Na2CO3+Ca(OH)
2==
BaCl2
+
NaOH -----
(复分解反应)
无↓
符合复分解反应的条件:生成物中有气体或沉淀或水.
反应物均要可溶于水。
三、盐的化学性质3
CaCO3↓
+2NaOH
(4)盐(溶液)+盐(溶液)—两种新盐
(复分解反应)
NaCl
+
AgNO3
==
符合复分解反应的条件:生成物中有气体或沉淀或水.
反应物均要可溶于水。
三、盐的化学性质4
AgCl
↓
+NaNO3
复分解反应
由两种化合物互相交换成分,生成另外两种化合物的反应。
在水溶液中互相交换离子。
元素化合价不变
1
2
3
生成物中有沉淀、气体或水
定义:
特点:
条件:
4
发生复分解反应的物质类别:
3、在以下的反应中:属于复分解反应类型的是
A、Fe+H2SO4==FeSO4+H2
↑
B、CO2+Ca(OH)2==CaCO3↓
+H2O
C
、H2CO3==H2O+CO2
↑
D、
NaCl
+
AgNO3
==
AgCl
↓
+NaNO3
(
)
4、部分酸、碱和盐的溶解性:
绝大多数的酸都___溶于水;碱中能溶于水的只有_
_____________________,
微溶于水;
四大类可溶性盐是__________________;盐酸盐
只有____不溶,其余都能溶于水;硫酸盐中______不
溶,_____________微溶,其余都能溶于水;碳酸盐
中
能溶于水的只有________________________,
微溶的是_____,其余都不能溶于水。
能
KOH、
NaOH、氨水、
Ba(OH)2
钾盐、钠盐、铵盐和硝酸盐
AgCl
BaSO4
CaSO4
、Ag2SO4
K2CO3
、Na2CO3、(NH4)2CO3.
MgCO3
Ca(OH)
2
5、给盐酸、氯化锌、硫酸钠、碳酸钠、氢氧化钡这五种物质分类。将其化学式填入空格中。酸
,碱
,盐
,这五种物质两两相互能发生化学反应的共有
种。写出反应的化学方程式。
HCl
Ba(OH)2
ZnCl2
Na2SO4
Na2CO3
6
HCl
Ba(OH)2
ZnCl2
Na2SO4
Na2CO3
1
4
3
5
6
2
1、2HCl+Ba(OH)2==BaCl2+2H2O
2、2HCl+Na2CO3==2NaCl+H2O+CO2
↑
3、Ba(OH)2+ZnCl2
==BaCl2+Zn
(OH)2
↓
4、Ba(OH)2+Na2SO4
==BaSO4
↓+2NaOH
5、Ba(OH)2+Na2CO3
==BaCO3+2NaOH
6
、
ZnCl2
+Na2CO3
==ZnCO3
↓
+2NaCl
金属
S
H2
He
Fe
K
H2O
Fe2O3
CO2
HCl
H2SO4
NaOH
Mg(OH)2
BaCl2
CuSO4
CaCO3
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
非金属
复分解反应
4、发生复分解反应的物质类别:
④.酸
+
碱
—盐
+
水
①.盐
+
酸
——新盐+新酸
②.盐(溶液)+碱(溶液)
—新盐+新碱
③.盐(溶液)+
盐(溶液)----
两种新盐
复分解反应
⑤
.金属氧化物+酸——盐+水
6、以下反应中属于复分解反应类型的有
A、CuO+H2SO4
==CuSO4
+H2O
C、NaOH+HCl==H2O+NaCl
D、
Na2CO3+2HCl==2NaCl+H2O+CO2↑
E、CO2+Ca(OH)2==CaCO3
↓
+H2O
第一关
闯关拿奖
1.下列几组物质按酸、碱、盐顺序排列的是(
)
第一关
A.KNO3、NaOH、HCl
B.Ca(OH)2、HCl、NaCl
C.H2SO4、Na2CO3、Ba(OH)2
D.HNO3、KOH、CuSO4
2、下列物质中属于氧化物的是(
)
第二关
A、食盐
你拥有的奖品
C、白酒
D、干冰
B、空气
恭喜你,过关了!
第二关
奖
去第三关
你拥有的奖品
第三关
你拥有的奖品
3、下列盐的用途中,错误的是
(
)
A.用含亚硝酸钠的工业用盐烹调食物
B.用碳酸钙作补钙剂
C.用氯化钠配制生理盐水
D.用碳酸氢钠治疗胃酸过多
第四关
你拥有的奖品
4、下列各组物质能在pH=1的无色溶液中大量共存的是
(
)
K2SO4
Ba(OH)2
KCl
Cu(NO3)2
NaCl
KNO3
C.
Na2CO3
KNO3
NH4Cl
D.
MgSO4
NaNO3
KCl
第五关
你拥有的奖品
5、右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
(
)
?A.反应后溶液的pH大于7
?B.反应前的溶液均可导电,
反应后的溶液不导电
?C.反应后溶液中存在的粒子只
有Na+和Cl―
?
D.反应前后所有元素的化合价均无变化
恭喜你拥有了奖杯,请发表一下获奖感言,这节课有什么收获?
恳请批评指正
