山东省东平县实验中学2019-2020学年第二学期八年级化学-3.1.1-原子的构成(24张ppt)
文档属性
| 名称 | 山东省东平县实验中学2019-2020学年第二学期八年级化学-3.1.1-原子的构成(24张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-05 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
第一课时
原子的结构
第三单元第一节
原子的构成
2.保持氧气化学性质的粒子是(
),保持二氧化碳化学性质的粒子是(
),所以,_____分子性质相同,_____分子性质不同。
1.构成物质的微粒有(
)、(
).
3.在直流电作用下,(
)被破坏,分成氢原子和氧原子,每(
)重新组合构成一个(
),许多氢分子聚集成(
);每两个氧原子重新组合构成一个氧分子,许多氧分子聚集成氧气。
2.保持氧气化学性质的粒子是氧分子,保持二氧化碳化学性质的粒子是二氧化碳分子,所以,同种物质分子性质相同,不同种物质分子性质不同。
1.构成物质的微粒有分子、原子
3.在直流电作用下,水分子被破坏,分成氢原子和氧原子,每两个氢原子重新组合构成一个氢分子,许多氢分子聚集成氢气;每两个氧原子重新组合构成一个氧分子,许多氧分子聚集成氧气。
1、通过学习原子的结构发现史,认识原子构成,通过对“α粒子轰击金箔实验”的分析,推出原子是由原子核和核外电子构成的。
2.分析原子的结构,理解原子中“核电荷数、质子数、核外电子数”的关系。
3.通过分析原子中各种微粒的质量关系,了解原子的质量主要集中在原子核上。
学习目标
近代科学原子论(1803年)
一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球
英国化学家道尔顿
(J.Dalton
,
1766~1844)
汤姆森发现了电子(1897年)
英国物理学家汤姆森
(J.J.Thomson
,1856~1940)
电子是一种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆森的原子模型是怎样的?成立吗?
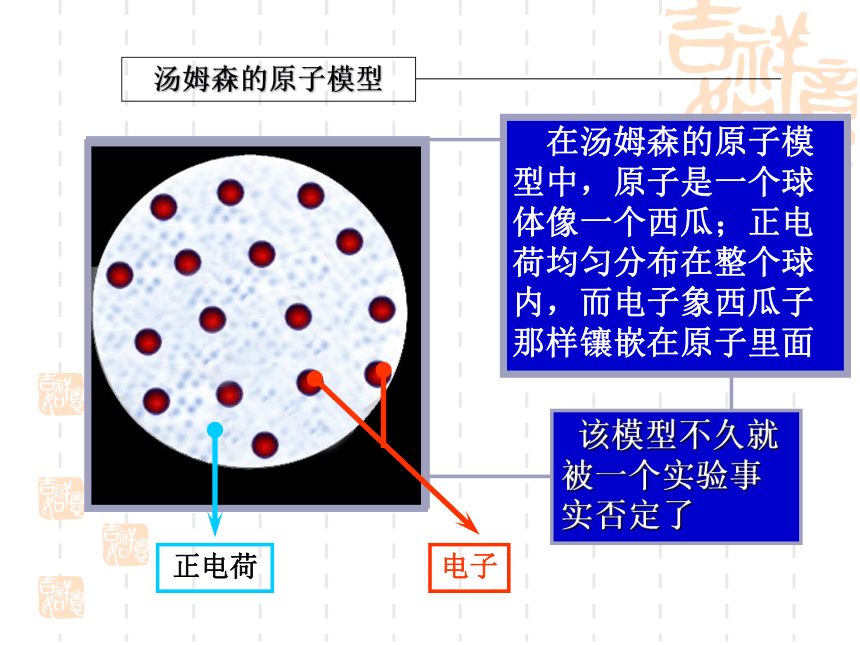
汤姆森的原子模型
在汤姆森的原子模型中,原子是一个球体像一个西瓜;正电荷均匀分布在整个球内,而电子象西瓜子那样镶嵌在原子里面
电子
正电荷
该模型不久就被一个实验事实否定了
α粒子散射实验(1911年)
——原子有核
卢瑟福和他的助手做了著名α粒子散射实验。
英国科学家卢瑟福
(E.Rutherford,1871~1937)
由卢瑟福对“α粒子轰击金箔实验”的结果说明了什么问题?α粒子有什么特点?
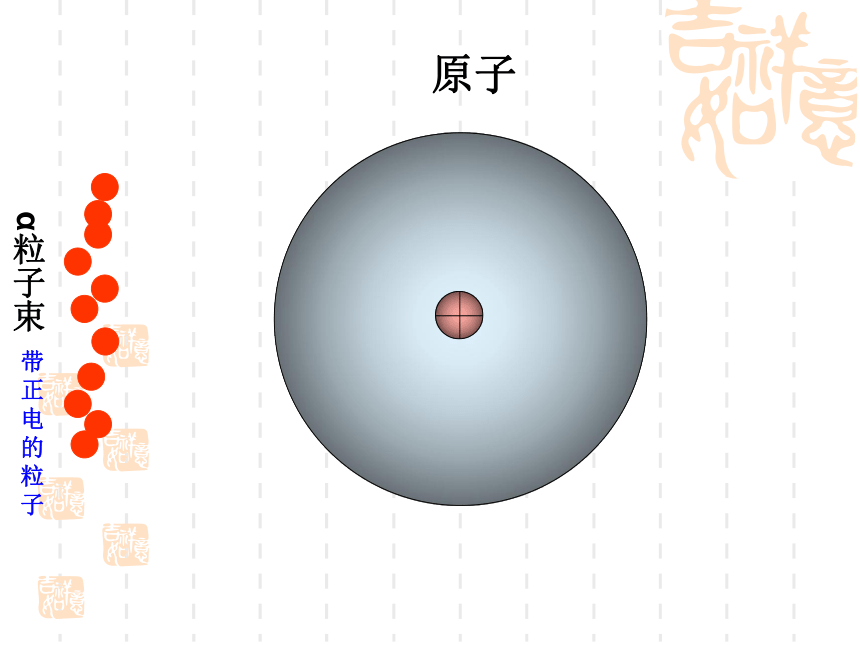
原子
α粒子束
带正电的粒子
原子
α粒子束
α粒子是带正电、质量比电子大的多的微粒
α粒子未发生偏转
α粒子发生偏转
α粒子束
α粒子被反弹
科学家是怎样认识原子的
卢瑟福
1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带正电荷的粒子)轰击金箔时,发现:
1、大多数α粒子能穿透金箔,而且不改变原来的运动方向;
2、也有一小部分α粒子改变了原来的运动路径;
3、甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。
交流共享
结合以上实验的3个实验现象,分析原子结构的以下特点:
1.现象1说明了什么?
2.现象2说明了什么?
3.现象3说明了什么?
原子内有很大的空间
这个微粒体积很小、质量很大。
原子内有一个带正电的微粒
原子是由居于原子中心的带正电的原子核和核外带负电的电子构成,电子在原子核外绕核做高速运动。
若将原子比做一
个庞大的体育
场,而原子核只
相当于一只蚂
蚁。
原子核:带正电、质量大、体积小。
电子的质量很小,几乎可忽略不计,原子的质量几乎都集中在原子核上,但原子核的体积却很小。那么原子核能否再分呢?它具有什么特点?质子或电子所带电荷数与它们的个数具有什么关系?
揭开原子核的秘密
实验证明:原子核是由带正电的质子和不带电的中子构成。如:碳原子
小结
原子
_____
______
___
___
(每个
带一个单位
电荷)
(不带电)
(每个
带一个单位的
电荷)
质子
中子
原子核
核外电子
核电荷数:原子核所带的正电荷数
质子
电子
正
负
核电荷数=质子数
几种原子的构成
原子
核内质子数
中子数
核外电子数
氢
1
0
1
碳
6
6
6
氧
8
8
8
钠
11
12
11
镁
12
12
12
你认为原子整体显电性吗?
“质子数”、“核电荷数”、
“核外电子数”之间的关系是什么。
核电荷数=质子数=核外电子数
不同的原子质子数不同。质子数不一定等于中子数。氢原子核没有中子。
思考
为什么说原子的质量主要集中在原子核上?为什么说原子不显电性?
知识的拓展
实验证明,质子和中子是由更小的微粒构成的。
有关原子的结构和性质仍有探索和研究中……
畅谈收获:
1、这节课你学到了哪些知识?
2、通过这节课,你在学习方法和思想上有哪些收获?
核电荷数=质子数=核外电子数
原子
原子核
核外电子
质子
中子
(每个质子带一个单位正电荷)
(不带电)
(每个电子带一个单位的负电荷)
书面作业
能力训练p68.
【真题训练】1题和3题,把错误的选项改成正确的一句话,写在作业本上。
当堂达标
2、原子由
和
构成,原子核又由
和
构成
3、原子中一定含有的微粒是——
4、某原子的质子数为26,则核外电子数为
,中子数比质子数多4,则该原子中所含微粒总为
.
11
钠
8
电子数
氧
碳
1
氢
质子数
原子种类
核电荷数
1.填写下表
1
6
6
8
11
11
8
1
6
原子核
电子
质子
中子
质子和电子
82
26
第一课时
原子的结构
第三单元第一节
原子的构成
2.保持氧气化学性质的粒子是(
),保持二氧化碳化学性质的粒子是(
),所以,_____分子性质相同,_____分子性质不同。
1.构成物质的微粒有(
)、(
).
3.在直流电作用下,(
)被破坏,分成氢原子和氧原子,每(
)重新组合构成一个(
),许多氢分子聚集成(
);每两个氧原子重新组合构成一个氧分子,许多氧分子聚集成氧气。
2.保持氧气化学性质的粒子是氧分子,保持二氧化碳化学性质的粒子是二氧化碳分子,所以,同种物质分子性质相同,不同种物质分子性质不同。
1.构成物质的微粒有分子、原子
3.在直流电作用下,水分子被破坏,分成氢原子和氧原子,每两个氢原子重新组合构成一个氢分子,许多氢分子聚集成氢气;每两个氧原子重新组合构成一个氧分子,许多氧分子聚集成氧气。
1、通过学习原子的结构发现史,认识原子构成,通过对“α粒子轰击金箔实验”的分析,推出原子是由原子核和核外电子构成的。
2.分析原子的结构,理解原子中“核电荷数、质子数、核外电子数”的关系。
3.通过分析原子中各种微粒的质量关系,了解原子的质量主要集中在原子核上。
学习目标
近代科学原子论(1803年)
一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球
英国化学家道尔顿
(J.Dalton
,
1766~1844)
汤姆森发现了电子(1897年)
英国物理学家汤姆森
(J.J.Thomson
,1856~1940)
电子是一种带负电、有一定质量的微粒,普遍存在于各种原子之中。
汤姆森的原子模型是怎样的?成立吗?
汤姆森的原子模型
在汤姆森的原子模型中,原子是一个球体像一个西瓜;正电荷均匀分布在整个球内,而电子象西瓜子那样镶嵌在原子里面
电子
正电荷
该模型不久就被一个实验事实否定了
α粒子散射实验(1911年)
——原子有核
卢瑟福和他的助手做了著名α粒子散射实验。
英国科学家卢瑟福
(E.Rutherford,1871~1937)
由卢瑟福对“α粒子轰击金箔实验”的结果说明了什么问题?α粒子有什么特点?
原子
α粒子束
带正电的粒子
原子
α粒子束
α粒子是带正电、质量比电子大的多的微粒
α粒子未发生偏转
α粒子发生偏转
α粒子束
α粒子被反弹
科学家是怎样认识原子的
卢瑟福
1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带正电荷的粒子)轰击金箔时,发现:
1、大多数α粒子能穿透金箔,而且不改变原来的运动方向;
2、也有一小部分α粒子改变了原来的运动路径;
3、甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。
交流共享
结合以上实验的3个实验现象,分析原子结构的以下特点:
1.现象1说明了什么?
2.现象2说明了什么?
3.现象3说明了什么?
原子内有很大的空间
这个微粒体积很小、质量很大。
原子内有一个带正电的微粒
原子是由居于原子中心的带正电的原子核和核外带负电的电子构成,电子在原子核外绕核做高速运动。
若将原子比做一
个庞大的体育
场,而原子核只
相当于一只蚂
蚁。
原子核:带正电、质量大、体积小。
电子的质量很小,几乎可忽略不计,原子的质量几乎都集中在原子核上,但原子核的体积却很小。那么原子核能否再分呢?它具有什么特点?质子或电子所带电荷数与它们的个数具有什么关系?
揭开原子核的秘密
实验证明:原子核是由带正电的质子和不带电的中子构成。如:碳原子
小结
原子
_____
______
___
___
(每个
带一个单位
电荷)
(不带电)
(每个
带一个单位的
电荷)
质子
中子
原子核
核外电子
核电荷数:原子核所带的正电荷数
质子
电子
正
负
核电荷数=质子数
几种原子的构成
原子
核内质子数
中子数
核外电子数
氢
1
0
1
碳
6
6
6
氧
8
8
8
钠
11
12
11
镁
12
12
12
你认为原子整体显电性吗?
“质子数”、“核电荷数”、
“核外电子数”之间的关系是什么。
核电荷数=质子数=核外电子数
不同的原子质子数不同。质子数不一定等于中子数。氢原子核没有中子。
思考
为什么说原子的质量主要集中在原子核上?为什么说原子不显电性?
知识的拓展
实验证明,质子和中子是由更小的微粒构成的。
有关原子的结构和性质仍有探索和研究中……
畅谈收获:
1、这节课你学到了哪些知识?
2、通过这节课,你在学习方法和思想上有哪些收获?
核电荷数=质子数=核外电子数
原子
原子核
核外电子
质子
中子
(每个质子带一个单位正电荷)
(不带电)
(每个电子带一个单位的负电荷)
书面作业
能力训练p68.
【真题训练】1题和3题,把错误的选项改成正确的一句话,写在作业本上。
当堂达标
2、原子由
和
构成,原子核又由
和
构成
3、原子中一定含有的微粒是——
4、某原子的质子数为26,则核外电子数为
,中子数比质子数多4,则该原子中所含微粒总为
.
11
钠
8
电子数
氧
碳
1
氢
质子数
原子种类
核电荷数
1.填写下表
1
6
6
8
11
11
8
1
6
原子核
电子
质子
中子
质子和电子
82
26
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
