苏教版高中化学必修二 2.1.1 《化学反应速率》 (共28张PPT)
文档属性
| 名称 | 苏教版高中化学必修二 2.1.1 《化学反应速率》 (共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 933.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-06 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第一单元
化学反应速率与反应限度
第1课时
化学反应速率
2020年4月8日
专题2
【自学】归纳出化学反应速率的定义、表示方法、表达式及单位。
【学习目标】
1.了解化学反应速率及其简单计算。
2.认识影响化学反应速率的因素。
或mol/(L·min)
mol/(L·s)
一、化学反应速率
1.定义:
3.表达式:
单位:
mol·
L
-1
·min-1
mol·
L
-1
·s-1
化学反应速率是用来衡量化学反应
进行的快慢程度的物理量。
2.表示方法:
例题1:
一密闭容器中有N2和H2,反应开始时,N2浓度为2mol/L,H2浓度为5mol/L,两分钟后,测得N2浓度为1.8mol/L,求两分钟内N2、H2、NH3的平均反应速率分别是多少?比较三者速率有何联系?
4.应用化学反应速率的注意事项:
③方程式:
aA+bB=cC+dD,
变化量之比=反应速率之比
=化学计量数之比
=
a
:
b
:
c
:
d
①化学反应速率表示的是一段时间内的
平均速率,均取正值。
②同一反应的速率可用不同物质来表示,
其数值可能不同,但表示的意义相同,
所以需要指明具体物质,如v
(B)。
④
对于固体物质或气态反应中的液体物质,反应在其表面进行,它们的“浓度”是不变的,因此不用纯液体和固体表示化学反应速率。
即学即练:
在
反应中:2s内,测得生成NH3
的平均反应速率为0.4mol·L-1·s-1
,则2s时N2的物质的量浓
N2+3H2
2NH3
度改变了多少?
注意:对于同一化学反应,在相同的反应时间内,用不同的物质来表示的化学反应速率的数值可能是不同的。比较不同反应的速率大小时,需换算成同一物质的速率且单位相同来比较。
例题2
从大到小:②=③>①
>
④
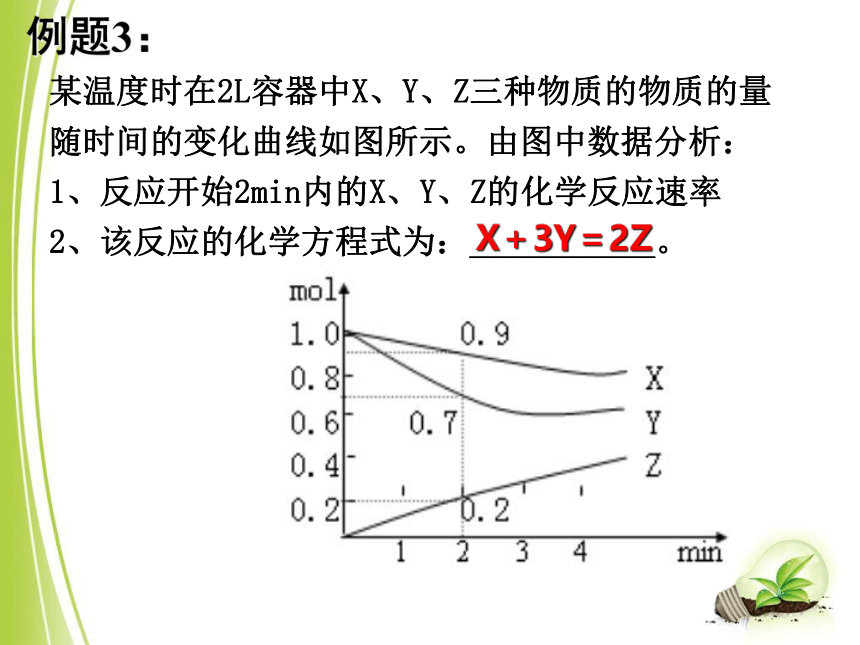
某温度时在2L容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析:
1、反应开始2min内的X、Y、Z的化学反应速率
2、该反应的化学方程式为:___________。
例题3:
X+3Y=2Z
将食品置于低温条件下,常常可以保存更长的时间。为什么?
加酶洗衣粉的去污能力比普通洗衣粉要强的多。为什么?
向炉膛鼓风,炉子中火就会越烧越旺。为什么?
二、化学反应速率的影响因素
1.
决定因素(内因):
2.
外界条件(外因):
自学:请同学们阅读课本31页,归纳出影响化学
反应速率的因素有哪些?
温度、催化剂、浓度......
反应物本身的性质
实验研究的方法:
固定其他条件,只改变一个条件,观察改变条件对反应速率的影响。
对比实验法
请设计实验说明温度、浓度、催化剂的改变分别对该反应速率的影响。
实验探究:影响双氧水分解速率的因素
提供可选用的试剂:4%、12%的过氧化氢溶液、MnO2粉末、1mol/L
FeCl3
、热水
要求:说出实验目的、实验现象和
结论
外界条件对化学反应速率的影响
水浴加热产生
气泡快
加入二氧化锰粉末产生气泡快
加热能加快反应速率
使用催化剂能加快反应速率
浓度大的产生气泡快
增大反应物的浓度能加快反应速率
实验方案
实验现象
结论
实验一:取2只试管,各加入5
mL
12%的过氧化氢溶液,用水浴加热其中1支试管。
实验二:取2只试管,各加入5
mL
4%的过氧化氢溶液,往其中1支试管中加入少量二氧化锰粉末
实验三:取2只试管,各加入5
mL
4%、12%的过氧化氢溶液,分别滴入几滴0.2
mol·L-1氯化铁溶液。
外界条件对反应速率的影响
结论:当其他条件不变时,
升高温度,化学反应速率
降低温度,化学反应速率
1.温度
加快
减慢
外界条件对反应速率的影响
结论:当其他条件不变时,
使用正催化剂,化学反应速率
使用负催化剂,化学反应速率
2.催化剂
加快;
减慢。
外界条件对反应速率的影响
结论:当其他条件不变时,
增加反应物的浓度,化学反应速率
降低反应物的浓度,化学反应速率
强调:对于固体和纯液体来说,浓度都是不变的,固体和纯液体的量对于化学反应速率几乎不产生影响。
3.浓度
加快;
减慢。
已知:气体压强与浓度的关系
其他条件不变时,压强
气体浓度
思考:压强改变对反应速率有什么影响?
越大。
越大。
外界条件对反应速率的影响
仅适用于有气体参加的反应
结论:当其他条件不变时,
增加压强,化学反应速率
降低压强,化学反应速率
4.压强
加快;
减慢。
5.其他因素
外界条件对反应速率的影响
如:反应物接触面积的大小、
固体反应物的颗粒大小
等
用铁与稀硫酸反应制取氢气时,下列不能使氢气生成速率加大的是(
)
A.不用室温下的稀硫酸,改用热的稀硫酸
B.不用稀硫酸,改用98℅的浓硫酸
C.不用1
mol/L稀硫酸,改用2
mol/L硫酸
D.不用铁片,改用铁粉
B
例题4:
把除去氧化膜的镁条投入到盛有少量盐酸的
试管中,产生氢气的速率如图所示,在下列
因素中,影响反应速率的因素是(
)
速率
t3
t1
t2
时间
①盐酸的浓度
②镁条的表面积
③溶液的温度
④Cl-的浓度
A.
①④
B.
③④
C.
①②③
D.
②③
例题5:
C
为了研究碳酸钙与稀盐酸反应的反应速率,一位同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制如图曲线。请分析讨论以下问题。
(1)在0--t1、t1--t2、t2--t3各相同的时间段里,反应速率最大的是_______时间段,收集到气体最多的是______时间段。
(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。
(3)在t4后,为什么收集到的气体的体积不再增加?
⑵开始时C(H+)大,该反应的反应速率大;
t1—t2由于反应放热温度升高,所以速率迅速增大;最后是因为C(H+)减小了,反应速率减慢.
2.向下列四种盐酸溶液中,分别加入等质量的碳酸钙,其中反应速率最大的是(
)
A.10
mL、2
mol·L-1
B.20
mL、2
mol·L-1
C.10
mL、4
mol·L-1
D.40
mL、1
mol·L-1
C
即学即练:
1.把下列金属分别投入0.1mol·L-1盐酸中,能发生反应但反应最缓慢的是(
)
A
Fe
B
Al
C
Mg
D
Cu
A
谢谢!
第一单元
化学反应速率与反应限度
第1课时
化学反应速率
2020年4月8日
专题2
【自学】归纳出化学反应速率的定义、表示方法、表达式及单位。
【学习目标】
1.了解化学反应速率及其简单计算。
2.认识影响化学反应速率的因素。
或mol/(L·min)
mol/(L·s)
一、化学反应速率
1.定义:
3.表达式:
单位:
mol·
L
-1
·min-1
mol·
L
-1
·s-1
化学反应速率是用来衡量化学反应
进行的快慢程度的物理量。
2.表示方法:
例题1:
一密闭容器中有N2和H2,反应开始时,N2浓度为2mol/L,H2浓度为5mol/L,两分钟后,测得N2浓度为1.8mol/L,求两分钟内N2、H2、NH3的平均反应速率分别是多少?比较三者速率有何联系?
4.应用化学反应速率的注意事项:
③方程式:
aA+bB=cC+dD,
变化量之比=反应速率之比
=化学计量数之比
=
a
:
b
:
c
:
d
①化学反应速率表示的是一段时间内的
平均速率,均取正值。
②同一反应的速率可用不同物质来表示,
其数值可能不同,但表示的意义相同,
所以需要指明具体物质,如v
(B)。
④
对于固体物质或气态反应中的液体物质,反应在其表面进行,它们的“浓度”是不变的,因此不用纯液体和固体表示化学反应速率。
即学即练:
在
反应中:2s内,测得生成NH3
的平均反应速率为0.4mol·L-1·s-1
,则2s时N2的物质的量浓
N2+3H2
2NH3
度改变了多少?
注意:对于同一化学反应,在相同的反应时间内,用不同的物质来表示的化学反应速率的数值可能是不同的。比较不同反应的速率大小时,需换算成同一物质的速率且单位相同来比较。
例题2
从大到小:②=③>①
>
④
某温度时在2L容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析:
1、反应开始2min内的X、Y、Z的化学反应速率
2、该反应的化学方程式为:___________。
例题3:
X+3Y=2Z
将食品置于低温条件下,常常可以保存更长的时间。为什么?
加酶洗衣粉的去污能力比普通洗衣粉要强的多。为什么?
向炉膛鼓风,炉子中火就会越烧越旺。为什么?
二、化学反应速率的影响因素
1.
决定因素(内因):
2.
外界条件(外因):
自学:请同学们阅读课本31页,归纳出影响化学
反应速率的因素有哪些?
温度、催化剂、浓度......
反应物本身的性质
实验研究的方法:
固定其他条件,只改变一个条件,观察改变条件对反应速率的影响。
对比实验法
请设计实验说明温度、浓度、催化剂的改变分别对该反应速率的影响。
实验探究:影响双氧水分解速率的因素
提供可选用的试剂:4%、12%的过氧化氢溶液、MnO2粉末、1mol/L
FeCl3
、热水
要求:说出实验目的、实验现象和
结论
外界条件对化学反应速率的影响
水浴加热产生
气泡快
加入二氧化锰粉末产生气泡快
加热能加快反应速率
使用催化剂能加快反应速率
浓度大的产生气泡快
增大反应物的浓度能加快反应速率
实验方案
实验现象
结论
实验一:取2只试管,各加入5
mL
12%的过氧化氢溶液,用水浴加热其中1支试管。
实验二:取2只试管,各加入5
mL
4%的过氧化氢溶液,往其中1支试管中加入少量二氧化锰粉末
实验三:取2只试管,各加入5
mL
4%、12%的过氧化氢溶液,分别滴入几滴0.2
mol·L-1氯化铁溶液。
外界条件对反应速率的影响
结论:当其他条件不变时,
升高温度,化学反应速率
降低温度,化学反应速率
1.温度
加快
减慢
外界条件对反应速率的影响
结论:当其他条件不变时,
使用正催化剂,化学反应速率
使用负催化剂,化学反应速率
2.催化剂
加快;
减慢。
外界条件对反应速率的影响
结论:当其他条件不变时,
增加反应物的浓度,化学反应速率
降低反应物的浓度,化学反应速率
强调:对于固体和纯液体来说,浓度都是不变的,固体和纯液体的量对于化学反应速率几乎不产生影响。
3.浓度
加快;
减慢。
已知:气体压强与浓度的关系
其他条件不变时,压强
气体浓度
思考:压强改变对反应速率有什么影响?
越大。
越大。
外界条件对反应速率的影响
仅适用于有气体参加的反应
结论:当其他条件不变时,
增加压强,化学反应速率
降低压强,化学反应速率
4.压强
加快;
减慢。
5.其他因素
外界条件对反应速率的影响
如:反应物接触面积的大小、
固体反应物的颗粒大小
等
用铁与稀硫酸反应制取氢气时,下列不能使氢气生成速率加大的是(
)
A.不用室温下的稀硫酸,改用热的稀硫酸
B.不用稀硫酸,改用98℅的浓硫酸
C.不用1
mol/L稀硫酸,改用2
mol/L硫酸
D.不用铁片,改用铁粉
B
例题4:
把除去氧化膜的镁条投入到盛有少量盐酸的
试管中,产生氢气的速率如图所示,在下列
因素中,影响反应速率的因素是(
)
速率
t3
t1
t2
时间
①盐酸的浓度
②镁条的表面积
③溶液的温度
④Cl-的浓度
A.
①④
B.
③④
C.
①②③
D.
②③
例题5:
C
为了研究碳酸钙与稀盐酸反应的反应速率,一位同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制如图曲线。请分析讨论以下问题。
(1)在0--t1、t1--t2、t2--t3各相同的时间段里,反应速率最大的是_______时间段,收集到气体最多的是______时间段。
(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。
(3)在t4后,为什么收集到的气体的体积不再增加?
⑵开始时C(H+)大,该反应的反应速率大;
t1—t2由于反应放热温度升高,所以速率迅速增大;最后是因为C(H+)减小了,反应速率减慢.
2.向下列四种盐酸溶液中,分别加入等质量的碳酸钙,其中反应速率最大的是(
)
A.10
mL、2
mol·L-1
B.20
mL、2
mol·L-1
C.10
mL、4
mol·L-1
D.40
mL、1
mol·L-1
C
即学即练:
1.把下列金属分别投入0.1mol·L-1盐酸中,能发生反应但反应最缓慢的是(
)
A
Fe
B
Al
C
Mg
D
Cu
A
谢谢!
