人教版高二化学选修4第三章 第四节 难溶电解质的溶解平衡(共19张PPT)
文档属性
| 名称 | 人教版高二化学选修4第三章 第四节 难溶电解质的溶解平衡(共19张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-08 21:20:32 | ||
图片预览






文档简介
(共19张PPT)
第三章水溶液中的离子平衡
第四节---难溶电解质的溶解平衡
温习旧知
1、溶解度的定义?
2、什么是饱和溶液?
在一定温度下,某固态物质在100克溶剂
里达到饱和状态时所溶解的质量。
一定温度下,不能再溶解溶质的溶液叫饱和
溶液
一、沉淀溶解平衡:
小组讨论:
将氯化钾溶液和硝酸银溶液混合,会发生怎样的离子反应?
二者反应是否能沉淀完全离子浓度变为0吗?
你能设计实验加以证明吗?
实验探究1:
实验操作:2mL0.2mol/L硝酸银和3mL0.2mol/L氯化钾完全反应后静置,向上层清液中加入KI溶液观察现象
实验现象:有黄色沉淀生成
实验结论:
AgNO3和KCl混合后溶液中有Ag+,二者反应没有进行到底
一、沉淀溶解平衡:
为什么?
AgCl溶解度:1.5×10-4g
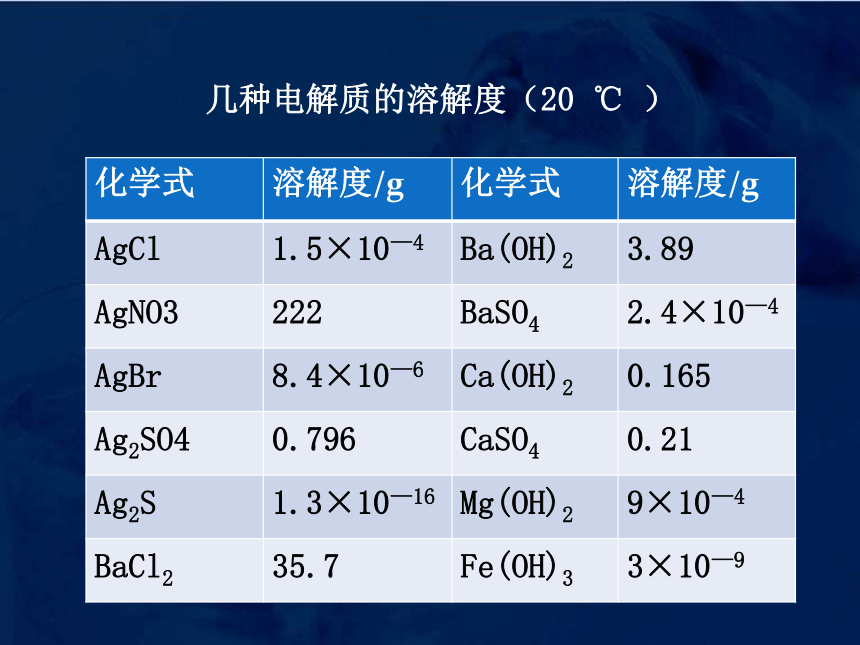
几种电解质的溶解度(20
℃
)
化学式
溶解度/g
化学式
溶解度/g
AgCl
1.5×10—4
Ba(OH)2
3.89
AgNO3
222
BaSO4
2.4×10—4
AgBr
8.4×10—6
Ca(OH)2
0.165
Ag2SO4
0.796
CaSO4
0.21
Ag2S
1.3×10—16
Mg(OH)2
9×10—4
BaCl2
35.7
Fe(OH)3
3×10—9
一、沉淀溶解平衡:
3、生成沉淀的离子反应能发生的原因:生成物的溶解度很小
总结:
1、溶与不溶是相对的,绝对不溶的物质是不存在的。
2、通常把溶解度<0.01g的电解质称为难溶电解质
(通常离子浓度<1×10—5mol/L认为沉淀完全)
思考与交流二:
影响难溶电解质溶解平衡的因素有哪些?
用下列已知药品和仪器设计实验验证
硝酸钾、氢氧化钙、氯化钠、碳酸钙、盐酸、蒸馏水、酒精灯
Ca(OH)2溶解度曲线
Cl-浓度增大,平衡逆向移动
CO32-+2H+=H2O+CO2
CO32-浓度减小,平衡正向移动
升高温度平衡正移
升高温度平衡逆移
思考与交流:
美丽的溶洞是如何形成的?
难看的龋齿又是如何形成的?
提示:牙齿的主要成分是Ca5(PO4)3OH
CaCO3(S)
Ca2+
(aq)
+
CO32-
(aq)
+CO2+H2O=HCO3-
+4H+=3HPO42-
+
H2O
1、若将0.001mol/L的NaCl溶液和0.001mol/L
AgNO3溶液等体积混合,是否会产生白色沉淀?
二、溶度积常数:
自主学习:请用平衡常数的相关知识完成下面的例题
解:混合后的溶液中:
QC=
C(Ag+).C(Cl-)=0.0005
mol/L×
0.0005mol/L
=2.5×10—7>1.8×10-10
沉淀溶解过程向左进行,因此会形成沉淀
二、溶度积常数:
溶度积规则
Qc=Ksp
饱和溶液
Qc>Ksp
产生沉淀
Qc<Ksp
未饱和溶液
对于类型相似的物质:Ksp越大,溶解度越大
物质
溶解度/g
溶度积
AgCl
1.5×10—5
1.8×10—10
AgBr
8.4×10—6
7.7×10—13
Ag2CrO4
1.4×10-3
9.0×10—12
Ag2SO4
0.796
1.4×10—5
二、溶度积常数:
总结:
1、影响溶度积的因素:温度
2、应用:
⑴溶度积规则
Qc=Ksp
饱和溶液
Qc>Ksp
过饱和溶液
Qc<Ksp
未饱和溶液
⑵对于组成相似的物质:Ksp越大,溶解度越大
课堂小结
难溶电解质
的溶解平衡
影响溶解
平衡的因素
溶度积
内因
溶度及规则
外因
谢谢大家!
第三章水溶液中的离子平衡
第四节---难溶电解质的溶解平衡
温习旧知
1、溶解度的定义?
2、什么是饱和溶液?
在一定温度下,某固态物质在100克溶剂
里达到饱和状态时所溶解的质量。
一定温度下,不能再溶解溶质的溶液叫饱和
溶液
一、沉淀溶解平衡:
小组讨论:
将氯化钾溶液和硝酸银溶液混合,会发生怎样的离子反应?
二者反应是否能沉淀完全离子浓度变为0吗?
你能设计实验加以证明吗?
实验探究1:
实验操作:2mL0.2mol/L硝酸银和3mL0.2mol/L氯化钾完全反应后静置,向上层清液中加入KI溶液观察现象
实验现象:有黄色沉淀生成
实验结论:
AgNO3和KCl混合后溶液中有Ag+,二者反应没有进行到底
一、沉淀溶解平衡:
为什么?
AgCl溶解度:1.5×10-4g
几种电解质的溶解度(20
℃
)
化学式
溶解度/g
化学式
溶解度/g
AgCl
1.5×10—4
Ba(OH)2
3.89
AgNO3
222
BaSO4
2.4×10—4
AgBr
8.4×10—6
Ca(OH)2
0.165
Ag2SO4
0.796
CaSO4
0.21
Ag2S
1.3×10—16
Mg(OH)2
9×10—4
BaCl2
35.7
Fe(OH)3
3×10—9
一、沉淀溶解平衡:
3、生成沉淀的离子反应能发生的原因:生成物的溶解度很小
总结:
1、溶与不溶是相对的,绝对不溶的物质是不存在的。
2、通常把溶解度<0.01g的电解质称为难溶电解质
(通常离子浓度<1×10—5mol/L认为沉淀完全)
思考与交流二:
影响难溶电解质溶解平衡的因素有哪些?
用下列已知药品和仪器设计实验验证
硝酸钾、氢氧化钙、氯化钠、碳酸钙、盐酸、蒸馏水、酒精灯
Ca(OH)2溶解度曲线
Cl-浓度增大,平衡逆向移动
CO32-+2H+=H2O+CO2
CO32-浓度减小,平衡正向移动
升高温度平衡正移
升高温度平衡逆移
思考与交流:
美丽的溶洞是如何形成的?
难看的龋齿又是如何形成的?
提示:牙齿的主要成分是Ca5(PO4)3OH
CaCO3(S)
Ca2+
(aq)
+
CO32-
(aq)
+CO2+H2O=HCO3-
+4H+=3HPO42-
+
H2O
1、若将0.001mol/L的NaCl溶液和0.001mol/L
AgNO3溶液等体积混合,是否会产生白色沉淀?
二、溶度积常数:
自主学习:请用平衡常数的相关知识完成下面的例题
解:混合后的溶液中:
QC=
C(Ag+).C(Cl-)=0.0005
mol/L×
0.0005mol/L
=2.5×10—7>1.8×10-10
沉淀溶解过程向左进行,因此会形成沉淀
二、溶度积常数:
溶度积规则
Qc=Ksp
饱和溶液
Qc>Ksp
产生沉淀
Qc<Ksp
未饱和溶液
对于类型相似的物质:Ksp越大,溶解度越大
物质
溶解度/g
溶度积
AgCl
1.5×10—5
1.8×10—10
AgBr
8.4×10—6
7.7×10—13
Ag2CrO4
1.4×10-3
9.0×10—12
Ag2SO4
0.796
1.4×10—5
二、溶度积常数:
总结:
1、影响溶度积的因素:温度
2、应用:
⑴溶度积规则
Qc=Ksp
饱和溶液
Qc>Ksp
过饱和溶液
Qc<Ksp
未饱和溶液
⑵对于组成相似的物质:Ksp越大,溶解度越大
课堂小结
难溶电解质
的溶解平衡
影响溶解
平衡的因素
溶度积
内因
溶度及规则
外因
谢谢大家!
