人教版五四学制九年级化学:第三单元 课题2 酸和碱的中和反应 (共22张PPT)
文档属性
| 名称 | 人教版五四学制九年级化学:第三单元 课题2 酸和碱的中和反应 (共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-09 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
课题2
酸和碱的中和反应
把无色的NaOH溶液和无色稀盐酸混合在一起,它们之间能否发生反应?
在一支试管中先后倒入少量NaOH溶液和稀盐酸,振荡后观察。
现象:
结论:
无现象。
(1)能反应
(2)不反应
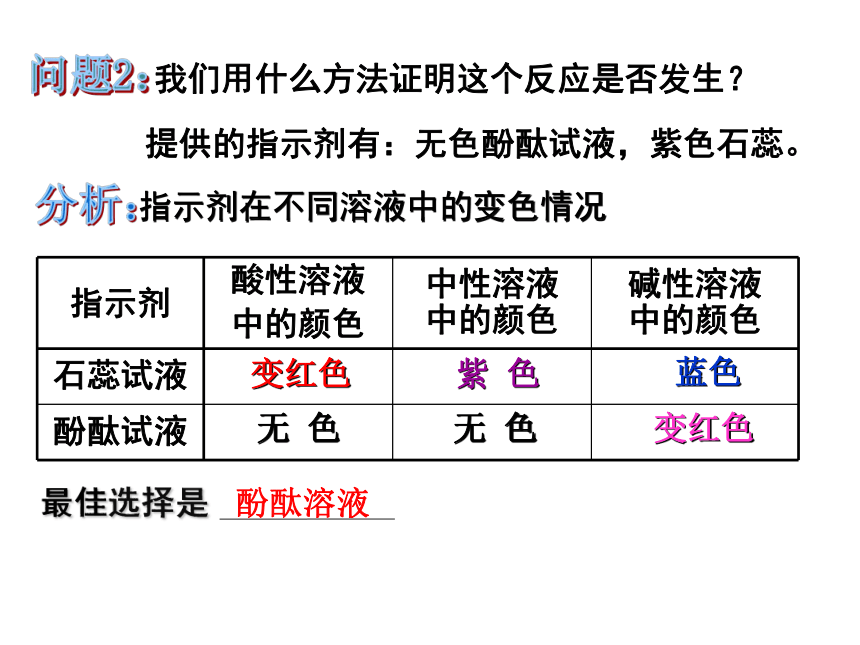
指示剂在不同溶液中的变色情况
无
色
无
色
变红色
蓝色
变红色
紫
色
我们用什么方法证明这个反应是否发生?
提供的指示剂有:无色酚酞试液,紫色石蕊。
酚酞溶液
指示剂
酸性溶液
中的颜色
中性溶液
中的颜色
碱性溶液
中的颜色
石蕊试液
酚酞试液
NaOH
溶液
酚酞试液
红色
逐滴加入稀盐酸
无色
稀HCl
无色
无色
酚酞试液
利用给出的药品讨论、设计实验方案
药品有:NaOH
溶液,稀HCl,无色酚酞溶液
(一)
(二)
哪种方案更好?你的选择是
(一)
红色
溶液由红色逐渐变为无色
玻璃棒上有白色固体生成
加入盐酸前溶
液呈
性,加入
盐酸后,溶液
呈
碱性(填是、不)。
碱
不
白色固体是氯化钠
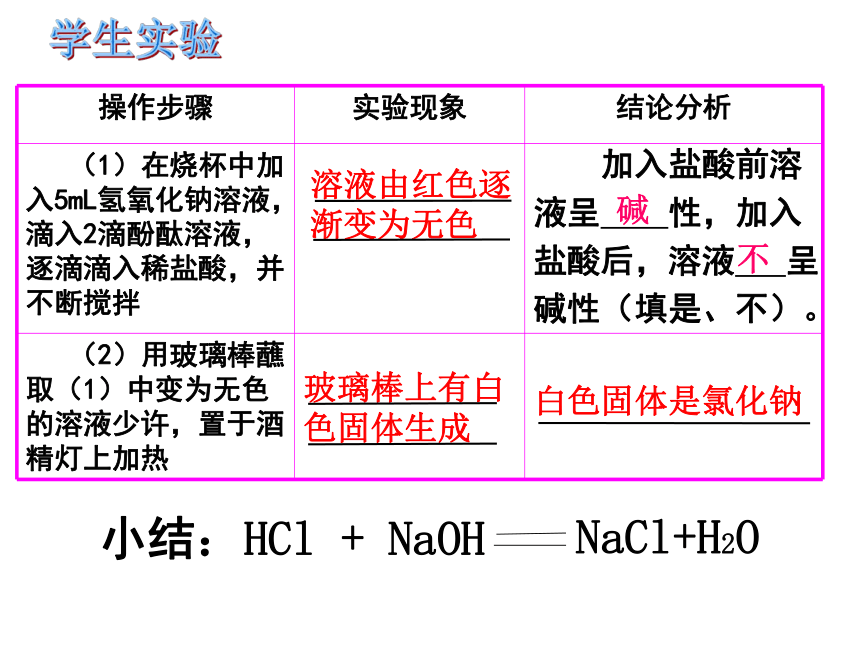
小结:HCl
+
NaOH
NaCl+H2O
操作步骤
实验现象
结论分析
(1)在烧杯中加入5mL氢氧化钠溶液,滴入2滴酚酞溶液,逐滴滴入稀盐酸,并不断搅拌
(2)用玻璃棒蘸取(1)中变为无色的溶液少许,置于酒精灯上加热
答:防止稀盐酸滴加过量。
答:起指示作用,根据酚酞溶液由红色变为无色来判断NaOH和HCl反应。
2.
为什么在操作中必须逐滴滴入稀盐酸?
1.
酚酞在实验中起什么作用?
HCl
+
NaOH
NaCl
HCl
+
Ca(OH)2
H2SO4+
NaOH
CaCl2+
2H2O
Na2SO4+
2H2O
2
2
+
H2O
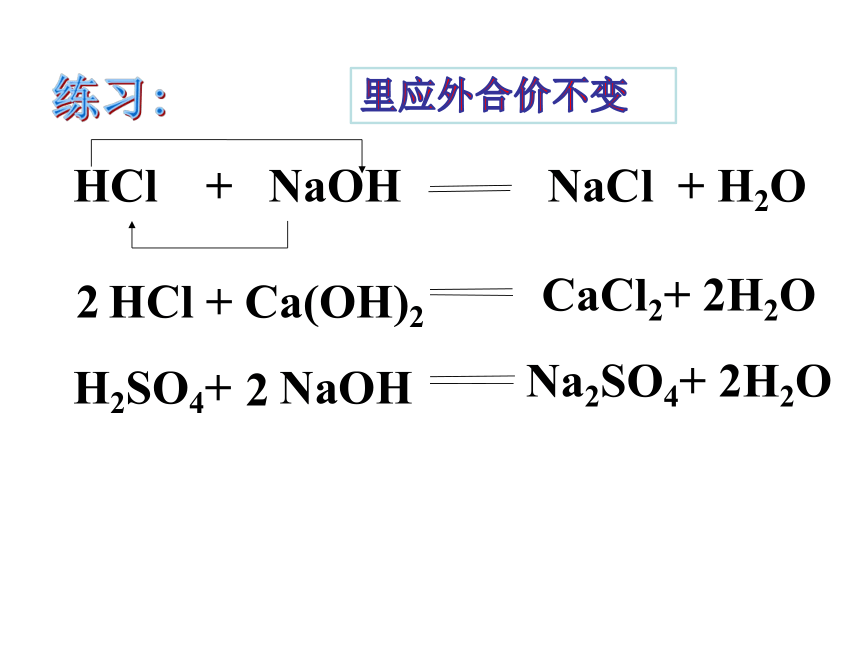
HCl
+
NaOH
=
NaCl
+
H2O
2HCl
+
Ca(OH)2
=
CaCl2
+
2H2O
H2SO4
+
2NaOH
=
Na2SO4
+
2H2O
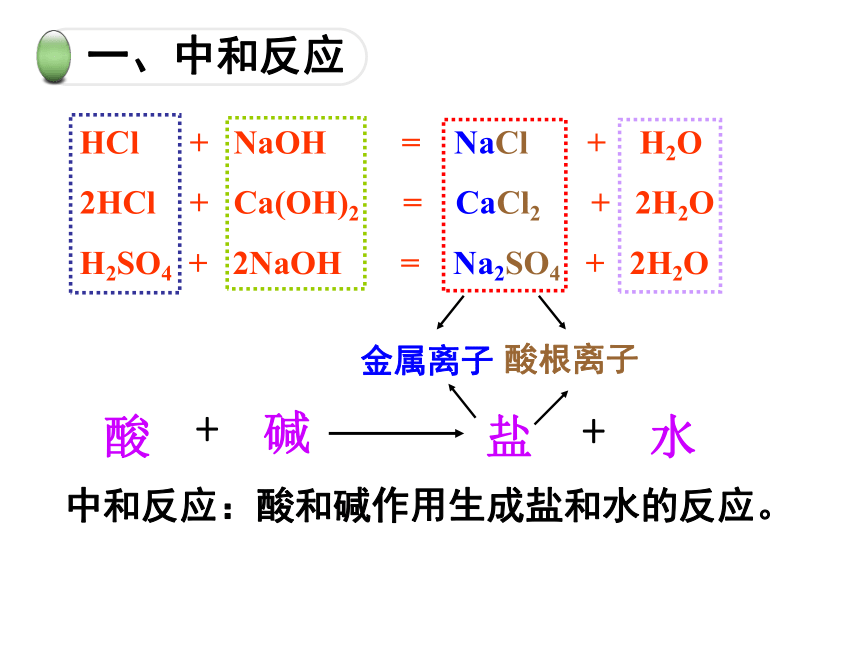
中和反应:酸和碱作用生成盐和水的反应。
一、中和反应
金属离子
酸根离子
酸
碱
水
盐
+
+
Fe2O3
+
3H2SO4
=
Fe2(SO4)3
+
3H2O
CO2
+
Ca(OH)2
=
CaCO3
↓
+
H2O
中和反应一定会生成盐和水,那么,
生成盐和水的反应一定是中和反应吗?
不一定
1.下列反应中属于中和反应的是(
)
A.Zn
+
2HCl
ZnCl2
+H2↑
B.CuO
+
2HCl
CuCl2+
H2O
C.Ba(OH)2+
H2SO4
BaSO4
↓+
2H2O
D.
AgNO3+HCl
AgCl↓
+HNO3
C
二.中和反应在实际中的应用
你能说出其中的原理吗?
问题(一)
问题(二):中和硫酸工厂废水
处理方法:
可用熟石灰进行中和处理,原理是:
。
问题(三):用于医药
试写出胃康—U治胃酸过多的原理。
此药中含有氢氧化铝
3HCl+Al(OH)3=AlCl3+3H2O
⑴
中和胃酸过多
⑵
中和蚁酸
思考:可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质,如:肥皂水等。
答:不可以,因为NaOH的碱性太强,具有强的腐蚀性。
问题(三):用于医药
你还能举出生活中利用中和反应
的实例吗?
四.调配食物
添加食醋(CH3COOH)
1.定义:酸和碱作用生成盐和水的反应。
课题2
酸和碱的中和反应
中和反应
例如
:HCl
+
NaOH
=
NaCl
+
H2O
2HCl
+
Ca(OH)2
=
CaCl2
+
2H2O
H2SO4
+
2NaOH
=
Na2SO4
+
2H2O
2.实质:H++OH-=H2O
3.在实际中的应用:
(1)农业上;(2)工业上;
(3)医疗上;(4)生活中。
课题2
酸和碱的中和反应
把无色的NaOH溶液和无色稀盐酸混合在一起,它们之间能否发生反应?
在一支试管中先后倒入少量NaOH溶液和稀盐酸,振荡后观察。
现象:
结论:
无现象。
(1)能反应
(2)不反应
指示剂在不同溶液中的变色情况
无
色
无
色
变红色
蓝色
变红色
紫
色
我们用什么方法证明这个反应是否发生?
提供的指示剂有:无色酚酞试液,紫色石蕊。
酚酞溶液
指示剂
酸性溶液
中的颜色
中性溶液
中的颜色
碱性溶液
中的颜色
石蕊试液
酚酞试液
NaOH
溶液
酚酞试液
红色
逐滴加入稀盐酸
无色
稀HCl
无色
无色
酚酞试液
利用给出的药品讨论、设计实验方案
药品有:NaOH
溶液,稀HCl,无色酚酞溶液
(一)
(二)
哪种方案更好?你的选择是
(一)
红色
溶液由红色逐渐变为无色
玻璃棒上有白色固体生成
加入盐酸前溶
液呈
性,加入
盐酸后,溶液
呈
碱性(填是、不)。
碱
不
白色固体是氯化钠
小结:HCl
+
NaOH
NaCl+H2O
操作步骤
实验现象
结论分析
(1)在烧杯中加入5mL氢氧化钠溶液,滴入2滴酚酞溶液,逐滴滴入稀盐酸,并不断搅拌
(2)用玻璃棒蘸取(1)中变为无色的溶液少许,置于酒精灯上加热
答:防止稀盐酸滴加过量。
答:起指示作用,根据酚酞溶液由红色变为无色来判断NaOH和HCl反应。
2.
为什么在操作中必须逐滴滴入稀盐酸?
1.
酚酞在实验中起什么作用?
HCl
+
NaOH
NaCl
HCl
+
Ca(OH)2
H2SO4+
NaOH
CaCl2+
2H2O
Na2SO4+
2H2O
2
2
+
H2O
HCl
+
NaOH
=
NaCl
+
H2O
2HCl
+
Ca(OH)2
=
CaCl2
+
2H2O
H2SO4
+
2NaOH
=
Na2SO4
+
2H2O
中和反应:酸和碱作用生成盐和水的反应。
一、中和反应
金属离子
酸根离子
酸
碱
水
盐
+
+
Fe2O3
+
3H2SO4
=
Fe2(SO4)3
+
3H2O
CO2
+
Ca(OH)2
=
CaCO3
↓
+
H2O
中和反应一定会生成盐和水,那么,
生成盐和水的反应一定是中和反应吗?
不一定
1.下列反应中属于中和反应的是(
)
A.Zn
+
2HCl
ZnCl2
+H2↑
B.CuO
+
2HCl
CuCl2+
H2O
C.Ba(OH)2+
H2SO4
BaSO4
↓+
2H2O
D.
AgNO3+HCl
AgCl↓
+HNO3
C
二.中和反应在实际中的应用
你能说出其中的原理吗?
问题(一)
问题(二):中和硫酸工厂废水
处理方法:
可用熟石灰进行中和处理,原理是:
。
问题(三):用于医药
试写出胃康—U治胃酸过多的原理。
此药中含有氢氧化铝
3HCl+Al(OH)3=AlCl3+3H2O
⑴
中和胃酸过多
⑵
中和蚁酸
思考:可不可以用NaOH来中和胃酸、蚁酸?为什么?
可涂抹一些含有碱性物质,如:肥皂水等。
答:不可以,因为NaOH的碱性太强,具有强的腐蚀性。
问题(三):用于医药
你还能举出生活中利用中和反应
的实例吗?
四.调配食物
添加食醋(CH3COOH)
1.定义:酸和碱作用生成盐和水的反应。
课题2
酸和碱的中和反应
中和反应
例如
:HCl
+
NaOH
=
NaCl
+
H2O
2HCl
+
Ca(OH)2
=
CaCl2
+
2H2O
H2SO4
+
2NaOH
=
Na2SO4
+
2H2O
2.实质:H++OH-=H2O
3.在实际中的应用:
(1)农业上;(2)工业上;
(3)医疗上;(4)生活中。
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
