人教版高中化学选修4第三章 第三节 盐类的水解(共22张PPT)
文档属性
| 名称 | 人教版高中化学选修4第三章 第三节 盐类的水解(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-13 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
第三章
水溶液中的离子平衡
第三节
盐类的水解
天堂之境:
玻利维亚
乌尤尼盐湖
食用纯碱(主要成分Na2CO3
)通常加在面团里用来去除酸味。我们会用它来制作面条、面包、蛋糕、馒头还有肉制品等色香味俱全的食品。它在食品中并不是起着调味的作用,它的作用是提高干货发胀速度,使产品疏松和嫩化。。
它明明是盐为何要称为“碱”?
你还记得溶液酸碱性的判断标准是什么吗?
【知识回顾】
那盐溶液呈什么性呢?
c(H+)
与c(OH-)的相对大小
怎么确定呢?
【演示实验】
Ⅰ:用PH计分别测定下列溶液的酸碱性。
(1)
NaCl、Na2SO4
、
(2)NH4Cl、
Al2(SO4)3
、MgCl2
、
(3)Na2CO3
、
CH3COONa、
一、探究盐溶液的酸碱性的规律
(1)
NaCl、Na2SO4
、
PH=7
呈中性
(2)NH4Cl、
Al2(SO4)3
PH<7
呈酸性
(3)Na2CO3
、
CH3COONa
PH>7
呈碱性
【实验结果】
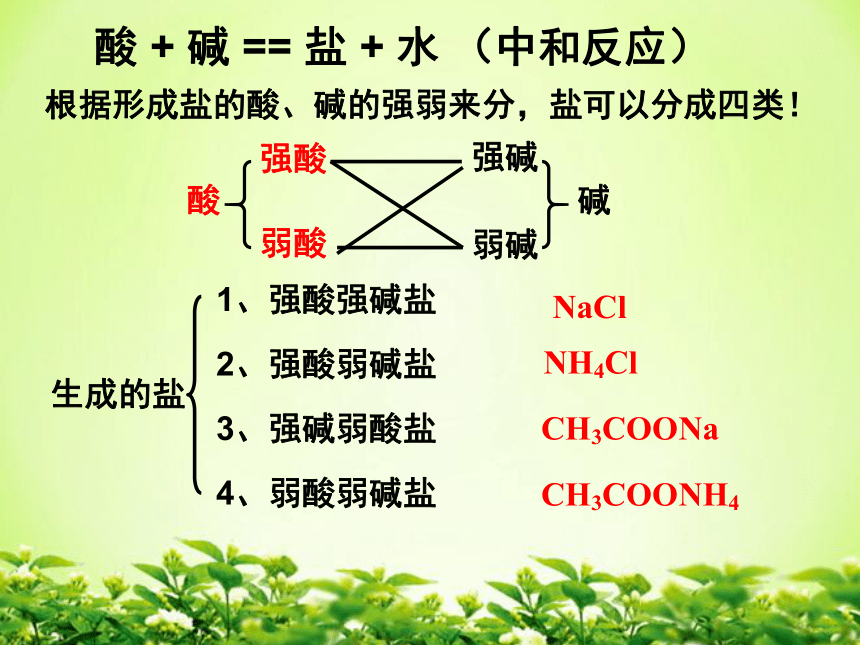
根据形成盐的酸、碱的强弱来分,盐可以分成四类!
酸
+
碱
==
盐
+
水
(中和反应)
酸
强酸
弱酸
弱碱
强碱
碱
生成的盐
1、强酸强碱盐
2、强酸弱碱盐
3、强碱弱酸盐
4、弱酸弱碱盐
NaCl
NH4Cl
CH3COONH4
CH3COONa
盐溶液
溶液的
酸碱性
生成该盐的酸和碱
盐的类型
酸
碱
NaCl
Na2SO4
NH4Cl
Al2(SO4)3
Na2CO3
CH3COONa
【练一练】
盐溶液
溶液的
酸碱性
生成该盐的酸和碱
盐的类型
酸
碱
NaCl
Na2SO4
NH4Cl
Al2(SO4)3
Na2CO3
CH3COONa
pH=7
中性
CH3COOH
NaOH
H2CO3
NaOH
HCl
NaOH
H2SO4
NaOH
HCl
NH3·H2O
H2SO4
Al(OH)3
强碱
弱酸盐
强酸
强碱盐
pH=7
中性
pH<7
酸性
pH<7
酸性
pH>7
碱性
pH>7
碱性
强酸
弱碱盐
你能不能根据表中数据找出盐溶液的酸碱性与生成该盐的酸碱的强弱,盐的类别的关系,并总结成规律?
盐溶液酸碱性的规律:
【结论1】
谁强显谁性,同强显中性!
即:强酸弱碱盐呈酸性
强碱弱酸盐呈碱性
强酸强碱盐呈中性
①NaClO
②CaCl2
③(NH4)2SO4
④CuSO4
⑤CH3COOK
⑥NaBr
以上溶液中,呈酸性的有
,
碱性的有
,中性的有
。
【活学活用】
③④
①⑤
②⑥
为什么不同的盐溶液会呈现不同酸碱性?
CH3COONa的水溶液显碱性的原因:
讨论:
(1)写出水电离的方程式?
(2)写出醋酸钠在水溶液中电离的方程式?
(3)CH3COONa溶液中存在着几种离子?
(4)溶液中哪些离子可以结合成弱电解质?
(5)生成弱电解质时对水的电离平衡有何影响?
二、盐溶液呈现不同酸碱性的原因
CH3COONa溶液显碱性!
CH3COONa
=
CH3COO-
+
Na+
H2O
H+
+
OH-
c(H+)
=c(OH-)
CH3COOH
c(H+)
<c(OH-)
化学方程式:CH3COONa
+
H2
O
CH3COOH+NaOH
离子方程式
:CH3COO-
+H2O
CH3COOH+OH-
探究原因
促进
关键
请同学们按照同样的方法分析
NH4Cl溶液为什么显酸性?
NaCl溶液为什么显中性?
小试牛刀
小试牛刀
思考与交流
通过上面的探究活动,我们发现有的盐不影响水的电离平衡;有的盐能和水中的离子反应促进了水的电离平衡,我们把这叫做盐类的水解。
归纳整理
盐类的水解概念:在水溶液中盐电离出来的弱阳离子或弱阴离子与水电离出来的OH-或H+
结合生成弱电解质的反应,叫做盐类的水解。
归纳整理
条件
实质
概念理解
盐类水解的条件:
盐易溶,有弱离子
盐类水解的实质:
促进了水的电离平衡
使c(H+)
≠
c(OH-)
水解反应与中和反应的关系:
酸+碱
盐+水
中和
水解
盐类水解规律:
有弱才水解;
无弱不水解;
谁弱谁水解;
谁强显谁性;
同强显中性;
记住啦!
1.在溶液中,不能发生水解的离子是( )
A、ClO
-
B、CO32-
C、Fe3+
D、SO42--
D
配套练习
2.?
氯化铵溶液中离子浓度从大到小排列正确的是(
)
A
NH4+
、H
+
、OH-、Cl_
B
Cl
_
、
NH4+
、H
+
、OH
_
C
H
+、
Cl_
、
NH4+
、OH
_
D
Cl-、
NH4+
、
OH-
、H
+
B
课堂小结
一、探究盐溶液的酸碱性
二、盐溶液呈现不同酸碱性的原因
三、盐类的水解
1、盐类水解的定义
2、盐类水解的条件
3、盐类水解的实质
4、盐类水解的规律
作
业
课本:第
59
页
1,4,7
课后思考:
1.Na2CO3溶液的水解情况如何?怎样写水解的离子方程式?
2.请同学们根据所学知识并查阅资料,分析泡沫灭火器的原理。
谢谢光临!
请多指导!
第三章
水溶液中的离子平衡
第三节
盐类的水解
天堂之境:
玻利维亚
乌尤尼盐湖
食用纯碱(主要成分Na2CO3
)通常加在面团里用来去除酸味。我们会用它来制作面条、面包、蛋糕、馒头还有肉制品等色香味俱全的食品。它在食品中并不是起着调味的作用,它的作用是提高干货发胀速度,使产品疏松和嫩化。。
它明明是盐为何要称为“碱”?
你还记得溶液酸碱性的判断标准是什么吗?
【知识回顾】
那盐溶液呈什么性呢?
c(H+)
与c(OH-)的相对大小
怎么确定呢?
【演示实验】
Ⅰ:用PH计分别测定下列溶液的酸碱性。
(1)
NaCl、Na2SO4
、
(2)NH4Cl、
Al2(SO4)3
、MgCl2
、
(3)Na2CO3
、
CH3COONa、
一、探究盐溶液的酸碱性的规律
(1)
NaCl、Na2SO4
、
PH=7
呈中性
(2)NH4Cl、
Al2(SO4)3
PH<7
呈酸性
(3)Na2CO3
、
CH3COONa
PH>7
呈碱性
【实验结果】
根据形成盐的酸、碱的强弱来分,盐可以分成四类!
酸
+
碱
==
盐
+
水
(中和反应)
酸
强酸
弱酸
弱碱
强碱
碱
生成的盐
1、强酸强碱盐
2、强酸弱碱盐
3、强碱弱酸盐
4、弱酸弱碱盐
NaCl
NH4Cl
CH3COONH4
CH3COONa
盐溶液
溶液的
酸碱性
生成该盐的酸和碱
盐的类型
酸
碱
NaCl
Na2SO4
NH4Cl
Al2(SO4)3
Na2CO3
CH3COONa
【练一练】
盐溶液
溶液的
酸碱性
生成该盐的酸和碱
盐的类型
酸
碱
NaCl
Na2SO4
NH4Cl
Al2(SO4)3
Na2CO3
CH3COONa
pH=7
中性
CH3COOH
NaOH
H2CO3
NaOH
HCl
NaOH
H2SO4
NaOH
HCl
NH3·H2O
H2SO4
Al(OH)3
强碱
弱酸盐
强酸
强碱盐
pH=7
中性
pH<7
酸性
pH<7
酸性
pH>7
碱性
pH>7
碱性
强酸
弱碱盐
你能不能根据表中数据找出盐溶液的酸碱性与生成该盐的酸碱的强弱,盐的类别的关系,并总结成规律?
盐溶液酸碱性的规律:
【结论1】
谁强显谁性,同强显中性!
即:强酸弱碱盐呈酸性
强碱弱酸盐呈碱性
强酸强碱盐呈中性
①NaClO
②CaCl2
③(NH4)2SO4
④CuSO4
⑤CH3COOK
⑥NaBr
以上溶液中,呈酸性的有
,
碱性的有
,中性的有
。
【活学活用】
③④
①⑤
②⑥
为什么不同的盐溶液会呈现不同酸碱性?
CH3COONa的水溶液显碱性的原因:
讨论:
(1)写出水电离的方程式?
(2)写出醋酸钠在水溶液中电离的方程式?
(3)CH3COONa溶液中存在着几种离子?
(4)溶液中哪些离子可以结合成弱电解质?
(5)生成弱电解质时对水的电离平衡有何影响?
二、盐溶液呈现不同酸碱性的原因
CH3COONa溶液显碱性!
CH3COONa
=
CH3COO-
+
Na+
H2O
H+
+
OH-
c(H+)
=c(OH-)
CH3COOH
c(H+)
<c(OH-)
化学方程式:CH3COONa
+
H2
O
CH3COOH+NaOH
离子方程式
:CH3COO-
+H2O
CH3COOH+OH-
探究原因
促进
关键
请同学们按照同样的方法分析
NH4Cl溶液为什么显酸性?
NaCl溶液为什么显中性?
小试牛刀
小试牛刀
思考与交流
通过上面的探究活动,我们发现有的盐不影响水的电离平衡;有的盐能和水中的离子反应促进了水的电离平衡,我们把这叫做盐类的水解。
归纳整理
盐类的水解概念:在水溶液中盐电离出来的弱阳离子或弱阴离子与水电离出来的OH-或H+
结合生成弱电解质的反应,叫做盐类的水解。
归纳整理
条件
实质
概念理解
盐类水解的条件:
盐易溶,有弱离子
盐类水解的实质:
促进了水的电离平衡
使c(H+)
≠
c(OH-)
水解反应与中和反应的关系:
酸+碱
盐+水
中和
水解
盐类水解规律:
有弱才水解;
无弱不水解;
谁弱谁水解;
谁强显谁性;
同强显中性;
记住啦!
1.在溶液中,不能发生水解的离子是( )
A、ClO
-
B、CO32-
C、Fe3+
D、SO42--
D
配套练习
2.?
氯化铵溶液中离子浓度从大到小排列正确的是(
)
A
NH4+
、H
+
、OH-、Cl_
B
Cl
_
、
NH4+
、H
+
、OH
_
C
H
+、
Cl_
、
NH4+
、OH
_
D
Cl-、
NH4+
、
OH-
、H
+
B
课堂小结
一、探究盐溶液的酸碱性
二、盐溶液呈现不同酸碱性的原因
三、盐类的水解
1、盐类水解的定义
2、盐类水解的条件
3、盐类水解的实质
4、盐类水解的规律
作
业
课本:第
59
页
1,4,7
课后思考:
1.Na2CO3溶液的水解情况如何?怎样写水解的离子方程式?
2.请同学们根据所学知识并查阅资料,分析泡沫灭火器的原理。
谢谢光临!
请多指导!
