第04节 原子的能级结构 :35张PPT
文档属性
| 名称 | 第04节 原子的能级结构 :35张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 361.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-06-13 00:00:00 | ||
图片预览







文档简介
(共35张PPT)
18.4
原子的能级结构
新课标高中物理选修3-5
第十八章
原子结构
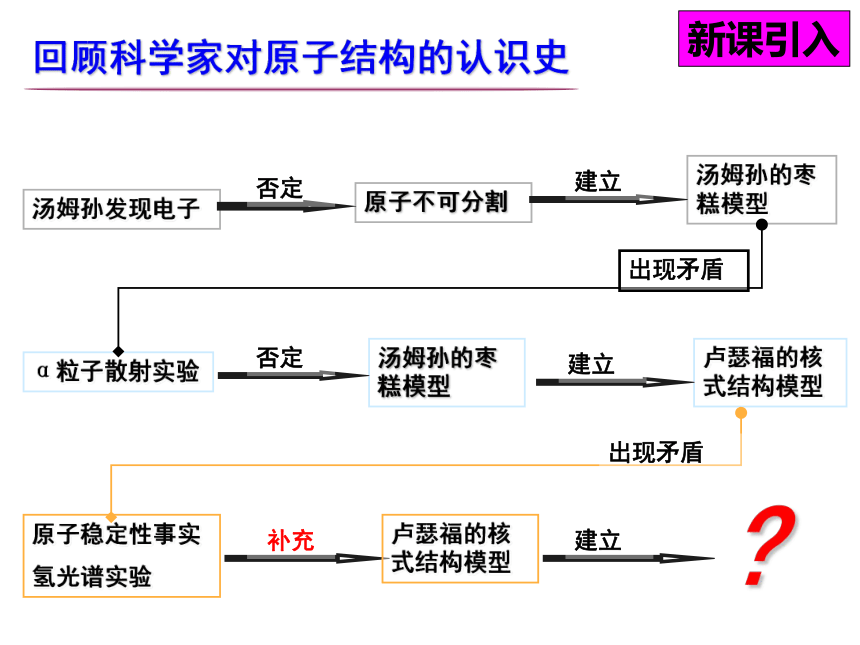
汤姆孙发现电子
汤姆孙的枣糕模型
α粒子散射实验
卢瑟福的核式结构模型
回顾科学家对原子结构的认识史
原子不可分割
汤姆孙的枣糕模型
原子稳定性事实
氢光谱实验
卢瑟福的核式结构模型
?
新课引入
三个模块
一、玻尔原子理论基本假设
二、玻尔理论对氢光谱的解释
三、玻尔模型的局限性
玻尔的原子模型
阅读课本并思考
1、什么是能级、定态、基态、激发态?
2、玻尔原子理论有几个假设?轨道半径公式如何?能级公式如何?
3、何为跃迁?跃迁有什么规律特点?
一、玻尔原子理论基本假设
新课教学
一、玻尔原子理论基本假设
1、玻尔原子模型:
(1)原子中的电子在
引力的作用下,绕
做圆周运动;
(2)电子绕核运动的轨道是
的;
(3)电子在这些轨道上绕核的转动是
的,不产生
。
库仑
原子核
稳定
电磁辐射
量子化
(4)当电子在不同轨道上运动时,原子处于不同的状态中,具有不同的能量,即原子的能量是
的,这些量子化的能量值叫做
,原子中这些具有确定能量的稳定状态,称为
。能量最低的状态叫做
,其他的能量状态叫做
。
量子化
能级
定态
基态
激发态
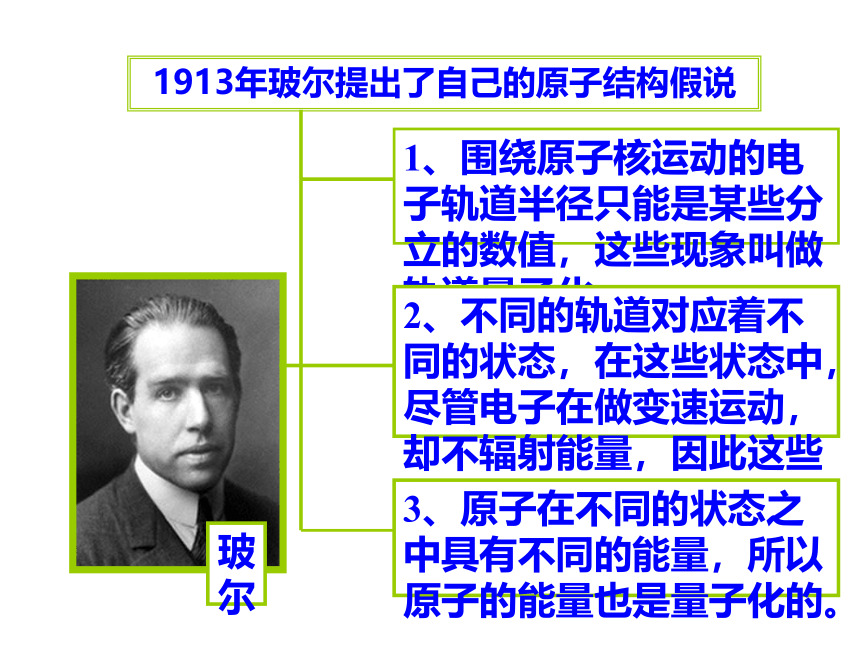
1、围绕原子核运动的电子轨道半径只能是某些分立的数值,这些现象叫做轨道量子化;
2、不同的轨道对应着不同的状态,在这些状态中,尽管电子在做变速运动,却不辐射能量,因此这些状态是稳定的;
3、原子在不同的状态之中具有不同的能量,所以原子的能量也是量子化的。
1913年玻尔提出了自己的原子结构假说
玻尔
2、玻尔理论的三个假设
轨道假设
电子不能在任意半径的轨道上运行,而只能在某些轨道上运行,即电子的可能轨道是不连续的。
能级假设
原子只能处于一系列不连续的能量状态中,这些状态叫定态。处于稳定状态的电子,虽做变速运动但不辐射能量。
跃迁假设
原子从一个定态跃迁到另一个定态时,它辐射或吸收一定频率的光子,光子的能量由这个定态的能量差决定。
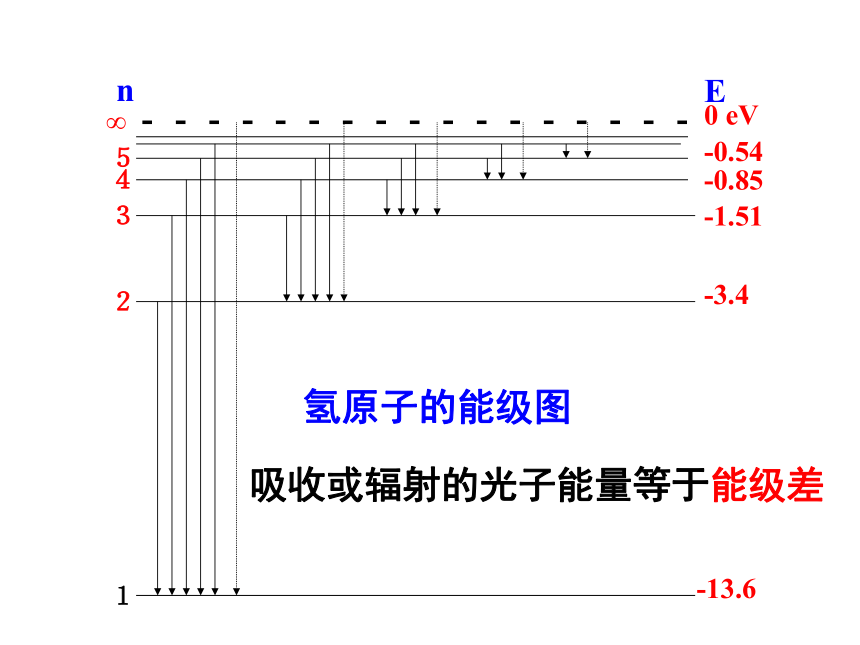
氢原子的能级图
-----------------
1
2
3
4
5
-13.6
-3.4
-1.51
-0.85
-0.54
0
eV
n
E
∞
吸收或辐射的光子能量等于能级差
n=6
n=5
n=4
n=1
n=3
n=2
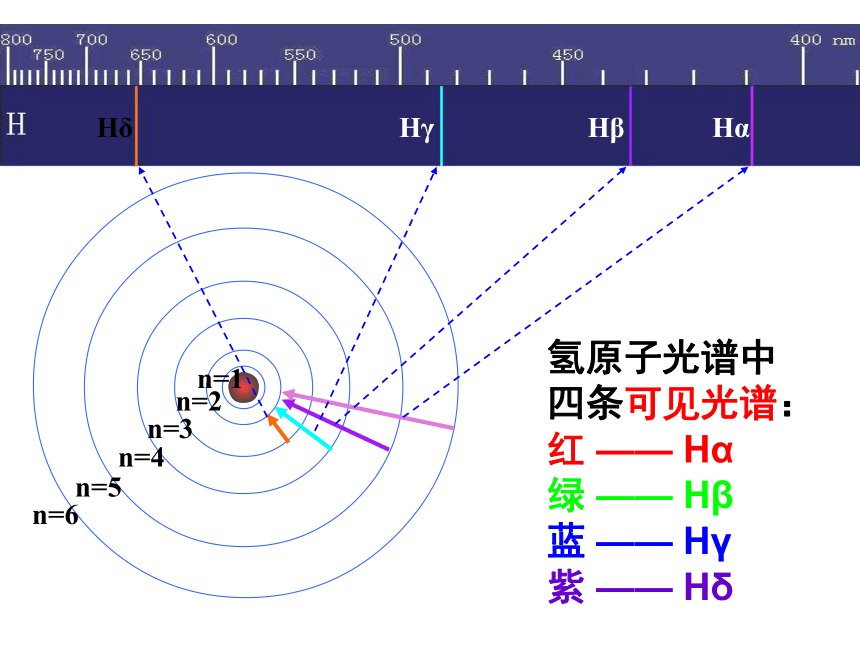
Hδ
Hγ
Hβ
Hα
氢原子光谱中
四条可见光谱:
红
——
Hα
绿
——
Hβ
蓝
——
Hγ
紫
——
Hδ
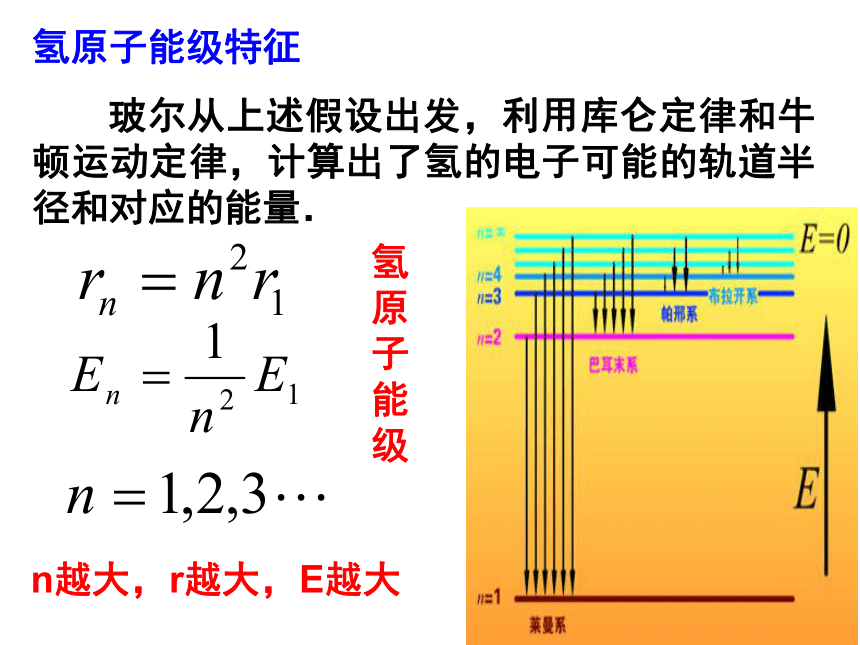
氢原子能级特征
玻尔从上述假设出发,利用库仑定律和牛顿运动定律,计算出了氢的电子可能的轨道半径和对应的能量.
氢原子能级
n越大,r越大,E越大
1、(单)根据玻尔理论,氢原子中,量子数n越大,则下列说法中不正确的是(
)
A、电子轨道半径越大
B、核外电子的速率越大
C、氢原子能级的能量越大
D、核外电子的电势能越大
B
3、跃迁:原子由一个能量态变为另一个能量态的过程。
当电子从能量较高的定态轨道(其能量记为Em)跃迁到能量较低的定态轨道(其能量记为En,m>n)时,会放出能量为hυ的光子,该光子的能量hυ
=
,该式被称为频率条件,又称为辐射条件。光子能量由前后两个能级的
决定。
反之,电子吸收光子时会从较低的能量态跃迁到较高的能量态。
Em
-En
能级差
电子从一个轨道到另一个轨道,不是以螺旋线的形式改变半径大小的,而是从一个轨道上“跳跃”到另一个轨道上.
2、(双)氢原子的核外电子由离原子核较远的轨道跃迁到离核较近的轨道上时,下列说法中正确的是(
)
A.核外电子受力变小
B.原子的能量减少
C.氢原子要吸收一定频率的光子
D.氢原子要放出一定频率的光子
BD
于是,可以近似认为原子核是固定不动的,原子的能量就可以认为是电子的动能与电子和核的电势能之和,即(取无限远出的电势能为0)基态能量E1=-13.6eV.
氢原子的能级图中的能量为什么是负值?
3.(单)用能量为12.6
eV的光子去照射一群处于基态的氢原子,受光子的照射后,下列关于这群氢原子的跃迁的说法正确的是(
)
A.原子能跃迁到n=2的激发态上
B.原子能跃迁到n=3的激发态上
C.原子能跃迁到n=4的激发态上
D.原子不能跃迁
D
4.(单)如图为玻尔理论中氢原子最低的四个能级.处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光中,波长最长的是(
)
A.n=4
跃迁到
n=1
时辐射的光子
B.n=4
跃迁到
n=3
时辐射的光子
C.n=2
跃迁到
n=1
时辐射的光子
D.n=3
跃迁到
n=2
时辐射的光子
B
[分析]氢原子能级跃迁的可能情况
氢原子核外电子从高能级向低能级跃迁时可能直接跃迁到基态,也可能先跃迁到其他低能级的激发态,然后再到基态,因此处于n能级的电子向低能级跃迁时就有很多可能性,其可能的值为
种可能情况.
巴耳末公式中有正整数n出现,这里也用正整数n(或m)来表示氢原子的能级,它们之间是否有某种联系?
二、玻尔理论对氢光谱的解释
1、巴耳末公式
2、气体导电时发光的机理
3、氢原子光谱的不连续性
4、不同的原子具有不同的特征谱线
一、玻尔原子理论基本假设
1、玻尔原子模型
①库仑力充当向心力
②轨道量子化
③能级
定态
基态
激发态
2、玻尔理论的三个假设
①
能量量子化
②频率条件
③轨道公式、能量公式
④能量的定义
3、跃迁
①定义
②跃迁规律:特定频率
③跃迁特点:跳跃
二、玻尔理论对氢光谱的解释
1、巴耳末公式
2、气体导电时发光的机理
3、氢原子光谱的不连续性
4、不同的原子具有不同的特征谱线
小结
作业:
课本P63第1至第4小题
二、玻尔理论对氢光谱的解释(4个)
1、解释巴耳末公式
按照玻尔理论,从高能级跃迁到低能级辐射的光子的能量为hυ
=Em
-En
;巴耳末公式中的正整数n和2正好代表能级跃迁之前和之后所处的
的量子数n和2,因此,巴耳末公式代表的是电子从量子数分别为n=3,4,5,6……的能级
向
量子数为2的能级跃迁时发出的光谱线。
定态轨道
①理论上的计算和实验测量的
符合得很好;
②玻尔理论也很好地解释甚至预言了氢原子的其他谱线系。
玻尔理论对巴耳末公式解释的合理性
里德伯常量
氢原子光谱的其他线系
莱曼系
红外区还有三个线系
帕邢系
布喇开系
普丰特系
紫外线区
通常情况下,原子处于基态,基态是最稳定的。气体放电管中的原子受到高速运动的电子的撞击,有可能向上跃迁到激发态。处于激发态的原子是不稳定的,会自发地向能量较低的能级跃迁,放出光子,最终回到基态。这是气态导电时发光的机理。
2、解释气体导电时发光的机理
3、解释氢原子光谱的不连续性
原子从较高能级向低能级跃迁时放出光子的能量等于前后
,由于原子的能级是
的,所以放出的光子的能量也是
的,因此原子的发射光谱只有一些分立的亮线。
能级之差
分立
分立
由于不同的原子具有不同的结构,能级各不相同,因此辐射(或吸收)的光子频率也不相同。这就是不同元素的原子具有不同的特征谱线的原因。
4、解释不同的原子具有不同的特征谱线
5.(单)根据玻尔理论,下列关于氢原子的论述正确的是(
)
A.若氢原子由能量为En的定态向低能级跃迁,则氢原子要辐射的光子能量为hν=En
B.电子沿某一轨道绕核运动,若圆周运动的频率为ν,则其发光的频率也是ν
C.一个氢原子中的电子从一个半径为ra的轨道自发地直接跃迁到另一半径为rb的轨道,已知ra>rb,则此过程原子要辐射某一频率的光子
D.氢原子吸收光子后,将从高能级向低能级跃迁
C
1、根据巴尔末公式,
时计算出的氢原子光谱的谱线是量子数为5的能及跃迁到量子数为2的能级形成的。
2、根据波尔理论,原子处于一系列不连续的能量状态中,原子从较高能级E2跃迁到较低能级E1时辐射的光子能量满足
。由于原子能级是分立的,能级差也是分立的,辐射的光子的能量也是分立的,有确定的频率,所以原子光谱只有一些分立的亮线。
3、大量原子处在n=3的能级上,能辐射3种频率的光。波长最短的光是从n=3的能级跃迁到n=1的能级时发出的光。
4、各种波长的复色光通过物质时,原子吸收了跟它的原子谱线波长相同的那些光子,使连续的复色光谱背景上出现了暗线。由于原子只能吸收能量大小满足两个能级之差
的光子,从低能态E1跃迁高能态E2,在复色光谱中形成一条暗线,这条暗线刚好E2与跃迁E1到发出的光子的明线相对应。因此,各种原子吸收光谱中的每一条暗线都跟该原子发射光谱中的一条亮线对应。
原子能量量子化的另一证据:原子吸收电子能量的分立性
18.4
原子的能级结构
新课标高中物理选修3-5
第十八章
原子结构
汤姆孙发现电子
汤姆孙的枣糕模型
α粒子散射实验
卢瑟福的核式结构模型
回顾科学家对原子结构的认识史
原子不可分割
汤姆孙的枣糕模型
原子稳定性事实
氢光谱实验
卢瑟福的核式结构模型
?
新课引入
三个模块
一、玻尔原子理论基本假设
二、玻尔理论对氢光谱的解释
三、玻尔模型的局限性
玻尔的原子模型
阅读课本并思考
1、什么是能级、定态、基态、激发态?
2、玻尔原子理论有几个假设?轨道半径公式如何?能级公式如何?
3、何为跃迁?跃迁有什么规律特点?
一、玻尔原子理论基本假设
新课教学
一、玻尔原子理论基本假设
1、玻尔原子模型:
(1)原子中的电子在
引力的作用下,绕
做圆周运动;
(2)电子绕核运动的轨道是
的;
(3)电子在这些轨道上绕核的转动是
的,不产生
。
库仑
原子核
稳定
电磁辐射
量子化
(4)当电子在不同轨道上运动时,原子处于不同的状态中,具有不同的能量,即原子的能量是
的,这些量子化的能量值叫做
,原子中这些具有确定能量的稳定状态,称为
。能量最低的状态叫做
,其他的能量状态叫做
。
量子化
能级
定态
基态
激发态
1、围绕原子核运动的电子轨道半径只能是某些分立的数值,这些现象叫做轨道量子化;
2、不同的轨道对应着不同的状态,在这些状态中,尽管电子在做变速运动,却不辐射能量,因此这些状态是稳定的;
3、原子在不同的状态之中具有不同的能量,所以原子的能量也是量子化的。
1913年玻尔提出了自己的原子结构假说
玻尔
2、玻尔理论的三个假设
轨道假设
电子不能在任意半径的轨道上运行,而只能在某些轨道上运行,即电子的可能轨道是不连续的。
能级假设
原子只能处于一系列不连续的能量状态中,这些状态叫定态。处于稳定状态的电子,虽做变速运动但不辐射能量。
跃迁假设
原子从一个定态跃迁到另一个定态时,它辐射或吸收一定频率的光子,光子的能量由这个定态的能量差决定。
氢原子的能级图
-----------------
1
2
3
4
5
-13.6
-3.4
-1.51
-0.85
-0.54
0
eV
n
E
∞
吸收或辐射的光子能量等于能级差
n=6
n=5
n=4
n=1
n=3
n=2
Hδ
Hγ
Hβ
Hα
氢原子光谱中
四条可见光谱:
红
——
Hα
绿
——
Hβ
蓝
——
Hγ
紫
——
Hδ
氢原子能级特征
玻尔从上述假设出发,利用库仑定律和牛顿运动定律,计算出了氢的电子可能的轨道半径和对应的能量.
氢原子能级
n越大,r越大,E越大
1、(单)根据玻尔理论,氢原子中,量子数n越大,则下列说法中不正确的是(
)
A、电子轨道半径越大
B、核外电子的速率越大
C、氢原子能级的能量越大
D、核外电子的电势能越大
B
3、跃迁:原子由一个能量态变为另一个能量态的过程。
当电子从能量较高的定态轨道(其能量记为Em)跃迁到能量较低的定态轨道(其能量记为En,m>n)时,会放出能量为hυ的光子,该光子的能量hυ
=
,该式被称为频率条件,又称为辐射条件。光子能量由前后两个能级的
决定。
反之,电子吸收光子时会从较低的能量态跃迁到较高的能量态。
Em
-En
能级差
电子从一个轨道到另一个轨道,不是以螺旋线的形式改变半径大小的,而是从一个轨道上“跳跃”到另一个轨道上.
2、(双)氢原子的核外电子由离原子核较远的轨道跃迁到离核较近的轨道上时,下列说法中正确的是(
)
A.核外电子受力变小
B.原子的能量减少
C.氢原子要吸收一定频率的光子
D.氢原子要放出一定频率的光子
BD
于是,可以近似认为原子核是固定不动的,原子的能量就可以认为是电子的动能与电子和核的电势能之和,即(取无限远出的电势能为0)基态能量E1=-13.6eV.
氢原子的能级图中的能量为什么是负值?
3.(单)用能量为12.6
eV的光子去照射一群处于基态的氢原子,受光子的照射后,下列关于这群氢原子的跃迁的说法正确的是(
)
A.原子能跃迁到n=2的激发态上
B.原子能跃迁到n=3的激发态上
C.原子能跃迁到n=4的激发态上
D.原子不能跃迁
D
4.(单)如图为玻尔理论中氢原子最低的四个能级.处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光中,波长最长的是(
)
A.n=4
跃迁到
n=1
时辐射的光子
B.n=4
跃迁到
n=3
时辐射的光子
C.n=2
跃迁到
n=1
时辐射的光子
D.n=3
跃迁到
n=2
时辐射的光子
B
[分析]氢原子能级跃迁的可能情况
氢原子核外电子从高能级向低能级跃迁时可能直接跃迁到基态,也可能先跃迁到其他低能级的激发态,然后再到基态,因此处于n能级的电子向低能级跃迁时就有很多可能性,其可能的值为
种可能情况.
巴耳末公式中有正整数n出现,这里也用正整数n(或m)来表示氢原子的能级,它们之间是否有某种联系?
二、玻尔理论对氢光谱的解释
1、巴耳末公式
2、气体导电时发光的机理
3、氢原子光谱的不连续性
4、不同的原子具有不同的特征谱线
一、玻尔原子理论基本假设
1、玻尔原子模型
①库仑力充当向心力
②轨道量子化
③能级
定态
基态
激发态
2、玻尔理论的三个假设
①
能量量子化
②频率条件
③轨道公式、能量公式
④能量的定义
3、跃迁
①定义
②跃迁规律:特定频率
③跃迁特点:跳跃
二、玻尔理论对氢光谱的解释
1、巴耳末公式
2、气体导电时发光的机理
3、氢原子光谱的不连续性
4、不同的原子具有不同的特征谱线
小结
作业:
课本P63第1至第4小题
二、玻尔理论对氢光谱的解释(4个)
1、解释巴耳末公式
按照玻尔理论,从高能级跃迁到低能级辐射的光子的能量为hυ
=Em
-En
;巴耳末公式中的正整数n和2正好代表能级跃迁之前和之后所处的
的量子数n和2,因此,巴耳末公式代表的是电子从量子数分别为n=3,4,5,6……的能级
向
量子数为2的能级跃迁时发出的光谱线。
定态轨道
①理论上的计算和实验测量的
符合得很好;
②玻尔理论也很好地解释甚至预言了氢原子的其他谱线系。
玻尔理论对巴耳末公式解释的合理性
里德伯常量
氢原子光谱的其他线系
莱曼系
红外区还有三个线系
帕邢系
布喇开系
普丰特系
紫外线区
通常情况下,原子处于基态,基态是最稳定的。气体放电管中的原子受到高速运动的电子的撞击,有可能向上跃迁到激发态。处于激发态的原子是不稳定的,会自发地向能量较低的能级跃迁,放出光子,最终回到基态。这是气态导电时发光的机理。
2、解释气体导电时发光的机理
3、解释氢原子光谱的不连续性
原子从较高能级向低能级跃迁时放出光子的能量等于前后
,由于原子的能级是
的,所以放出的光子的能量也是
的,因此原子的发射光谱只有一些分立的亮线。
能级之差
分立
分立
由于不同的原子具有不同的结构,能级各不相同,因此辐射(或吸收)的光子频率也不相同。这就是不同元素的原子具有不同的特征谱线的原因。
4、解释不同的原子具有不同的特征谱线
5.(单)根据玻尔理论,下列关于氢原子的论述正确的是(
)
A.若氢原子由能量为En的定态向低能级跃迁,则氢原子要辐射的光子能量为hν=En
B.电子沿某一轨道绕核运动,若圆周运动的频率为ν,则其发光的频率也是ν
C.一个氢原子中的电子从一个半径为ra的轨道自发地直接跃迁到另一半径为rb的轨道,已知ra>rb,则此过程原子要辐射某一频率的光子
D.氢原子吸收光子后,将从高能级向低能级跃迁
C
1、根据巴尔末公式,
时计算出的氢原子光谱的谱线是量子数为5的能及跃迁到量子数为2的能级形成的。
2、根据波尔理论,原子处于一系列不连续的能量状态中,原子从较高能级E2跃迁到较低能级E1时辐射的光子能量满足
。由于原子能级是分立的,能级差也是分立的,辐射的光子的能量也是分立的,有确定的频率,所以原子光谱只有一些分立的亮线。
3、大量原子处在n=3的能级上,能辐射3种频率的光。波长最短的光是从n=3的能级跃迁到n=1的能级时发出的光。
4、各种波长的复色光通过物质时,原子吸收了跟它的原子谱线波长相同的那些光子,使连续的复色光谱背景上出现了暗线。由于原子只能吸收能量大小满足两个能级之差
的光子,从低能态E1跃迁高能态E2,在复色光谱中形成一条暗线,这条暗线刚好E2与跃迁E1到发出的光子的明线相对应。因此,各种原子吸收光谱中的每一条暗线都跟该原子发射光谱中的一条亮线对应。
原子能量量子化的另一证据:原子吸收电子能量的分立性
同课章节目录
