第02节 热力学第一定律 :20张PPT
文档属性
| 名称 | 第02节 热力学第一定律 :20张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 184.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-06-14 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
日寒暑温凉之变
如瓦石之类
置之火则热
置之水则寒
特因外物有去有来
吹之即凉
呵之即温
——尹喜《关尹子》
热身实验:想办法使铁丝变热
复习回顾
绝热状态下,单纯对物体做功可改变物体内能。
W=ΔU
单纯向物体传热也可改变物体内能。
Q=ΔU
如果既对物体做功,又向物体传热,内能增加量如何表示??
热力学第一定律
一、文字描述:一个热力学系统,内能增加量等于外界对它传递的热量与外界对它做的功之和。
二、描述的是内能增加量,热量,功的定量关系。
三、表达式:
ΔU=Q+W
焦耳实验再思考:
明确研究的“系统”是什么?“外界”是什么?
以水为系统:内能改变靠热传递
以电热丝为系统:电流做功,
同时对水传热
明确各个量的意义:ΔU=Q+W
W:外界对系统做的功
Q:外界向系统传递的热量
外界对系统做功,W为正
有机械功,有电场力对电荷做功,有热学中活塞与气缸的功
系统对外界做功,W为负
系统与外界有温度差时,系统与外界交换的能量。
反映系统与外界之间
热学状态的交互变化
外界对系统传热,Q为正
系统对外界传热,Q为负
内能:
微观解释:分子势能与分子动能的总和
不包括系统的宏观机械运动所具有的能,反映的是系统的热学性质。
内能增加,ΔU为正
内能减少,ΔU为负
内能增量ΔU
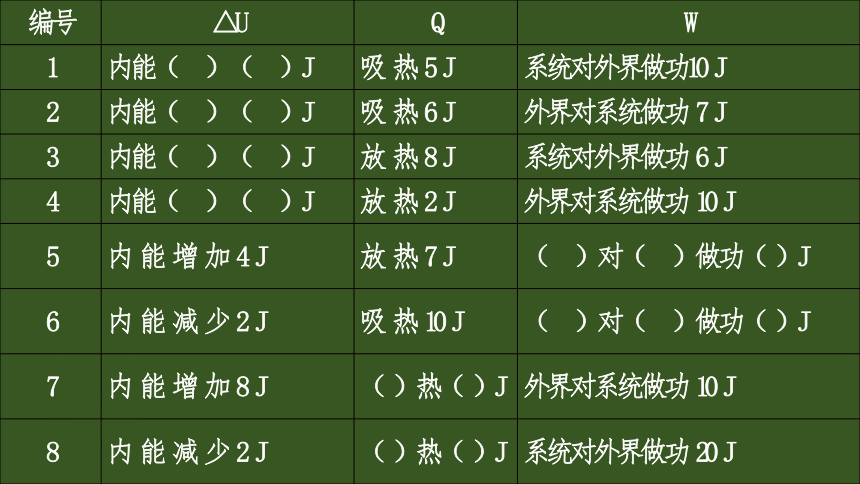
编号
△U
Q
W
1
内能(
)(
)J
吸
热
5
J
系统对外界做功10
J
2
内能(
)(
)J
吸
热
6
J
外界对系统做功
7
J
3
内能(
)(
)J
放
热
8
J
系统对外界做功
6
J
4
内能(
)(
)J
放
热
2
J
外界对系统做功
10
J
5
内
能
增
加
4
J
放
热
7
J
(
)对(
)做功(
)J
6
内
能
减
少
2
J
吸
热
10
J
(
)对(
)做功(
)J
7
内
能
增
加
8
J
(
)热(
)J
外界对系统做功
10
J
8
内
能
减
少
2
J
(
)热(
)J
系统对外界做功
20
J
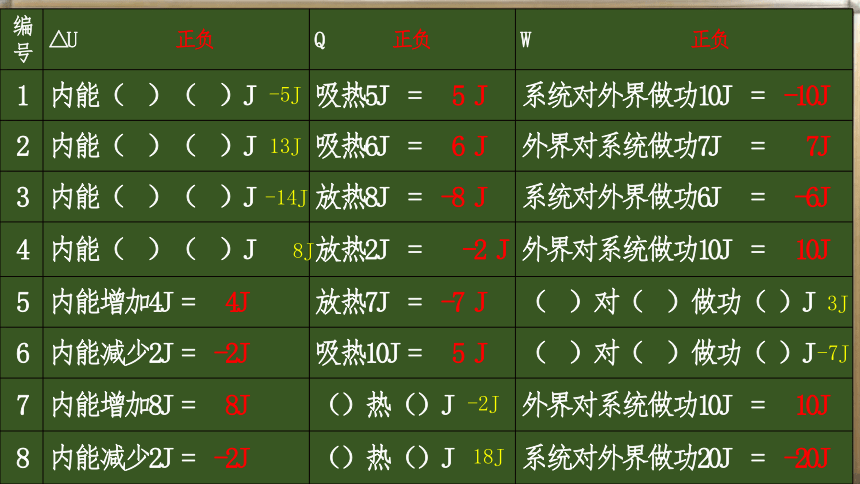
编号
△U
正负
Q
正负
W
正负
1
内能(
)(
)J
吸热5J
=
5
J
系统对外界做功10J
=
-10J
2
内能(
)(
)J
吸热6J
=
6
J
外界对系统做功7J
=
7J
3
内能(
)(
)J
放热8J
=
-8
J
系统对外界做功6J
=
-6J
4
内能(
)(
)J
放热2J
=
-2
J
外界对系统做功10J
=
10J
5
内能增加4J
=
4J
放热7J
=
-7
J
(
)对(
)做功(
)J
6
内能减少2J
=
-2J
吸热10J
=
5
J
(
)对(
)做功(
)J
7
内能增加8J
=
8J
()热()J
外界对系统做功10J
=
10J
8
内能减少2J
=
-2J
()热()J
系统对外界做功20J
=
-20J
-5J
13J
-14J
8J
18J
-2J
-7J
3J
实验验证:内能改变是热传递和做功的共同结果
器材:可读式温度传感器
大号针筒
热水/冰水
毛巾
热力学第一定律是
能量守恒定律在热学领域的体现。
能量既不会凭空产生,
也不会凭空消失,
它只能从一种形式转化为另一种形式,或者从一个物体转移到别的物体,
在转化或转移的过程中,
能量的总量保持不变。
能量守恒定律:
能量守恒定律
能量守恒定律
过渡渲染:只用水
永动机:不需要消耗任何形式的能量,而永远对外界做功的机器。
不可能制成!违背了热力学第一定律
1.知道了热力学第一定律的内容及表达式
2.对热力学第一定律进行理解,尤其是表达式中三个物理量的理解和正负的意义。
3.会应用热力学第一定律对热力学过程进行简单的分析和定量计算。
4.理解能量守恒定律及其重大意义。
5.知道永动机无法制成的原因。
6.体会科学家持之以恒的科学精神和科学发展与社会进步密不可分。
以一定量的理想气体为系统
F
压缩气体:
外界对气体做正功。
S
气体膨胀:
系统对外界做功
外界对气体做负功
F
S
日寒暑温凉之变
如瓦石之类
置之火则热
置之水则寒
特因外物有去有来
吹之即凉
呵之即温
——尹喜《关尹子》
热身实验:想办法使铁丝变热
复习回顾
绝热状态下,单纯对物体做功可改变物体内能。
W=ΔU
单纯向物体传热也可改变物体内能。
Q=ΔU
如果既对物体做功,又向物体传热,内能增加量如何表示??
热力学第一定律
一、文字描述:一个热力学系统,内能增加量等于外界对它传递的热量与外界对它做的功之和。
二、描述的是内能增加量,热量,功的定量关系。
三、表达式:
ΔU=Q+W
焦耳实验再思考:
明确研究的“系统”是什么?“外界”是什么?
以水为系统:内能改变靠热传递
以电热丝为系统:电流做功,
同时对水传热
明确各个量的意义:ΔU=Q+W
W:外界对系统做的功
Q:外界向系统传递的热量
外界对系统做功,W为正
有机械功,有电场力对电荷做功,有热学中活塞与气缸的功
系统对外界做功,W为负
系统与外界有温度差时,系统与外界交换的能量。
反映系统与外界之间
热学状态的交互变化
外界对系统传热,Q为正
系统对外界传热,Q为负
内能:
微观解释:分子势能与分子动能的总和
不包括系统的宏观机械运动所具有的能,反映的是系统的热学性质。
内能增加,ΔU为正
内能减少,ΔU为负
内能增量ΔU
编号
△U
Q
W
1
内能(
)(
)J
吸
热
5
J
系统对外界做功10
J
2
内能(
)(
)J
吸
热
6
J
外界对系统做功
7
J
3
内能(
)(
)J
放
热
8
J
系统对外界做功
6
J
4
内能(
)(
)J
放
热
2
J
外界对系统做功
10
J
5
内
能
增
加
4
J
放
热
7
J
(
)对(
)做功(
)J
6
内
能
减
少
2
J
吸
热
10
J
(
)对(
)做功(
)J
7
内
能
增
加
8
J
(
)热(
)J
外界对系统做功
10
J
8
内
能
减
少
2
J
(
)热(
)J
系统对外界做功
20
J
编号
△U
正负
Q
正负
W
正负
1
内能(
)(
)J
吸热5J
=
5
J
系统对外界做功10J
=
-10J
2
内能(
)(
)J
吸热6J
=
6
J
外界对系统做功7J
=
7J
3
内能(
)(
)J
放热8J
=
-8
J
系统对外界做功6J
=
-6J
4
内能(
)(
)J
放热2J
=
-2
J
外界对系统做功10J
=
10J
5
内能增加4J
=
4J
放热7J
=
-7
J
(
)对(
)做功(
)J
6
内能减少2J
=
-2J
吸热10J
=
5
J
(
)对(
)做功(
)J
7
内能增加8J
=
8J
()热()J
外界对系统做功10J
=
10J
8
内能减少2J
=
-2J
()热()J
系统对外界做功20J
=
-20J
-5J
13J
-14J
8J
18J
-2J
-7J
3J
实验验证:内能改变是热传递和做功的共同结果
器材:可读式温度传感器
大号针筒
热水/冰水
毛巾
热力学第一定律是
能量守恒定律在热学领域的体现。
能量既不会凭空产生,
也不会凭空消失,
它只能从一种形式转化为另一种形式,或者从一个物体转移到别的物体,
在转化或转移的过程中,
能量的总量保持不变。
能量守恒定律:
能量守恒定律
能量守恒定律
过渡渲染:只用水
永动机:不需要消耗任何形式的能量,而永远对外界做功的机器。
不可能制成!违背了热力学第一定律
1.知道了热力学第一定律的内容及表达式
2.对热力学第一定律进行理解,尤其是表达式中三个物理量的理解和正负的意义。
3.会应用热力学第一定律对热力学过程进行简单的分析和定量计算。
4.理解能量守恒定律及其重大意义。
5.知道永动机无法制成的原因。
6.体会科学家持之以恒的科学精神和科学发展与社会进步密不可分。
以一定量的理想气体为系统
F
压缩气体:
外界对气体做正功。
S
气体膨胀:
系统对外界做功
外界对气体做负功
F
S
同课章节目录
- 第一章 分子动理论
- 第01节 物体是由大量分子组成的
- 第02节 测量分子的大小
- 第03节 分子的热运动
- 第04节 分子间的相互作用力
- 第05节 物体的内能
- 第06节 气体分子运动的统计规律
- 第二章 固体、液体和气体
- 第01节 晶体的宏观特征
- 第02节 晶体的微观结构
- 第03节 固体新材料
- 第04节 液体的性质 液晶
- 第05节 液体的表面张力
- 第06节 气体状态参量
- 第07节 气体实验定律(Ⅰ)
- 第08节 气体实验定律(Ⅱ)
- 第09节 饱和蒸汽 空气的湿度
- 第三章 热力学基础
- 第01节 内能 功 热量
- 第02节 热力学第一定律
- 第03节 能量守恒定律
- 第04节 热力学第二定律
- 第05节 能源与可持续发展
- 第06节 研究性学习 能源的开发利用
