人教版高中化学选修四4.1 原电池(共21张PPT)
文档属性
| 名称 | 人教版高中化学选修四4.1 原电池(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-15 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
学生预测实验现象:
1、电流计指针发生偏转吗?
2、两个电极上都有什么现象?
预测实验现象:
1、电流计指针偏转
2、锌片逐渐溶解,铜片表面有红色物质析出
1、电流计指针发生偏转
2、锌片表面有黑色物质析出,铜片表面有红色物质析出
学生观察实验现象:
1、电流计指针发生偏转吗?
2、两个电极上都有什么现象?
3、断开导线后锌片表面继续有黑色物质析出
在上述实验中实验现象为什么与预期现象不一致呢?锌片上产生的黑色物质是什么?它是如何产生的?
此黑色物质是铜,它是锌片与硫酸铜溶液直接发生置换反应生成的铜
根据实验现象分析单液原电池的缺点:
1、电流不稳定
2、工作效率低
3、断路损耗
如何才能得到持续稳定的电流?即用什么办法避免Cu2+在锌片上被还原析出铜,以延长电池放电时间提高供电效率?
根据以下实验用品讨论如何改进原电池装置?设计出相应的实验方案
,可画出装置图
实验用品:锌片、铜片、导线、灵敏电流计、烧杯(2个)、硫酸锌溶液、硫酸铜溶液、长纸条、饱和氯化钾溶液
温馨提示:让锌片与硫酸铜溶液不直接接触
ZnSO4溶液
CuSO4溶液
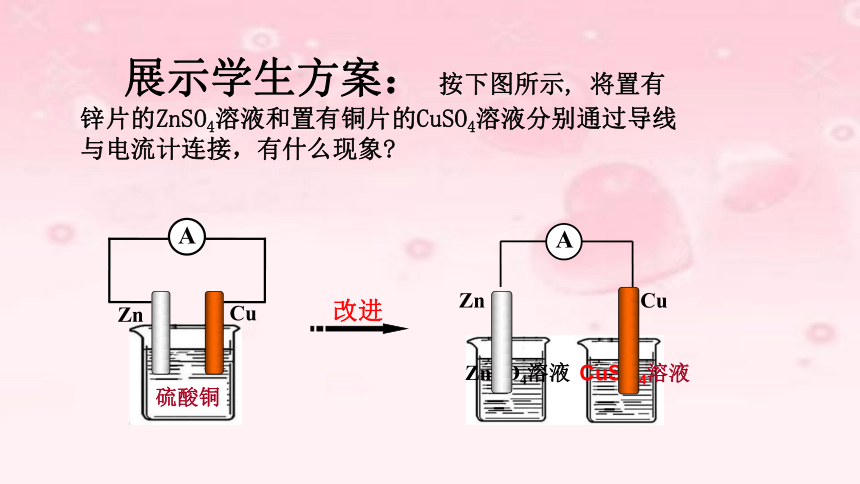
展示学生方案:
按下图所示,
将置有锌片的ZnSO4溶液和置有铜片的CuSO4溶液分别通过导线与电流计连接,有什么现象?
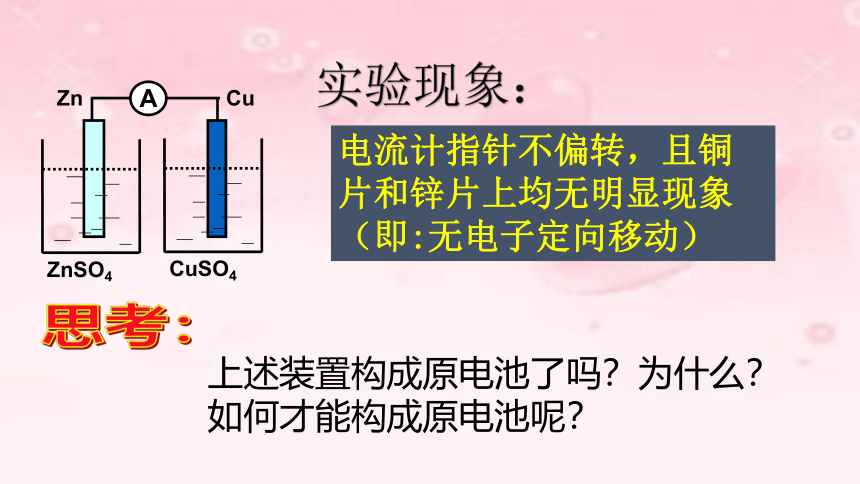
电流计指针不偏转,且铜片和锌片上均无明显现象(即:无电子定向移动)
实验现象:
?
思考:选择什么实验用品使该处形成闭合的通路呢?
盐桥:在U型管中装满用饱和KCl溶液和琼脂作成的冻胶。
盐桥制法:1)将热的琼胶溶液倒入U形管中(注意不要产生裂隙),将冷却后的U形管浸泡在KCl或NH4NO3的饱和溶液中即可。2)将KCl或NH4NO3的饱和溶液装入U形管,用棉花堵住管口即可。
实验现象:
有盐桥存在时电流计指针发生偏转,即有电流通过电路。锌片逐渐溶解,铜片表面有红色固体析出
取出盐桥,电流计指针回到零点,说明没有电流通过。
注意观察两电极的现象及电流计的变化,取出盐桥后会如何?
盐桥的作用:(1)形成闭合回路
(2)平衡电荷,保持溶液的电中性
盐桥的作用是什么?
改进后的原电池装置有哪些优点?
1.产生持续、稳定的电流
2.能量转换率高
3.防止自放电
讨论:
提供电子的物质(负极Zn)
接受电子的场所(正极Cu)
阴离子(Cl-)
负极:氧化反应
Zn-2e-
=Zn2+
正极:还原反应
Cu2++2e-
=
Cu
导线中的电子
负极液(ZnSO4)
正极液(CuSO4)
盐桥(KCl)
阳离子(K+)
阳离子Zn2+
阳离子Cu2+
双液原电池工作原理
2、双液原电池
(1)盐桥的作用:?形成闭合回路
?平衡电荷,保持溶液的电中性
(2)优点:
?产生持续、稳定的电流
?能量转换率高
?
防止自放电
(3)双液原电池工作原理
1、单液原电池
缺点:(1)电流不稳定
(2)工作效率低
(3)断路耗损
1.关于如图所示装置的叙述,正确的是
(
)
A.铜是阳极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
D
2.有关如图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )
A.铜片上有气泡逸出
B.取出盐桥后,电流计依然发生偏转
C.反应中,盐桥中的K+会移向CuSO4溶液
D.反应前后铜片质量不改变
C
学生预测实验现象:
1、电流计指针发生偏转吗?
2、两个电极上都有什么现象?
预测实验现象:
1、电流计指针偏转
2、锌片逐渐溶解,铜片表面有红色物质析出
1、电流计指针发生偏转
2、锌片表面有黑色物质析出,铜片表面有红色物质析出
学生观察实验现象:
1、电流计指针发生偏转吗?
2、两个电极上都有什么现象?
3、断开导线后锌片表面继续有黑色物质析出
在上述实验中实验现象为什么与预期现象不一致呢?锌片上产生的黑色物质是什么?它是如何产生的?
此黑色物质是铜,它是锌片与硫酸铜溶液直接发生置换反应生成的铜
根据实验现象分析单液原电池的缺点:
1、电流不稳定
2、工作效率低
3、断路损耗
如何才能得到持续稳定的电流?即用什么办法避免Cu2+在锌片上被还原析出铜,以延长电池放电时间提高供电效率?
根据以下实验用品讨论如何改进原电池装置?设计出相应的实验方案
,可画出装置图
实验用品:锌片、铜片、导线、灵敏电流计、烧杯(2个)、硫酸锌溶液、硫酸铜溶液、长纸条、饱和氯化钾溶液
温馨提示:让锌片与硫酸铜溶液不直接接触
ZnSO4溶液
CuSO4溶液
展示学生方案:
按下图所示,
将置有锌片的ZnSO4溶液和置有铜片的CuSO4溶液分别通过导线与电流计连接,有什么现象?
电流计指针不偏转,且铜片和锌片上均无明显现象(即:无电子定向移动)
实验现象:
?
思考:选择什么实验用品使该处形成闭合的通路呢?
盐桥:在U型管中装满用饱和KCl溶液和琼脂作成的冻胶。
盐桥制法:1)将热的琼胶溶液倒入U形管中(注意不要产生裂隙),将冷却后的U形管浸泡在KCl或NH4NO3的饱和溶液中即可。2)将KCl或NH4NO3的饱和溶液装入U形管,用棉花堵住管口即可。
实验现象:
有盐桥存在时电流计指针发生偏转,即有电流通过电路。锌片逐渐溶解,铜片表面有红色固体析出
取出盐桥,电流计指针回到零点,说明没有电流通过。
注意观察两电极的现象及电流计的变化,取出盐桥后会如何?
盐桥的作用:(1)形成闭合回路
(2)平衡电荷,保持溶液的电中性
盐桥的作用是什么?
改进后的原电池装置有哪些优点?
1.产生持续、稳定的电流
2.能量转换率高
3.防止自放电
讨论:
提供电子的物质(负极Zn)
接受电子的场所(正极Cu)
阴离子(Cl-)
负极:氧化反应
Zn-2e-
=Zn2+
正极:还原反应
Cu2++2e-
=
Cu
导线中的电子
负极液(ZnSO4)
正极液(CuSO4)
盐桥(KCl)
阳离子(K+)
阳离子Zn2+
阳离子Cu2+
双液原电池工作原理
2、双液原电池
(1)盐桥的作用:?形成闭合回路
?平衡电荷,保持溶液的电中性
(2)优点:
?产生持续、稳定的电流
?能量转换率高
?
防止自放电
(3)双液原电池工作原理
1、单液原电池
缺点:(1)电流不稳定
(2)工作效率低
(3)断路耗损
1.关于如图所示装置的叙述,正确的是
(
)
A.铜是阳极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
D
2.有关如图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )
A.铜片上有气泡逸出
B.取出盐桥后,电流计依然发生偏转
C.反应中,盐桥中的K+会移向CuSO4溶液
D.反应前后铜片质量不改变
C
