物质的量(一)
图片预览











文档简介
(共59张PPT)
第三章 物质的量
第一节 物质的量
(第一课时)
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢?
思考:
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义?
思考:
积小成大,聚微成宏
(1) 1个碳原子和1个氧分子在加热条件下化合生成1个二氧化碳分子 (2) 12份质量的碳与32份质量的氧在点燃条件下化合生成44份质量的二氧化碳
1. 能否用托盘天平称量1粒米的质量 如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义 3. 化学反应的实质:是原子的重组 而实际实验时是称量物质的质量 说明分子、原子、离子等微观粒子与可称量的物质之间有一定的联系?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量 如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义 3. 化学反应的实质:是原子的重组 而实际实验时是称量物质的质量 说明分子、原子、离子等微观粒子与可称量的物质之间有一定的联系? 科学上用物质的量这个物理量把一定数目的原子、分子或离子等微观粒子与可称量的物质联系起来
思考:
积小成大,聚微成宏
回顾:我们学过哪些物理量?它们的单位是什么?
回顾:我们学过哪些物理量?它们的单位是什么?
物理量 单位 质量 千克 长度 米 时间 秒 电流强度 安培
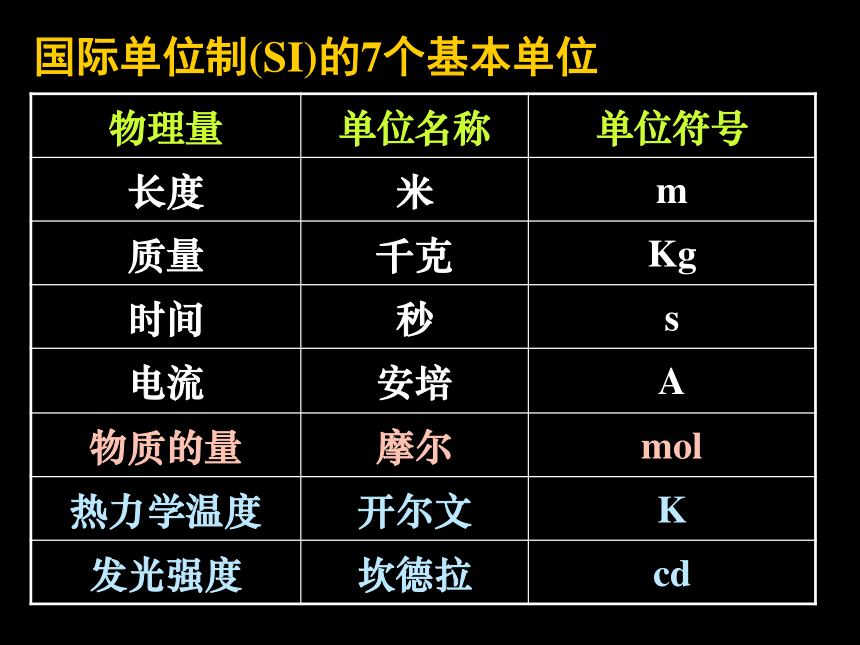
国际单位制(SI)的7个基本单位
物理量 单位名称 单位符号
长度 米 m
质量 千克 Kg
时间 秒 s
电流 安培 A
物质的量 摩尔 mol
热力学温度 开尔文 K
发光强度 坎德拉 cd
国际单位制(SI)的7个基本单位
一、物质的量和摩尔
一、物质的量和摩尔 1、物质的量
(1) 概念:是表示含有一定数目粒子的集体的物理量。
一、物质的量和摩尔 1、物质的量
(1) 概念:是表示含有一定数目粒子的集体的物理量。 (2) 说明: a. 是七个国际基本物理量之一
b. 是一个专有名词,由固定字数组成,不能分割、不能增减。
c. 符号为“n”
d. 微粒是指:分子、原子、离子、中子、电子等
e. 粒子必须十分明确,且用化学式表示
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准:
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准:
每一基本物理量的单位都有 它的标准,如质量单位---千 克的标准是国际千克原器。
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol
请举出一些日常生 活中的表示一定数 目物体的集体单位
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol (4) 特点:大、小、广
请举出一些日常生 活中的表示一定数 目物体的集体单位
思考: 已知:一个碳原子的质量为1.993× 10-23g 求: 0.012kg碳-12中所含的碳原子数?
思考: 已知:一个碳原子的质量为1.993× 10-23g 求: 0.012kg碳-12中所含的碳原子数?
解:
碳原子数 =
12g
1.993 × 10-23g
6.02×1023
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
两个变式(1) N=n NA (2)
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
正确 3mol H2O
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
正确 3mol H2O
正确 0.5mol CO2
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
0.3 6.02 1023
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
0.3 6.02 1023
1
2
3 6.02 1023
课堂练习: 1、0.5molNa2SO4含有____molNa+; _________molSO42-;约含____个O。 2、0.1molNH4+中约含有_______个 N,约含有________个H。
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23
Fe 56 9.032 10-23
H2SO4 98 1.628 10-22
H2O 18 2.990 10-23
Na+ 23 3.821 10-23
OH- 17 2.824 10-23
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23 NA
Fe 56 9.032 10-23 NA
H2SO4 98 1.628 10-22 NA
H2O 18 2.990 10-23 NA
Na+ 23 3.821 10-23 NA
OH- 17 2.824 10-23 NA
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23 NA 12
Fe 56 9.032 10-23 NA 56
H2SO4 98 1.628 10-22 NA 98
H2O 18 2.990 10-23 NA 18
Na+ 23 3.821 10-23 NA 23
OH- 17 2.824 10-23 NA 17
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
2. 分析以上计算结果可得出什么规律? (1) 1mol任何原子的质量(以克为单位)在数 值上等于这种原子的相对原子质量。 (2) 1mol任何分子的质量(以克为单位)在数 值上等于这种分子的相对分子质量。 (3) 1mol任何离子的质量(以克为单位)在数 值上等于这种离子的式量。 二、摩尔质量 1. 1mol物质的质量: 1mol任何微粒或物质的质量是以克为单位时,在数值上等于该微粒的相对原子质量或相对分子质量。
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
23
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
23
58.5
2、摩尔质量
(1) 定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2) 符号:M
(3) 单位:g/mol或kg/mol
(4) 数值:等于物质或粒子的式量
(5) 物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: n(mol)=
(6) 物质的量、摩尔质量、物质的质量;阿伏加得罗常数、 6.02 1023等之间的区别。
2、摩尔质量
(1) 定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2) 符号:M
(3) 单位:g/mol或kg/mol
(4) 数值:等于物质或粒子的式量
(5) 物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: n(mol)=
(6) 物质的量、摩尔质量、物质的质量;阿伏加得罗常数、 6.02 1023等之间的区别。
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克?
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
微观粒子的个数
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
纽带或桥梁
微观粒子的个数
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
5.55
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
5.55
134
第三章 物质的量
第一节 物质的量
(第一课时)
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢?
思考:
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量?如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义?
思考:
积小成大,聚微成宏
(1) 1个碳原子和1个氧分子在加热条件下化合生成1个二氧化碳分子 (2) 12份质量的碳与32份质量的氧在点燃条件下化合生成44份质量的二氧化碳
1. 能否用托盘天平称量1粒米的质量 如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义 3. 化学反应的实质:是原子的重组 而实际实验时是称量物质的质量 说明分子、原子、离子等微观粒子与可称量的物质之间有一定的联系?
思考:
积小成大,聚微成宏
1. 能否用托盘天平称量1粒米的质量 如何知道1粒米的质量呢? 2. “C+O2=CO2”这一方程式表示的含义 3. 化学反应的实质:是原子的重组 而实际实验时是称量物质的质量 说明分子、原子、离子等微观粒子与可称量的物质之间有一定的联系? 科学上用物质的量这个物理量把一定数目的原子、分子或离子等微观粒子与可称量的物质联系起来
思考:
积小成大,聚微成宏
回顾:我们学过哪些物理量?它们的单位是什么?
回顾:我们学过哪些物理量?它们的单位是什么?
物理量 单位 质量 千克 长度 米 时间 秒 电流强度 安培
国际单位制(SI)的7个基本单位
物理量 单位名称 单位符号
长度 米 m
质量 千克 Kg
时间 秒 s
电流 安培 A
物质的量 摩尔 mol
热力学温度 开尔文 K
发光强度 坎德拉 cd
国际单位制(SI)的7个基本单位
一、物质的量和摩尔
一、物质的量和摩尔 1、物质的量
(1) 概念:是表示含有一定数目粒子的集体的物理量。
一、物质的量和摩尔 1、物质的量
(1) 概念:是表示含有一定数目粒子的集体的物理量。 (2) 说明: a. 是七个国际基本物理量之一
b. 是一个专有名词,由固定字数组成,不能分割、不能增减。
c. 符号为“n”
d. 微粒是指:分子、原子、离子、中子、电子等
e. 粒子必须十分明确,且用化学式表示
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准:
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准:
每一基本物理量的单位都有 它的标准,如质量单位---千 克的标准是国际千克原器。
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol
请举出一些日常生 活中的表示一定数 目物体的集体单位
2. 摩尔
(1) 概念:是物质的量的单位,简称摩。
(2) 符号:mol (3) 标准: 摩尔的标准: 以0.012kg 12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与0.012kg 12C中所含的碳原子数目相同,则它的物质的量为1mol (4) 特点:大、小、广
请举出一些日常生 活中的表示一定数 目物体的集体单位
思考: 已知:一个碳原子的质量为1.993× 10-23g 求: 0.012kg碳-12中所含的碳原子数?
思考: 已知:一个碳原子的质量为1.993× 10-23g 求: 0.012kg碳-12中所含的碳原子数?
解:
碳原子数 =
12g
1.993 × 10-23g
6.02×1023
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
(5) 数值:阿佛加德罗常数,用NA表示。
(6) 规定:1mol任何粒子的粒子数叫做阿佛加德罗常数。
(7) 近似值:6.02 1023
(8) 物质的量、阿佛加德罗常数与粒子数(符号为N)之间的关系:
n=
N
NA
物质的量
阿佛加德罗常数
粒子数
两个变式(1) N=n NA (2)
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
正确 3mol H2O
***思考*** 判断下列说法是否正确
(A) 1 摩尔氧 (B) 1 摩尔氧原子
(C) 2 摩尔分子氢
(D) 3 摩尔 水
(E) 0.5 摩 二氧化碳
错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子
正确 1mol O
错误,2mol H2
正确 3mol H2O
正确 0.5mol CO2
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
0.3 6.02 1023
1. 1molH2O中多少mol的H,多少mol的O 2. 1molC中约含有___________个碳原子 3. 0.3 mol H2SO4含有_____________个硫酸分子 4. 1molNa2CO3中含有_____molNa+、 ______molCO32-离子,共含有离子的个数约为______________个。
***思考***
6.02 1023
0.3 6.02 1023
1
2
3 6.02 1023
课堂练习: 1、0.5molNa2SO4含有____molNa+; _________molSO42-;约含____个O。 2、0.1molNH4+中约含有_______个 N,约含有________个H。
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23
Fe 56 9.032 10-23
H2SO4 98 1.628 10-22
H2O 18 2.990 10-23
Na+ 23 3.821 10-23
OH- 17 2.824 10-23
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23 NA
Fe 56 9.032 10-23 NA
H2SO4 98 1.628 10-22 NA
H2O 18 2.990 10-23 NA
Na+ 23 3.821 10-23 NA
OH- 17 2.824 10-23 NA
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
粒子符号 物质的式量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993 10-23 NA 12
Fe 56 9.032 10-23 NA 56
H2SO4 98 1.628 10-22 NA 98
H2O 18 2.990 10-23 NA 18
Na+ 23 3.821 10-23 NA 23
OH- 17 2.824 10-23 NA 17
***思考***
1. 1mol任何物质都约含有6.02 1023个粒子,那么这1mol物质的质量到底有多大?
2. 分析以上计算结果可得出什么规律? (1) 1mol任何原子的质量(以克为单位)在数 值上等于这种原子的相对原子质量。 (2) 1mol任何分子的质量(以克为单位)在数 值上等于这种分子的相对分子质量。 (3) 1mol任何离子的质量(以克为单位)在数 值上等于这种离子的式量。 二、摩尔质量 1. 1mol物质的质量: 1mol任何微粒或物质的质量是以克为单位时,在数值上等于该微粒的相对原子质量或相对分子质量。
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
23
课堂练习: 1. 填空: (1)1molCu质量是_____________克 (2)1molO2质量是_____________克
(3) 1molCO2质量是____________克
(4) 1molCl-质量是_____________克
(5) 1molNa+质量是____________克
(6) 1molNaCl质量是___________克
64
32
44
35.5
23
58.5
2、摩尔质量
(1) 定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2) 符号:M
(3) 单位:g/mol或kg/mol
(4) 数值:等于物质或粒子的式量
(5) 物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: n(mol)=
(6) 物质的量、摩尔质量、物质的质量;阿伏加得罗常数、 6.02 1023等之间的区别。
2、摩尔质量
(1) 定义:单位物质的量的物质所具有的质量叫做摩尔质量。
(2) 符号:M
(3) 单位:g/mol或kg/mol
(4) 数值:等于物质或粒子的式量
(5) 物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: n(mol)=
(6) 物质的量、摩尔质量、物质的质量;阿伏加得罗常数、 6.02 1023等之间的区别。
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克?
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
微观粒子的个数
课堂练习: (1) O2的摩尔质量是多少?
(2) H2SO4的摩尔质量是多少?
(3) 100molH2O的质量是多少克?
(4) 0.1molOH-的质量是多少克? 3. 物质的量的意义:是联系宏观和微观的纽带或桥梁。 表达式:
m
M
M
NA
NA
n
N
宏观物体的质量
纽带或桥梁
微观粒子的个数
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
5.55
1. 24.5gH2SO4的物质的量是多少?
2. 71gNa2SO4中含有Na+和SO42-的物质的量各是多少? 3. 含有1.505 1022个分子的物质,其质量为0.7g,求该物质的相对分子质量。 4. 12.25gKClO3中所含的Cl原子数与多少克CaCl2中所含的Cl-离子个数相等? 5. 一定条件下,16gA和22gB恰好反应生成C和4.5gD,在相同条件下8gA和15gB反应可生成D和0.125molC,则C的式量是多少?
课堂练习:
0.25mol
1mol, 0.5mol
28
5.55
134
