人教版必修1 4.3硫和氮的氧化物--硫(二氧化硫和三氧化硫)(共19张PPT)
文档属性
| 名称 | 人教版必修1 4.3硫和氮的氧化物--硫(二氧化硫和三氧化硫)(共19张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 423.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-17 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第1课时
二氧化硫和三氧化硫
学习目标:
1、了解硫在自然界的存在,认识硫单质的主要性质和用途;
2.了解二氧化硫的物理性质,掌握二氧化硫的化学性质;
3.了解三氧化硫的主要性质。
一
预习检测
1、硫的存在及性质
(1)游离态:存在于
或
。
(2)化合态
a
主要以
形式存在。硫还是组成某些
的生命元素。
火山喷口
地壳岩层
硫化物和硫酸盐
蛋白质
b
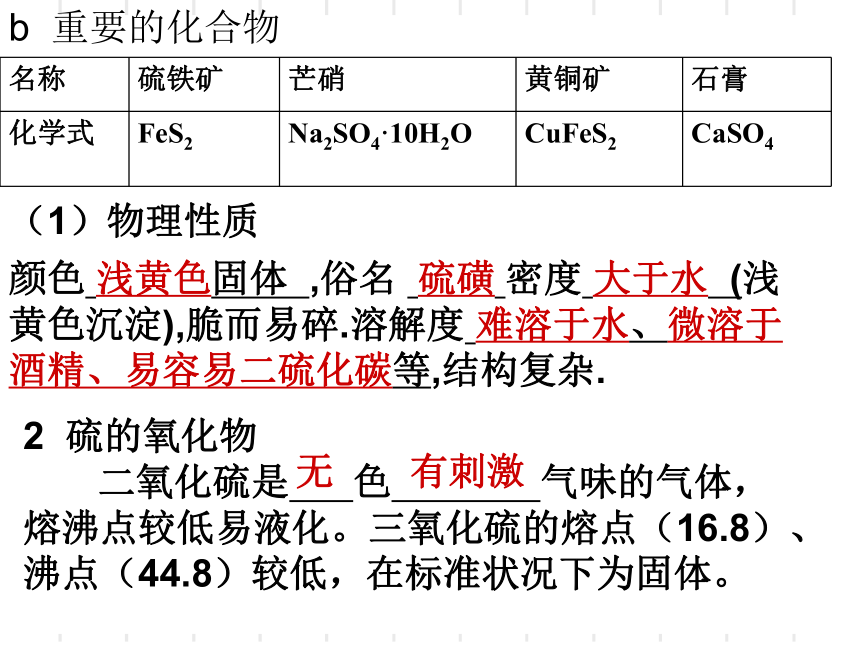
重要的化合物
(1)物理性质
颜色
浅黄色固体
,俗名
硫磺
密度
大于水
(浅黄色沉淀),脆而易碎.溶解度
难溶于水、微溶于酒精、易容易二硫化碳等,结构复杂.
2
硫的氧化物
二氧化硫是
色
气味的气体,熔沸点较低易液化。三氧化硫的熔点(16.8)、沸点(44.8)较低,在标准状况下为固体。
无
有刺激
名称
硫铁矿
芒硝
黄铜矿
石膏
化学式
FeS2
Na2SO4·10H2O
CuFeS2
CaSO4
二
问题引导下的再学习
1、硫的化学性质
(1)S在空气中燃烧
S在纯氧中燃烧
S
+
O2
==
SO2
现象:
淡蓝色火焰
蓝紫色火焰
注意:S和O2直接燃烧反应不能生成SO3
(2)
S与金属反应:如与Fe、
Cu
等反应。
Fe
+
S==FeS
2Cu
+
S
==Cu2S
比较:2Fe+3Cl2
==2FeCl3
说明氧化性:Cl2
Fe3+
S
Fe2+
>
>
>
思考:Fe3+与S2-能否大量共存?
不能
3Fe+2O2===Fe3O4
(3)S与H2的反应方程式
S
+
H2
==
H2S
已知:H2S中S元素的化合价为-2价,H2S的溶液是二元弱酸。分析H2S和氢硫酸(H2S)可能的化学性质。
①H2S有较强的还原性。
2H2S+O2==2H2O+2S
2H2S+3O2==2H2O+2SO2
H2S+Cl2==2HCl+S
2FeCl3+H2S==2FeCl2+S+2HCl
②与碱和碱性氧化物反应
H2S+2NaOH==Na2S+
2H2O
Na2S+2HCl=2NaCl+H2S↑
H2S是弱酸,所以H+和S2-不能大量共存。提供了一种尾气吸收方法。
③与某些盐反应
2FeCl3+H2S==2FeCl2+S+2HCl
H2S
+
CuSO4
==
CuS↓
+
H2SO4
反应特点:弱酸制备强酸。
反应能发生的条件:CuS不溶于强酸H2SO4
分析下面反应不能发生的原因?
CO2+CaCl2==CaCO3
↓
+2HCl
不能发生反应。
因为生成的CaCO3能与HCl反应。
应用:提供了一种除去硫化氢气体的方法,将气体通过盛有硫酸铜溶液的洗气瓶。
二、二氧化硫的化学性质
(1)SO2与水的反应,其反应的化学方程式:
SO2
+
H2O
H2SO3
==
生成的亚硫酸不稳定,易分解成SO2和H2O.
可逆反应;在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
可逆反应的判断:
①反应条件相同。
2H2+O2===2H2O
2H2O===2H2+O2
点燃
通电
是否可逆反应
②可逆反应方程式书写要写可逆符号。
③可逆反应判断方法:在同一反应体系中反应物和生成物能够共存的反应,一定是可逆反应。
在氯水中存在四种物质:H2O
Cl2
HCl
HClO
分析氯气与水的反应是否为可逆反应?化学方程式怎样写?
是可逆反应。方程式:Cl2+H2O
HCl+HClO
④可逆反应的特点:所有反应物都不能反应完。反应物和生成物能够共存于同一体系
(2)
SO2
是酸性氧化物,具有酸性氧化物的通性:能与碱性氧化物、碱、某些盐反应。
写出二氧化硫与
CaO
NaOH
Na2CO3
反应的化学方程式。
CaO+SO2=CaSO3
SO2+2NaOH=Na2SO3+H2O
SO2气体有毒,有强烈的刺激性气味。实验室制备SO2要注意尾气吸收。
方法是
。
盛有碱石灰的干燥管或氢氧化钠的洗气瓶。
由于SO2气体在水中溶解度较大,用氢氧化钠洗气时有时要有防倒吸装置。
倒扣的漏斗。
SO2+Na2CO3==Na2SO3+CO2↑
说明:亚硫酸(H2SO3)的酸性比碳酸强。提供了一种除去SO2的方法。
CO2气体中混有SO2杂质气体,如何除去SO2得到纯净的CO2气体?
将混合气体依次通过饱和NaHCO3和浓硫酸。
(3)SO2中S元素化合价
价,从氧化还原反应的角度去分析SO2既有
性
又有
性。
+4
氧化
还原
a
氧化性
2H2S
+
SO2
=
3S+
2H2O
SO2的氧化性只此一个。
此氧化还原反应是同种元素的归中反应。常用于推断题。
A,B,C三种化合物,有两种元素组成。甲,乙为两种单质,它们有如下关系
(1)A,B,C中含有乙元素的是
。
(2)乙单质是
(金属,非金属)
理由是:
(3)A,B,C
可能是
(4)方程式是:
A
B
非金属
A(SO2)B(H2S)C(H2O)
S+O2==SO2
SO2+2H2S==3S+2H2O
2H2S+3O2=2SO2+2H2O
b
还原性
SO2
的还原性较强,能被O2
、氯水、溴水、碘水、KMnO4
溶液等氧化。
写出下列方程式:
2SO2
+
O2
2SO3
催化剂
SO2+Cl2+2H2O==H2SO4+2HCl
SO2+Br2+2H2O==H2SO4+2HBr
SO2+I2+2H2O==H2SO4+2Hl
补充:2H2SO3+O2==2H2SO4
Na2SO3+Cl2+H2O==Na2SO4+2HCl
Fe3+
ClO-
MnO4-
NO3-
(H+)与S2-
SO32-不能大量共存。
Na2SO3中硫的化合价为
价,它能被O2
、
KMnO4
溶液等氧化吗?
+4
讨论:冬天燃煤时常加入一定量碳酸钙,解释原因?
SO2与酸性高锰酸钾反应的产物是硫酸同时使酸性高锰酸钾褪色,提供了一种检验并除去SO2的方法。
已知浓硫酸与木炭在加热时发生如下反应C+2H2SO4(浓)===CO2↑+2SO2↑+2H2O,利用如图所示装置检验反应产物:
写出ABCD装置中的药品及其作用。
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是
,作用是
。
B中加入的试剂是
,作用是
。
C中加入的试剂是
,作用是除尽
气体。
D中加入的试剂是
,作用是
。
无水硫酸铜
检验
H2O
品红溶液
检验
SO2
足量酸性
KMnO4
溶液
SO2
澄清石灰水
检验
CO2
(4)SO2
的漂白性
将二氧化硫通人品红溶液中,现象为
,这说明了二氧化硫具有
作用;再对褪色后的溶液加热,现象为
。可以利用此性质鉴别S02气体
品红溶液褪色
漂白
又恢复为红色
补充(1)漂白有三种
①Na2O2
H2O2
HClO是氧化漂白,特点漂白后颜色不能恢复,包括品红、石蕊、酚酞、有色布条等。
②SO2的漂白是化合漂白,特点漂白后加热能恢复。
③活性炭的漂白是吸附漂白,活性炭能吸附有色和有毒的物质。
(2)SO2只能使品红、有色布条褪色,不能使石蕊、酚酞褪色。
将氯气、SO2分别通入到石蕊溶液中,现象是:
氯气使石蕊溶液先变红后褪色。
SO2使石蕊溶液只变红不褪色。
将氯气和SO2按体积比为1
:1混合通入到石蕊溶液中,现象是
。
只变红不褪色
SO2
+Cl2
+2
H20==H2S04
+2HC1
三、SO3的化学性质
SO3
是酸性性氧化物具有酸性氧化物通性:与水、与碱、与碱性氧化物反应。
SO3+H2O=H2SO4
SO3+2NaOH=Na2SO4+
H2O
SO3+CaO==CaSO4
当堂训练
1.下列说法不正确的是
(
)
A.硫是一种黄色的不能溶于水的晶体
B.硫的化合物常存在于火山喷出的气体中
C.硫在空气中燃烧的产物是二氧化硫
D.硫在纯氧中燃烧的产物是三氧化硫
2.下列关于S02的说法中,不正确的是
(
)
A.S02是硫及某些含硫化合物在空气中燃烧的产物
B.S02具有漂白性,可以使品红溶液褪色
C.S02与水反应生成H2S04
D.S02是一种大气污染物,它主要来自于化石燃料的燃烧
D
C
3.将S02气体通入显红色的酚酞试液中,发现红色消失,主要是因为S02
(
)
A.有漂白性
B.有还原性
C.有氧化性
D.溶于水后显酸性
4.为除去S02气体中的少量HCl气体杂质,应选用的试剂是(
)
A
水
B
饱和的NaHSO3溶液
C饱和的NaOH溶液
D饱和的Na2CO3溶液
5
导致下列现象的主要原因与排放S02
有关的是(
)
A酸雨
B光化学烟雾
C臭氧空洞
D温室效应
D
B
A
6、大约4000年前,埃及人已经用硫燃烧所形成的二氧化硫漂白布匹。在古罗马著名诗人荷马的著作里也讲到硫燃烧有消毒和漂白作用。
下列物质①潮湿的氯气;②二氧化硫;③活性炭;④过氧化钠都具有漂白性,其漂白原理相同的是
(
)
A.①③
B.②③
C.①④
D.②④
C
7、全社会都在倡导诚信,然而总是有一部分不法商贩在背道而驰。,有些商贩为了使银耳增白,就用硫黄(燃烧硫黄)对银耳进行熏制,用这种方法制取的洁白的银耳对人体是有害的。
这些不法商贩增白银耳利用的是
(
)
A.SO2的漂白性
B.SO2的还原性
C
SO2的漂白件
D.SO2的还原性
C
6.甲同学向品红溶液中通入一种气体后,品红溶液褪色。乙同学设计一个很简单的实验即知甲同学通入的是Cl2
还是S02
,他的实验方案是
将褪色后的溶液加热,恢复为红色则通入的是SO2,不能恢复为红色,证明通入的是氯气。
课堂小结:
1、S的化学性质
2、SO2的化学性质
3、SO3的化学性质
作业:随堂练习。
第1课时
二氧化硫和三氧化硫
学习目标:
1、了解硫在自然界的存在,认识硫单质的主要性质和用途;
2.了解二氧化硫的物理性质,掌握二氧化硫的化学性质;
3.了解三氧化硫的主要性质。
一
预习检测
1、硫的存在及性质
(1)游离态:存在于
或
。
(2)化合态
a
主要以
形式存在。硫还是组成某些
的生命元素。
火山喷口
地壳岩层
硫化物和硫酸盐
蛋白质
b
重要的化合物
(1)物理性质
颜色
浅黄色固体
,俗名
硫磺
密度
大于水
(浅黄色沉淀),脆而易碎.溶解度
难溶于水、微溶于酒精、易容易二硫化碳等,结构复杂.
2
硫的氧化物
二氧化硫是
色
气味的气体,熔沸点较低易液化。三氧化硫的熔点(16.8)、沸点(44.8)较低,在标准状况下为固体。
无
有刺激
名称
硫铁矿
芒硝
黄铜矿
石膏
化学式
FeS2
Na2SO4·10H2O
CuFeS2
CaSO4
二
问题引导下的再学习
1、硫的化学性质
(1)S在空气中燃烧
S在纯氧中燃烧
S
+
O2
==
SO2
现象:
淡蓝色火焰
蓝紫色火焰
注意:S和O2直接燃烧反应不能生成SO3
(2)
S与金属反应:如与Fe、
Cu
等反应。
Fe
+
S==FeS
2Cu
+
S
==Cu2S
比较:2Fe+3Cl2
==2FeCl3
说明氧化性:Cl2
Fe3+
S
Fe2+
>
>
>
思考:Fe3+与S2-能否大量共存?
不能
3Fe+2O2===Fe3O4
(3)S与H2的反应方程式
S
+
H2
==
H2S
已知:H2S中S元素的化合价为-2价,H2S的溶液是二元弱酸。分析H2S和氢硫酸(H2S)可能的化学性质。
①H2S有较强的还原性。
2H2S+O2==2H2O+2S
2H2S+3O2==2H2O+2SO2
H2S+Cl2==2HCl+S
2FeCl3+H2S==2FeCl2+S+2HCl
②与碱和碱性氧化物反应
H2S+2NaOH==Na2S+
2H2O
Na2S+2HCl=2NaCl+H2S↑
H2S是弱酸,所以H+和S2-不能大量共存。提供了一种尾气吸收方法。
③与某些盐反应
2FeCl3+H2S==2FeCl2+S+2HCl
H2S
+
CuSO4
==
CuS↓
+
H2SO4
反应特点:弱酸制备强酸。
反应能发生的条件:CuS不溶于强酸H2SO4
分析下面反应不能发生的原因?
CO2+CaCl2==CaCO3
↓
+2HCl
不能发生反应。
因为生成的CaCO3能与HCl反应。
应用:提供了一种除去硫化氢气体的方法,将气体通过盛有硫酸铜溶液的洗气瓶。
二、二氧化硫的化学性质
(1)SO2与水的反应,其反应的化学方程式:
SO2
+
H2O
H2SO3
==
生成的亚硫酸不稳定,易分解成SO2和H2O.
可逆反应;在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
可逆反应的判断:
①反应条件相同。
2H2+O2===2H2O
2H2O===2H2+O2
点燃
通电
是否可逆反应
②可逆反应方程式书写要写可逆符号。
③可逆反应判断方法:在同一反应体系中反应物和生成物能够共存的反应,一定是可逆反应。
在氯水中存在四种物质:H2O
Cl2
HCl
HClO
分析氯气与水的反应是否为可逆反应?化学方程式怎样写?
是可逆反应。方程式:Cl2+H2O
HCl+HClO
④可逆反应的特点:所有反应物都不能反应完。反应物和生成物能够共存于同一体系
(2)
SO2
是酸性氧化物,具有酸性氧化物的通性:能与碱性氧化物、碱、某些盐反应。
写出二氧化硫与
CaO
NaOH
Na2CO3
反应的化学方程式。
CaO+SO2=CaSO3
SO2+2NaOH=Na2SO3+H2O
SO2气体有毒,有强烈的刺激性气味。实验室制备SO2要注意尾气吸收。
方法是
。
盛有碱石灰的干燥管或氢氧化钠的洗气瓶。
由于SO2气体在水中溶解度较大,用氢氧化钠洗气时有时要有防倒吸装置。
倒扣的漏斗。
SO2+Na2CO3==Na2SO3+CO2↑
说明:亚硫酸(H2SO3)的酸性比碳酸强。提供了一种除去SO2的方法。
CO2气体中混有SO2杂质气体,如何除去SO2得到纯净的CO2气体?
将混合气体依次通过饱和NaHCO3和浓硫酸。
(3)SO2中S元素化合价
价,从氧化还原反应的角度去分析SO2既有
性
又有
性。
+4
氧化
还原
a
氧化性
2H2S
+
SO2
=
3S+
2H2O
SO2的氧化性只此一个。
此氧化还原反应是同种元素的归中反应。常用于推断题。
A,B,C三种化合物,有两种元素组成。甲,乙为两种单质,它们有如下关系
(1)A,B,C中含有乙元素的是
。
(2)乙单质是
(金属,非金属)
理由是:
(3)A,B,C
可能是
(4)方程式是:
A
B
非金属
A(SO2)B(H2S)C(H2O)
S+O2==SO2
SO2+2H2S==3S+2H2O
2H2S+3O2=2SO2+2H2O
b
还原性
SO2
的还原性较强,能被O2
、氯水、溴水、碘水、KMnO4
溶液等氧化。
写出下列方程式:
2SO2
+
O2
2SO3
催化剂
SO2+Cl2+2H2O==H2SO4+2HCl
SO2+Br2+2H2O==H2SO4+2HBr
SO2+I2+2H2O==H2SO4+2Hl
补充:2H2SO3+O2==2H2SO4
Na2SO3+Cl2+H2O==Na2SO4+2HCl
Fe3+
ClO-
MnO4-
NO3-
(H+)与S2-
SO32-不能大量共存。
Na2SO3中硫的化合价为
价,它能被O2
、
KMnO4
溶液等氧化吗?
+4
讨论:冬天燃煤时常加入一定量碳酸钙,解释原因?
SO2与酸性高锰酸钾反应的产物是硫酸同时使酸性高锰酸钾褪色,提供了一种检验并除去SO2的方法。
已知浓硫酸与木炭在加热时发生如下反应C+2H2SO4(浓)===CO2↑+2SO2↑+2H2O,利用如图所示装置检验反应产物:
写出ABCD装置中的药品及其作用。
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是
,作用是
。
B中加入的试剂是
,作用是
。
C中加入的试剂是
,作用是除尽
气体。
D中加入的试剂是
,作用是
。
无水硫酸铜
检验
H2O
品红溶液
检验
SO2
足量酸性
KMnO4
溶液
SO2
澄清石灰水
检验
CO2
(4)SO2
的漂白性
将二氧化硫通人品红溶液中,现象为
,这说明了二氧化硫具有
作用;再对褪色后的溶液加热,现象为
。可以利用此性质鉴别S02气体
品红溶液褪色
漂白
又恢复为红色
补充(1)漂白有三种
①Na2O2
H2O2
HClO是氧化漂白,特点漂白后颜色不能恢复,包括品红、石蕊、酚酞、有色布条等。
②SO2的漂白是化合漂白,特点漂白后加热能恢复。
③活性炭的漂白是吸附漂白,活性炭能吸附有色和有毒的物质。
(2)SO2只能使品红、有色布条褪色,不能使石蕊、酚酞褪色。
将氯气、SO2分别通入到石蕊溶液中,现象是:
氯气使石蕊溶液先变红后褪色。
SO2使石蕊溶液只变红不褪色。
将氯气和SO2按体积比为1
:1混合通入到石蕊溶液中,现象是
。
只变红不褪色
SO2
+Cl2
+2
H20==H2S04
+2HC1
三、SO3的化学性质
SO3
是酸性性氧化物具有酸性氧化物通性:与水、与碱、与碱性氧化物反应。
SO3+H2O=H2SO4
SO3+2NaOH=Na2SO4+
H2O
SO3+CaO==CaSO4
当堂训练
1.下列说法不正确的是
(
)
A.硫是一种黄色的不能溶于水的晶体
B.硫的化合物常存在于火山喷出的气体中
C.硫在空气中燃烧的产物是二氧化硫
D.硫在纯氧中燃烧的产物是三氧化硫
2.下列关于S02的说法中,不正确的是
(
)
A.S02是硫及某些含硫化合物在空气中燃烧的产物
B.S02具有漂白性,可以使品红溶液褪色
C.S02与水反应生成H2S04
D.S02是一种大气污染物,它主要来自于化石燃料的燃烧
D
C
3.将S02气体通入显红色的酚酞试液中,发现红色消失,主要是因为S02
(
)
A.有漂白性
B.有还原性
C.有氧化性
D.溶于水后显酸性
4.为除去S02气体中的少量HCl气体杂质,应选用的试剂是(
)
A
水
B
饱和的NaHSO3溶液
C饱和的NaOH溶液
D饱和的Na2CO3溶液
5
导致下列现象的主要原因与排放S02
有关的是(
)
A酸雨
B光化学烟雾
C臭氧空洞
D温室效应
D
B
A
6、大约4000年前,埃及人已经用硫燃烧所形成的二氧化硫漂白布匹。在古罗马著名诗人荷马的著作里也讲到硫燃烧有消毒和漂白作用。
下列物质①潮湿的氯气;②二氧化硫;③活性炭;④过氧化钠都具有漂白性,其漂白原理相同的是
(
)
A.①③
B.②③
C.①④
D.②④
C
7、全社会都在倡导诚信,然而总是有一部分不法商贩在背道而驰。,有些商贩为了使银耳增白,就用硫黄(燃烧硫黄)对银耳进行熏制,用这种方法制取的洁白的银耳对人体是有害的。
这些不法商贩增白银耳利用的是
(
)
A.SO2的漂白性
B.SO2的还原性
C
SO2的漂白件
D.SO2的还原性
C
6.甲同学向品红溶液中通入一种气体后,品红溶液褪色。乙同学设计一个很简单的实验即知甲同学通入的是Cl2
还是S02
,他的实验方案是
将褪色后的溶液加热,恢复为红色则通入的是SO2,不能恢复为红色,证明通入的是氯气。
课堂小结:
1、S的化学性质
2、SO2的化学性质
3、SO3的化学性质
作业:随堂练习。
