人教版高二化学选修5第二章第一节 脂肪烃----乙炔(共17张PPT)
文档属性
| 名称 | 人教版高二化学选修5第二章第一节 脂肪烃----乙炔(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 435.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-18 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
乙烯球棍模型
乙烯的化学性质:
1、氧化反应
2、加成反应
3、加聚反应
一、乙炔的分子式、结构式和电子式
分子式
C2H2
结构式
H—C?C—H
电子式
H
:
C┇┇C
:
H
乙炔
炔烃
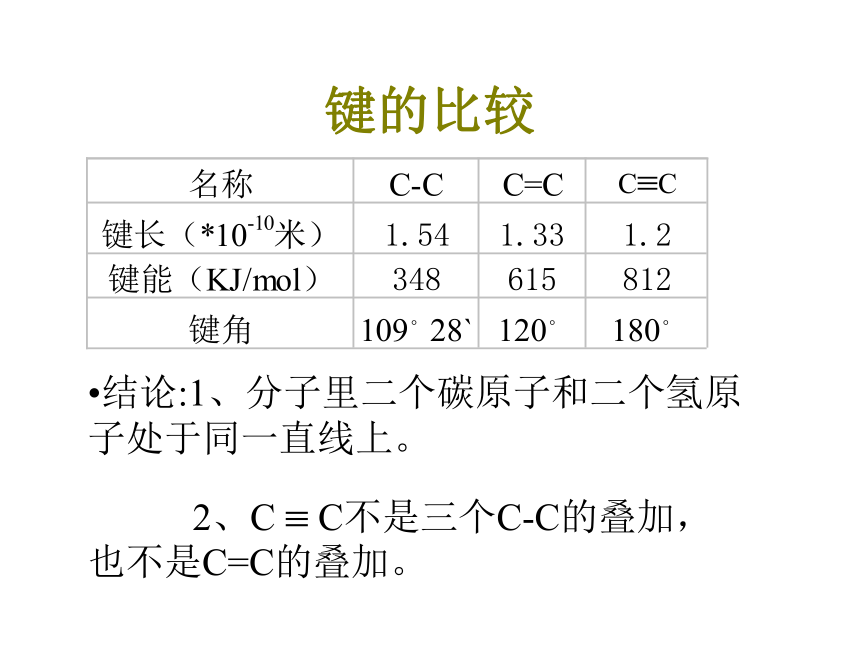
键的比较
结论:1、分子里二个碳原子和二个氢原子处于同一直线上。
2、C
?
C不是三个C-C的叠加,也不是C=C的叠加。
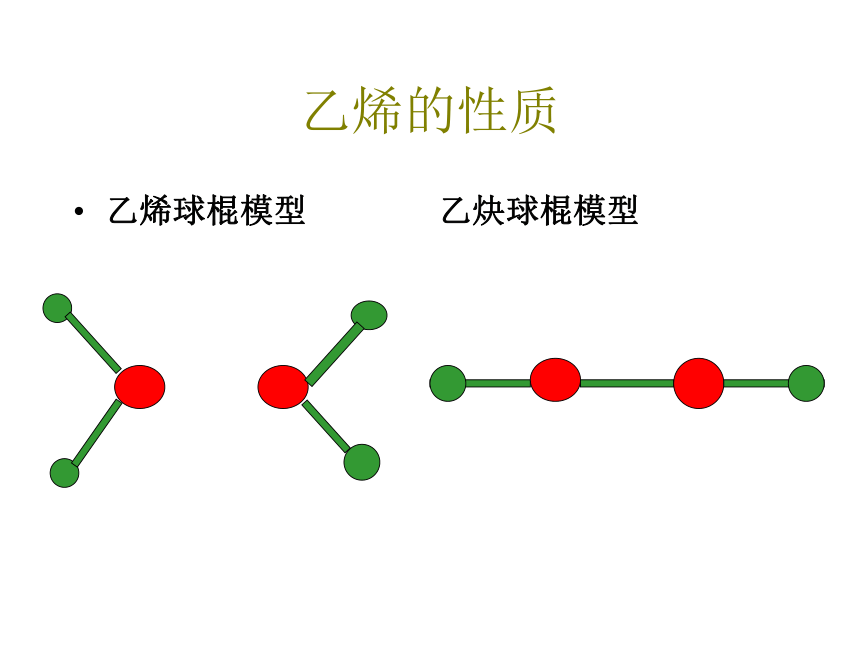
乙炔的性质
乙炔球棍模型
一、乙炔的物理性质
乙烯的性质
乙烯球棍模型
乙炔球棍模型
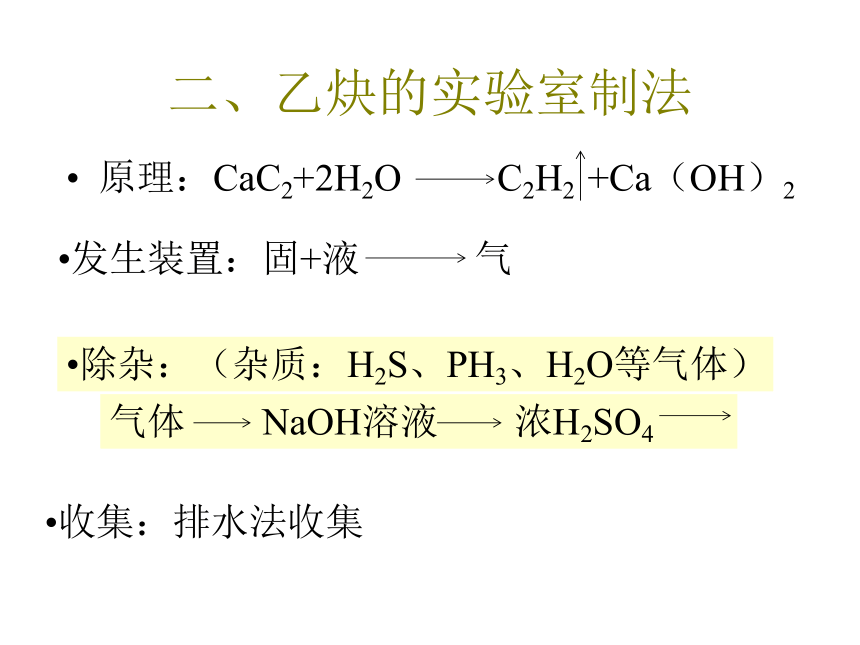
二、乙炔的实验室制法
原理:CaC2+2H2O
C2H2
+Ca(OH)2
收集:排水法收集
除杂:(杂质:H2S、PH3、H2O等气体)
2、能否用启普发生器作为制乙炔的发生装置?
答:电石可与水蒸气发生剧烈反应,放出大量热,变成粉末,堵塞启普发生器,所以不能用启普发生器。
1、反应生成的乙炔常混有PH3、H2S等气体而具有臭味,通过什么溶液除去混有的气体?
答:NaOH溶液
3、制乙炔反应中,为什么用饱和食盐水代替水发生反应?
答:碳化钙与饱和食盐水反应不剧烈,得到气流平稳。
乙炔的化学性质
(1)氧化反应
乙炔的化学性质
(2)加成反应
H—C?C—H+H
—H
催?化
剂
H2C=CH2
Br
Br
H—C=C—H
+Br-Br
H-C
—
C-H
Br
Br
Br
Br
如何用乙炔和氯化氢为原料生产聚氯乙烯?
四、炔烃
烯烃:链烃分子里含有碳碳双键的不饱和烃。
1、炔烃:链烃分子里含有碳碳叁键的不饱和烃。
通式:CnH2n-2
2、命名(与烯烃相似)
例如:CH3
C?CH
1-丙炔
(CH3)3C
C?CH
CH3
C?CCH3
3,3-二甲基-1-丁炔
2-丁炔
试给下列结构简式命名:
3、炔烃的性质
(1)物理性质:随碳原子数增多发生递变。
(2)化学性质:与乙炔相似
本节课内容
一、乙炔的结构
二、乙炔的实验室制法
三、乙炔的性质
1、物理性质
2、化学性质
(1)氧化反应(2)加成反应
四、炔烃
使用乙炔不当,发生爆炸,造成事故。请你设计一实验证明:乙炔和空气混和气遇明火会发生爆炸。
答:用一小薄膜袋装混合气后,用一条带火焰的长木条点燃
谢谢大家的合作,再见!
乙烯球棍模型
乙烯的化学性质:
1、氧化反应
2、加成反应
3、加聚反应
一、乙炔的分子式、结构式和电子式
分子式
C2H2
结构式
H—C?C—H
电子式
H
:
C┇┇C
:
H
乙炔
炔烃
键的比较
结论:1、分子里二个碳原子和二个氢原子处于同一直线上。
2、C
?
C不是三个C-C的叠加,也不是C=C的叠加。
乙炔的性质
乙炔球棍模型
一、乙炔的物理性质
乙烯的性质
乙烯球棍模型
乙炔球棍模型
二、乙炔的实验室制法
原理:CaC2+2H2O
C2H2
+Ca(OH)2
收集:排水法收集
除杂:(杂质:H2S、PH3、H2O等气体)
2、能否用启普发生器作为制乙炔的发生装置?
答:电石可与水蒸气发生剧烈反应,放出大量热,变成粉末,堵塞启普发生器,所以不能用启普发生器。
1、反应生成的乙炔常混有PH3、H2S等气体而具有臭味,通过什么溶液除去混有的气体?
答:NaOH溶液
3、制乙炔反应中,为什么用饱和食盐水代替水发生反应?
答:碳化钙与饱和食盐水反应不剧烈,得到气流平稳。
乙炔的化学性质
(1)氧化反应
乙炔的化学性质
(2)加成反应
H—C?C—H+H
—H
催?化
剂
H2C=CH2
Br
Br
H—C=C—H
+Br-Br
H-C
—
C-H
Br
Br
Br
Br
如何用乙炔和氯化氢为原料生产聚氯乙烯?
四、炔烃
烯烃:链烃分子里含有碳碳双键的不饱和烃。
1、炔烃:链烃分子里含有碳碳叁键的不饱和烃。
通式:CnH2n-2
2、命名(与烯烃相似)
例如:CH3
C?CH
1-丙炔
(CH3)3C
C?CH
CH3
C?CCH3
3,3-二甲基-1-丁炔
2-丁炔
试给下列结构简式命名:
3、炔烃的性质
(1)物理性质:随碳原子数增多发生递变。
(2)化学性质:与乙炔相似
本节课内容
一、乙炔的结构
二、乙炔的实验室制法
三、乙炔的性质
1、物理性质
2、化学性质
(1)氧化反应(2)加成反应
四、炔烃
使用乙炔不当,发生爆炸,造成事故。请你设计一实验证明:乙炔和空气混和气遇明火会发生爆炸。
答:用一小薄膜袋装混合气后,用一条带火焰的长木条点燃
谢谢大家的合作,再见!
