人教版高二化学选修5第一章第二节 有机化合物的结构特点 (共47张PPT)
文档属性
| 名称 | 人教版高二化学选修5第一章第二节 有机化合物的结构特点 (共47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 947.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-18 00:00:00 | ||
图片预览








文档简介
(共47张PPT)
第二节
有机化合物的结构特点
第一章
认识有机化合物
据统计:
到目前为止,有机物已经超过了七千万种,
而无机物只有十几万种,每年新合成的化
合物中90﹪以上是有机物。
有机物的种类为什么如此繁多呢?
3.多个碳原子可相互结合成链状(可带支链),
也可以结合成环状,碳链与碳环间也可相结合。
一.有机化合物中碳原子的成键特点:
1.碳原子不仅可以跟其它原子形成4个共价键,
而且碳原子之间也能以共价键相结合。
2.碳原子间不仅可以形成稳定的单键,还可形成稳定的双键或三键。
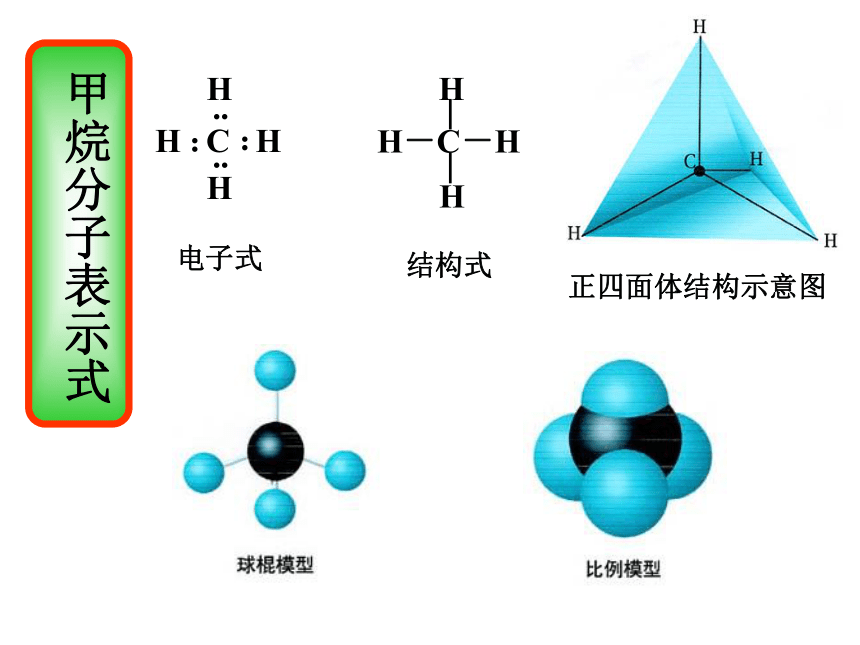
电子式
结构式
正四面体结构示意图
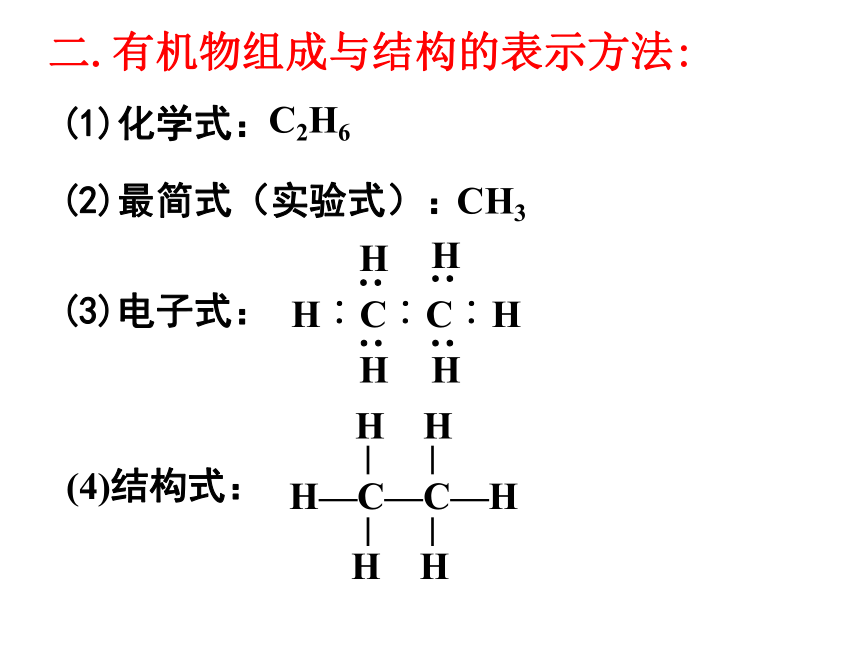
二.有机物组成与结构的表示方法:
(1)化学式:
C2H6
(2)最简式(实验式):
CH3
(3)电子式:
(4)结构式:
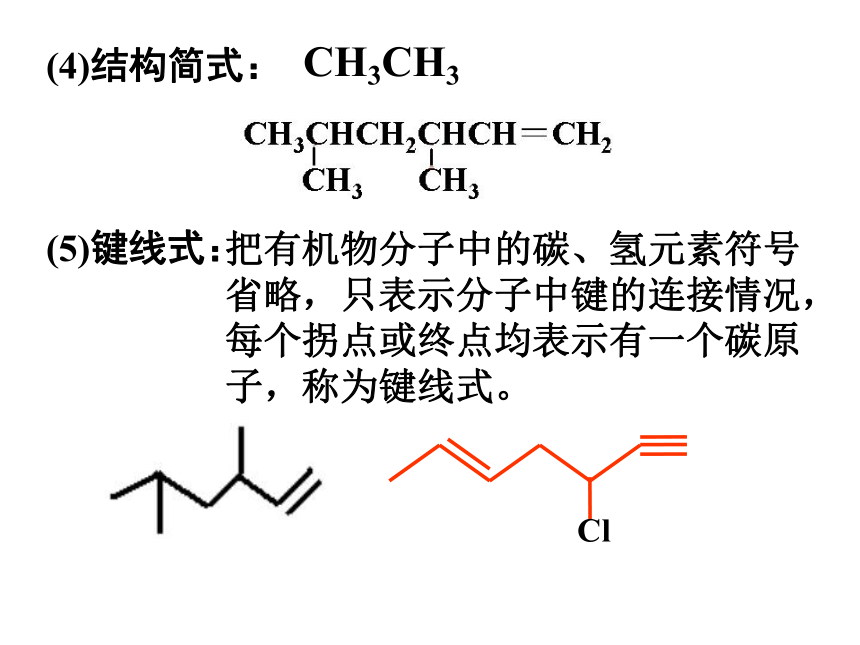
(5)键线式:
把有机物分子中的碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有一个碳原子,称为键线式。
(4)结构简式:
CH3CH3
三.有机化合物的同分异构现象
1.同分异构体:
分子式相同,而结构不同的化合物互为
同分异构体。
三同:
分子式、分子组成、相对分子质量相同
两不同:
结构、性质不同
相对分子质量相同的不同化合物一定互为同分异构体.
×
CH3COOH与CH3CH2CH2OH
CH3CH2OH
CH3OCH3
碳碳双键在碳链中的位置不同而产生的异构
C=C-C-C、
C-C=C-C
碳链骨架(直链,支链,环状)的不同而产生的异构
C-C-C-C、C-C-C
?
C
产生的原因
示例
异构
类型
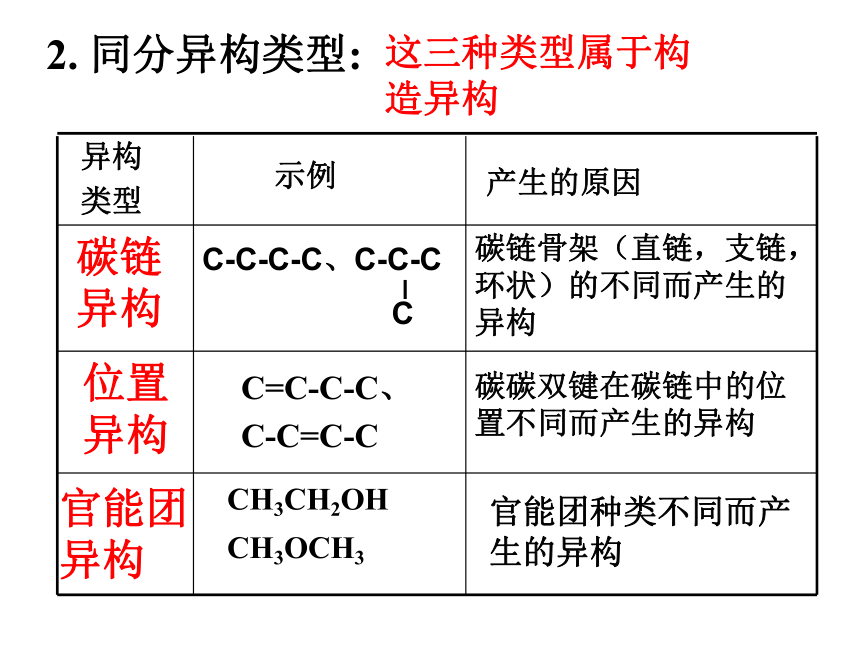
2.
同分异构类型:
碳链异构
位置异构
官能团异构
官能团种类不同而产生的异构
这三种类型属于构造异构
3.
烷烃同分异构体的书写
讨论:(1)书写C7H16
的同分异构体
(2)书写C4H8的异构体
(3)书写C4H10O的异构体
(1)减碳法
(适用于烷烃)
同分异构体的书写口诀:
主链由长到短;支链由整到散;
位置由心到边;排布对邻间。
(2)插入法(适用于烯烃、炔烃、酯等)
先根据给定的碳原子数写出烷烃的同分异构体的碳链骨架,再将官能团插入碳链中。
如书写分子式为C4H8的烯烃的同分异构体(插入双键),双键可分别在①、②、③号位置:
(3)取代法(适用于醇、卤代烃、醛、酸异构)
先碳链异构,后位置异构。如书写分子式为C5H12O的醇的同分异构体。如图(图中数字即为—OH接入后的位置,即这样的醇合计为8种):
?
常见的官能团︿类别﹀异构现象
一、不饱和度(Ω)
有机物分子不饱和程度的量化标志。
以饱和有机物为准,每缺少2个H原子即为一个不饱和度,所以不饱和度即为缺氢指数。
1个
、C=O、一个单键的环,
Ω=1;
1个
C≡C
,
Ω=2;
1个苯环,
Ω=4。
如果已知有机物结构式或结构简式,根据:
如果已知有机物的化学式CnHmOx
(m
≤2n+2)时,则该分子具有不饱和度。
分子的不饱和度(Ω)与分子结构的关系:
1、若Ω=0,分子是饱和链状结构(烷烃和烷基的Ω=0
)
2、若Ω=1,分子中有一个双键或一个环;
3、若Ω=2,说明分子中有两个双键或一个三键;或一个双键和一个环;或两个环;余此类推;
4、若Ω≥4,说明分子中很可能有苯环。
5、若为含氧有机物,计算时可不考虑氧原子,如:
CH2=CH2、C2H4O、C2H4O2的Ω均为1。
6、有机物中的卤原子视作氢原子计算Ω。如:C2H3Cl的Ω为1,其它基如-NO2、-NH2、-SO3H
等都视为氢原子。
2.同分异构体数目的判断方法
(1)基元法
如丁基有4种同分异构体,则丁醇有4种同分异构体。
(2)对称法(又称等效氢法)
等效氢法的判断可按下列三点进行
①同一甲基上的氢原子是等效的;
②同一碳原子上所连甲基上的氢原子是等效的;
③处于对称位置上的氢原子是等效的。
常见一元取代物只有一种的10个碳原子以内的烷烃
CH3CH3
CH4
例如:对称轴
CH3CH2CH2CH2CH3
① ② ③
②
①
②
①
③
①
②
CH3-CH2-CH-CH2-CH3
①
CH2
②
CH3
CH3
CH3
–
C
–
CH2-
CH3
①
CH3
②
③
a
对称技巧
1.环状结构(BHNH)3称为无机苯,它和苯是等电子体,
(BHNH)3的结构简式如图。
无机苯的一氯代物的同分异构体共有(
)
A.5种
B.4种
C.3种
D.2种
D
(3)换元法
如二氯苯(C6H4Cl2)有3种同分异构体,四氯苯也有3种同分异构体(将H替代Cl)。
已知二甲苯的同分异构体有三种,请你用最简捷的方法推出四甲苯有几种同分异构体。
练习:已知化学式为C12H12的物质A的结构简式为
A苯环上的二溴代物有9种同分异构体,以此推断
A苯环上的四溴代物的异构体数目有
(
)
A.9种
B.
10种
C.
11种
D.
12种
A
(4)定一移二法
对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代基,以确定同分异构体数目。
(5)分配法
适用于分析醚、酮、酯的同分异构体
1、主链上有4个碳原子的某烷烃,有两种同分异构体,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有(
)?
?
?A.2种???
B.3种???
C.4种???
D.5种?
C
2、某烃的一种同分异构体只能生成1种一氯代物,该
烃的分子式可以是(
???
)??
A.C3H8???
B.
C4H10???
C.
C5H12
???
D.
C6H14
?
??
?
C
3、一氯丁烯(C4H7C1)的同分异构体只有8种,某学生却写了如下10种:
其中,两两等同的式子是_________和_________,__________和________。
F
G
I
J
4.进行一氯取代后,只能生成3种沸点不同的产物的烷烃是(
)
A、(CH3)2CHCH2CH2CH3
B、(CH3CH2)2CHCH3
C、(CH3)2CHCH(CH3)2
D、(CH3)3CCH2CH3
D
三、共面共线问题:思维原型:
共面分子:
共线分子:
BD
BC
CD
下列物质在结构上有什么异同?
分子式
结构简式
名称
CH4
CH4
甲烷
C2H6
CH3CH3
乙烷
C3H8
CH3CH2CH3
丙烷
C4H10
CH3(CH2)2CH3
丁烷
C5H12
CH3(CH2)3CH3
戊烷
C17H36
CH3(CH2)15CH3
十七烷
下列物质在结构上有什么异同?
分子式
结构简式
名称
C2H4
CH2=CH2
乙烯
C3H6
CH2=CHCH3
丙烯
C4H8
CH2=CHCH2CH3
1-丁烯
C5H10
CH2=CHCH2CH2CH3
1-戊烯
四.同系物:
结构相似、分子组成上相差一个或若干个CH2原子团的物质互相称为同系物。
1.概念:
2.判断:
结构相似—官能团的种类与个数相同
(或碳骨架相同)
组成差CH2—C原子数不同
1.下列哪组是同系物?( )
A.CH3CH2CH2CH3
CH3CH(CH3)CH3
B.CH3CH3
CH3CH(CH3)CH3
C.CH3-CH=CH2
D.CH3CH2OH
E.CH3CH2CH2Br
CH3CH2Cl
B
乙二醇
与
丙三醇
甲酸甲酯
与
二乙酸乙二酯
乙酸
与
软脂酸
乙二酸二乙酯
与
二乙酸乙二酯
A
B
C
D
E
C
回
2、下列属于同系物的一组是(
)
属于苯的同系物的是
。
3
属于乙烯的同系物的是
。
7
属于乙醇的同系物的是
。
5
属于乙酸乙酯的同系物的是
。
12
顺反异构
1、产生顺反异构的条件
?分子中存在限制旋转的因素,如双键或脂环。
?每个不能自由旋转的碳原子必须连有2个不同的原子或原子团。
顺-1,2-环丙二甲酸
熔点137℃
反-1,2-环丙二甲酸
熔点178℃
2、顺反异构的命名
顺反命名法
2个相同原子或原子团处于
π
键或脂环平面同侧
的异构体称为顺式,处于异侧的称为反式。
Z、E命名法
先根据次序规则确定连接在双键碳原子上的原子或原子团的大小顺序。
当2个较大的原子或原子团在双键的同侧时,为Z构型,在异侧的为E构型。
例子:
若a>b,d
>
e,则它们的构型分别为
对映异构
两个分子成镜面对称,但又不能完全重叠,我们把这两个分子称为一对对映体,它们成对映异构(或旋光异构)。
手性(手征性):实物与镜像不能完全重叠的特性。
手性分子:具有手性的分子。
手性与旋光性的关系:手性分子一定有旋光性;反之,具有旋光性的分子一定是手性分子。
分子是否具有手性是产生旋光性和对映异构的根本原因和充分必要条件。
有手性C的分子,可能是手性分子,可能有旋光性;
无手性C的分子,可能是手性分子,可能有旋光性;
只含一个手性C的分子,一定是手性分子,一定有旋光性。
手性碳原子:通常把与四个互不相同的原子或基团相连的碳原子称为手性碳原子,用
标出。
手性碳原子
手性
D-甘油醛
L-甘油醛
D-葡萄糖
D-果糖
第二节
有机化合物的结构特点
第一章
认识有机化合物
据统计:
到目前为止,有机物已经超过了七千万种,
而无机物只有十几万种,每年新合成的化
合物中90﹪以上是有机物。
有机物的种类为什么如此繁多呢?
3.多个碳原子可相互结合成链状(可带支链),
也可以结合成环状,碳链与碳环间也可相结合。
一.有机化合物中碳原子的成键特点:
1.碳原子不仅可以跟其它原子形成4个共价键,
而且碳原子之间也能以共价键相结合。
2.碳原子间不仅可以形成稳定的单键,还可形成稳定的双键或三键。
电子式
结构式
正四面体结构示意图
二.有机物组成与结构的表示方法:
(1)化学式:
C2H6
(2)最简式(实验式):
CH3
(3)电子式:
(4)结构式:
(5)键线式:
把有机物分子中的碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有一个碳原子,称为键线式。
(4)结构简式:
CH3CH3
三.有机化合物的同分异构现象
1.同分异构体:
分子式相同,而结构不同的化合物互为
同分异构体。
三同:
分子式、分子组成、相对分子质量相同
两不同:
结构、性质不同
相对分子质量相同的不同化合物一定互为同分异构体.
×
CH3COOH与CH3CH2CH2OH
CH3CH2OH
CH3OCH3
碳碳双键在碳链中的位置不同而产生的异构
C=C-C-C、
C-C=C-C
碳链骨架(直链,支链,环状)的不同而产生的异构
C-C-C-C、C-C-C
?
C
产生的原因
示例
异构
类型
2.
同分异构类型:
碳链异构
位置异构
官能团异构
官能团种类不同而产生的异构
这三种类型属于构造异构
3.
烷烃同分异构体的书写
讨论:(1)书写C7H16
的同分异构体
(2)书写C4H8的异构体
(3)书写C4H10O的异构体
(1)减碳法
(适用于烷烃)
同分异构体的书写口诀:
主链由长到短;支链由整到散;
位置由心到边;排布对邻间。
(2)插入法(适用于烯烃、炔烃、酯等)
先根据给定的碳原子数写出烷烃的同分异构体的碳链骨架,再将官能团插入碳链中。
如书写分子式为C4H8的烯烃的同分异构体(插入双键),双键可分别在①、②、③号位置:
(3)取代法(适用于醇、卤代烃、醛、酸异构)
先碳链异构,后位置异构。如书写分子式为C5H12O的醇的同分异构体。如图(图中数字即为—OH接入后的位置,即这样的醇合计为8种):
?
常见的官能团︿类别﹀异构现象
一、不饱和度(Ω)
有机物分子不饱和程度的量化标志。
以饱和有机物为准,每缺少2个H原子即为一个不饱和度,所以不饱和度即为缺氢指数。
1个
、C=O、一个单键的环,
Ω=1;
1个
C≡C
,
Ω=2;
1个苯环,
Ω=4。
如果已知有机物结构式或结构简式,根据:
如果已知有机物的化学式CnHmOx
(m
≤2n+2)时,则该分子具有不饱和度。
分子的不饱和度(Ω)与分子结构的关系:
1、若Ω=0,分子是饱和链状结构(烷烃和烷基的Ω=0
)
2、若Ω=1,分子中有一个双键或一个环;
3、若Ω=2,说明分子中有两个双键或一个三键;或一个双键和一个环;或两个环;余此类推;
4、若Ω≥4,说明分子中很可能有苯环。
5、若为含氧有机物,计算时可不考虑氧原子,如:
CH2=CH2、C2H4O、C2H4O2的Ω均为1。
6、有机物中的卤原子视作氢原子计算Ω。如:C2H3Cl的Ω为1,其它基如-NO2、-NH2、-SO3H
等都视为氢原子。
2.同分异构体数目的判断方法
(1)基元法
如丁基有4种同分异构体,则丁醇有4种同分异构体。
(2)对称法(又称等效氢法)
等效氢法的判断可按下列三点进行
①同一甲基上的氢原子是等效的;
②同一碳原子上所连甲基上的氢原子是等效的;
③处于对称位置上的氢原子是等效的。
常见一元取代物只有一种的10个碳原子以内的烷烃
CH3CH3
CH4
例如:对称轴
CH3CH2CH2CH2CH3
① ② ③
②
①
②
①
③
①
②
CH3-CH2-CH-CH2-CH3
①
CH2
②
CH3
CH3
CH3
–
C
–
CH2-
CH3
①
CH3
②
③
a
对称技巧
1.环状结构(BHNH)3称为无机苯,它和苯是等电子体,
(BHNH)3的结构简式如图。
无机苯的一氯代物的同分异构体共有(
)
A.5种
B.4种
C.3种
D.2种
D
(3)换元法
如二氯苯(C6H4Cl2)有3种同分异构体,四氯苯也有3种同分异构体(将H替代Cl)。
已知二甲苯的同分异构体有三种,请你用最简捷的方法推出四甲苯有几种同分异构体。
练习:已知化学式为C12H12的物质A的结构简式为
A苯环上的二溴代物有9种同分异构体,以此推断
A苯环上的四溴代物的异构体数目有
(
)
A.9种
B.
10种
C.
11种
D.
12种
A
(4)定一移二法
对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代基,以确定同分异构体数目。
(5)分配法
适用于分析醚、酮、酯的同分异构体
1、主链上有4个碳原子的某烷烃,有两种同分异构体,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有(
)?
?
?A.2种???
B.3种???
C.4种???
D.5种?
C
2、某烃的一种同分异构体只能生成1种一氯代物,该
烃的分子式可以是(
???
)??
A.C3H8???
B.
C4H10???
C.
C5H12
???
D.
C6H14
?
??
?
C
3、一氯丁烯(C4H7C1)的同分异构体只有8种,某学生却写了如下10种:
其中,两两等同的式子是_________和_________,__________和________。
F
G
I
J
4.进行一氯取代后,只能生成3种沸点不同的产物的烷烃是(
)
A、(CH3)2CHCH2CH2CH3
B、(CH3CH2)2CHCH3
C、(CH3)2CHCH(CH3)2
D、(CH3)3CCH2CH3
D
三、共面共线问题:思维原型:
共面分子:
共线分子:
BD
BC
CD
下列物质在结构上有什么异同?
分子式
结构简式
名称
CH4
CH4
甲烷
C2H6
CH3CH3
乙烷
C3H8
CH3CH2CH3
丙烷
C4H10
CH3(CH2)2CH3
丁烷
C5H12
CH3(CH2)3CH3
戊烷
C17H36
CH3(CH2)15CH3
十七烷
下列物质在结构上有什么异同?
分子式
结构简式
名称
C2H4
CH2=CH2
乙烯
C3H6
CH2=CHCH3
丙烯
C4H8
CH2=CHCH2CH3
1-丁烯
C5H10
CH2=CHCH2CH2CH3
1-戊烯
四.同系物:
结构相似、分子组成上相差一个或若干个CH2原子团的物质互相称为同系物。
1.概念:
2.判断:
结构相似—官能团的种类与个数相同
(或碳骨架相同)
组成差CH2—C原子数不同
1.下列哪组是同系物?( )
A.CH3CH2CH2CH3
CH3CH(CH3)CH3
B.CH3CH3
CH3CH(CH3)CH3
C.CH3-CH=CH2
D.CH3CH2OH
E.CH3CH2CH2Br
CH3CH2Cl
B
乙二醇
与
丙三醇
甲酸甲酯
与
二乙酸乙二酯
乙酸
与
软脂酸
乙二酸二乙酯
与
二乙酸乙二酯
A
B
C
D
E
C
回
2、下列属于同系物的一组是(
)
属于苯的同系物的是
。
3
属于乙烯的同系物的是
。
7
属于乙醇的同系物的是
。
5
属于乙酸乙酯的同系物的是
。
12
顺反异构
1、产生顺反异构的条件
?分子中存在限制旋转的因素,如双键或脂环。
?每个不能自由旋转的碳原子必须连有2个不同的原子或原子团。
顺-1,2-环丙二甲酸
熔点137℃
反-1,2-环丙二甲酸
熔点178℃
2、顺反异构的命名
顺反命名法
2个相同原子或原子团处于
π
键或脂环平面同侧
的异构体称为顺式,处于异侧的称为反式。
Z、E命名法
先根据次序规则确定连接在双键碳原子上的原子或原子团的大小顺序。
当2个较大的原子或原子团在双键的同侧时,为Z构型,在异侧的为E构型。
例子:
若a>b,d
>
e,则它们的构型分别为
对映异构
两个分子成镜面对称,但又不能完全重叠,我们把这两个分子称为一对对映体,它们成对映异构(或旋光异构)。
手性(手征性):实物与镜像不能完全重叠的特性。
手性分子:具有手性的分子。
手性与旋光性的关系:手性分子一定有旋光性;反之,具有旋光性的分子一定是手性分子。
分子是否具有手性是产生旋光性和对映异构的根本原因和充分必要条件。
有手性C的分子,可能是手性分子,可能有旋光性;
无手性C的分子,可能是手性分子,可能有旋光性;
只含一个手性C的分子,一定是手性分子,一定有旋光性。
手性碳原子:通常把与四个互不相同的原子或基团相连的碳原子称为手性碳原子,用
标出。
手性碳原子
手性
D-甘油醛
L-甘油醛
D-葡萄糖
D-果糖
