第二章第3节氧气
图片预览



文档简介
第二章 §2.3 氧气(第1课时)
班级 学号 姓名
一、学习目标:
1、通过活动让学生了解实验室制取氧气的方法
2、通过对比实验,让学生知道制取氧气时二氧化锰是一种催化剂,并了解催化剂的特点
3、通过实验装置,让学生了解实验仪器、装置的连接以及实验过程中的注意事项
4、通过课外实验,让学生了解排水法收集气体的方法。
二、课前预习:
1、液化空气的方法分离空气中的氧气需要 的压强和 的温度,在实验室里很难完成
2、实验室中可以利用 、 、 等物质来制取氧气。
3、二氧化锰在分解过氧化氢制取氧气的实验中起到了 的作用,从而 了过氧化氢的分解速度。
4、过氧化氢分解制取氧气的文字表达式:
5、 氧气可以用 方法来收集,说明氧气是一种 的气体。
三、课内导学:
1、液化空气(低温高压):分离空气中的 和 。
2、实验室制取氧气(分解过氧化氢H2O2或加热分解高锰酸钾)
活动1:分解过氧化氢制取氧气
1.取三支洁净的试管
(1)向第一支试管中加入少量过氧化氢溶液,你观察到的现象是:
(2)向第一支试管中加入少量过氧化氢溶液,再加入少量二氧化锰粉末,你观察到的现象:
(3)向第一支试管中加入少量过氧化氢溶液,再加入一小块猪肝,你观察到的现象是:
2.当上述第二和第三支试管中加入有关物质后,在试管中伸入带火星的木条,可以观察到的现象是: ,推测从第二和第三支试管中放出的气体可能是 ,二氧化锰和猪肝的作用是 ,比较上述三种方法,其中更适合于在实验室制取氧气的方法是 。并说出你的理由:
3.分解过氧化氢制取氧气
(1)区分发生装置和收集装置
(2)认识仪器:① ②
③ ④ ⑤
①中装有 ,②中装有
(3)过氧化氢分解制取氧气的文字表达式:
(4)收集氧气的方法是 法,而排水法是收集微溶于水或难溶于水的气体,说明氧气是一种 于水的气体(不易溶、易溶)
(5)怎样检验收集的气体为氧气?
(6)用排水法收集氧气前,应注意检验装置的气密性
先将导管伸入水槽中后,用手握住发生装置一段时间后,观察是否有少量气泡产生。若有,则表示气密性良好。
(7)当实验时,不要立即收集气体,待气泡 冒出的时候,再进行收集。
3、认识催化剂(阅读小资料:催化剂)
(1)催化剂可以 化学反应的速度。
二氧化锰使过氧化氢的分解速度大大的 了
(2)某一类催化剂只能催化特定的化学反应
(3)将实验后的二氧化锰烘干后称其质量,发现所得的质量与所加二氧化锰的质量一样
而且该二氧化锰能继续催化过氧化氢,没有影响其本身的化学本质。
结论:催化剂在指在化学反应中能 其他物质的化学反应的 ,而本身的 和 在反应前后均不改变。
四、当堂训练:
1.实验室中制取氧气可用过氧化氢、 、 等物质。过氧化氢俗称
,通常是 色的液体,用它制氧气的化学反应用文字表达为
。为了加快(改变)其反应速度,可在过氧化氢 溶液中
加入少量 色的二氧化锰作 。
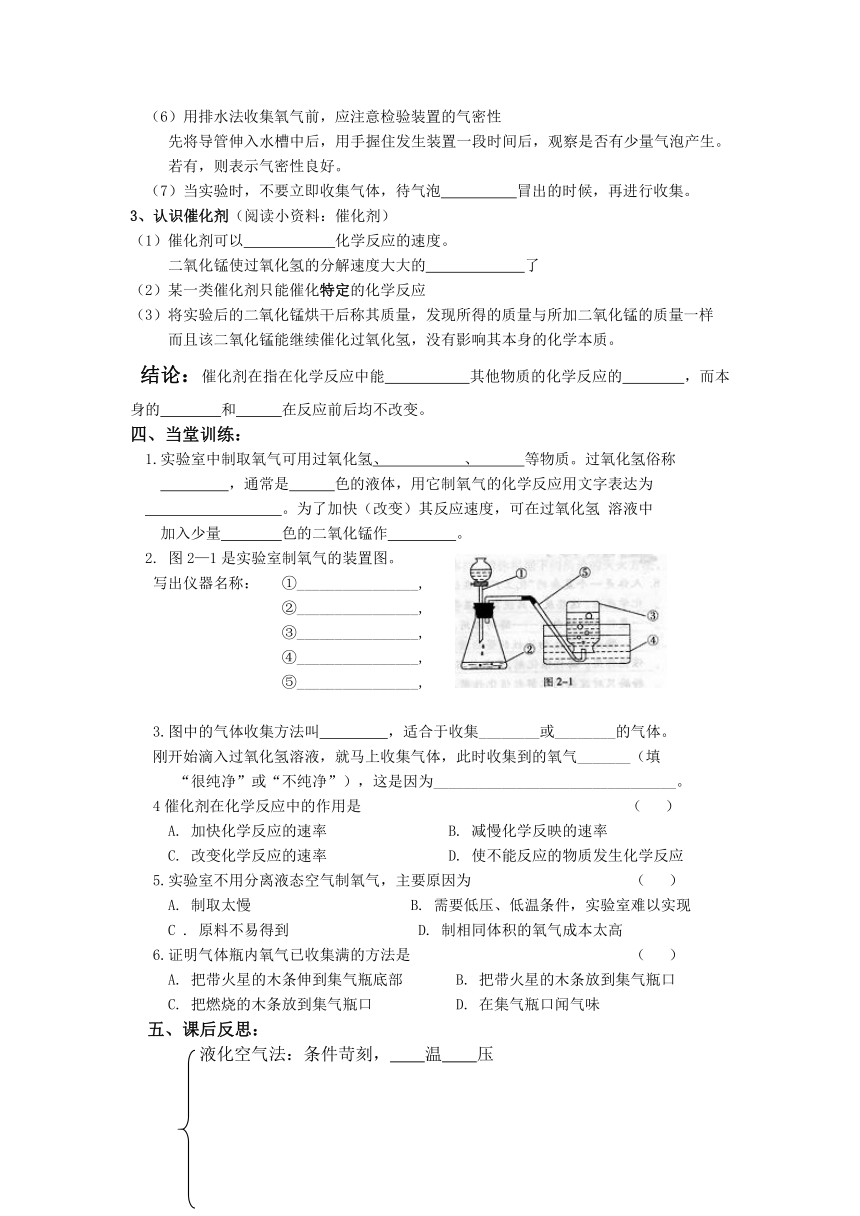
2. 图2—1是实验室制氧气的装置图。
写出仪器名称: ①________________,
②________________,
③________________,
④________________,
⑤________________,
3.图中的气体收集方法叫 ,适合于收集________或________的气体。
刚开始滴入过氧化氢溶液,就马上收集气体,此时收集到的氧气_______(填
“很纯净”或“不纯净”),这是因为________________________________。
4催化剂在化学反应中的作用是 ( )
A. 加快化学反应的速率 B. 减慢化学反映的速率
C. 改变化学反应的速率 D. 使不能反应的物质发生化学反应
5.实验室不用分离液态空气制氧气,主要原因为 ( )
A. 制取太慢 B. 需要低压、低温条件,实验室难以实现
C . 原料不易得到 D. 制相同体积的氧气成本太高
6.证明气体瓶内氧气已收集满的方法是 ( )
A. 把带火星的木条伸到集气瓶底部 B. 把带火星的木条放到集气瓶口
C. 把燃烧的木条放到集气瓶口 D. 在集气瓶口闻气味
五、课后反思:
液化空气法:条件苛刻, 温 压
二氧化锰
氧气 反应文字表达式:过氧化氢 氧气+水
实验室制法: 法收集:氧气是一种微溶于水的气体
催化剂:改变了反应速度,但在反应前后催化剂本身的质量和化学性质
六、课后作业:
1.下列物质中不宜用实验室制取氧气的是( )
A.氯酸钾 B.空气 C.空气 D.过氧化氢
2.将空气液化的条件是( )
A.高温高压 B.高温低压 C.低温高压 D.低温低压
3.实验室用过氧化氢制取氧气的装置,如图所示,当过氧化氢滴入锥形瓶中时,锥形瓶中的气体的压强( )
A.大与大气压 B.小于大气压
C.等于大气压 D.无法确定
4.上题图中锥形瓶中放入的二氧化锰的作用是 ( )
A.直接与过氧化氢反应 B.分解后放出其中的氧气
C.使过氧化氢缓慢分解 D.加快过氧化氢的分解速度
5.可用排水法收集的气体应具备的性质是( )
A.密度比水小的多 B.没有刺激性的气体 C.难溶或微溶于水 D.完全不溶于水
6.有三支相同的试管,甲中放少量的二氧化锰,乙放入一小块猪肝,丙是空的。
(1)分别向三支试管中加入2mL 过氧化氢溶液,观察到的现象是:
甲: 乙: 丙:
(2)将带火星的木条伸入三支试管,能使木条复燃的是
(3)在此实验中二氧化锰的作用是 ,猪肝的作用是
(4)比较甲与丙、甲与乙可得出的结论是
7.吃米饭多嚼会觉得甜,这是唾液中的 ,使米饭中的淀粉转化成了 的缘故。
8.收集气体的方法除了用排水法以外,气体密度比空气小的还可用向下排空气法,
气体密度比空气大的也可用向上排空气法,如图2-2所示。空气在标准状况下的密度是1.293g/L,下表中既能用排水法收集,又能用向上排空气法收集的气体是( )
9.拒报导,我国科学家经10余年攻关努力,在被称为“第四代催化剂”的纳米金属簇催化剂研究领域取得重大突破,提出用高分子保护方法制备纳米级金属胶体的新理论,找到了破解提高纳米金属簇催化效率这一世界难题的技术路径,为金属簇催化剂的加工业应用提供了坚实的理论基础和实施方案。
催化剂的研究一直是各国科学家技术竞争的主要领域,而在催化剂的研究中,如何提高催化剂效率则是这一竞争的核心问题。大量的研究结果表明,催化剂颗粒达到纳米级时会表现出独特的效应,从而导致催化火星和选择性的飞跃。
对催化剂来说,很重要的一个指标是
导致催化活性和选择性飞跃的是催化剂的颗粒必须达到 级。
10.人体是一个复杂的“化工厂”,在这个“化工厂”里,同时进行着许多互相协同配合的化学反应。这些反应只能在体温条件下温和地进行,还要求有较高的速率。这就要靠一类特殊的蛋白质-----------酶的作用
酶是具有生物活性的蛋白质,对于许多生物体内进行的复杂的放应具有很强的催化作用。 酶作催化剂,其条件温和,即不需加热;反应快,效率高;催化专一性,如淀粉酶只对淀粉的水解起催化作用。
(1)你认为在哪一温度范围内酶的活性最强(即催化效果最好)
(2)淀粉酶能否对蛋白质水解起催化作用?
第二章 §2.3 氧气(第2课时)
班级 学号 姓名
实验室制取氧气
一、学习目标:
1、初步学会实验室利用高锰酸钾制取氧气装置的装配、连接方法和气密性检查。
2、通过生活中的例子了解氧气的物理性质
3、通过活动,了解氧气的化学性质
4、通过对不同性质的比较,区分物理性质和化学性质
二、课前预习:
1、氧气可以用哪些方法来收集? , 。
2、物质的性质一般可以分为 和 ,不通过化学反应就能表现出来的性质叫 ,通过化学反应才能表现出来的性质叫 。
3、氧气是一种 色、 味, 质量的 体,密度比空气 , 溶于水,这些是氧气的 性质。
三、课内导学:
氧气是我们日常生活中不可缺少的物质,它具有广泛的用途,如急救病人、电氧焊、炼钢、登山、潜水等都需要较为纯净的氧气,如何制取氧气?通过上一节课的学习,我们知道空气中含有氧气和氮气,可以用液化空气的方法分离空气中的氮气和氧气。但需要加压和降低到很低的温度,这在实验室是很难作到的。因而我们今天就来学习一下如何在实验室制取氧气。
一、利用高锰酸钾制氧气:
1、药品:
2、原理: (表达式)
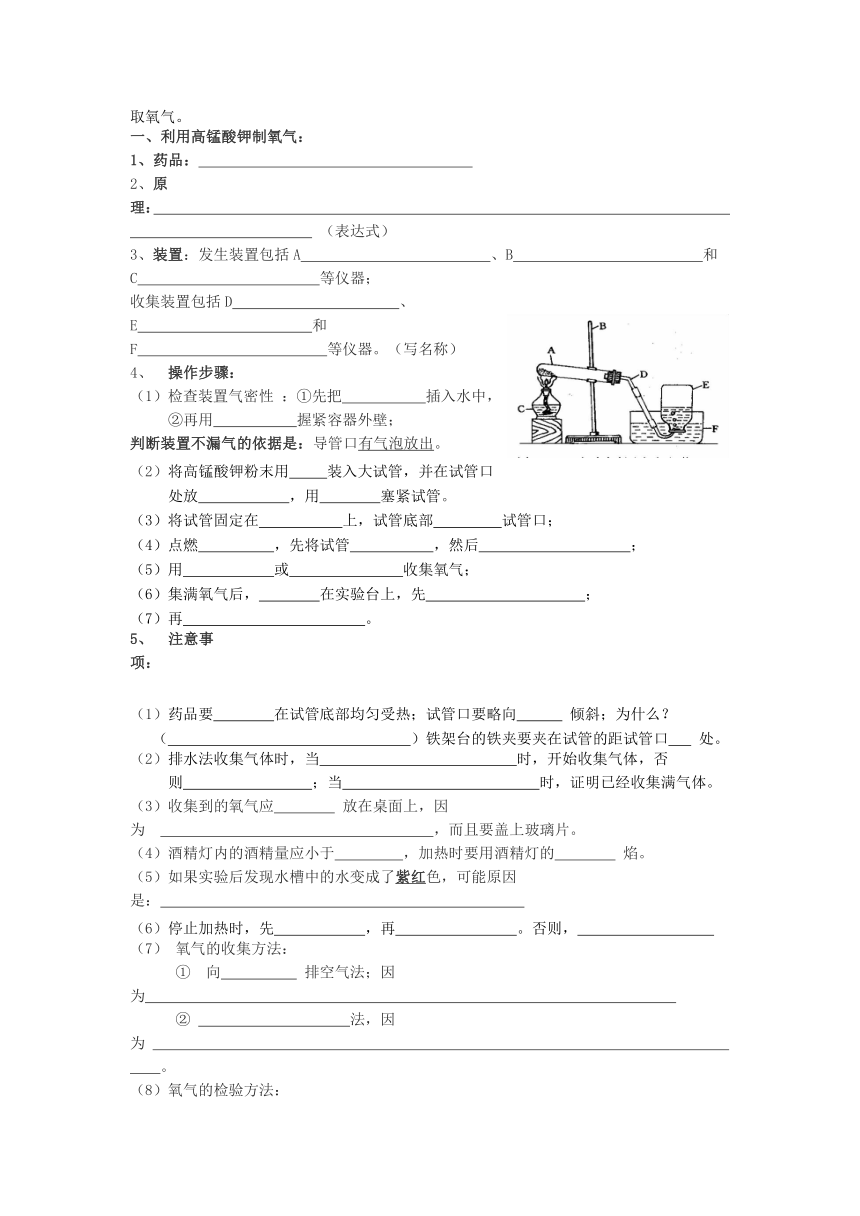
3、装置:发生装置包括A 、B 和C 等仪器;
收集装置包括D 、E 和F 等仪器。(写名称)
4、 操作步骤:
(1)检查装置气密性 :①先把 插入水中,
②再用 握紧容器外壁;
判断装置不漏气的依据是:导管口有气泡放出。
(2)将高锰酸钾粉末用 装入大试管,并在试管口
处放 ,用 塞紧试管。
(3)将试管固定在 上,试管底部 试管口;
(4)点燃 ,先将试管 ,然后 ;
(5)用 或 收集氧气;
(6)集满氧气后, 在实验台上,先 ;
(7)再 。
5、 注意事项:
(1)药品要 在试管底部均匀受热;试管口要略向 倾斜;为什么?( )铁架台的铁夹要夹在试管的距试管口 处。
(2)排水法收集气体时,当 时,开始收集气体,否
则 ;当 时,证明已经收集满气体。
(3)收集到的氧气应 放在桌面上,因为 ,而且要盖上玻璃片。
(4)酒精灯内的酒精量应小于 ,加热时要用酒精灯的 焰。
(5)如果实验后发现水槽中的水变成了紫红色,可能原因是:
(6)停止加热时,先 ,再 。否则,
(7) 氧气的收集方法:
① 向 排空气法;因为
② 法,因为 。
(8)氧气的检验方法:
用一根 的木条伸入待测气体中,如果木条 ,证明该气体是氧气。
(9)氧气的验满方法:
用一根 的木条放在集气瓶 ,如果 ,证明
二、氧气的物理性质
1、结合生活经验,小组讨论氧气的物理性质
氧气有颜色吗? 氧气的密度怎么样? 略大于空气
氧气是什么状态? 氧气的水溶性怎样?
氧气有气味吗? 其他
结论1:氧气的物理性质
1) 色、 气味的气体。
2)密度比空气 ,1.429克/升。
3)水溶性: 。
结论2:这些不需要通过化学反应就能表现出来的性质我们称之为 性质,如:颜色、状态、气味、味道、密度、水溶性等。
2、活动:怎样才能检验一种气体是否是氧气
氮气的物理性质:氮气是一种 色 味的 体,密度比空气略 , 溶于水
问题:一瓶空气、一瓶氮气和一瓶氧气怎样才能把他们区分开?
方案:将带火星的木条分别伸入三个集气瓶中,观察所发生的现象
猜想:
实验现象:在空气中: 在氮气中: 在氧气中:
结论:氧气能够使带火星的木条 ,我们可以用它来检验氧气。 像这些需要通过化学反应才能表现出来的性质,我们称之为 性质。
三、氧气的化学性质
活动:铁丝、蜡烛等分别在空气和氧气中燃烧
实验药品和器材:细铁丝、木炭、蜡烛、硫磺、氧气、细沙或水、火柴
酒精灯、集气瓶、燃烧匙、镊子
观察要点:反应物的状态和颜色,物质在空气中和氧气中燃烧分别有什么现象,有什么生成物产生以及它的状态。
观察实验,并完成下列表格
实验 主要产物 现 象
在空气中 在氧气中
铁丝燃烧
木炭燃烧
蜡烛燃烧
硫磺燃烧
木炭在氧气中燃烧文字表达式:碳(C)+ 氧气(O2)二氧化碳(CO2)
铁丝在氧气中燃烧文字表达式:铁(Fe) + 氧气(O2)四氧化三铁(Fe3O4)
蜡烛在氧气中燃烧文字表达式:石蜡+ 氧气(O2)二氧化碳(CO2)+ 水(H2O
硫磺在氧气中燃烧文字表达式:硫磺(S)+氧气(O2)二氧化硫(SO2)
讨论:为什么铁丝在点燃前要在氧气瓶的底部装有一些细沙或水?
结论:氧气能与许多物质发生反应,如氧气能与木炭、硫磺、蜡烛等 反应,同样也能和铁等 反应,而且反应程度比较剧烈,产生光和热,因此氧气是一种 的非金属 。
提问:为什么物质在氧气中反应比在空气中燃烧更剧烈呢?
四、氧气的用途
(1)供给呼吸:医疗上急救病人,登山、潜水、航空、宇航提供呼吸
(2)支持燃烧:炼钢、气焊与气接、液氧炸弹、火箭助燃剂
四、当堂训练
1.氧气的下列性质中,属于化学性质的是 ( )
A.无色无味 B.常温下是气体
C.密度比空气大 D.能使带有余烬的木条复燃
2.能区别氧气和氮气的方法是 ( )
A.闻气味 B.看颜色
C.看能否溶于水 D.将带有火星的木条分别插入两种气体中
3.水通电可以分解成氢气和氧气,这是水的 ( )
A.物理性质 B.化学性质 C.状态变化 D.汽化现象
4.硫磺在氧气中燃烧时,观察到的现象是 ( )
A.生成浓厚的烟 B.剧烈燃烧,火星四射,生成黑色固体
C.发出明亮的蓝紫色火焰 D.剧烈燃烧,发出白光
5.下列物质在氧气中燃烧时,生成黑色国体的是 ( )
A.木炭 B.铁丝 C.蜡烛 D.硫磺
6.下列有关氧气的化学性质的叙述正确的是 ( )
A.氧气是一种不活泼的非金属单质 B.氧气只能与金属发生反应
C.氧气只能与非金属发生反应 D.氧气是一种活泼的非金属单质
7.物质的物理性质有 、 、 、 、 、 等,物理性质不需要通过化学反应就能表现出来
8.实验室制取氧气时,装药品的大试管口应 ( )
(A)朝下 (B)朝上 (C)略向下倾斜 (D)略向上倾斜
9.实验室采用排水法收集氧气时,需将导气管伸入盛满水的集气瓶,这个操作应在( )
(A)加热固体药品前 (B)与加热固体药品同时
(C)开始有气泡放出时 (D)气泡连续并均匀放出时
10.在实验室里,我们通常用加热 或用
和 混和的方法来制取氧气。由于氧气 溶于水,因此可以用 收集;又因为氧气的密度比空气 ,因此又可以用 法收集。
五、学后反思:
六、课后作业:
1、下列有关实验室制取氧气的说法中不正确的是 ( )
A.固体药品应平铺在试管底部 B. 酒精灯里的酒精的量不能超过其容积的三分之二
C.应用酒精灯的外焰加热 D.用排水集气法收集氧气时先停止加热,再从水中取出导管。
2、在实验室用高锰酸钾受热分解制氧气时,试管口略微向下倾斜的原因是( )
A.氧气的密度大,易导出 B、防止药品中水分挥发在试管口冷凝倒流,导致试管炸裂
C、试管底部高,便于加热 D.可以产生较多的氧气
3、下列变化是化学变化的是( )
A.工业上分离空气制取氧气 B.冰融化成水
C.高锰酸钾受热分解 D.汽油挥发
4、下列物质中含有氧气的是( )
A、二氧化锰 B、过氧化氢 C、空气 D、高锰酸钾
5、如下图所示的装置中,其中收集氧气时可选用( )
A.①和② B.②和③ C.①和④ D.①和⑤
6、某气体既能用排水法收集,又能用向上排空气法收集,则该气体具有的物理性质( )
A.难溶于水,密度比空气密度大 B.难溶于水,密度比空气密度小
C.易溶于水,密度比空气密度大 D.易溶于水,密度比空气密度小
7. 下列气体中,不可以用排水法收集的气体是( )
A.氧气 B.氢气 C.二氧化碳 D.甲烷
标准状况下密度 1.429克/升 0.089克/升 1.978克/升 0.714克/升
在水中的溶解性 不易溶于水 难溶于水 能溶于水 难溶于水
8、如图所示,过氧化氢(H2O2)在催化剂二氧化锰的作用下,迅速分解放出大量氧气。下列现象正确的是 ( )
A.气球胀大,红墨水左移 B.气球缩小,红墨水右移
C.气球胀大,红墨水右移 D.气球缩小,红墨水左移
9、用向上排空气法收集氧气时,验满的方法是 ( )
A.看集气瓶周围是否有气泡冒出
B.用带火星的木条伸入集气瓶中,看是否复燃
C.用燃烧的木条伸入集气瓶中,看燃烧是否更旺
D.用带火星的木条放在集气瓶口,看是否复燃
10.右图是小涵同学在实验室用高锰酸钾制取氧气的装置,指出图中错在哪里、错误的后果及改正方法。
5.物质的化学性质是指通过 才能表现出来的性质,如 等。
6.乙炔在氧气中燃烧产生的高温可用于 ,液氢在液氧中燃烧可产生巨大的能量,故液氢可用做 。
7.下列关于氧气性质的叙述错误的是( )
A.氧气具有可燃性 B.标准情况下,氧气的密度略大于空气
C.氧气不易溶于水 D.通常情况下,氧气是无色、无味的气体
8.下列关于物质在氧气中燃烧现象的描述错误的是( )
A.木炭在氧气中燃烧,有黑烟生成
B.细铁丝在氧气中燃烧,有黑色固体生成
C.蜡烛在氧气中燃烧,瓶壁有水雾出现
D.红磷在氧气中燃烧,有大量的白烟生成
9.将带火星的木条插入一瓶无色的气体中,木条复燃。说明瓶中的这种气体可能是( )
A.氮气 B.氧气
C.空气 D.二氧化碳
10.下列说法正确的是( )
A.氧气是一种可燃物,可以作燃料
B.液氢既液态的氢气,可用做航天飞机的燃料
C.乙炔能在氧气中燃烧产生高温,这是乙炔的物理性质
D.氧气能供人呼吸,这是氧气的物理性质之一
11.下列现象可用氧气的物理性质解释的是( )
A.白磷在40℃时即可燃烧,烈日下白磷不经点燃就可燃烧
B.铁丝在氧气中燃烧,火星四射
C.实验室制取氧气时,最好用排水法而不用向上排空气法收集
D.氧气可以使带火星的木条复燃。
12.要除去密封容器内空气中的氧气,并不混入其他气体,可燃物应选用 ( )
A. 硫 B. 木炭
C. 磷 D. 蜡烛
13. 1777年舍勒在《火与空气》一书中指出:空气由两种物质不同的"火空气"和"浊空
气"组成,其中"火空气"可以帮助燃烧,维持生命.下列物质不能与"火空气"发生反应
的是 ( )
A. 木炭 B.石蜡 C. 水 D. 酒精
14.实验操作时,我们要注意许多细节问题,如:
(1) 铁丝在氧气中燃烧时,放出大量的热,能使铁丝熔化。所以,在做铁丝在氧气中
的燃烧实验时,集气瓶底要放少量水或沙,这是为了_____________________
_________________________。
(2)用排水法收集氧气时,集气瓶内必须先盛满水,在水槽中倒置后,瓶中不留
气泡。这是为了___________________________________________________。
(3)用过氧化氢制氧气时,分液漏斗中的过氧化氢水溶液必须缓缓地滴入锥形瓶中。
这是为了__________________________________________________________。
15、通过燃烧除去密闭容器中的氧气,且不产生其它气体,可选用的物质是( )
A、红磷 B、蜡烛
C、木炭 D、煤
16、下列物质在氧气中燃烧时,产生有刺激性气味的气体的是 ( )
A、镁带 B、红磷
C、硫粉 D、铁丝
17、做细铁丝在氧气中燃烧的实验时,操作或现象不正确的是 ( )
A、先在酒精灯上加热细铁丝
B、盛氧气的集气瓶底没有水或沙子
C、生成物为黑色固体
D、剧烈燃烧、火星四射、放出热量5.
18、A—E是描述一些物质在氧气中燃烧时发生的现象,选择正确的序号填在后面的括号内
(1)铁丝在氧气中剧烈燃烧。( ) (2)硫在氧气中燃烧。 ( )
(3)碳在氧气中燃烧。( )
A.发出白光 B.发出微弱的淡蓝色火焰 C、火星四射
D、有水雾生成 E.发出明亮的蓝紫色火焰
19、现有A、B、C、D四种物质。A是无色无味的气体,B在A中剧烈燃烧,火星四射,放出大量热,同时生成一种黑色固体C。D是一种无色的气体,把D通入澄清的石灰水中,石灰水变浑浊。试判断A、B、C、D各是什么物质,请将答案填在空格内:
A是 ;B是 ;C是 ;D是 。
20、阅读下面科普短文,然后回答问题。
臭氧在通常状况下是淡蓝色,有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成氧气,并放出大量的热。臭氧的氧化能力比氧气强得多。
臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害,它是一切生命的保护层。超音速飞机排出的废气中有一氧化碳、二氧化碳、一氧化氮等气体,家用电冰箱中的制冷剂“氟里昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加。如不采取措施,后果不堪设想。
氧气和臭氧是不是同种物质?
(2)将带火星的木条伸入盛有臭氧的集气瓶中可以观察到的现象是什么?
[ (3)应采取什么方法保护臭氧层? 。
第二章 第三节 氧气(第3课时)
(一)学习目标
1、能比较燃烧、缓慢氧化的异同点。
2、了解燃烧的条件。
3、根据燃烧条件明确灭火方法。
4、了解火灾自救的一办方法。
(二)课前预习:
1、燃烧是指可燃物跟氧气发生的一种 、 、的 反应。可燃物燃烧所需的最低温度叫 。
2、燃烧需要三个基本条件: 、 、 。缺少其中的任何一个条件,燃烧都 (填“能"或“不能”)发生。
3、灭火的方法有: 、 、 。
4、常用的灭火器有 、 、和 。
当图书馆、档案室等处发生火灾时,可以用 灭火器灭火。
(三)课内导学
一、燃烧和缓慢氧化
1、燃烧的概念:燃烧是指可燃物跟氧气发生的一种 、 的氧化反应。
2、燃烧的条件P57
1)用坩锅钳或镊子夹取分别蘸有酒精、水的小棉花球放到酒精灯火焰上片刻,观察实验现象 。
2)用坩锅钳或镊子分别夹取干的、蘸有水的小棉花球,放到酒精灯火焰上片刻,观察实验现象 。
点燃酒精灯,再小心地盖上酒精灯帽,观察实验现象。
。
总结燃烧必须同事满足三个条件:
一是要有 :二是要有 :三是要达到 。
3、缓慢氧化:
1)概念:速率比较缓慢的氧化叫缓慢氧化。如生物呼吸、钢铁生锈都是缓慢氧化。
(氧化反应就是物质与氧发生的反应。)
2)缓慢氧化的特点:速率缓慢,不 但 。
4、燃烧和缓慢氧化的比较:
相同点:都是 反应,都能 热。
不同点:缓慢氧化速率缓慢,不能 ,燃烧反应速率剧烈,能 。
灭火的一般方法
根据可燃物燃烧的条件可知灭火的一般方法:
。
。
生活中发生火灾时常用水来灭火,其理由是:
。
。
议一议 下列情况着火时该怎么办?并说出以下灭火方法的原理。
烧菜时油锅着火怎么办?
建筑物着火怎么办?
文件档案、精密仪器着火怎么办?
想一想 水是否在任何情况下都能灭火?
常见灭火器介绍
常见灭火器有 、 、 、 。当图书馆、档案室等处发生火灾时,可以用 灭火器来灭火。
火灾自救
发生火灾时,要保持镇定,先 ,然后 。如果火势扩散,应尽快通知家人和邻居设法离开现场,沿途要关上大门,以 ,切勿乘电梯以免 。
。如果无法离开现场,应采取下列措施:
室内浓烟密布时,应 在地上爬行及用 掩住口鼻。
用 等物品塞住门和窗户的缝隙,以免浓烟呛人。
打开 ,呼救。
当堂训练
燃烧需要三个基本条件: 、 、 。缺少其中的任何一个条件,燃烧都 (填“能"或“不能”)发生。
2.灭火,即不让燃烧继续发生,可采法有 。
森林严禁用火,一单森林着火,灭火的方式多种多样。请你根据下列所给的灭火方法,说明相应的灭火原理。
有水源的地方用水浇灭。原理: 。
用鼓风机的强风吹灭。原理: 。
用树枝拍打将火打灭。原理: 。
用飞机投放干粉将火熄灭。原理: 。
在火场边缘将树木砍光,以防过火。原理: 。
使白磷燃烧的最低温度是40。C,紅磷燃燒的最低温度是240。C.图2-3中一小块白磷a和少量红磷b放在烧杯上方的薄铜片上,还有一小块白磷c放在80。C的水中稍过一会儿,可看到现象是a ,b ,c ..(填"燃烧",或"不燃烧").如果用一根导管向白磷c吹空气(与c接触),则可看到的 ,通过上述实验可知,白磷应保存在 .
常用的灭火器类型: , , .
课后反思
燃烧需要三个基本条件: 、 、 。
灭火的方法有: 、 、 。
常见灭器有 、 、 、 。
六.课后作业:
1、烧菜锅中的油着火,熄灭的最好方法是( )
A、浇水 B、撒沙土 C、盖上锅盖 D、使用灭火器
2、下列说法错误的是( )
A、木炭在氧气中燃烧比在空气中更旺,同时发出白光,生成二氧化碳
B、细铁丝在氧气里燃烧,火星四射,生成黑色的四氧化三铁
C、用灯帽盖灭酒精灯火焰,其目的使酒精隔绝空气而灭火
D、要达到灭火的目的,一定要在隔绝空气的同时,降低燃烧物的着火点
3、1994年12月8日,在克拉玛依友谊宫火灾中,有288名中学生和37名教师葬身火海。为此,我们每个人都要懂得消防知识,学会逃生。如果遇上高层楼房的下层起火,火势凶猛无法扑灭时,上层的人逃生措施正确的是( )
①沿楼道迅速下楼;②用湿毛巾堵住口鼻;③匍匐前进,寻找安全出口;④封闭房门;⑤迅速转移至阳台,用绳索下坠;⑥跳楼。
A、①②③④ B、③④⑤⑥ C、②③④⑤ D、①②④⑤
4、下列不属于燃烧条件的是( )
A、可燃物 B、温度
C、氧气(空气) D、接触面积大小
5、酒精可以点燃,但放在敞口容器里的酒精并不会自行燃烧起来,这主要是因为
( )
A、容器里没有空气 B、室温比酒精的燃点低得多
C、酒精是一种难燃的物质 D、容器里的酒精质量太少
6、下列物质中不属于易燃易爆物的是( )
A、氮气 B、白磷 C、液化气 D、汽油
7、某人救火,身上的衣服被烧起来,这时可采取的方法是( )
①跳入河中,或用自来水冲。 ②用被子将这个人裹起来
③就地打滚 ④向这个人喷二氧化碳
A、①④ B、②③ C、②④ D、①②③
8、酒精灯不能用嘴吹灭,而要用灯帽盖灭,从灭火原理分析,这是( )
A、降低温度 B、消除可燃物
C、隔绝空气 D、降低酒精的着火点
9、交通部门规定,乘坐车船时不能带易燃易爆物品,鞭炮是禁止携带的物品之一,这是因为车子开动时( )
A、鞭炮的着火点会升高
B、鞭炮着火点会降低
C、振动使鞭炮温度升高,达到燃点引起爆炸
D、鞭炮会损坏
10、蜡烛火焰用嘴一吹就熄灭。关于火焰熄灭的原因,小明与小东各有解释。
小明认为:人吹出来的是二氧化碳,二氧化碳吹到火焰上,灯芯因缺氧而停止燃烧。小东则认为:人吹出来的气中含有很多氧气,不足以使火焰熄灭,火焰熄灭的主要原因是人吹出的气流带走了灯芯的很多热量,从而使灯芯的温度降低,温度低于燃烧的最低温度时,火焰就熄灭。
你支持谁的观点?谈一谈你的看法
如何证明小东说的“人吹出来的气中含有许多氧气”?想一个简单的实验加以证明。
有一个棉花仓库起火,在消防车还未来到之前,很多人想取灭火,但仓库管理员不准开仓库门。你认为这位仓库管理员的做法有没有道理?说一说你的理由。
当你在电影院、商场等人口密集的地方遭遇火灾时,应怎样自救?
班级 学号 姓名
一、学习目标:
1、通过活动让学生了解实验室制取氧气的方法
2、通过对比实验,让学生知道制取氧气时二氧化锰是一种催化剂,并了解催化剂的特点
3、通过实验装置,让学生了解实验仪器、装置的连接以及实验过程中的注意事项
4、通过课外实验,让学生了解排水法收集气体的方法。
二、课前预习:
1、液化空气的方法分离空气中的氧气需要 的压强和 的温度,在实验室里很难完成
2、实验室中可以利用 、 、 等物质来制取氧气。
3、二氧化锰在分解过氧化氢制取氧气的实验中起到了 的作用,从而 了过氧化氢的分解速度。
4、过氧化氢分解制取氧气的文字表达式:
5、 氧气可以用 方法来收集,说明氧气是一种 的气体。
三、课内导学:
1、液化空气(低温高压):分离空气中的 和 。
2、实验室制取氧气(分解过氧化氢H2O2或加热分解高锰酸钾)
活动1:分解过氧化氢制取氧气
1.取三支洁净的试管
(1)向第一支试管中加入少量过氧化氢溶液,你观察到的现象是:
(2)向第一支试管中加入少量过氧化氢溶液,再加入少量二氧化锰粉末,你观察到的现象:
(3)向第一支试管中加入少量过氧化氢溶液,再加入一小块猪肝,你观察到的现象是:
2.当上述第二和第三支试管中加入有关物质后,在试管中伸入带火星的木条,可以观察到的现象是: ,推测从第二和第三支试管中放出的气体可能是 ,二氧化锰和猪肝的作用是 ,比较上述三种方法,其中更适合于在实验室制取氧气的方法是 。并说出你的理由:
3.分解过氧化氢制取氧气
(1)区分发生装置和收集装置
(2)认识仪器:① ②
③ ④ ⑤
①中装有 ,②中装有
(3)过氧化氢分解制取氧气的文字表达式:
(4)收集氧气的方法是 法,而排水法是收集微溶于水或难溶于水的气体,说明氧气是一种 于水的气体(不易溶、易溶)
(5)怎样检验收集的气体为氧气?
(6)用排水法收集氧气前,应注意检验装置的气密性
先将导管伸入水槽中后,用手握住发生装置一段时间后,观察是否有少量气泡产生。若有,则表示气密性良好。
(7)当实验时,不要立即收集气体,待气泡 冒出的时候,再进行收集。
3、认识催化剂(阅读小资料:催化剂)
(1)催化剂可以 化学反应的速度。
二氧化锰使过氧化氢的分解速度大大的 了
(2)某一类催化剂只能催化特定的化学反应
(3)将实验后的二氧化锰烘干后称其质量,发现所得的质量与所加二氧化锰的质量一样
而且该二氧化锰能继续催化过氧化氢,没有影响其本身的化学本质。
结论:催化剂在指在化学反应中能 其他物质的化学反应的 ,而本身的 和 在反应前后均不改变。
四、当堂训练:
1.实验室中制取氧气可用过氧化氢、 、 等物质。过氧化氢俗称
,通常是 色的液体,用它制氧气的化学反应用文字表达为
。为了加快(改变)其反应速度,可在过氧化氢 溶液中
加入少量 色的二氧化锰作 。
2. 图2—1是实验室制氧气的装置图。
写出仪器名称: ①________________,
②________________,
③________________,
④________________,
⑤________________,
3.图中的气体收集方法叫 ,适合于收集________或________的气体。
刚开始滴入过氧化氢溶液,就马上收集气体,此时收集到的氧气_______(填
“很纯净”或“不纯净”),这是因为________________________________。
4催化剂在化学反应中的作用是 ( )
A. 加快化学反应的速率 B. 减慢化学反映的速率
C. 改变化学反应的速率 D. 使不能反应的物质发生化学反应
5.实验室不用分离液态空气制氧气,主要原因为 ( )
A. 制取太慢 B. 需要低压、低温条件,实验室难以实现
C . 原料不易得到 D. 制相同体积的氧气成本太高
6.证明气体瓶内氧气已收集满的方法是 ( )
A. 把带火星的木条伸到集气瓶底部 B. 把带火星的木条放到集气瓶口
C. 把燃烧的木条放到集气瓶口 D. 在集气瓶口闻气味
五、课后反思:
液化空气法:条件苛刻, 温 压
二氧化锰
氧气 反应文字表达式:过氧化氢 氧气+水
实验室制法: 法收集:氧气是一种微溶于水的气体
催化剂:改变了反应速度,但在反应前后催化剂本身的质量和化学性质
六、课后作业:
1.下列物质中不宜用实验室制取氧气的是( )
A.氯酸钾 B.空气 C.空气 D.过氧化氢
2.将空气液化的条件是( )
A.高温高压 B.高温低压 C.低温高压 D.低温低压
3.实验室用过氧化氢制取氧气的装置,如图所示,当过氧化氢滴入锥形瓶中时,锥形瓶中的气体的压强( )
A.大与大气压 B.小于大气压
C.等于大气压 D.无法确定
4.上题图中锥形瓶中放入的二氧化锰的作用是 ( )
A.直接与过氧化氢反应 B.分解后放出其中的氧气
C.使过氧化氢缓慢分解 D.加快过氧化氢的分解速度
5.可用排水法收集的气体应具备的性质是( )
A.密度比水小的多 B.没有刺激性的气体 C.难溶或微溶于水 D.完全不溶于水
6.有三支相同的试管,甲中放少量的二氧化锰,乙放入一小块猪肝,丙是空的。
(1)分别向三支试管中加入2mL 过氧化氢溶液,观察到的现象是:
甲: 乙: 丙:
(2)将带火星的木条伸入三支试管,能使木条复燃的是
(3)在此实验中二氧化锰的作用是 ,猪肝的作用是
(4)比较甲与丙、甲与乙可得出的结论是
7.吃米饭多嚼会觉得甜,这是唾液中的 ,使米饭中的淀粉转化成了 的缘故。
8.收集气体的方法除了用排水法以外,气体密度比空气小的还可用向下排空气法,
气体密度比空气大的也可用向上排空气法,如图2-2所示。空气在标准状况下的密度是1.293g/L,下表中既能用排水法收集,又能用向上排空气法收集的气体是( )
9.拒报导,我国科学家经10余年攻关努力,在被称为“第四代催化剂”的纳米金属簇催化剂研究领域取得重大突破,提出用高分子保护方法制备纳米级金属胶体的新理论,找到了破解提高纳米金属簇催化效率这一世界难题的技术路径,为金属簇催化剂的加工业应用提供了坚实的理论基础和实施方案。
催化剂的研究一直是各国科学家技术竞争的主要领域,而在催化剂的研究中,如何提高催化剂效率则是这一竞争的核心问题。大量的研究结果表明,催化剂颗粒达到纳米级时会表现出独特的效应,从而导致催化火星和选择性的飞跃。
对催化剂来说,很重要的一个指标是
导致催化活性和选择性飞跃的是催化剂的颗粒必须达到 级。
10.人体是一个复杂的“化工厂”,在这个“化工厂”里,同时进行着许多互相协同配合的化学反应。这些反应只能在体温条件下温和地进行,还要求有较高的速率。这就要靠一类特殊的蛋白质-----------酶的作用
酶是具有生物活性的蛋白质,对于许多生物体内进行的复杂的放应具有很强的催化作用。 酶作催化剂,其条件温和,即不需加热;反应快,效率高;催化专一性,如淀粉酶只对淀粉的水解起催化作用。
(1)你认为在哪一温度范围内酶的活性最强(即催化效果最好)
(2)淀粉酶能否对蛋白质水解起催化作用?
第二章 §2.3 氧气(第2课时)
班级 学号 姓名
实验室制取氧气
一、学习目标:
1、初步学会实验室利用高锰酸钾制取氧气装置的装配、连接方法和气密性检查。
2、通过生活中的例子了解氧气的物理性质
3、通过活动,了解氧气的化学性质
4、通过对不同性质的比较,区分物理性质和化学性质
二、课前预习:
1、氧气可以用哪些方法来收集? , 。
2、物质的性质一般可以分为 和 ,不通过化学反应就能表现出来的性质叫 ,通过化学反应才能表现出来的性质叫 。
3、氧气是一种 色、 味, 质量的 体,密度比空气 , 溶于水,这些是氧气的 性质。
三、课内导学:
氧气是我们日常生活中不可缺少的物质,它具有广泛的用途,如急救病人、电氧焊、炼钢、登山、潜水等都需要较为纯净的氧气,如何制取氧气?通过上一节课的学习,我们知道空气中含有氧气和氮气,可以用液化空气的方法分离空气中的氮气和氧气。但需要加压和降低到很低的温度,这在实验室是很难作到的。因而我们今天就来学习一下如何在实验室制取氧气。
一、利用高锰酸钾制氧气:
1、药品:
2、原理: (表达式)
3、装置:发生装置包括A 、B 和C 等仪器;
收集装置包括D 、E 和F 等仪器。(写名称)
4、 操作步骤:
(1)检查装置气密性 :①先把 插入水中,
②再用 握紧容器外壁;
判断装置不漏气的依据是:导管口有气泡放出。
(2)将高锰酸钾粉末用 装入大试管,并在试管口
处放 ,用 塞紧试管。
(3)将试管固定在 上,试管底部 试管口;
(4)点燃 ,先将试管 ,然后 ;
(5)用 或 收集氧气;
(6)集满氧气后, 在实验台上,先 ;
(7)再 。
5、 注意事项:
(1)药品要 在试管底部均匀受热;试管口要略向 倾斜;为什么?( )铁架台的铁夹要夹在试管的距试管口 处。
(2)排水法收集气体时,当 时,开始收集气体,否
则 ;当 时,证明已经收集满气体。
(3)收集到的氧气应 放在桌面上,因为 ,而且要盖上玻璃片。
(4)酒精灯内的酒精量应小于 ,加热时要用酒精灯的 焰。
(5)如果实验后发现水槽中的水变成了紫红色,可能原因是:
(6)停止加热时,先 ,再 。否则,
(7) 氧气的收集方法:
① 向 排空气法;因为
② 法,因为 。
(8)氧气的检验方法:
用一根 的木条伸入待测气体中,如果木条 ,证明该气体是氧气。
(9)氧气的验满方法:
用一根 的木条放在集气瓶 ,如果 ,证明
二、氧气的物理性质
1、结合生活经验,小组讨论氧气的物理性质
氧气有颜色吗? 氧气的密度怎么样? 略大于空气
氧气是什么状态? 氧气的水溶性怎样?
氧气有气味吗? 其他
结论1:氧气的物理性质
1) 色、 气味的气体。
2)密度比空气 ,1.429克/升。
3)水溶性: 。
结论2:这些不需要通过化学反应就能表现出来的性质我们称之为 性质,如:颜色、状态、气味、味道、密度、水溶性等。
2、活动:怎样才能检验一种气体是否是氧气
氮气的物理性质:氮气是一种 色 味的 体,密度比空气略 , 溶于水
问题:一瓶空气、一瓶氮气和一瓶氧气怎样才能把他们区分开?
方案:将带火星的木条分别伸入三个集气瓶中,观察所发生的现象
猜想:
实验现象:在空气中: 在氮气中: 在氧气中:
结论:氧气能够使带火星的木条 ,我们可以用它来检验氧气。 像这些需要通过化学反应才能表现出来的性质,我们称之为 性质。
三、氧气的化学性质
活动:铁丝、蜡烛等分别在空气和氧气中燃烧
实验药品和器材:细铁丝、木炭、蜡烛、硫磺、氧气、细沙或水、火柴
酒精灯、集气瓶、燃烧匙、镊子
观察要点:反应物的状态和颜色,物质在空气中和氧气中燃烧分别有什么现象,有什么生成物产生以及它的状态。
观察实验,并完成下列表格
实验 主要产物 现 象
在空气中 在氧气中
铁丝燃烧
木炭燃烧
蜡烛燃烧
硫磺燃烧
木炭在氧气中燃烧文字表达式:碳(C)+ 氧气(O2)二氧化碳(CO2)
铁丝在氧气中燃烧文字表达式:铁(Fe) + 氧气(O2)四氧化三铁(Fe3O4)
蜡烛在氧气中燃烧文字表达式:石蜡+ 氧气(O2)二氧化碳(CO2)+ 水(H2O
硫磺在氧气中燃烧文字表达式:硫磺(S)+氧气(O2)二氧化硫(SO2)
讨论:为什么铁丝在点燃前要在氧气瓶的底部装有一些细沙或水?
结论:氧气能与许多物质发生反应,如氧气能与木炭、硫磺、蜡烛等 反应,同样也能和铁等 反应,而且反应程度比较剧烈,产生光和热,因此氧气是一种 的非金属 。
提问:为什么物质在氧气中反应比在空气中燃烧更剧烈呢?
四、氧气的用途
(1)供给呼吸:医疗上急救病人,登山、潜水、航空、宇航提供呼吸
(2)支持燃烧:炼钢、气焊与气接、液氧炸弹、火箭助燃剂
四、当堂训练
1.氧气的下列性质中,属于化学性质的是 ( )
A.无色无味 B.常温下是气体
C.密度比空气大 D.能使带有余烬的木条复燃
2.能区别氧气和氮气的方法是 ( )
A.闻气味 B.看颜色
C.看能否溶于水 D.将带有火星的木条分别插入两种气体中
3.水通电可以分解成氢气和氧气,这是水的 ( )
A.物理性质 B.化学性质 C.状态变化 D.汽化现象
4.硫磺在氧气中燃烧时,观察到的现象是 ( )
A.生成浓厚的烟 B.剧烈燃烧,火星四射,生成黑色固体
C.发出明亮的蓝紫色火焰 D.剧烈燃烧,发出白光
5.下列物质在氧气中燃烧时,生成黑色国体的是 ( )
A.木炭 B.铁丝 C.蜡烛 D.硫磺
6.下列有关氧气的化学性质的叙述正确的是 ( )
A.氧气是一种不活泼的非金属单质 B.氧气只能与金属发生反应
C.氧气只能与非金属发生反应 D.氧气是一种活泼的非金属单质
7.物质的物理性质有 、 、 、 、 、 等,物理性质不需要通过化学反应就能表现出来
8.实验室制取氧气时,装药品的大试管口应 ( )
(A)朝下 (B)朝上 (C)略向下倾斜 (D)略向上倾斜
9.实验室采用排水法收集氧气时,需将导气管伸入盛满水的集气瓶,这个操作应在( )
(A)加热固体药品前 (B)与加热固体药品同时
(C)开始有气泡放出时 (D)气泡连续并均匀放出时
10.在实验室里,我们通常用加热 或用
和 混和的方法来制取氧气。由于氧气 溶于水,因此可以用 收集;又因为氧气的密度比空气 ,因此又可以用 法收集。
五、学后反思:
六、课后作业:
1、下列有关实验室制取氧气的说法中不正确的是 ( )
A.固体药品应平铺在试管底部 B. 酒精灯里的酒精的量不能超过其容积的三分之二
C.应用酒精灯的外焰加热 D.用排水集气法收集氧气时先停止加热,再从水中取出导管。
2、在实验室用高锰酸钾受热分解制氧气时,试管口略微向下倾斜的原因是( )
A.氧气的密度大,易导出 B、防止药品中水分挥发在试管口冷凝倒流,导致试管炸裂
C、试管底部高,便于加热 D.可以产生较多的氧气
3、下列变化是化学变化的是( )
A.工业上分离空气制取氧气 B.冰融化成水
C.高锰酸钾受热分解 D.汽油挥发
4、下列物质中含有氧气的是( )
A、二氧化锰 B、过氧化氢 C、空气 D、高锰酸钾
5、如下图所示的装置中,其中收集氧气时可选用( )
A.①和② B.②和③ C.①和④ D.①和⑤
6、某气体既能用排水法收集,又能用向上排空气法收集,则该气体具有的物理性质( )
A.难溶于水,密度比空气密度大 B.难溶于水,密度比空气密度小
C.易溶于水,密度比空气密度大 D.易溶于水,密度比空气密度小
7. 下列气体中,不可以用排水法收集的气体是( )
A.氧气 B.氢气 C.二氧化碳 D.甲烷
标准状况下密度 1.429克/升 0.089克/升 1.978克/升 0.714克/升
在水中的溶解性 不易溶于水 难溶于水 能溶于水 难溶于水
8、如图所示,过氧化氢(H2O2)在催化剂二氧化锰的作用下,迅速分解放出大量氧气。下列现象正确的是 ( )
A.气球胀大,红墨水左移 B.气球缩小,红墨水右移
C.气球胀大,红墨水右移 D.气球缩小,红墨水左移
9、用向上排空气法收集氧气时,验满的方法是 ( )
A.看集气瓶周围是否有气泡冒出
B.用带火星的木条伸入集气瓶中,看是否复燃
C.用燃烧的木条伸入集气瓶中,看燃烧是否更旺
D.用带火星的木条放在集气瓶口,看是否复燃
10.右图是小涵同学在实验室用高锰酸钾制取氧气的装置,指出图中错在哪里、错误的后果及改正方法。
5.物质的化学性质是指通过 才能表现出来的性质,如 等。
6.乙炔在氧气中燃烧产生的高温可用于 ,液氢在液氧中燃烧可产生巨大的能量,故液氢可用做 。
7.下列关于氧气性质的叙述错误的是( )
A.氧气具有可燃性 B.标准情况下,氧气的密度略大于空气
C.氧气不易溶于水 D.通常情况下,氧气是无色、无味的气体
8.下列关于物质在氧气中燃烧现象的描述错误的是( )
A.木炭在氧气中燃烧,有黑烟生成
B.细铁丝在氧气中燃烧,有黑色固体生成
C.蜡烛在氧气中燃烧,瓶壁有水雾出现
D.红磷在氧气中燃烧,有大量的白烟生成
9.将带火星的木条插入一瓶无色的气体中,木条复燃。说明瓶中的这种气体可能是( )
A.氮气 B.氧气
C.空气 D.二氧化碳
10.下列说法正确的是( )
A.氧气是一种可燃物,可以作燃料
B.液氢既液态的氢气,可用做航天飞机的燃料
C.乙炔能在氧气中燃烧产生高温,这是乙炔的物理性质
D.氧气能供人呼吸,这是氧气的物理性质之一
11.下列现象可用氧气的物理性质解释的是( )
A.白磷在40℃时即可燃烧,烈日下白磷不经点燃就可燃烧
B.铁丝在氧气中燃烧,火星四射
C.实验室制取氧气时,最好用排水法而不用向上排空气法收集
D.氧气可以使带火星的木条复燃。
12.要除去密封容器内空气中的氧气,并不混入其他气体,可燃物应选用 ( )
A. 硫 B. 木炭
C. 磷 D. 蜡烛
13. 1777年舍勒在《火与空气》一书中指出:空气由两种物质不同的"火空气"和"浊空
气"组成,其中"火空气"可以帮助燃烧,维持生命.下列物质不能与"火空气"发生反应
的是 ( )
A. 木炭 B.石蜡 C. 水 D. 酒精
14.实验操作时,我们要注意许多细节问题,如:
(1) 铁丝在氧气中燃烧时,放出大量的热,能使铁丝熔化。所以,在做铁丝在氧气中
的燃烧实验时,集气瓶底要放少量水或沙,这是为了_____________________
_________________________。
(2)用排水法收集氧气时,集气瓶内必须先盛满水,在水槽中倒置后,瓶中不留
气泡。这是为了___________________________________________________。
(3)用过氧化氢制氧气时,分液漏斗中的过氧化氢水溶液必须缓缓地滴入锥形瓶中。
这是为了__________________________________________________________。
15、通过燃烧除去密闭容器中的氧气,且不产生其它气体,可选用的物质是( )
A、红磷 B、蜡烛
C、木炭 D、煤
16、下列物质在氧气中燃烧时,产生有刺激性气味的气体的是 ( )
A、镁带 B、红磷
C、硫粉 D、铁丝
17、做细铁丝在氧气中燃烧的实验时,操作或现象不正确的是 ( )
A、先在酒精灯上加热细铁丝
B、盛氧气的集气瓶底没有水或沙子
C、生成物为黑色固体
D、剧烈燃烧、火星四射、放出热量5.
18、A—E是描述一些物质在氧气中燃烧时发生的现象,选择正确的序号填在后面的括号内
(1)铁丝在氧气中剧烈燃烧。( ) (2)硫在氧气中燃烧。 ( )
(3)碳在氧气中燃烧。( )
A.发出白光 B.发出微弱的淡蓝色火焰 C、火星四射
D、有水雾生成 E.发出明亮的蓝紫色火焰
19、现有A、B、C、D四种物质。A是无色无味的气体,B在A中剧烈燃烧,火星四射,放出大量热,同时生成一种黑色固体C。D是一种无色的气体,把D通入澄清的石灰水中,石灰水变浑浊。试判断A、B、C、D各是什么物质,请将答案填在空格内:
A是 ;B是 ;C是 ;D是 。
20、阅读下面科普短文,然后回答问题。
臭氧在通常状况下是淡蓝色,有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成氧气,并放出大量的热。臭氧的氧化能力比氧气强得多。
臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害,它是一切生命的保护层。超音速飞机排出的废气中有一氧化碳、二氧化碳、一氧化氮等气体,家用电冰箱中的制冷剂“氟里昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加。如不采取措施,后果不堪设想。
氧气和臭氧是不是同种物质?
(2)将带火星的木条伸入盛有臭氧的集气瓶中可以观察到的现象是什么?
[ (3)应采取什么方法保护臭氧层? 。
第二章 第三节 氧气(第3课时)
(一)学习目标
1、能比较燃烧、缓慢氧化的异同点。
2、了解燃烧的条件。
3、根据燃烧条件明确灭火方法。
4、了解火灾自救的一办方法。
(二)课前预习:
1、燃烧是指可燃物跟氧气发生的一种 、 、的 反应。可燃物燃烧所需的最低温度叫 。
2、燃烧需要三个基本条件: 、 、 。缺少其中的任何一个条件,燃烧都 (填“能"或“不能”)发生。
3、灭火的方法有: 、 、 。
4、常用的灭火器有 、 、和 。
当图书馆、档案室等处发生火灾时,可以用 灭火器灭火。
(三)课内导学
一、燃烧和缓慢氧化
1、燃烧的概念:燃烧是指可燃物跟氧气发生的一种 、 的氧化反应。
2、燃烧的条件P57
1)用坩锅钳或镊子夹取分别蘸有酒精、水的小棉花球放到酒精灯火焰上片刻,观察实验现象 。
2)用坩锅钳或镊子分别夹取干的、蘸有水的小棉花球,放到酒精灯火焰上片刻,观察实验现象 。
点燃酒精灯,再小心地盖上酒精灯帽,观察实验现象。
。
总结燃烧必须同事满足三个条件:
一是要有 :二是要有 :三是要达到 。
3、缓慢氧化:
1)概念:速率比较缓慢的氧化叫缓慢氧化。如生物呼吸、钢铁生锈都是缓慢氧化。
(氧化反应就是物质与氧发生的反应。)
2)缓慢氧化的特点:速率缓慢,不 但 。
4、燃烧和缓慢氧化的比较:
相同点:都是 反应,都能 热。
不同点:缓慢氧化速率缓慢,不能 ,燃烧反应速率剧烈,能 。
灭火的一般方法
根据可燃物燃烧的条件可知灭火的一般方法:
。
。
生活中发生火灾时常用水来灭火,其理由是:
。
。
议一议 下列情况着火时该怎么办?并说出以下灭火方法的原理。
烧菜时油锅着火怎么办?
建筑物着火怎么办?
文件档案、精密仪器着火怎么办?
想一想 水是否在任何情况下都能灭火?
常见灭火器介绍
常见灭火器有 、 、 、 。当图书馆、档案室等处发生火灾时,可以用 灭火器来灭火。
火灾自救
发生火灾时,要保持镇定,先 ,然后 。如果火势扩散,应尽快通知家人和邻居设法离开现场,沿途要关上大门,以 ,切勿乘电梯以免 。
。如果无法离开现场,应采取下列措施:
室内浓烟密布时,应 在地上爬行及用 掩住口鼻。
用 等物品塞住门和窗户的缝隙,以免浓烟呛人。
打开 ,呼救。
当堂训练
燃烧需要三个基本条件: 、 、 。缺少其中的任何一个条件,燃烧都 (填“能"或“不能”)发生。
2.灭火,即不让燃烧继续发生,可采法有 。
森林严禁用火,一单森林着火,灭火的方式多种多样。请你根据下列所给的灭火方法,说明相应的灭火原理。
有水源的地方用水浇灭。原理: 。
用鼓风机的强风吹灭。原理: 。
用树枝拍打将火打灭。原理: 。
用飞机投放干粉将火熄灭。原理: 。
在火场边缘将树木砍光,以防过火。原理: 。
使白磷燃烧的最低温度是40。C,紅磷燃燒的最低温度是240。C.图2-3中一小块白磷a和少量红磷b放在烧杯上方的薄铜片上,还有一小块白磷c放在80。C的水中稍过一会儿,可看到现象是a ,b ,c ..(填"燃烧",或"不燃烧").如果用一根导管向白磷c吹空气(与c接触),则可看到的 ,通过上述实验可知,白磷应保存在 .
常用的灭火器类型: , , .
课后反思
燃烧需要三个基本条件: 、 、 。
灭火的方法有: 、 、 。
常见灭器有 、 、 、 。
六.课后作业:
1、烧菜锅中的油着火,熄灭的最好方法是( )
A、浇水 B、撒沙土 C、盖上锅盖 D、使用灭火器
2、下列说法错误的是( )
A、木炭在氧气中燃烧比在空气中更旺,同时发出白光,生成二氧化碳
B、细铁丝在氧气里燃烧,火星四射,生成黑色的四氧化三铁
C、用灯帽盖灭酒精灯火焰,其目的使酒精隔绝空气而灭火
D、要达到灭火的目的,一定要在隔绝空气的同时,降低燃烧物的着火点
3、1994年12月8日,在克拉玛依友谊宫火灾中,有288名中学生和37名教师葬身火海。为此,我们每个人都要懂得消防知识,学会逃生。如果遇上高层楼房的下层起火,火势凶猛无法扑灭时,上层的人逃生措施正确的是( )
①沿楼道迅速下楼;②用湿毛巾堵住口鼻;③匍匐前进,寻找安全出口;④封闭房门;⑤迅速转移至阳台,用绳索下坠;⑥跳楼。
A、①②③④ B、③④⑤⑥ C、②③④⑤ D、①②④⑤
4、下列不属于燃烧条件的是( )
A、可燃物 B、温度
C、氧气(空气) D、接触面积大小
5、酒精可以点燃,但放在敞口容器里的酒精并不会自行燃烧起来,这主要是因为
( )
A、容器里没有空气 B、室温比酒精的燃点低得多
C、酒精是一种难燃的物质 D、容器里的酒精质量太少
6、下列物质中不属于易燃易爆物的是( )
A、氮气 B、白磷 C、液化气 D、汽油
7、某人救火,身上的衣服被烧起来,这时可采取的方法是( )
①跳入河中,或用自来水冲。 ②用被子将这个人裹起来
③就地打滚 ④向这个人喷二氧化碳
A、①④ B、②③ C、②④ D、①②③
8、酒精灯不能用嘴吹灭,而要用灯帽盖灭,从灭火原理分析,这是( )
A、降低温度 B、消除可燃物
C、隔绝空气 D、降低酒精的着火点
9、交通部门规定,乘坐车船时不能带易燃易爆物品,鞭炮是禁止携带的物品之一,这是因为车子开动时( )
A、鞭炮的着火点会升高
B、鞭炮着火点会降低
C、振动使鞭炮温度升高,达到燃点引起爆炸
D、鞭炮会损坏
10、蜡烛火焰用嘴一吹就熄灭。关于火焰熄灭的原因,小明与小东各有解释。
小明认为:人吹出来的是二氧化碳,二氧化碳吹到火焰上,灯芯因缺氧而停止燃烧。小东则认为:人吹出来的气中含有很多氧气,不足以使火焰熄灭,火焰熄灭的主要原因是人吹出的气流带走了灯芯的很多热量,从而使灯芯的温度降低,温度低于燃烧的最低温度时,火焰就熄灭。
你支持谁的观点?谈一谈你的看法
如何证明小东说的“人吹出来的气中含有许多氧气”?想一个简单的实验加以证明。
有一个棉花仓库起火,在消防车还未来到之前,很多人想取灭火,但仓库管理员不准开仓库门。你认为这位仓库管理员的做法有没有道理?说一说你的理由。
当你在电影院、商场等人口密集的地方遭遇火灾时,应怎样自救?
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
