鲁教版(五四制)九下化学 2.2碱及其性质 教案
文档属性
| 名称 | 鲁教版(五四制)九下化学 2.2碱及其性质 教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 84.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-22 00:00:00 | ||
图片预览

文档简介
《碱及其性质》教学设计
1、
设计思想
总的思路是先设置情景,通过“活动与探究”,让学生归纳总结常见碱的性质,通过小组内的讨论合作,探究CO2和NaOH的反应。以学生为主体,培养学生的探究能力和动手操作能力,激发学生学习化学的兴趣。
1、知识与技能:
(1)通过实验探究认识氢氧化钠和氢氧化钙的化学性质。了解其用途。
(2)通过探究氢氧化钠和氢氧化钙的化学性质归纳总结碱的通性及差异性并分析其原因
2、过程与方法:
通过一些探究活动,进一步认识与体验科学探究的过程;学会用碱的有关性质解释有关生活现象。
3、情感态度与价值观:
(1)通过实验设计及实验分析,培养学生的创新能力。
(2)通过学生亲身参与科学探究活动,激发学习化学的兴趣,培养学生尊重事实的科学态度,发展善于合作,勤于思考的科学精神。
2、
教学的重点和难点
1、
教学重点:NaOH和Ca(OH)2的性质
2、
教学难点:碱的通性及差异性
3、
实验准备:
NaOH溶液、澄清的石灰水、盐酸、蒸馏水、石蕊试液、酚酞试液、烧杯、试管、装满CO2软塑料瓶4个、生锈的铁钉、氯化铜溶液、碳酸钠溶液
四、教学过程
教学过程
教学环节
教师为主的活动
学生为主的活动
设计意图
创设情境
【视频引入】请同学们看视频“红色喷泉”【解释】烧瓶中装满氨气,胶头滴管中盛放的是水。当挤压胶头时看到什么现象?认真观看,描述现象,并解释其原因。【过渡】氨水是一种碱,能使酚酞变红,碱还有哪些化学性质呐?我们一起学习第二课时【板书】碱及其性质目标明确开始今天的学习
观看视频思考问题【讲述】描述现象解释原因,因为氨气极易溶于水,形成压强差,氨水使酚酞变红。生:读学习目标
通过视频导入引出新问题,激发学生的求知欲并且引导学生描述实验现象解释实验现象。
化学性质探究
【设疑】常见的碱有哪些?下面就以氢氧化钠、氢氧化钙为例来通过实验探究碱
的化学性质
了解探究的内容,表现出极大的兴趣认真仔细阅读实验内容明确实验步骤及注意事项
通过实验激发学生学习兴趣,培养安全实验的操作意识,及规范操作。增强学生们团结协作的意识。
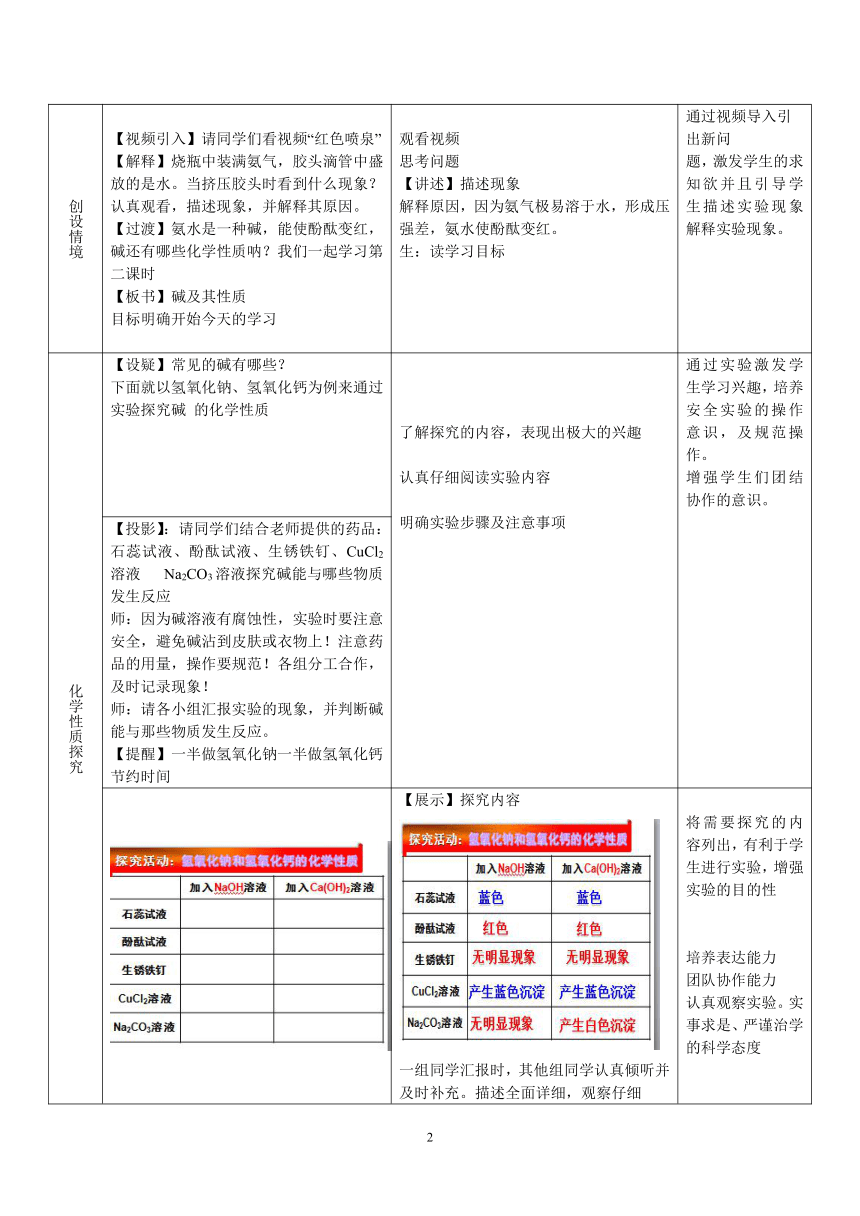
【投影】:请同学们结合老师提供的药品:石蕊试液、酚酞试液、生锈铁钉、CuCl2溶液
Na2CO3溶液探究碱能与哪些物质发生反应师:因为碱溶液有腐蚀性,实验时要注意安全,避免碱沾到皮肤或衣物上!注意药品的用量,操作要规范!各组分工合作,及时记录现象!师:请各小组汇报实验的现象,并判断碱能与那些物质发生反应。【提醒】一半做氢氧化钠一半做氢氧化钙节约时间
【展示】探究内容一组同学汇报时,其他组同学认真倾听并及时补充。描述全面详细,观察仔细
将需要探究的内容列出,有利于学生进行实验,增强实验的目的性培养表达能力团队协作能力认真观察实验。实事求是、严谨治学的科学态度
【问】通过实验探究NaOH溶液和Ca(OH)2溶液都能与哪些物质发生化学反应?实验研究证明:生成蓝色氢氧化铜沉淀。Ca(OH)2溶液能与碳酸钠溶液发生化学反应生成白色的碳酸钙沉淀。【过渡】两种碱还能与哪些物质发生反应?【演示实验】向两个盛有二氧化碳气体的矿泉水瓶里分别加入等量氢氧化钠溶液和氢氧化钙溶液,立即盖紧瓶塞,振荡,观察现象。
【答】能与NaOH溶液和Ca(OH)2溶液都能与氯化铜溶液发生化学反应,NaOH溶液碳酸钠溶液发生化学反应。【写】结合信息书写化学方程式2NaOH
+
CuCl2
=
Cu(OH)2
↓
+NaCl
Ca(OH)2
+
Na2CO3
=
CaCO3↓+
2NaOH
观看实验,描述现象
提高学生获取信息书写化学方程式的技能。
氢氧化钠与二氧化碳反应探究
【问】有的同学认为“实验2中矿泉水瓶变瘪,不足以证明CO2与NaOH溶液发生反应,因为CO2溶解在水中也会产生类似的现象。”你同意这种观点吗?充分肯定学生的实验设计【得出结论】确实发生了反应。【归纳方法】采用对比的方法,
控制变量排除干扰。还有哪些方法?
【讨论】可以证明氢氧化钠减少或者证明反应产生了碳酸钠,
有人说用酚酞,
有人说加盐酸。【讨论并实验】各组在点滴板上做碳酸钠溶液与酚酞的反应,
发现碳酸钠也能使酚酞变红色,
不能用这个方法。在试管里做氢氧化钠与盐酸的实验,
没有气泡产生,
可以用这个方法。
利用压强的变化设计实验,充分联系已学知识,利用身边仪器和物品培养学生从多角度分析问题,
反思问题的学习习惯和方法。培养学生实验探究的目标意识和优选意识增强学习兴趣,进行方法教育。进行简单的交流和评价,
体现探究的开放性。通过实验产生认知冲突,激发学生对学生借鉴之前学过的一些实验的设计思路和方法,发挥创新思维,
设计各种形式的实验装置。新问题的探索对学生进行控制变量、对比实验等科学方法的教育,
培养学生探究能力,
体现探究的严密性,
深刻性。
【提问】常见的碱有哪些主要的用途?【归纳】碱的通性1、碱能与酸碱指示剂作用2、碱能与非金属氧化物作用生成盐和水3、碱能与某些盐反应生成新碱和新盐【提问】碱为什么具有相似的化学性质,又有不同?
提示:类比酸的通性和差异性
看图片,了解碱的用途阅读教材
碱的用途生:回顾实验内容对比NaOH和Ca(OH)2的性质,类比酸的通性和差异性,分析原因生:通性:溶液中有相同的阴离子OH_
差异性:溶液中有不同的金属阳离子
联系生活实际采用类比的方法从微观角度分析
板书设计
第二节
碱及其性质一、碱的化学性质碱的通性:(OH_)1、碱能与酸碱指示剂作用2、碱能与非金属氧化物作用生成盐和水3、碱能与某些盐反应生成新碱和新盐碱的差异性(金属离子)二、碱的用途1、氢氧化钙用途:
2、氢氧化钠用途:
PAGE
4
1、
设计思想
总的思路是先设置情景,通过“活动与探究”,让学生归纳总结常见碱的性质,通过小组内的讨论合作,探究CO2和NaOH的反应。以学生为主体,培养学生的探究能力和动手操作能力,激发学生学习化学的兴趣。
1、知识与技能:
(1)通过实验探究认识氢氧化钠和氢氧化钙的化学性质。了解其用途。
(2)通过探究氢氧化钠和氢氧化钙的化学性质归纳总结碱的通性及差异性并分析其原因
2、过程与方法:
通过一些探究活动,进一步认识与体验科学探究的过程;学会用碱的有关性质解释有关生活现象。
3、情感态度与价值观:
(1)通过实验设计及实验分析,培养学生的创新能力。
(2)通过学生亲身参与科学探究活动,激发学习化学的兴趣,培养学生尊重事实的科学态度,发展善于合作,勤于思考的科学精神。
2、
教学的重点和难点
1、
教学重点:NaOH和Ca(OH)2的性质
2、
教学难点:碱的通性及差异性
3、
实验准备:
NaOH溶液、澄清的石灰水、盐酸、蒸馏水、石蕊试液、酚酞试液、烧杯、试管、装满CO2软塑料瓶4个、生锈的铁钉、氯化铜溶液、碳酸钠溶液
四、教学过程
教学过程
教学环节
教师为主的活动
学生为主的活动
设计意图
创设情境
【视频引入】请同学们看视频“红色喷泉”【解释】烧瓶中装满氨气,胶头滴管中盛放的是水。当挤压胶头时看到什么现象?认真观看,描述现象,并解释其原因。【过渡】氨水是一种碱,能使酚酞变红,碱还有哪些化学性质呐?我们一起学习第二课时【板书】碱及其性质目标明确开始今天的学习
观看视频思考问题【讲述】描述现象解释原因,因为氨气极易溶于水,形成压强差,氨水使酚酞变红。生:读学习目标
通过视频导入引出新问题,激发学生的求知欲并且引导学生描述实验现象解释实验现象。
化学性质探究
【设疑】常见的碱有哪些?下面就以氢氧化钠、氢氧化钙为例来通过实验探究碱
的化学性质
了解探究的内容,表现出极大的兴趣认真仔细阅读实验内容明确实验步骤及注意事项
通过实验激发学生学习兴趣,培养安全实验的操作意识,及规范操作。增强学生们团结协作的意识。
【投影】:请同学们结合老师提供的药品:石蕊试液、酚酞试液、生锈铁钉、CuCl2溶液
Na2CO3溶液探究碱能与哪些物质发生反应师:因为碱溶液有腐蚀性,实验时要注意安全,避免碱沾到皮肤或衣物上!注意药品的用量,操作要规范!各组分工合作,及时记录现象!师:请各小组汇报实验的现象,并判断碱能与那些物质发生反应。【提醒】一半做氢氧化钠一半做氢氧化钙节约时间
【展示】探究内容一组同学汇报时,其他组同学认真倾听并及时补充。描述全面详细,观察仔细
将需要探究的内容列出,有利于学生进行实验,增强实验的目的性培养表达能力团队协作能力认真观察实验。实事求是、严谨治学的科学态度
【问】通过实验探究NaOH溶液和Ca(OH)2溶液都能与哪些物质发生化学反应?实验研究证明:生成蓝色氢氧化铜沉淀。Ca(OH)2溶液能与碳酸钠溶液发生化学反应生成白色的碳酸钙沉淀。【过渡】两种碱还能与哪些物质发生反应?【演示实验】向两个盛有二氧化碳气体的矿泉水瓶里分别加入等量氢氧化钠溶液和氢氧化钙溶液,立即盖紧瓶塞,振荡,观察现象。
【答】能与NaOH溶液和Ca(OH)2溶液都能与氯化铜溶液发生化学反应,NaOH溶液碳酸钠溶液发生化学反应。【写】结合信息书写化学方程式2NaOH
+
CuCl2
=
Cu(OH)2
↓
+NaCl
Ca(OH)2
+
Na2CO3
=
CaCO3↓+
2NaOH
观看实验,描述现象
提高学生获取信息书写化学方程式的技能。
氢氧化钠与二氧化碳反应探究
【问】有的同学认为“实验2中矿泉水瓶变瘪,不足以证明CO2与NaOH溶液发生反应,因为CO2溶解在水中也会产生类似的现象。”你同意这种观点吗?充分肯定学生的实验设计【得出结论】确实发生了反应。【归纳方法】采用对比的方法,
控制变量排除干扰。还有哪些方法?
【讨论】可以证明氢氧化钠减少或者证明反应产生了碳酸钠,
有人说用酚酞,
有人说加盐酸。【讨论并实验】各组在点滴板上做碳酸钠溶液与酚酞的反应,
发现碳酸钠也能使酚酞变红色,
不能用这个方法。在试管里做氢氧化钠与盐酸的实验,
没有气泡产生,
可以用这个方法。
利用压强的变化设计实验,充分联系已学知识,利用身边仪器和物品培养学生从多角度分析问题,
反思问题的学习习惯和方法。培养学生实验探究的目标意识和优选意识增强学习兴趣,进行方法教育。进行简单的交流和评价,
体现探究的开放性。通过实验产生认知冲突,激发学生对学生借鉴之前学过的一些实验的设计思路和方法,发挥创新思维,
设计各种形式的实验装置。新问题的探索对学生进行控制变量、对比实验等科学方法的教育,
培养学生探究能力,
体现探究的严密性,
深刻性。
【提问】常见的碱有哪些主要的用途?【归纳】碱的通性1、碱能与酸碱指示剂作用2、碱能与非金属氧化物作用生成盐和水3、碱能与某些盐反应生成新碱和新盐【提问】碱为什么具有相似的化学性质,又有不同?
提示:类比酸的通性和差异性
看图片,了解碱的用途阅读教材
碱的用途生:回顾实验内容对比NaOH和Ca(OH)2的性质,类比酸的通性和差异性,分析原因生:通性:溶液中有相同的阴离子OH_
差异性:溶液中有不同的金属阳离子
联系生活实际采用类比的方法从微观角度分析
板书设计
第二节
碱及其性质一、碱的化学性质碱的通性:(OH_)1、碱能与酸碱指示剂作用2、碱能与非金属氧化物作用生成盐和水3、碱能与某些盐反应生成新碱和新盐碱的差异性(金属离子)二、碱的用途1、氢氧化钙用途:
2、氢氧化钠用途:
PAGE
4
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
