高中化学人教版选修四 4.4金属的电化学腐蚀与防护 课件(44张ppt)
文档属性
| 名称 | 高中化学人教版选修四 4.4金属的电化学腐蚀与防护 课件(44张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 24.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-22 00:00:00 | ||
图片预览











文档简介
(共44张PPT)
第四章
第四节
金属的电化学腐蚀与防护
高二年级
化学
炼
钢
轧
钢
习以为常的金属腐蚀现象
我国每年因腐蚀而造成的经济损失占国民生产总值的5%左右。金属材料使用量的90%
以上是钢铁,由钢铁造成的损失约
7
000
亿美元,超过每年各项大灾(火灾、风灾及地震等)损失的总和。
——《中国腐蚀调查报告》
什么是金属的腐蚀?
地球上,腐蚀时刻都在发生,它被称作金属的癌症。为了提高公众对金属腐蚀的重视程度,世界腐蚀组织把每年的4月24日,定为“世界腐蚀日”。
习以为常的金属腐蚀现象
Fe2O3˙xH2O
Cu2(OH)2CO3
一、金属的腐蚀
1.概念:金属与周围的气体或液体物质发生氧化还原
反应而引起损耗的现象。
2.本质:金属原子失去电子,转化为阳离子的过程。
影响金属腐蚀的因素有哪些呢?
M-ne-
Mn+
影响金属腐蚀的因素
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:
金属所处的环境
生石灰
蒸馏水
食盐水
铁钉锈蚀实验
影响金属腐蚀的外在因素主要包括哪些呢?
钢制燃气灶炉头使用一段时间后被腐蚀原因?
氧化性气体在高温条件下使钢材表面生成铁的氧化物
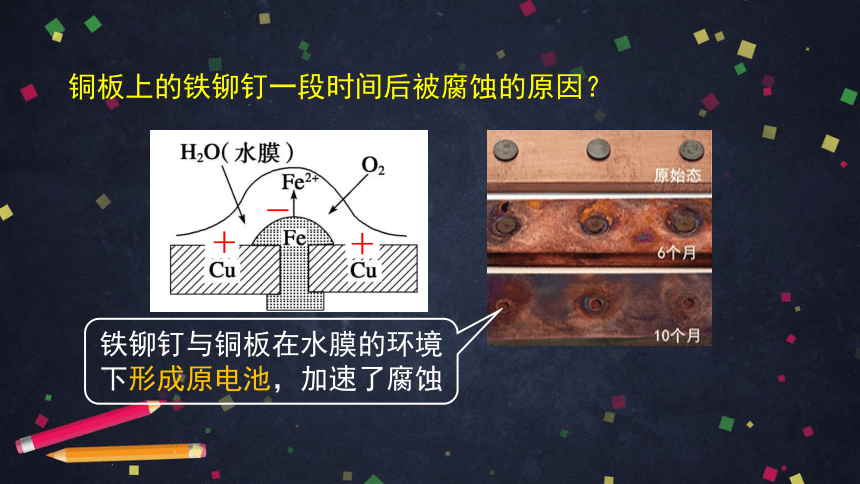
铜板上的铁铆钉一段时间后被腐蚀的原因?
-
+
+
铁铆钉与铜板在水膜的环境下形成原电池,加速了腐蚀
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:
温度、湿度、酸碱性、金属纯度……
影响金属腐蚀的因素
金属所处的环境
这两种金属腐蚀的原理一样吗?
直接发生化学反应引起的金属腐蚀
形成原电池引起的金属腐蚀
一、金属的腐蚀
3.类别:
化学腐蚀:
电化学腐蚀:
金属与接触到的干燥气体(如O2、Cl2、SO2等)
或非电解质液体(如石油)
等直接发生化学反应引起
的腐蚀。
不纯的金属与电解质溶液接触时,发生原电池反应,比较活泼的金属失去电子而
被氧化引起的腐蚀。
对比归纳
化学腐蚀
电化学腐蚀
条件
特征
结果
金属与氧化性物质
直接接触
不纯金属与电解质溶液
及氧化剂接触
无电流产生
有微弱电流产生
金属被氧化
相对活泼的金属被氧化
二者往往同时发生,但电化学腐蚀更普遍。
钢架桥生锈属于哪种金属腐蚀?
电解质溶液
Fe2+
e-
e-
e-
e-
猜想:
①空气中的O2
是常见氧化剂
②铁锈的成分:
Fe2O3˙xH2O
Fe-2e-
Fe2+
+
-
在正极得到电子?
实验1:将酸洗除锈的铁钉,用饱和食盐水浸泡后,放入
下图所示装置,几分钟后观察导管中水柱的变化。
消耗的一定是氧气吗?
视频以10倍速度快进播放
资料
实验2:用传感器测量铁钉腐蚀过程中密闭装置内氧气含量
的变化。
氧气含量
测定传感器
资料
电解质溶液
Fe2+
e-
e-
e-
e-
吸氧腐蚀
O2+4e-+2H2O
4OH-
2Fe+O2+2H2O
2Fe(OH)2
Fe-2e-
Fe2+
2Fe-4e-
2Fe2+
Fe2O3˙xH2O
脱水
4Fe(OH)2+O2+2H2O
4Fe(OH)3
+
-
O2
OH-
实验3:向烧杯中加入食盐水,将无锈铁钉和碳棒分别用导
线与电流计连接,再分别插入两个无底玻璃筒中。
【资料】3Fe2++2[Fe(CN)6]3-
Fe3[Fe(CN)6]2(蓝色沉淀)
取样后滴加
K3[Fe(CN)6]溶液
取样后滴加
酚酞溶液
铁钉
碳棒
实验3:向烧杯中加入食盐水,将无锈铁钉和碳棒分别用导
线与电流计连接,再分别插入两个无底玻璃筒中。
取样后滴加
K3[Fe(CN)6]溶液
取样后滴加
酚酞溶液
指针偏转
实验4:不同pH条件下,钢铁腐蚀体系中压强随时间变化。
压强传感器
电脑
数据采集器
一定pH的
醋酸溶液
铁和炭粉
电解质溶液
Fe2+
e-
e-
e-
e-
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
+
-
H2
H+
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
电解质溶液
Fe2+
e-
e-
e-
e-
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
析氢腐蚀
+
-
H2
H+
吸氧腐蚀
析氢腐蚀
条件
电极反应
负极(Fe)
正极(C)
总反应
水膜呈较强酸性
水膜酸性很弱或呈中性
Fe2O3˙xH2O
脱水
二者往往同时存在,但以吸氧腐蚀为主。
对比归纳
2Fe-4e-
2Fe2+
Fe-2e-
Fe2+
O2+4e-+2H2O
4OH-
2H++2e-
H2
2Fe+O2+2H2O
2Fe(OH)2
Fe+2H+
Fe2++H2
4Fe(OH)2+O2+2H2O
4Fe(OH)3
如何防止金属的腐蚀?
二、金属的防护
1.原理:
避免金属失去电子
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:金属所处的环境
温度、湿度、酸碱性、金属纯度……
改变?
调控?
影响金属腐蚀的因素
二、金属的防护
2.方法:
能否利用电化学方法解决金属电化学腐蚀的问题?
(1)改变组成:在钢铁中加入铬和镍制成“不锈钢”
(2)直接隔离:喷漆、涂油、电镀、表面钝化……
1.原理:
避免金属失去电子
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
C
+
—
Zn
e-
海水
Fe
—
-
+
A
e-
【思路一】
-
实验5:连接好装置,观察现象,一段时间后从Fe电极附近
取样,滴加K3[Fe(CN)6]溶液,观察溶液颜色变化。
A
NaCl溶液
Fe
—
—
Zn
Zn
Fe
6小时后
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
Zn
【思路一】
e-
锌合金
镁合金
+
-
-
e-
阳
阴
海水
Fe
—
—
C
e-
【思路二】
A
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
C
+
e-
利用电化学方法解决金属的电化学腐蚀
阳
阴
海水
【思路二】
—
C
Fe
—
海水
Fe
—
阳
阴
【思路二】
—
C
e-
牺牲阳极的
阴极保护法
外加电流的
阴极保护法
利用电化学方法解决金属的电化学腐蚀
原电池原理
电解池原理
A
海水
Fe
—
—
Zn
+
-
【思路一】
e-
利用电化学方法解决金属的电化学腐蚀
原电池原理
电解池原理
石墨
辅助阳极
牺牲阳极的
阴极保护法
外加电流的
阴极保护法
二、金属的防护
(3)电化学防护
①
牺牲阳极的阴极保护
②
外加电流的阴极保护
(原电池原理)
(电解池原理)
(1)改变组成:在钢铁中加入铬和镍制成“不锈钢”
(2)直接隔离:喷漆、涂油、电镀、表面钝化……
2.方法:
1.原理:
避免金属失去电子
归纳总结
金属腐蚀
化学腐蚀
电化学腐蚀
吸氧腐蚀
析氢腐蚀
金属防护
直接隔离
改变组成
电化学防护
牺牲阳极的阴极保护法(原电池原理)
外加电流的阴极保护法(电解池原理)
被保护金属
避免
本质
M-ne-
Mn+
+
-
下图中铁片腐蚀由快到慢的顺序为②③④①,对此你有何启发?
想一想
A
海水
Fe
Zn
海水
Fe
C
海水
Fe
C
A
海水
Fe
C
①
②
③
④
阴
阳
被保护
被保护
加速腐蚀
加速腐蚀
更快
更慢
能否利用金属的腐蚀服务于人类?
铁粉、炭粉、电解质溶液形成原电池,利用铁在吸氧腐蚀过程中释放的热量来为我们供暖。
使用前
使用后
能否利用金属的腐蚀服务于人类?
镁合金血管支架
一个月
五个月
三个月
聚合物涂层
降解产物
镁支架
应力腐蚀与腐蚀疲劳
加速实验装置
预测安全运行
时长与负载
国际首创核电
高温高压水
原位划伤再钝化测试装置
核用关键不可替换
材料的安全服役
牺牲阳极保护
分段涂层处理
腐蚀监测技术
港珠澳大桥
120
年安全使用寿命
第四章
第四节
金属的电化学腐蚀与防护
高二年级
化学
炼
钢
轧
钢
习以为常的金属腐蚀现象
我国每年因腐蚀而造成的经济损失占国民生产总值的5%左右。金属材料使用量的90%
以上是钢铁,由钢铁造成的损失约
7
000
亿美元,超过每年各项大灾(火灾、风灾及地震等)损失的总和。
——《中国腐蚀调查报告》
什么是金属的腐蚀?
地球上,腐蚀时刻都在发生,它被称作金属的癌症。为了提高公众对金属腐蚀的重视程度,世界腐蚀组织把每年的4月24日,定为“世界腐蚀日”。
习以为常的金属腐蚀现象
Fe2O3˙xH2O
Cu2(OH)2CO3
一、金属的腐蚀
1.概念:金属与周围的气体或液体物质发生氧化还原
反应而引起损耗的现象。
2.本质:金属原子失去电子,转化为阳离子的过程。
影响金属腐蚀的因素有哪些呢?
M-ne-
Mn+
影响金属腐蚀的因素
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:
金属所处的环境
生石灰
蒸馏水
食盐水
铁钉锈蚀实验
影响金属腐蚀的外在因素主要包括哪些呢?
钢制燃气灶炉头使用一段时间后被腐蚀原因?
氧化性气体在高温条件下使钢材表面生成铁的氧化物
铜板上的铁铆钉一段时间后被腐蚀的原因?
-
+
+
铁铆钉与铜板在水膜的环境下形成原电池,加速了腐蚀
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:
温度、湿度、酸碱性、金属纯度……
影响金属腐蚀的因素
金属所处的环境
这两种金属腐蚀的原理一样吗?
直接发生化学反应引起的金属腐蚀
形成原电池引起的金属腐蚀
一、金属的腐蚀
3.类别:
化学腐蚀:
电化学腐蚀:
金属与接触到的干燥气体(如O2、Cl2、SO2等)
或非电解质液体(如石油)
等直接发生化学反应引起
的腐蚀。
不纯的金属与电解质溶液接触时,发生原电池反应,比较活泼的金属失去电子而
被氧化引起的腐蚀。
对比归纳
化学腐蚀
电化学腐蚀
条件
特征
结果
金属与氧化性物质
直接接触
不纯金属与电解质溶液
及氧化剂接触
无电流产生
有微弱电流产生
金属被氧化
相对活泼的金属被氧化
二者往往同时发生,但电化学腐蚀更普遍。
钢架桥生锈属于哪种金属腐蚀?
电解质溶液
Fe2+
e-
e-
e-
e-
猜想:
①空气中的O2
是常见氧化剂
②铁锈的成分:
Fe2O3˙xH2O
Fe-2e-
Fe2+
+
-
在正极得到电子?
实验1:将酸洗除锈的铁钉,用饱和食盐水浸泡后,放入
下图所示装置,几分钟后观察导管中水柱的变化。
消耗的一定是氧气吗?
视频以10倍速度快进播放
资料
实验2:用传感器测量铁钉腐蚀过程中密闭装置内氧气含量
的变化。
氧气含量
测定传感器
资料
电解质溶液
Fe2+
e-
e-
e-
e-
吸氧腐蚀
O2+4e-+2H2O
4OH-
2Fe+O2+2H2O
2Fe(OH)2
Fe-2e-
Fe2+
2Fe-4e-
2Fe2+
Fe2O3˙xH2O
脱水
4Fe(OH)2+O2+2H2O
4Fe(OH)3
+
-
O2
OH-
实验3:向烧杯中加入食盐水,将无锈铁钉和碳棒分别用导
线与电流计连接,再分别插入两个无底玻璃筒中。
【资料】3Fe2++2[Fe(CN)6]3-
Fe3[Fe(CN)6]2(蓝色沉淀)
取样后滴加
K3[Fe(CN)6]溶液
取样后滴加
酚酞溶液
铁钉
碳棒
实验3:向烧杯中加入食盐水,将无锈铁钉和碳棒分别用导
线与电流计连接,再分别插入两个无底玻璃筒中。
取样后滴加
K3[Fe(CN)6]溶液
取样后滴加
酚酞溶液
指针偏转
实验4:不同pH条件下,钢铁腐蚀体系中压强随时间变化。
压强传感器
电脑
数据采集器
一定pH的
醋酸溶液
铁和炭粉
电解质溶液
Fe2+
e-
e-
e-
e-
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
+
-
H2
H+
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
电解质溶液
Fe2+
e-
e-
e-
e-
Fe-2e-
Fe2+
2H++2e-
H2
Fe+2H+
Fe2++H2
析氢腐蚀
+
-
H2
H+
吸氧腐蚀
析氢腐蚀
条件
电极反应
负极(Fe)
正极(C)
总反应
水膜呈较强酸性
水膜酸性很弱或呈中性
Fe2O3˙xH2O
脱水
二者往往同时存在,但以吸氧腐蚀为主。
对比归纳
2Fe-4e-
2Fe2+
Fe-2e-
Fe2+
O2+4e-+2H2O
4OH-
2H++2e-
H2
2Fe+O2+2H2O
2Fe(OH)2
Fe+2H+
Fe2++H2
4Fe(OH)2+O2+2H2O
4Fe(OH)3
如何防止金属的腐蚀?
二、金属的防护
1.原理:
避免金属失去电子
内因:金属自身的性质
K、Na、Al、Fe、Pt、Au
外因:金属所处的环境
温度、湿度、酸碱性、金属纯度……
改变?
调控?
影响金属腐蚀的因素
二、金属的防护
2.方法:
能否利用电化学方法解决金属电化学腐蚀的问题?
(1)改变组成:在钢铁中加入铬和镍制成“不锈钢”
(2)直接隔离:喷漆、涂油、电镀、表面钝化……
1.原理:
避免金属失去电子
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
C
+
—
Zn
e-
海水
Fe
—
-
+
A
e-
【思路一】
-
实验5:连接好装置,观察现象,一段时间后从Fe电极附近
取样,滴加K3[Fe(CN)6]溶液,观察溶液颜色变化。
A
NaCl溶液
Fe
—
—
Zn
Zn
Fe
6小时后
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
Zn
【思路一】
e-
锌合金
镁合金
+
-
-
e-
阳
阴
海水
Fe
—
—
C
e-
【思路二】
A
利用电化学方法解决金属的电化学腐蚀
A
海水
Fe
—
—
C
+
e-
利用电化学方法解决金属的电化学腐蚀
阳
阴
海水
【思路二】
—
C
Fe
—
海水
Fe
—
阳
阴
【思路二】
—
C
e-
牺牲阳极的
阴极保护法
外加电流的
阴极保护法
利用电化学方法解决金属的电化学腐蚀
原电池原理
电解池原理
A
海水
Fe
—
—
Zn
+
-
【思路一】
e-
利用电化学方法解决金属的电化学腐蚀
原电池原理
电解池原理
石墨
辅助阳极
牺牲阳极的
阴极保护法
外加电流的
阴极保护法
二、金属的防护
(3)电化学防护
①
牺牲阳极的阴极保护
②
外加电流的阴极保护
(原电池原理)
(电解池原理)
(1)改变组成:在钢铁中加入铬和镍制成“不锈钢”
(2)直接隔离:喷漆、涂油、电镀、表面钝化……
2.方法:
1.原理:
避免金属失去电子
归纳总结
金属腐蚀
化学腐蚀
电化学腐蚀
吸氧腐蚀
析氢腐蚀
金属防护
直接隔离
改变组成
电化学防护
牺牲阳极的阴极保护法(原电池原理)
外加电流的阴极保护法(电解池原理)
被保护金属
避免
本质
M-ne-
Mn+
+
-
下图中铁片腐蚀由快到慢的顺序为②③④①,对此你有何启发?
想一想
A
海水
Fe
Zn
海水
Fe
C
海水
Fe
C
A
海水
Fe
C
①
②
③
④
阴
阳
被保护
被保护
加速腐蚀
加速腐蚀
更快
更慢
能否利用金属的腐蚀服务于人类?
铁粉、炭粉、电解质溶液形成原电池,利用铁在吸氧腐蚀过程中释放的热量来为我们供暖。
使用前
使用后
能否利用金属的腐蚀服务于人类?
镁合金血管支架
一个月
五个月
三个月
聚合物涂层
降解产物
镁支架
应力腐蚀与腐蚀疲劳
加速实验装置
预测安全运行
时长与负载
国际首创核电
高温高压水
原位划伤再钝化测试装置
核用关键不可替换
材料的安全服役
牺牲阳极保护
分段涂层处理
腐蚀监测技术
港珠澳大桥
120
年安全使用寿命
