第2节 物质的酸碱性(课件 29张ppt)
文档属性
| 名称 | 第2节 物质的酸碱性(课件 29张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-06-23 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
第1章 物质及其变化
合作学习
酸的
你有过呕吐的经历吗?你感到胃液是什么味道的?
合作学习
归纳总结
2、电离:
带电的原子或原子集团。
1、离子:
一些物质溶解于水或受热熔化时,产生自由移动的离子的过程,叫做电离。
带正电荷的叫阳离子。
带负电荷的叫阴离子。
归纳总结
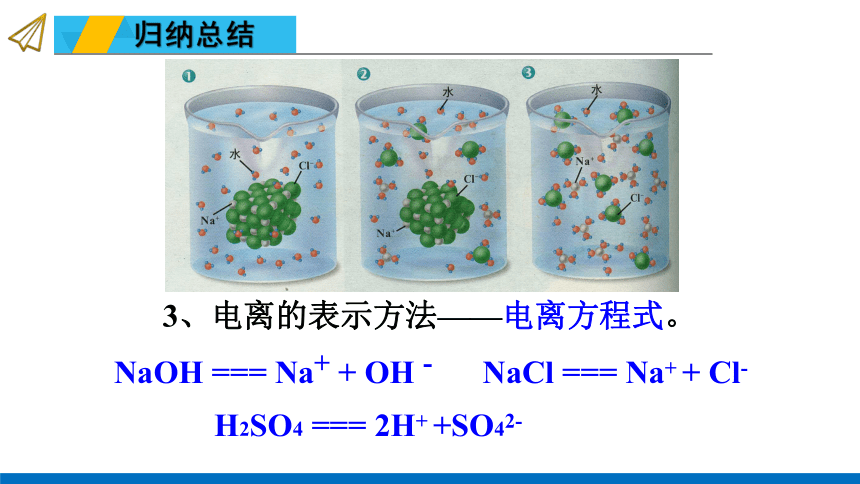
3、电离的表示方法——电离方程式。
NaOH
===
Na+
+
OH
-
NaCl
===
Na+
+
Cl-
H2SO4
===
2H+
+SO42-
归纳总结
4、一些物质电离时产生的阴阳离子所带电荷的总数一定相等。所以,这些物质的溶液不显电性。
5、电离方程式书写时,不必写条件,但要配平,使电荷总数,而原子团不能拆开。
课堂讲解
什么是酸?什么是酸性物质?
课堂讲解
胃酸、醋、酸梅、牛奶、可乐、雪碧等
说一说:生活中有哪些东西是酸的?
课堂讲解
食醋——醋酸,胃液——盐酸,柠檬、柑橘等水果中含有柠檬酸。
课堂讲解
这些物质在水中电离时,生成的阳离子全部都是氢离子(H+)。
那么,为什么说这些物质都是酸呢?
课堂讲解
盐酸:
硝酸:
硫酸:
HCl
===
H
+
+
Cl-
电离方程式:
HNO3
===
H
+
+
NO3-
H2SO4
==
2H
+
+
SO
42-
电离通式:
酸=
H+
+
酸根阴离子
什么是酸?
课堂讲解
盐酸的电离:
HCl
=
H+
+
Cl-
H+
H+
H+
课堂讲解
酸的涵义:
电离时产生的阳离子只有氢离子的化合物
。
强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
弱酸:醋酸(CH3COOH)
课堂反思
1.在水溶液里能电离产生氢离子的化合物一定是酸吗?
2.酸一定含氢元素与氧元素,对吗?
3.二氧化碳溶于水后也会产生氢离子,
二氧化碳是酸吗?
你是如何理解酸这种物质的?
合作探究
你知道生活中碱性的食物吗?
常见食物的碱性:茶、柿子、黄瓜、胡萝卜、萝卜、菠菜、葡萄、芋头、海带、葡萄干、马铃薯、卷心菜、笋、香菇类、油菜、南瓜、豆腐、香蕉、樱桃等。
合作探究
你去尝一个未成熟的柿子,会有什么感觉?
这是因为柿子里含有
物质
碱性
食用碱性食品时会感到涩味,洗澡时不小心有肥皂泡溅到嘴里也有这种感觉。
合作探究
什么是碱
1.未成熟的柿子中存在碱性物质,家用的洗涤剂中也存在着碱性物质;常见的物质中,NaOH、Ca(OH)2等物质都属于碱。
到底什么是碱?
课堂讲解
思考:电离产物的共同之处是什么?
NaOH
=
Na+
+
OH–
Ca(OH)2
=
Ca+
+
2OH–
Ba(OH)2
=
Ba++
2OH–
KOH
=
K
+
+
OH–
3.碱的涵义:碱是电离时产生的阴离子全部是OH-
的化合物。
2.碱的电离
课堂讲解
酸碱指示剂
1、定义:
在酸或碱溶液里能显示出不同颜色的物质。
2、常见的酸碱指示剂有:
紫色石蕊试液
无色酚酞试液
课堂讲解
3、酸碱指示剂可以定性地测定溶液的酸碱性。
4、常见指示剂在酸、碱性溶液中的颜色
红色
红色
红色
无色
蓝色
蓝色
不变色
不变色
指
示
剂
酸
性
溶
液
碱
性
溶
液
石蕊试液(紫色)
酚酞试液(无色)
蓝色石蕊试纸
红色石蕊试纸
归纳总结
石蕊遇酸变红,遇碱变蓝;
酚酞遇酸不变色,遇碱变红。
课堂讲解
自制酸碱指示剂
1、取一些月季花、菊花、丝瓜花、一串红等植物的花、果、枝叶切碎、捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂。
2、取食盐水、白醋、石灰水加以试验。并记录变色情况。
课堂讲解
1.pH是反应物质酸碱性强弱的指标。它的范围通常在0至14之间。
2.pH与溶液酸碱性之间的关系。
pH<7
溶液呈酸性,pH越小,酸性越强。
pH=7
溶液呈中性
pH>7
溶液呈碱性,pH越大,碱性越强
溶液酸碱性的强弱程度
课堂讲解
pH
是反映物质酸碱性强弱的指标,它的范围通常在0~14
之间。pH越低,酸性越强;pH
越高,碱性越强;pH
等于7
的物质呈中性。
课堂讲解
3.溶液pH测定
比较精确的测量用酸度计。
测定溶液酸碱度最常用、最简单的方法是使用pH试纸。测定方法是:用洁净的玻棒棒蘸取待测液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,看与哪种颜色最接近,从而确定待测溶液的pH。
课堂演练
1、下列物质不属于酸的是
(
)
A.HNO3
B.NaHCO3
C.H3PO4
D.HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?
B
课堂演练
4.下列各组离子属于酸电离产生的是(
)
A.H+、NO3-、SO42-
B.OH-、Ba2+
C.H+、Na+、SO42-
D.
Na+
、Ba2+、
Cl-
5.某一溶液的pH=2,该溶液呈
性,它能使紫色石蕊试液
色,无色酚酞试液
,使蓝色石蕊试纸变
色。
6.下表列出了家庭中某些物质的pH:
上述物质能使无色酚酞试液变红色的是
。
A
酸
红
不变色
蓝
牙膏、肥皂水
物质
醋
牙膏
食盐溶液
肥皂水
pH
3
9
7
10
课堂演练
7.将一定质量分数的硫酸溶液加水稀释,
下图正确表示pH变化的是(
)
A
第1章 物质及其变化
合作学习
酸的
你有过呕吐的经历吗?你感到胃液是什么味道的?
合作学习
归纳总结
2、电离:
带电的原子或原子集团。
1、离子:
一些物质溶解于水或受热熔化时,产生自由移动的离子的过程,叫做电离。
带正电荷的叫阳离子。
带负电荷的叫阴离子。
归纳总结
3、电离的表示方法——电离方程式。
NaOH
===
Na+
+
OH
-
NaCl
===
Na+
+
Cl-
H2SO4
===
2H+
+SO42-
归纳总结
4、一些物质电离时产生的阴阳离子所带电荷的总数一定相等。所以,这些物质的溶液不显电性。
5、电离方程式书写时,不必写条件,但要配平,使电荷总数,而原子团不能拆开。
课堂讲解
什么是酸?什么是酸性物质?
课堂讲解
胃酸、醋、酸梅、牛奶、可乐、雪碧等
说一说:生活中有哪些东西是酸的?
课堂讲解
食醋——醋酸,胃液——盐酸,柠檬、柑橘等水果中含有柠檬酸。
课堂讲解
这些物质在水中电离时,生成的阳离子全部都是氢离子(H+)。
那么,为什么说这些物质都是酸呢?
课堂讲解
盐酸:
硝酸:
硫酸:
HCl
===
H
+
+
Cl-
电离方程式:
HNO3
===
H
+
+
NO3-
H2SO4
==
2H
+
+
SO
42-
电离通式:
酸=
H+
+
酸根阴离子
什么是酸?
课堂讲解
盐酸的电离:
HCl
=
H+
+
Cl-
H+
H+
H+
课堂讲解
酸的涵义:
电离时产生的阳离子只有氢离子的化合物
。
强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
弱酸:醋酸(CH3COOH)
课堂反思
1.在水溶液里能电离产生氢离子的化合物一定是酸吗?
2.酸一定含氢元素与氧元素,对吗?
3.二氧化碳溶于水后也会产生氢离子,
二氧化碳是酸吗?
你是如何理解酸这种物质的?
合作探究
你知道生活中碱性的食物吗?
常见食物的碱性:茶、柿子、黄瓜、胡萝卜、萝卜、菠菜、葡萄、芋头、海带、葡萄干、马铃薯、卷心菜、笋、香菇类、油菜、南瓜、豆腐、香蕉、樱桃等。
合作探究
你去尝一个未成熟的柿子,会有什么感觉?
这是因为柿子里含有
物质
碱性
食用碱性食品时会感到涩味,洗澡时不小心有肥皂泡溅到嘴里也有这种感觉。
合作探究
什么是碱
1.未成熟的柿子中存在碱性物质,家用的洗涤剂中也存在着碱性物质;常见的物质中,NaOH、Ca(OH)2等物质都属于碱。
到底什么是碱?
课堂讲解
思考:电离产物的共同之处是什么?
NaOH
=
Na+
+
OH–
Ca(OH)2
=
Ca+
+
2OH–
Ba(OH)2
=
Ba++
2OH–
KOH
=
K
+
+
OH–
3.碱的涵义:碱是电离时产生的阴离子全部是OH-
的化合物。
2.碱的电离
课堂讲解
酸碱指示剂
1、定义:
在酸或碱溶液里能显示出不同颜色的物质。
2、常见的酸碱指示剂有:
紫色石蕊试液
无色酚酞试液
课堂讲解
3、酸碱指示剂可以定性地测定溶液的酸碱性。
4、常见指示剂在酸、碱性溶液中的颜色
红色
红色
红色
无色
蓝色
蓝色
不变色
不变色
指
示
剂
酸
性
溶
液
碱
性
溶
液
石蕊试液(紫色)
酚酞试液(无色)
蓝色石蕊试纸
红色石蕊试纸
归纳总结
石蕊遇酸变红,遇碱变蓝;
酚酞遇酸不变色,遇碱变红。
课堂讲解
自制酸碱指示剂
1、取一些月季花、菊花、丝瓜花、一串红等植物的花、果、枝叶切碎、捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂。
2、取食盐水、白醋、石灰水加以试验。并记录变色情况。
课堂讲解
1.pH是反应物质酸碱性强弱的指标。它的范围通常在0至14之间。
2.pH与溶液酸碱性之间的关系。
pH<7
溶液呈酸性,pH越小,酸性越强。
pH=7
溶液呈中性
pH>7
溶液呈碱性,pH越大,碱性越强
溶液酸碱性的强弱程度
课堂讲解
pH
是反映物质酸碱性强弱的指标,它的范围通常在0~14
之间。pH越低,酸性越强;pH
越高,碱性越强;pH
等于7
的物质呈中性。
课堂讲解
3.溶液pH测定
比较精确的测量用酸度计。
测定溶液酸碱度最常用、最简单的方法是使用pH试纸。测定方法是:用洁净的玻棒棒蘸取待测液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,看与哪种颜色最接近,从而确定待测溶液的pH。
课堂演练
1、下列物质不属于酸的是
(
)
A.HNO3
B.NaHCO3
C.H3PO4
D.HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?
B
课堂演练
4.下列各组离子属于酸电离产生的是(
)
A.H+、NO3-、SO42-
B.OH-、Ba2+
C.H+、Na+、SO42-
D.
Na+
、Ba2+、
Cl-
5.某一溶液的pH=2,该溶液呈
性,它能使紫色石蕊试液
色,无色酚酞试液
,使蓝色石蕊试纸变
色。
6.下表列出了家庭中某些物质的pH:
上述物质能使无色酚酞试液变红色的是
。
A
酸
红
不变色
蓝
牙膏、肥皂水
物质
醋
牙膏
食盐溶液
肥皂水
pH
3
9
7
10
课堂演练
7.将一定质量分数的硫酸溶液加水稀释,
下图正确表示pH变化的是(
)
A
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
