人教版高二化学选修5第三章第二节 醛 (共22张PPT)
文档属性
| 名称 | 人教版高二化学选修5第三章第二节 醛 (共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 483.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-24 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第三章
烃的含氧衍生物
第二节
醛
常见的醛
桂皮中含有肉桂醛
-CH=CH-CHO
杏仁中含有苯甲醛
-CHO
含有香草醛的兰花
-CHO
HO-
CH3O
前
言
2CH3CH2OH+O2
2CH3CHO+2H2O
催化剂
△
乙醛
我们已知:
教学目标:
1、了解乙醛的物理性质
2、掌握乙醛的加成反应和氧化反应
3、了解醛类的一般通性,甲醛性质与用途
教学难点:乙醛与弱氧化剂反应方程式书写
教学重点:乙醛的结构特点和化学性质
1、乙醛的物理性质
(1)无色
(2)有刺激性气味
(3)液体
(4)有毒
(5)易挥发;易燃烧
(6)与水、乙醇等互溶
(7)沸点:20.8℃
(8)密度小于水
(1)分子式:
(2)结构式:
2、乙醛的分子结构
(3)结构简式:
C2H4O
CH3CHO
官能团:
C
H
H
H
C
O
H
C
C
O
H
C
醛基
乙醛的核磁共振氢谱:两个峰。
乙醛分子有两种氢原子。较高峰-CH3中的氢原子;较低峰-CHO中的氢原子。
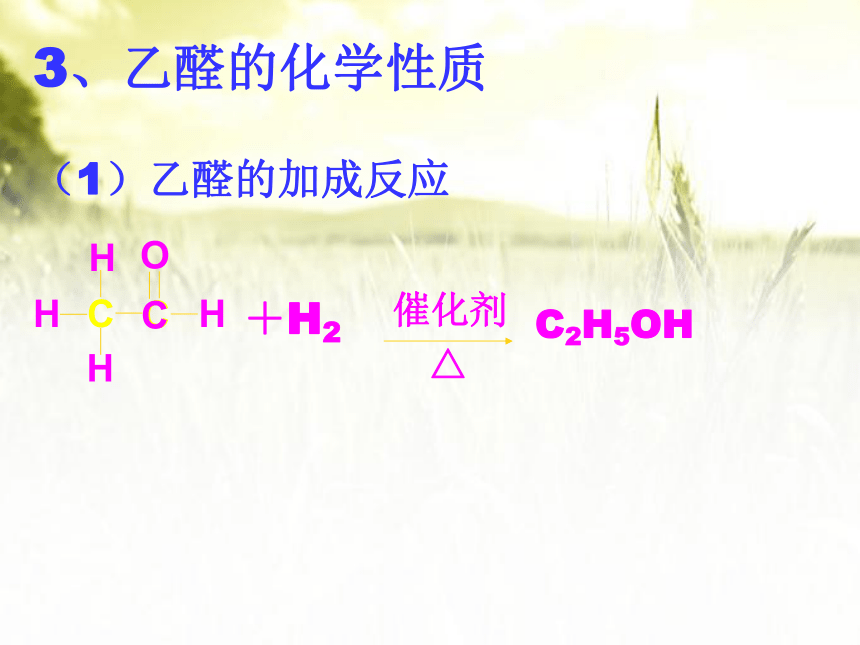
(1)乙醛的加成反应
C
H
H
H
C
O
H
C
+H2
催化剂
△
C2H5OH
3、乙醛的化学性质
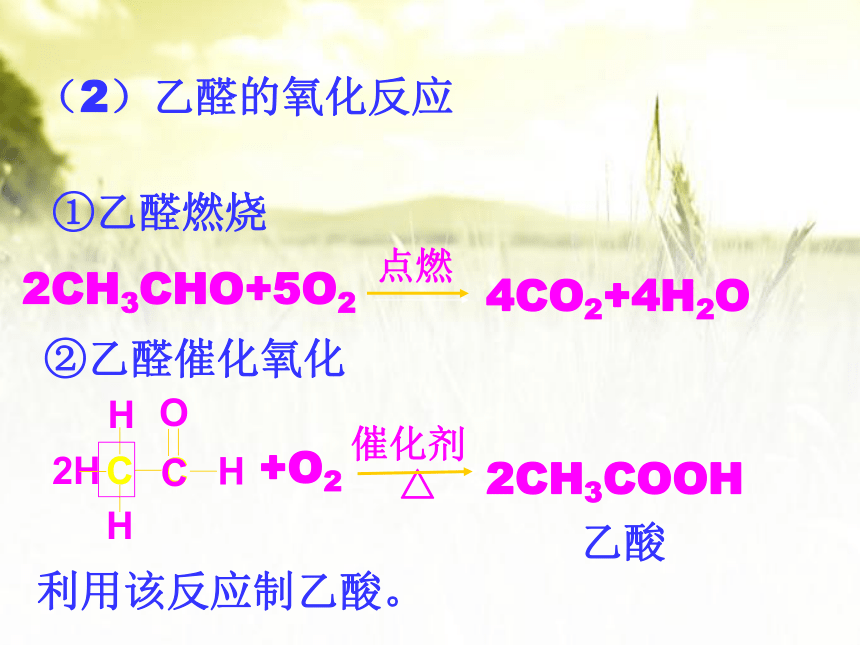
(2)乙醛的氧化反应
2CH3CHO+5O2
点燃
4CO2+4H2O
+O2
2CH3COOH
催化剂
△
乙酸
C
H
H
2H
C
O
H
C
利用该反应制乙酸。
①乙醛燃烧
②乙醛催化氧化
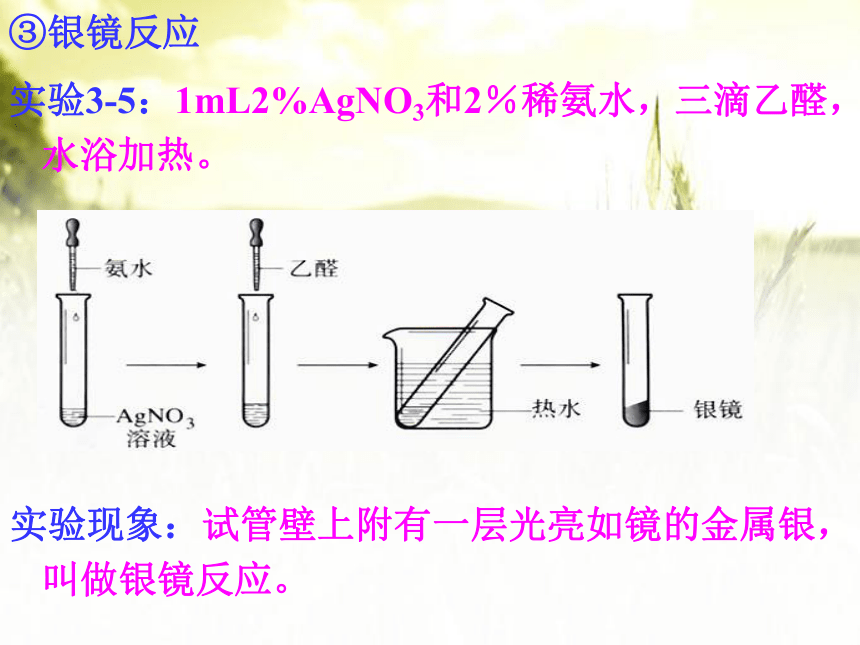
③银镜反应
实验3-5:1mL2%AgNO3和2%稀氨水,三滴乙醛,水浴加热。
实验现象:试管壁上附有一层光亮如镜的金属银,叫做银镜反应。
化学方程式:
AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
CH3CHO+2Ag(NH3)2OH
△
CH3COONH4+2Ag↓+3NH3+H2O
该反应可以检验醛基。
注意:
1、试管壁光滑洁净;
2、氨水防止过量;
3、水浴加热;
4、加热过程中试管不能振荡。
④与新制的Cu(OH)2反应
实验3-6:2mL10%NaOH和滴入2%硫酸铜4-6滴,振荡后加入0.5mL乙醛,加热。
实验现象:蓝色变为棕黄色变为红色沉淀
10%NaOH
2%CuSO4
乙醛
化学方程式:
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
该反应也可以检验醛基。
CH3CHO+2Cu(OH)2+NaOH
△
CH3COONa+Cu2O
↓
+3H2O
练习1:丙醛被银氨溶液氧化的方程式
CH3CH2CHO+2Ag(NH3)2OH
△
CH3CH2COONH4+2Ag↓+3NH3+H2O
练习2:丙醛被新制的Cu(OH)2氧化的方程式
CH3CH2CHO+2Cu(OH)2+NaOH
△
CH3CH2COONa+Cu2O
↓
+3H2O
二、醛类
1、醛的定义:烃基与醛基相连而构成的化合物。
简写成:RCHO
2、饱和一元醛的通式:CnH2nO
常见的醛:CH3CHO
3、醛的化学性质(联想乙醛)
1、物理性质
甲醛俗称蚁醛,无色具有强烈刺激性气味的气体,易溶于水。分子中有两个醛基。
质量分数为35%-40%的甲醛水溶液俗称福尔马林。
2、分子结构
三、甲醛
3、化学性质
甲醛和银氨溶液反应:
HCHO+4Ag(NH3)2OH
(NH4)2CO3+4Ag↓+6NH3+2H2O
△
甲醛和新制的Cu(OH)2反应:
HCHO+4Cu(OH)2+2NaOH
Na2CO3+2Cu2O↓+6H2O
△
4、用途
甲醛杀菌、防腐;甲醛还是重要的有机合成原料。
甲醛分子中相当于有两个醛基
小结:
(1)加成反应(与H2)
(2)氧化反应
三、甲醛
二、醛类
一.乙醛
1、物理性质
2、分子结构
3、化学性质
1、乙醛既有氧化性,又有还原性,以还原性为主
CH3CHO
乙醛
氧化
还原(加成)
CH3CH2OH
乙醇
CH3COOH
乙酸
氧化
有机物之间的转变实质是官能团之间的转变
2、
归纳总结
【达标练习】
1、下列配制银氨溶液的操作中,正确的是(??)。
A.在洁净的试管中加入1~2mLAgN03溶液,再加入过量浓氨水,振荡,混合均匀
B.在洁净的试管中加入1~2mL浓氨水,再加入AgNO3
溶液至过量
C.在洁净的试管中加入1~2mL稀氨水,再逐滴加入2%AgNO3
溶液至过量
D.在洁净的试管中加入2%AgNO3溶液1~2mL,逐滴加入2%稀氨水至沉淀恰好溶解为止
2、在下列有机物中:①乙醇,②苯乙烯,③甲醛,④苯酚,⑤苯甲醛,⑥溴乙烷
???
(1)能使酸性KMnO4溶液褪色的有_____________;
???
(2)能发生加聚反应的有___________;
???
(3)能与NaOH溶液反应的有___________;
???
(4)能发生银镜反应的有___________;
(5)能发生消去反应的有___________。
第三章
烃的含氧衍生物
第二节
醛
常见的醛
桂皮中含有肉桂醛
-CH=CH-CHO
杏仁中含有苯甲醛
-CHO
含有香草醛的兰花
-CHO
HO-
CH3O
前
言
2CH3CH2OH+O2
2CH3CHO+2H2O
催化剂
△
乙醛
我们已知:
教学目标:
1、了解乙醛的物理性质
2、掌握乙醛的加成反应和氧化反应
3、了解醛类的一般通性,甲醛性质与用途
教学难点:乙醛与弱氧化剂反应方程式书写
教学重点:乙醛的结构特点和化学性质
1、乙醛的物理性质
(1)无色
(2)有刺激性气味
(3)液体
(4)有毒
(5)易挥发;易燃烧
(6)与水、乙醇等互溶
(7)沸点:20.8℃
(8)密度小于水
(1)分子式:
(2)结构式:
2、乙醛的分子结构
(3)结构简式:
C2H4O
CH3CHO
官能团:
C
H
H
H
C
O
H
C
C
O
H
C
醛基
乙醛的核磁共振氢谱:两个峰。
乙醛分子有两种氢原子。较高峰-CH3中的氢原子;较低峰-CHO中的氢原子。
(1)乙醛的加成反应
C
H
H
H
C
O
H
C
+H2
催化剂
△
C2H5OH
3、乙醛的化学性质
(2)乙醛的氧化反应
2CH3CHO+5O2
点燃
4CO2+4H2O
+O2
2CH3COOH
催化剂
△
乙酸
C
H
H
2H
C
O
H
C
利用该反应制乙酸。
①乙醛燃烧
②乙醛催化氧化
③银镜反应
实验3-5:1mL2%AgNO3和2%稀氨水,三滴乙醛,水浴加热。
实验现象:试管壁上附有一层光亮如镜的金属银,叫做银镜反应。
化学方程式:
AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
CH3CHO+2Ag(NH3)2OH
△
CH3COONH4+2Ag↓+3NH3+H2O
该反应可以检验醛基。
注意:
1、试管壁光滑洁净;
2、氨水防止过量;
3、水浴加热;
4、加热过程中试管不能振荡。
④与新制的Cu(OH)2反应
实验3-6:2mL10%NaOH和滴入2%硫酸铜4-6滴,振荡后加入0.5mL乙醛,加热。
实验现象:蓝色变为棕黄色变为红色沉淀
10%NaOH
2%CuSO4
乙醛
化学方程式:
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
该反应也可以检验醛基。
CH3CHO+2Cu(OH)2+NaOH
△
CH3COONa+Cu2O
↓
+3H2O
练习1:丙醛被银氨溶液氧化的方程式
CH3CH2CHO+2Ag(NH3)2OH
△
CH3CH2COONH4+2Ag↓+3NH3+H2O
练习2:丙醛被新制的Cu(OH)2氧化的方程式
CH3CH2CHO+2Cu(OH)2+NaOH
△
CH3CH2COONa+Cu2O
↓
+3H2O
二、醛类
1、醛的定义:烃基与醛基相连而构成的化合物。
简写成:RCHO
2、饱和一元醛的通式:CnH2nO
常见的醛:CH3CHO
3、醛的化学性质(联想乙醛)
1、物理性质
甲醛俗称蚁醛,无色具有强烈刺激性气味的气体,易溶于水。分子中有两个醛基。
质量分数为35%-40%的甲醛水溶液俗称福尔马林。
2、分子结构
三、甲醛
3、化学性质
甲醛和银氨溶液反应:
HCHO+4Ag(NH3)2OH
(NH4)2CO3+4Ag↓+6NH3+2H2O
△
甲醛和新制的Cu(OH)2反应:
HCHO+4Cu(OH)2+2NaOH
Na2CO3+2Cu2O↓+6H2O
△
4、用途
甲醛杀菌、防腐;甲醛还是重要的有机合成原料。
甲醛分子中相当于有两个醛基
小结:
(1)加成反应(与H2)
(2)氧化反应
三、甲醛
二、醛类
一.乙醛
1、物理性质
2、分子结构
3、化学性质
1、乙醛既有氧化性,又有还原性,以还原性为主
CH3CHO
乙醛
氧化
还原(加成)
CH3CH2OH
乙醇
CH3COOH
乙酸
氧化
有机物之间的转变实质是官能团之间的转变
2、
归纳总结
【达标练习】
1、下列配制银氨溶液的操作中,正确的是(??)。
A.在洁净的试管中加入1~2mLAgN03溶液,再加入过量浓氨水,振荡,混合均匀
B.在洁净的试管中加入1~2mL浓氨水,再加入AgNO3
溶液至过量
C.在洁净的试管中加入1~2mL稀氨水,再逐滴加入2%AgNO3
溶液至过量
D.在洁净的试管中加入2%AgNO3溶液1~2mL,逐滴加入2%稀氨水至沉淀恰好溶解为止
2、在下列有机物中:①乙醇,②苯乙烯,③甲醛,④苯酚,⑤苯甲醛,⑥溴乙烷
???
(1)能使酸性KMnO4溶液褪色的有_____________;
???
(2)能发生加聚反应的有___________;
???
(3)能与NaOH溶液反应的有___________;
???
(4)能发生银镜反应的有___________;
(5)能发生消去反应的有___________。
