粗盐精制中的科学知识(课件 18张PPT)
文档属性
| 名称 | 粗盐精制中的科学知识(课件 18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-06-24 00:00:00 | ||
图片预览



文档简介
(共18张PPT)
中考专题复习
——粗盐精制中的科学知识
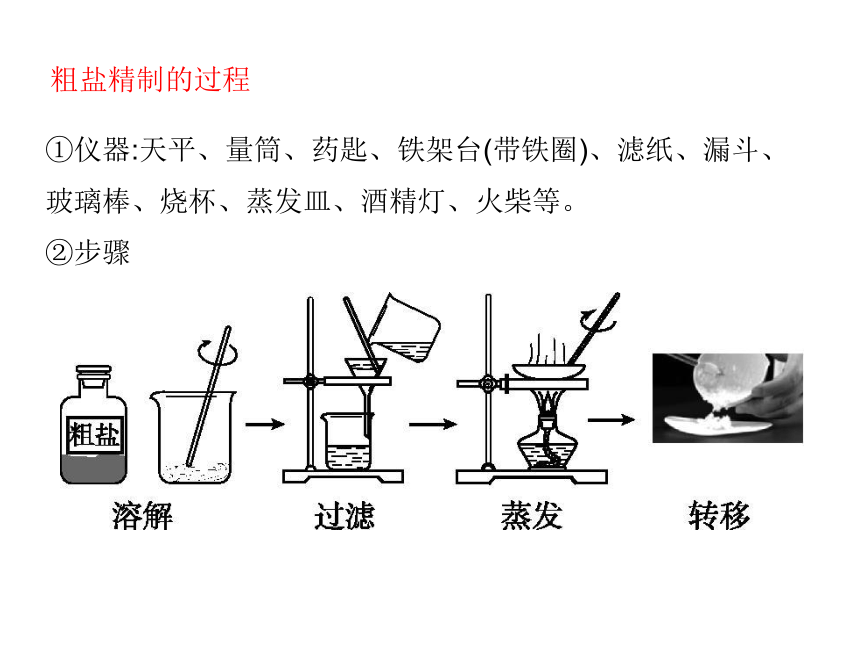
①仪器:天平、量筒、药匙、铁架台(带铁圈)、滤纸、漏斗、玻璃棒、烧杯、蒸发皿、酒精灯、火柴等。
②步骤
粗盐精制的过程
一、过滤(固液分离)
说明混合物分离的主要方法(过滤、蒸发)及操作要点
①过滤法及过滤实验操作
a.适用于将
和 分离。?
b.仪器:铁架台(带铁圈)、烧杯、
、
、滤纸等。?
c.注意“一贴、二低、三靠”:滤纸要紧贴 内壁;滤纸边缘要低于 边缘;液面要低于
边缘;烧杯嘴要紧靠 ;玻璃棒要轻靠
一边;漏斗末端要紧靠 内壁。?
不溶性固体
液体
漏斗
玻璃棒
漏斗
漏斗
滤纸
玻璃棒
三层滤纸
烧杯
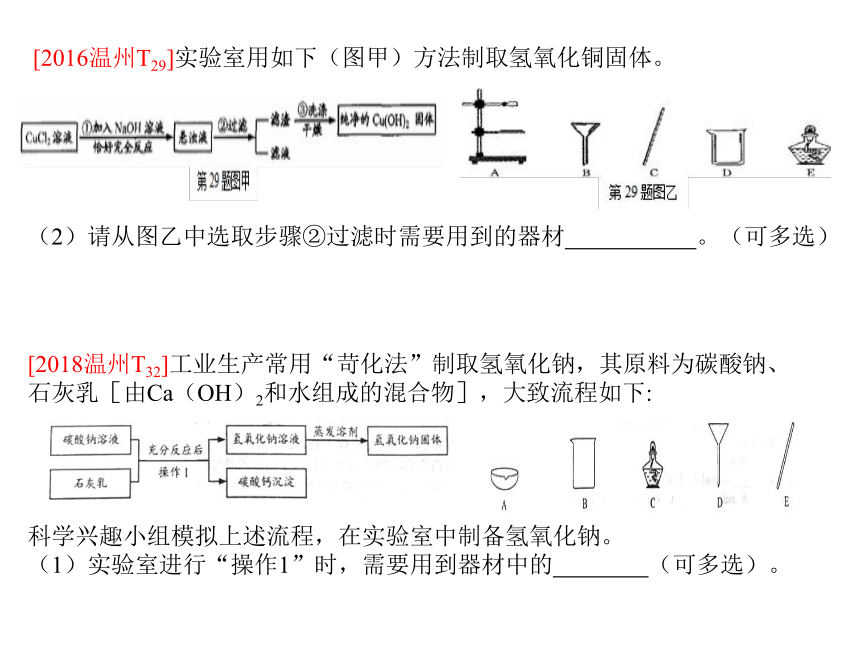
[2016温州T29]实验室用如下(图甲)方法制取氢氧化铜固体。
(2)请从图乙中选取步骤②过滤时需要用到的器材
。(可多选)
[2018温州T32]工业生产常用“苛化法”制取氢氧化钠,其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下:
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到器材中的
(可多选)。
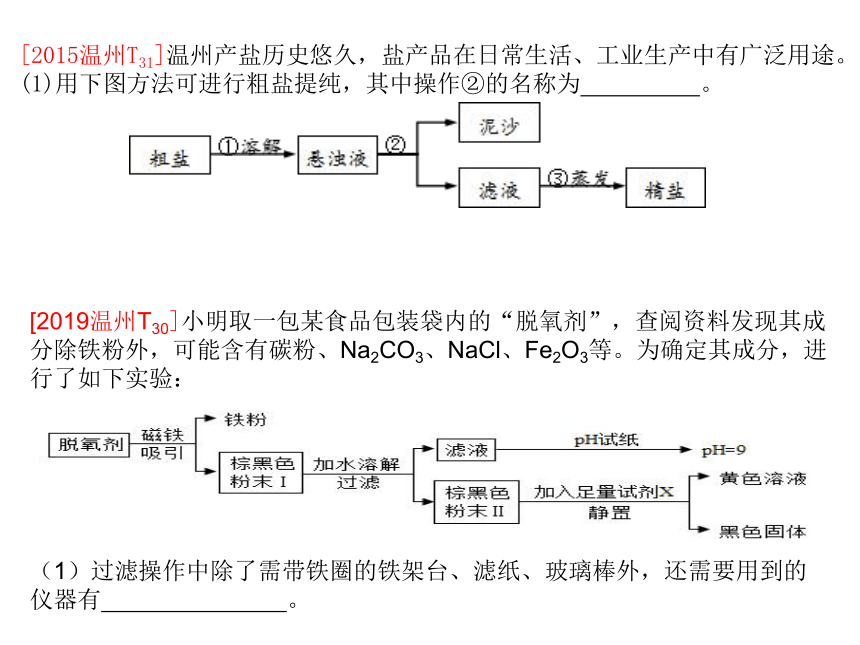
[2019温州T30]小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有
。
[2015温州T31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为
。
二、蒸发
a.仪器:三脚架(或带铁圈的铁架台)、 、 、酒精灯。?
b.注意事项:在蒸发过程中要不断地搅拌,当
时停止加热,剩余少量液体靠蒸发皿
蒸干,但仍需不停搅拌,直至冷却。?
蒸发皿
出现大量固体
玻璃棒
余热
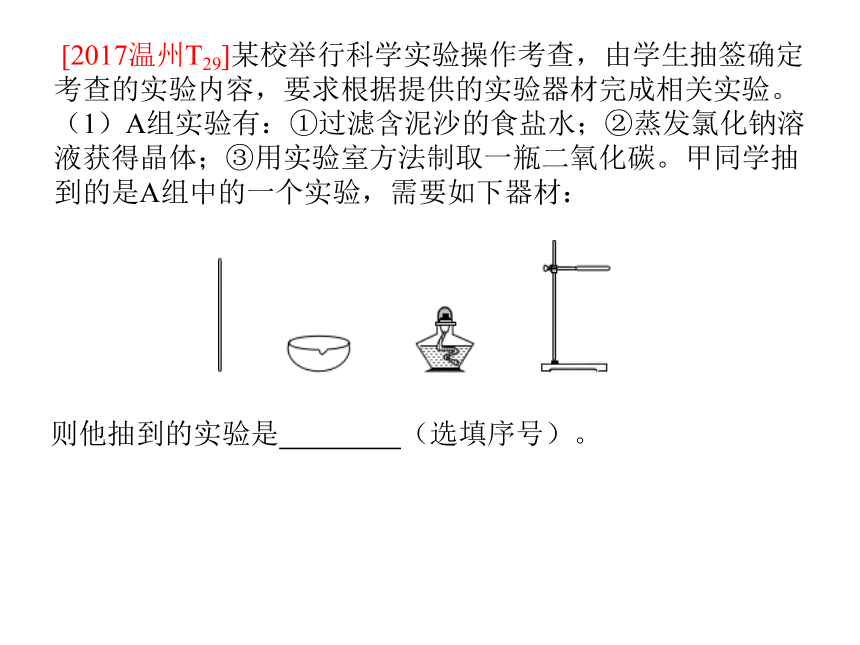
[2017温州T29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
则他抽到的实验是
(选填序号)。
溶液的质量
溶质的质量分数
三、溶质质量分数
溶质
[2016温州T29]实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤
①需配制200克溶质质量分数为4%的NaOH溶液,需NaOH固体
克。
[2017温州T29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
(2)乙同学抽到的是B组中的一个实验:配制50克10%的氯化钠溶液。为完成该实验,他应称取固体氯化钠
克。
[2015温州T31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。现有10千克溶质质量分数为25%的食盐水,若将其稀释到20%,需加水多少千克?
[2019温州T30]21.橘子罐头的生产过程中需要用稀盐酸和氢氧化钠去除橘络(橘瓣表面白色网状结构)
(2)去除橘络时,要控制好稀盐酸和氢氧化钠溶液的用量,以确保食品安全。某次生产过程中,要配制100千克质量分数为0.3%的氢氧化钠溶液,则需要氢氧化钠固体________千克。
原题呈现
[2015温州31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为
▲
。
(2)海水晒盐过程中,还能得到氯化镁(MgCl2)。工业上利用氯化镁在通电条件下分解,获得镁和氯气(Cl2)。写出这一反应的化学方程式:
▲
。
(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。现有10千克溶质质量分数为25%的食盐水,若将其稀释到20%,需加水多少千克?
[2016温州29]实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤
①需配制200克溶质质量分数为4%的NaOH溶液,需NaOH固体
克。
(2)请从图乙中选取步骤②过滤时需要用到的器材
。(可多选)
(3)步骤③需多次用蒸馏水清洗过滤装置中的滤渣,目的是去除残留在氢氧化铜表面的氯化钠溶液。实验中需要检验清洗后收集到的液体中是否含有氯化钠,写出检验的方法:
。
[2017温州29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
则他抽到的实验是
▲
(选填序号)。
(2)乙同学抽到的是B组中的一个实验:配制50克10%的氯化钠溶液。为完成该实验,他应称取固体氯化钠
▲
克。
(3)丙同学抽到的是B组中另一个实验:验证稀硫酸和氢氧化钠溶液的酸碱性。用到的试剂有:稀硫酸、氢氧化钠溶液、紫色石蕊试液。实验结束后,他将实验后的溶液全部倒入废液缸,混合溶液呈蓝色,则混合溶液中除石蕊外还含有的溶质为
▲
(写化学式)。
[2018温州32]工业生产常用“苛化法”制取氢氧化钠,其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下:科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到下列器材中的______(可多选)。
(2)制备氢氧化钠的化学方程式为:
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应计算所得氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1%)
[2019温州T30]小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有________
。
(2)写出用pH试纸测定滤液pH的方法:________。
(3)试剂X的名称是________。
课堂练习(龙湾模拟卷)
(乐清模拟卷)
课后作业
金卷七T29
金卷五T30
模拟卷四T29
中考专题复习
——粗盐精制中的科学知识
①仪器:天平、量筒、药匙、铁架台(带铁圈)、滤纸、漏斗、玻璃棒、烧杯、蒸发皿、酒精灯、火柴等。
②步骤
粗盐精制的过程
一、过滤(固液分离)
说明混合物分离的主要方法(过滤、蒸发)及操作要点
①过滤法及过滤实验操作
a.适用于将
和 分离。?
b.仪器:铁架台(带铁圈)、烧杯、
、
、滤纸等。?
c.注意“一贴、二低、三靠”:滤纸要紧贴 内壁;滤纸边缘要低于 边缘;液面要低于
边缘;烧杯嘴要紧靠 ;玻璃棒要轻靠
一边;漏斗末端要紧靠 内壁。?
不溶性固体
液体
漏斗
玻璃棒
漏斗
漏斗
滤纸
玻璃棒
三层滤纸
烧杯
[2016温州T29]实验室用如下(图甲)方法制取氢氧化铜固体。
(2)请从图乙中选取步骤②过滤时需要用到的器材
。(可多选)
[2018温州T32]工业生产常用“苛化法”制取氢氧化钠,其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下:
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到器材中的
(可多选)。
[2019温州T30]小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有
。
[2015温州T31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为
。
二、蒸发
a.仪器:三脚架(或带铁圈的铁架台)、 、 、酒精灯。?
b.注意事项:在蒸发过程中要不断地搅拌,当
时停止加热,剩余少量液体靠蒸发皿
蒸干,但仍需不停搅拌,直至冷却。?
蒸发皿
出现大量固体
玻璃棒
余热
[2017温州T29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
则他抽到的实验是
(选填序号)。
溶液的质量
溶质的质量分数
三、溶质质量分数
溶质
[2016温州T29]实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤
①需配制200克溶质质量分数为4%的NaOH溶液,需NaOH固体
克。
[2017温州T29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
(2)乙同学抽到的是B组中的一个实验:配制50克10%的氯化钠溶液。为完成该实验,他应称取固体氯化钠
克。
[2015温州T31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。现有10千克溶质质量分数为25%的食盐水,若将其稀释到20%,需加水多少千克?
[2019温州T30]21.橘子罐头的生产过程中需要用稀盐酸和氢氧化钠去除橘络(橘瓣表面白色网状结构)
(2)去除橘络时,要控制好稀盐酸和氢氧化钠溶液的用量,以确保食品安全。某次生产过程中,要配制100千克质量分数为0.3%的氢氧化钠溶液,则需要氢氧化钠固体________千克。
原题呈现
[2015温州31]温州产盐历史悠久,盐产品在日常生活、工业生产中有广泛用途。
(1)用下图方法可进行粗盐提纯,其中操作②的名称为
▲
。
(2)海水晒盐过程中,还能得到氯化镁(MgCl2)。工业上利用氯化镁在通电条件下分解,获得镁和氯气(Cl2)。写出这一反应的化学方程式:
▲
。
(3)腌制咸鸭蛋需要合适溶质质量分数的食盐水。现有10千克溶质质量分数为25%的食盐水,若将其稀释到20%,需加水多少千克?
[2016温州29]实验室用如下(图甲)方法制取氢氧化铜固体。
(1)步骤
①需配制200克溶质质量分数为4%的NaOH溶液,需NaOH固体
克。
(2)请从图乙中选取步骤②过滤时需要用到的器材
。(可多选)
(3)步骤③需多次用蒸馏水清洗过滤装置中的滤渣,目的是去除残留在氢氧化铜表面的氯化钠溶液。实验中需要检验清洗后收集到的液体中是否含有氯化钠,写出检验的方法:
。
[2017温州29]某校举行科学实验操作考查,由学生抽签确定考查的实验内容,要求根据提供的实验器材完成相关实验。
(1)A组实验有:①过滤含泥沙的食盐水;②蒸发氯化钠溶液获得晶体;③用实验室方法制取一瓶二氧化碳。甲同学抽到的是A组中的一个实验,需要如下器材:
则他抽到的实验是
▲
(选填序号)。
(2)乙同学抽到的是B组中的一个实验:配制50克10%的氯化钠溶液。为完成该实验,他应称取固体氯化钠
▲
克。
(3)丙同学抽到的是B组中另一个实验:验证稀硫酸和氢氧化钠溶液的酸碱性。用到的试剂有:稀硫酸、氢氧化钠溶液、紫色石蕊试液。实验结束后,他将实验后的溶液全部倒入废液缸,混合溶液呈蓝色,则混合溶液中除石蕊外还含有的溶质为
▲
(写化学式)。
[2018温州32]工业生产常用“苛化法”制取氢氧化钠,其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下:科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到下列器材中的______(可多选)。
(2)制备氢氧化钠的化学方程式为:
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应计算所得氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1%)
[2019温州T30]小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有________
。
(2)写出用pH试纸测定滤液pH的方法:________。
(3)试剂X的名称是________。
课堂练习(龙湾模拟卷)
(乐清模拟卷)
课后作业
金卷七T29
金卷五T30
模拟卷四T29
