高中化学人教版选修6第二单元课题二 物质的制备 氢氧化亚铁制备的实验探究 课件(26张PPT)
文档属性
| 名称 | 高中化学人教版选修6第二单元课题二 物质的制备 氢氧化亚铁制备的实验探究 课件(26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-25 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
审
活
氢氧化亚铁制备的实验探究
评
动
目录
contents
三
一
教材分析
Fe(OH)2的制备是人民教育出版社《普通高中课程标准实验教科书:化学1(必修)》第三章第二节“几种重要的金属化合物”中一个重要的演示实验。该实验能加深对二价铁和三价铁性质的理解,是氧化还原反应的具体应用,具有很强的探究性。
二
本实验安排在学生高中生涯的第一学期的末端,学生对高中知识也已经有了初步的认识,初步具备以探究为主的合作学习模式。在教师的日常课堂演示实验中,也常常运用提出假设——推理判断——实验验证——得出结论的探究学习方法。本次实验设计是学生分组探究讨论式自主合作学习。
学情分析
知识与技能
a.学生掌握二价铁的性质以及二价铁与三价铁的相互转化。
b.学生能够利用已有知识设计一种制备方法并能进行分析、对比、
评价。
过程与方法
a.通过创设问题情景引导学生体会发现、猜想、设计、实践的科学研究的基本方法。
b.通过合作学习,体会提出问题——实验探究——交流与评价的科学研究方法。
情感态度与价值观
a.学生通过实验设计及实践过程中体验科学研究的艰辛与喜悦。
b.学生通过师生,生生交流,培养协作意识和团队精神。
教学难点
本节内容的难点是设计制备氢氧化亚铁方案的具体实施。
教学重点
本节内容的重点是制备氢氧化亚铁的可行性的方案的设计。
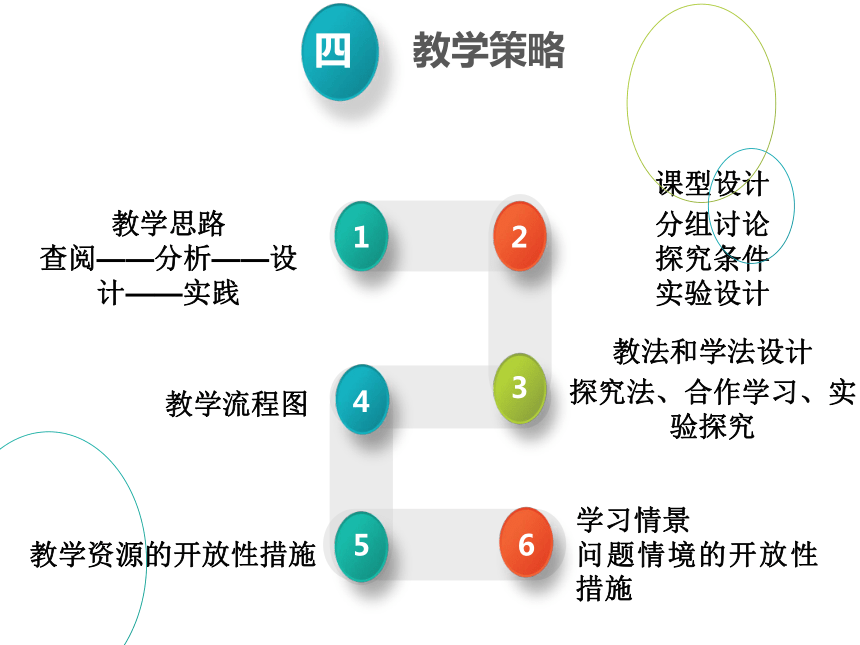
教学思路
查阅——分析——设计——实践
课型设计
分组讨论
探究条件
实验设计
教法和学法设计
探究法、合作学习、实验探究
教学流程图
教学资源的开放性措施
学习情景
问题情境的开放性措施
1
2
3
4
5
6
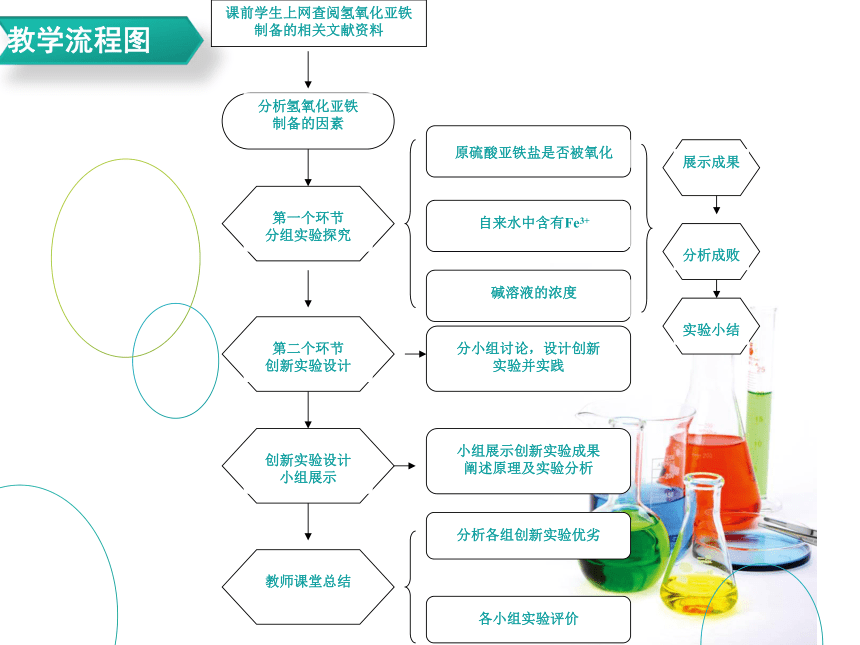
教学流程图
①Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
②温度升高,水中气体的溶解度降低
③2Fe3+
+
Fe
==
3Fe2+
④20%的氯化钠溶液中溶解氧的浓度下降了70%
①探究如何排除原料中Fe3+的干扰;
②优化碱液的浓度和精细化;
③实验设计还原性氛围来排除氧气的干扰,使得氢氧化亚铁免于氧化;
④创新实验免除油封,改用20%的氯化钠溶液来配制溶液,减少水中溶解氧的含量,实验简单易操作;
⑤运用电解硫酸钠溶液来制备氢氧化亚铁,实验一举多得,实验效果好。
试管、橡胶塞、胶头滴管、酒精灯、试管夹、药匙、烧杯、量筒、分液漏斗、直角弯管、托盘天平、药匙、玻璃棒、秒表
蒸馏水、氢氧化钠(s)、还原铁粉、稀硫酸、硫酸亚铁(s)、氯化钠(s)、煤油、硫酸钠(s)——固体药品均为分析纯
分析教材
找出问题
查阅资料
分析问题
设计实验
推理验证
教师总结
效果评价
4
学生通过实验和教材对比,发现理论和实践的不统一,激发学生学习探究的兴趣。
这一步的设计大大提高学生查阅资料,分析资料,信息提取的能力,同时推进了学生的逻辑推理思维和细节剖析能力。
探究实验一原亚铁盐被氧化为Fe3+和自来水自带Fe3+
探究实验二碱溶液的浓度
学生创新实验
教师点评实验效果的实验分析,辅助学生深刻理解实验和理论的误差,使得实践上升至理论,理论回落到实践。
问题的提出
按教材的方法进行实验,很难持续观察到白色沉淀这一现象。只能在开始的瞬间观察到灰绿夹杂白色,继而迅速加深,变成墨绿色,溶液中的浊液长时间处于深绿色状态。
只有经振荡后试管壁上才出现红色颗粒。实验结果与教材描述有一定差异,会令学生质疑Fe(OH)2的真实颜色以及Fe(OH)2的生成。
问题的分析
1、原亚铁盐被氧化为Fe3+
2、自来水自带Fe3+
3、滴加顺序与速率
4、碱溶液的浓度
5、沉淀的紧密度
6、Fe(OH)2自身的Schikorr歧化反应
7、溶液含有溶解氧
第一大组
分组实验探究
第二大组
分组实验探究
各小组
创新实验设计
1、原亚铁盐不纯被氧化为Fe3+
2、自来水自带Fe3+
步骤:分别用自来水、蒸馏水、加入铁粉的蒸馏水配制1mol/L硫酸亚铁和1mol/L氢氧化钠溶液;取2ml硫酸亚铁溶液于试管,往试管中滴加4ml氢氧化钠溶液,静置,观察实验现象,记录实验数据
探究实验一
实验原理:Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
实验时间:10min
问题的解决
3、碱溶液的浓度
探究实验二
实验原理:Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
步骤:蒸馏水配制1mol/L硫酸亚铁(加入过量的铁粉)和4种不同浓度的氢氧化钠溶液;取硫酸亚铁溶液底层2ml液体于四支试管,往试管中分别滴加4ml不同浓度氢氧化钠溶液,静置
,观察实验,并对比实验现象
实验时间:10min
实验安全教育
1、遵守化学实验室的规定
2、实验前熟悉实验原理、药品、和操作
3、所有实验操作一定要按标准实验操作进行
4、实验过程中突发事件务必通知实验老师前去处理
探究实验一&二结论
1、原亚铁盐被氧化为Fe3+
2、自来水自带Fe3+
3、碱溶液的浓度
亚铁盐长期存放的确会被氧化为Fe3+,并对实验室制备氢氧化亚铁沉淀带来干扰,处理方法,可加入还原性铁粉改善被氧化情况
自来水管氧化的确带来Fe3+,但这个含量比较少,影响不大。
碱溶液的浓度过低,生成沉淀量少,容易被氧化;碱溶液的浓度过高,生成非白色不明物质。解决办法——使用浓氨水代替强碱。
小结
蒸馏水配制硫酸亚铁溶液(含过量铁粉)和氨水反应制备氢氧化亚铁沉淀
创新实验探究
设计实验排除溶解氧对氢氧化亚铁制备的干扰
方法:
溶剂煮沸、
配制好的溶液油封、
在还原性气体中制备、
…………
实验时间:15min
第一组
煤油
第二组
FeSO4
NaOH固体
微加热
第三组
第四组
硫酸亚铁
铁粉
稀硫酸
NaOH
第五组
溶液均由20%的NaCl配制
第六组
硫酸钠
组别
团体合作
操作规范
简单易操作
实验效果
总评
第一组
第二组
第三组
第四组
第五组
第六组
实验原理:
Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
探究实验一原亚铁盐被氧化为Fe3+和自来水自带Fe3+
探究实验二碱溶液的浓度
创新实验设计——实验成果展示
实验效果评价
氢氧化亚铁制备的实验探究
谢
指
导
感谢各位评委老师指导
THANK
YOU
FOR
WATCHING
谢
审
活
氢氧化亚铁制备的实验探究
评
动
目录
contents
三
一
教材分析
Fe(OH)2的制备是人民教育出版社《普通高中课程标准实验教科书:化学1(必修)》第三章第二节“几种重要的金属化合物”中一个重要的演示实验。该实验能加深对二价铁和三价铁性质的理解,是氧化还原反应的具体应用,具有很强的探究性。
二
本实验安排在学生高中生涯的第一学期的末端,学生对高中知识也已经有了初步的认识,初步具备以探究为主的合作学习模式。在教师的日常课堂演示实验中,也常常运用提出假设——推理判断——实验验证——得出结论的探究学习方法。本次实验设计是学生分组探究讨论式自主合作学习。
学情分析
知识与技能
a.学生掌握二价铁的性质以及二价铁与三价铁的相互转化。
b.学生能够利用已有知识设计一种制备方法并能进行分析、对比、
评价。
过程与方法
a.通过创设问题情景引导学生体会发现、猜想、设计、实践的科学研究的基本方法。
b.通过合作学习,体会提出问题——实验探究——交流与评价的科学研究方法。
情感态度与价值观
a.学生通过实验设计及实践过程中体验科学研究的艰辛与喜悦。
b.学生通过师生,生生交流,培养协作意识和团队精神。
教学难点
本节内容的难点是设计制备氢氧化亚铁方案的具体实施。
教学重点
本节内容的重点是制备氢氧化亚铁的可行性的方案的设计。
教学思路
查阅——分析——设计——实践
课型设计
分组讨论
探究条件
实验设计
教法和学法设计
探究法、合作学习、实验探究
教学流程图
教学资源的开放性措施
学习情景
问题情境的开放性措施
1
2
3
4
5
6
教学流程图
①Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
②温度升高,水中气体的溶解度降低
③2Fe3+
+
Fe
==
3Fe2+
④20%的氯化钠溶液中溶解氧的浓度下降了70%
①探究如何排除原料中Fe3+的干扰;
②优化碱液的浓度和精细化;
③实验设计还原性氛围来排除氧气的干扰,使得氢氧化亚铁免于氧化;
④创新实验免除油封,改用20%的氯化钠溶液来配制溶液,减少水中溶解氧的含量,实验简单易操作;
⑤运用电解硫酸钠溶液来制备氢氧化亚铁,实验一举多得,实验效果好。
试管、橡胶塞、胶头滴管、酒精灯、试管夹、药匙、烧杯、量筒、分液漏斗、直角弯管、托盘天平、药匙、玻璃棒、秒表
蒸馏水、氢氧化钠(s)、还原铁粉、稀硫酸、硫酸亚铁(s)、氯化钠(s)、煤油、硫酸钠(s)——固体药品均为分析纯
分析教材
找出问题
查阅资料
分析问题
设计实验
推理验证
教师总结
效果评价
4
学生通过实验和教材对比,发现理论和实践的不统一,激发学生学习探究的兴趣。
这一步的设计大大提高学生查阅资料,分析资料,信息提取的能力,同时推进了学生的逻辑推理思维和细节剖析能力。
探究实验一原亚铁盐被氧化为Fe3+和自来水自带Fe3+
探究实验二碱溶液的浓度
学生创新实验
教师点评实验效果的实验分析,辅助学生深刻理解实验和理论的误差,使得实践上升至理论,理论回落到实践。
问题的提出
按教材的方法进行实验,很难持续观察到白色沉淀这一现象。只能在开始的瞬间观察到灰绿夹杂白色,继而迅速加深,变成墨绿色,溶液中的浊液长时间处于深绿色状态。
只有经振荡后试管壁上才出现红色颗粒。实验结果与教材描述有一定差异,会令学生质疑Fe(OH)2的真实颜色以及Fe(OH)2的生成。
问题的分析
1、原亚铁盐被氧化为Fe3+
2、自来水自带Fe3+
3、滴加顺序与速率
4、碱溶液的浓度
5、沉淀的紧密度
6、Fe(OH)2自身的Schikorr歧化反应
7、溶液含有溶解氧
第一大组
分组实验探究
第二大组
分组实验探究
各小组
创新实验设计
1、原亚铁盐不纯被氧化为Fe3+
2、自来水自带Fe3+
步骤:分别用自来水、蒸馏水、加入铁粉的蒸馏水配制1mol/L硫酸亚铁和1mol/L氢氧化钠溶液;取2ml硫酸亚铁溶液于试管,往试管中滴加4ml氢氧化钠溶液,静置,观察实验现象,记录实验数据
探究实验一
实验原理:Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
实验时间:10min
问题的解决
3、碱溶液的浓度
探究实验二
实验原理:Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
步骤:蒸馏水配制1mol/L硫酸亚铁(加入过量的铁粉)和4种不同浓度的氢氧化钠溶液;取硫酸亚铁溶液底层2ml液体于四支试管,往试管中分别滴加4ml不同浓度氢氧化钠溶液,静置
,观察实验,并对比实验现象
实验时间:10min
实验安全教育
1、遵守化学实验室的规定
2、实验前熟悉实验原理、药品、和操作
3、所有实验操作一定要按标准实验操作进行
4、实验过程中突发事件务必通知实验老师前去处理
探究实验一&二结论
1、原亚铁盐被氧化为Fe3+
2、自来水自带Fe3+
3、碱溶液的浓度
亚铁盐长期存放的确会被氧化为Fe3+,并对实验室制备氢氧化亚铁沉淀带来干扰,处理方法,可加入还原性铁粉改善被氧化情况
自来水管氧化的确带来Fe3+,但这个含量比较少,影响不大。
碱溶液的浓度过低,生成沉淀量少,容易被氧化;碱溶液的浓度过高,生成非白色不明物质。解决办法——使用浓氨水代替强碱。
小结
蒸馏水配制硫酸亚铁溶液(含过量铁粉)和氨水反应制备氢氧化亚铁沉淀
创新实验探究
设计实验排除溶解氧对氢氧化亚铁制备的干扰
方法:
溶剂煮沸、
配制好的溶液油封、
在还原性气体中制备、
…………
实验时间:15min
第一组
煤油
第二组
FeSO4
NaOH固体
微加热
第三组
第四组
硫酸亚铁
铁粉
稀硫酸
NaOH
第五组
溶液均由20%的NaCl配制
第六组
硫酸钠
组别
团体合作
操作规范
简单易操作
实验效果
总评
第一组
第二组
第三组
第四组
第五组
第六组
实验原理:
Fe
SO4
+
2NaOH
===
Fe(OH)2
+
Na
2SO4
探究实验一原亚铁盐被氧化为Fe3+和自来水自带Fe3+
探究实验二碱溶液的浓度
创新实验设计——实验成果展示
实验效果评价
氢氧化亚铁制备的实验探究
谢
指
导
感谢各位评委老师指导
THANK
YOU
FOR
WATCHING
谢
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
