鲁科版高中化学选修 有机化学基础2.1有机化学基本反应类型 课件(共61张PPT)
文档属性
| 名称 | 鲁科版高中化学选修 有机化学基础2.1有机化学基本反应类型 课件(共61张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 452.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-06-26 00:00:00 | ||
图片预览









文档简介
(共61张PPT)
有机化学
有机物的基本反应类型
有机化学反应:
有机反应主要包括八大基本类型:
取代反应、加成反应、消去反应、氧化反应、还原反应、加聚反应、缩聚反应、显色反应,
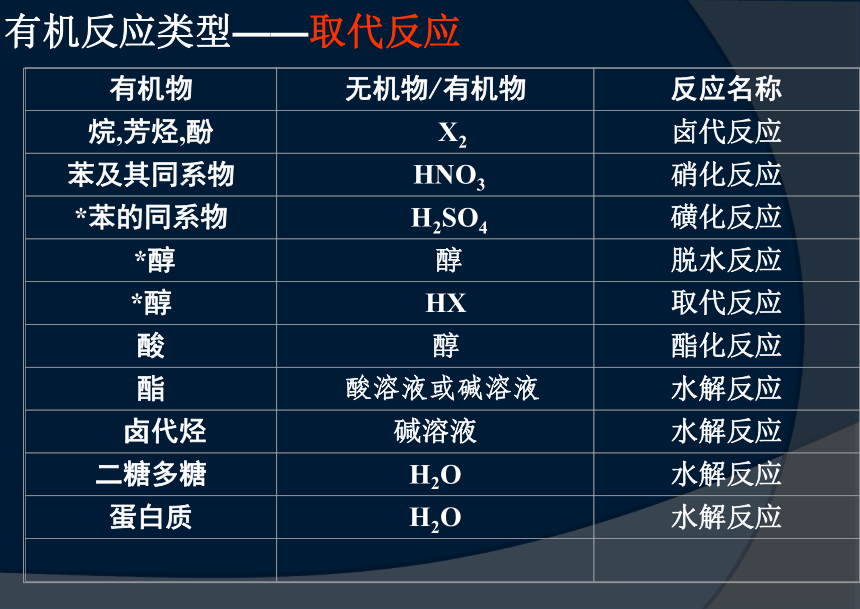
有机反应类型——取代反应
原理:“有进有出”
包括:卤代、硝化、酯化、水解、分子间脱水
一、取代反应
①
是一类有机反应;
②
是原子或原子团与另一原子或原子团的交换;
③
两种物质反应,生成两种物质,有进有出的;
④
该反应前后的有机物的空间结构没有发生变
化;
⑤
取代反应总是发生在单键上;
⑥
这是饱和化合物的特有反应。
有机反应类型——取代反应
1、卤代反应
烷烃的卤代,苯系芳烃的卤代,苯酚的卤代。
CH4+
Cl2→(条件、现象、产物、物质的量)
C
H
+
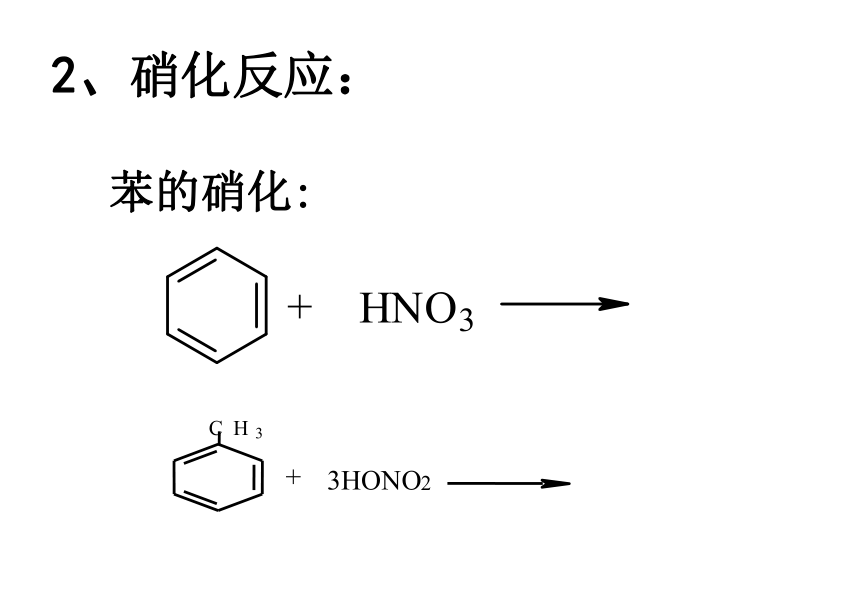
2、硝化反应:
苯的硝化:
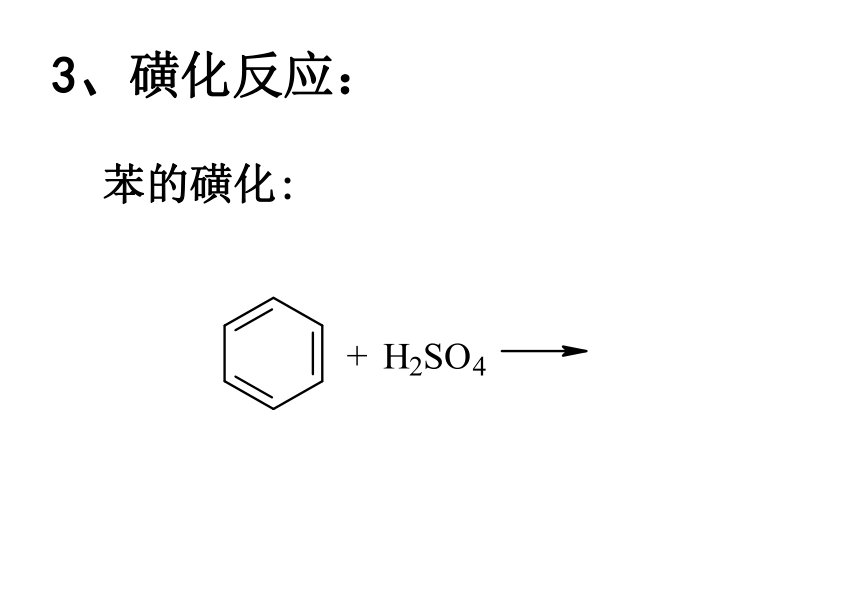
3、磺化反应:
苯的磺化:
4、酯化反应:
醇和羧酸酯化,醇和无机酸的酯化
CH3COOH+C2H5OH →
HOOCCOOH+C2H5OH →
HOOCCOOH+HOCH2CH2OH→
C2H5OH+HNO3→
(条件、现象、应用)
5、水解反应
(1)H2NCH2CONHCH2COOH+H2O→
(2)C12H22O11(蔗糖)+H2O→
(3)
C12H22O11(麦芽糖)+H2O
→
(4)(C6H10O5)n(淀粉)+H2O
→
(5)(C6H10O5)n(纤维素)+H2O
→
(条件、现象、应用)
6、皂化反应
NaOH→
(条件、现象、应用)
7、其它反应
(1)CaC2+H2O→
(2)2C2H5OH→
(3)C2H5OH+HBr→
(4)CH3COONa+
NaOH→
(条件、现象、应用)
有机反应类型——加成反应
原理:“有进无出”
包括:烯烃及含C=C的有机物、炔烃及含C≡C的有机物与H2、X2、HX、H2O加成、苯环、醛基、不饱和油脂与H2加成
二、加成反应
①
是一类有机反应;
②
加成反应发生在不饱和?碳?原子上;
③该反应中加进原子或原子团,只生成一种有机物?相当于化合反应),只进不出。
④加成前后的有机物的结构将发生变化,烯烃变烷烃,结构由平面形变立体形;炔烃变烯烃,结构由直线形变平面形;
⑤加成反应是不饱和化合物的较特有反应,另外,芳香族化合物也有可能发生加成反应。
有机反应类型——加成反应
和H2加成的条件一般是催化剂(Ni)+加热
和水加成时,一般在一定的温度、压强和催化剂条件下
不对称烯烃或炔烃和H2O、HX加成时可能产生两种产物
醛基的C=O只能和H2加成,不能和X2加成,而羧基和酯的C=O不能发生加成反应
若一种物质中同时存在C=C、醛基等多个官能团时,和氢气的加成反应可同时进行,也可以有选择地进行,看信息而定
(条件、现象、应用)
(1)C=C与H2、X2、HX、H2O:
(2)C≡C与H2、X2、HX、H2O:
(3)苯与H2
(4)醛与氢气加成:
(5)油脂氢化:
有机反应类型——消去反应
原理:“无进有出”
包括:醇消去H2O生成烯烃、
卤代烃消去HX生成烯烃
有机反应类型——消去反应
说明:
消去反应的实质:—OH或—X与所在碳相邻的碳原子上的-H结合生成H2O或HX而消去
不能发生消去反应的情况:—OH或—X所在的碳无相邻碳原子,或相邻碳原子上无氢(注意区分不能消去和不能氧化的醇)
有不对称消去的情况,由信息定产物
消去反应的条件:醇类是浓硫酸+加热;
卤代烃是NaOH醇溶液+加热
有机反应类型——氧化反应
原理:有机物得氧或去氢
包括:
燃烧反应、被空气(氧气)氧化、(醇是去氢氧化)
被酸性KMnO4溶液氧化,
醛基的银镜反应和被新制Cu(OH)2悬浊液氧化
烯烃被臭氧氧化
(O3,Zn/HCl,双键断裂,原双键碳变为C=O)
有机反应类型——氧化反应
说明:
有机物一般都可以发生氧化反应,此过程发生了碳碳键或碳氧键的断裂
醇氧化的规律:
伯醇氧化生成醛,如CH3CH2OH
仲醇氧化生成酮,如(CH3)2CHOH
叔醇不能被氧化,如(CH3)3COH
多官能团物质被氧化的顺序看信息
有机反应类型——还原反应
原理:有机物得氢或去氧
包括:烯、炔、苯环、醛、油脂等和氢气加成,
硝基被还原为氨基
(如硝基苯被Fe+HCl还原为苯胺)
说明:“氧化”和“还原”反应是针对有机物而言的,有机物被氧化则定义为氧化反应,有机物被还原则定义为还原反应
有机反应类型——加聚反应
类型(联系书上提到的高分子材料):
乙烯型加聚
聚丙烯、聚苯乙烯、聚氯乙烯、
聚丙烯腈、聚甲基丙烯酸甲酯(有机玻璃)
1,3-丁二烯型加聚(破两头,移中间)
天然橡胶(聚异戊二烯)
氯丁橡胶(聚一氯丁二烯)
含有双键的不同单体间的共聚
乙丙树脂(乙烯和丙烯共聚),
丁苯橡胶(丁二烯和苯乙烯共聚)
有机反应类型——加聚反应
说明
单体通常是含有C=C或C≡C的化合物
链节与单体的相对分子质量相等
产物中仅有高聚物,无其它小分子,但生成的高聚物因n值不同,是混合物
由加聚产物判断单体的“二、四”法
有机反应类型——缩聚反应
类型
酚醛缩聚(高聚物链节中含酚羟基)
苯酚和甲醛缩聚成酚醛树脂(电木)
氨基酸缩聚(高聚物链节中含酰胺键)
氨基酸缩合成多肽或蛋白质
醇酸缩聚(高聚物链节中含酯基)
乙二醇和乙二酸(或对苯二甲酸)的缩聚
有机反应类型——缩聚反应
说明
缩聚反应生成高分子和小分子,如H2O
若高分子化合物的链节并非完全以碳原子连接,如有酚羟基、-COO-、-CO-NH-等,则该高分子是缩聚反应的产物
判断缩聚反应的单体(水解法):
先判断缩聚类型,再解聚
解聚方法:先断开羰基与氧原子(或氮原子)之间的键,然后给羰基加上羟基,给氧或氮接上氢原子,链节两端的羰基、氧或氮也按此法接上羟基或氧原子
有机反应类型——显色反应
包括
苯酚遇FeCl3溶液显紫色
淀粉遇碘单质显蓝色
含苯环的蛋白质遇浓硝酸凝结显黄色
多羟基物质(甘油、葡萄糖)与新制Cu(OH)2悬浊液生成绛蓝色物质
有机反应类型——酯化反应拓展
机理:一般为羧酸脱羟基,醇脱氢
类型
一元羧酸和一元醇反应生成普通酯
二元羧酸和二元醇
部分酯化生成普通酯和1分子H2O,
或生成环状酯和2分子H2O,
或生成高聚酯和2n
H2O
羟基羧酸自身反应既可以部分酯化生成普通酯,也可以生成环状酯,还可以生成高聚酯。如乳酸分子
有机反应类型——酯化反应拓展
乙二酸和乙二醇酯化
有机反应类型——酯化反应拓展
其它酯
硝化甘油(三硝酸甘油酯)
硝酸纤维(纤维素硝酸酯)
油脂(硬脂酸甘油酯、软脂酸甘油酯、油酸甘油酯)
苯酚中的羟基也能发生酯化反应(且水解后还消耗NaOH)
有机反应类型——知识归纳
反应条件不同,反应不同
温度不同,产物和反应类型不同:
如乙醇在浓硫酸140℃和170℃的反应
溶剂不同,产物和反应类型不同:
如溴乙烷在NaOH的水溶液和醇溶液下的反应
催化剂不同,反应不同:
如甲苯在铁催化和光照条件下和氯气的取代反应
有机反应类型——知识归纳
书写有机化学反应的注意事项
写有机物的结构简式及反应条件
不漏写除了有机物外的其它无机小分子
如酯化反应、硝化反应、醇催化氧化、缩聚反应生成的H2O;卤代反应生成的HX等
配平:如醇、醛的催化氧化、银镜反应
专用名词不能出错
如,苯写“笨”、“酯”和“脂”混用、“硝化”写“消化”,
“水浴”写成“水狱”,“褪色”写成“腿色”
有机反应类型——知识归纳
反应条件
常
见
反
应
催化剂加热加压
乙烯水化、油脂氢化
催化剂
加热
烯、炔、苯环、醛加氢,
烯、炔和HX加成,醇的消去和氧化,乙醛和氧气反应,酯化反应
水浴加热
制硝基苯、银镜反应、蔗糖水解、
乙酸乙酯水解
只用催化剂
苯的溴代
只需加热
卤代烃消去、乙醛和Cu(OH)2反应
不需外加
条件
制乙炔,烯与炔加溴,烯、炔及苯的同系物被KMnO4氧化,苯酚的溴代,卤代烃的水解
有机反应类型——知识归纳
反应条件
反应类型
NaOH水溶液、加热
卤代烃或酯类的水解反应
NaOH醇溶液、加热
卤代烃的消去反应
稀H2SO4、加热
酯和糖类的水解反应
浓H2SO4、加热
酯化反应或苯环上的硝化反应
浓H2SO4、170℃
醇的消去反应
浓H2SO4、140℃
醇生成醚的取代反应
溴水
不饱和有机物的加成反应
浓溴水
苯酚的取代反应
有机反应类型——知识归纳
反应条件
反应类型
液Br2、Fe粉
苯环上的取代反应
X2、光照
烷烃或芳香烃烷基上的卤代
O2、Cu、加热
醇的催化氧化反应
O2或Ag(NH3)2OH或新制Cu(OH)2
醛的氧化反应
酸性KMnO4溶液
不饱和有机物或苯的同系物侧链上的氧化反应
H2、催化剂
不饱和有机物的加成反应
有机反应类型——加成反应
原理:“有进无出”
包括:烯烃及含C=C的有机物、炔烃及含C≡C的有机物与H2、X2、HX、H2O加成、苯环、醛基、不饱和油脂与H2加成
有机反应类型——加成反应
和H2加成的条件一般是催化剂(Ni)+加热
和水加成时,一般在一定的温度、压强和催化剂条件下
不对称烯烃或炔烃和H2O、HX加成时可能产生两种产物
醛基的C=O只能和H2加成,不能和X2加成,而羧基和酯的C=O不能发生加成反应
若一种物质中同时存在C=C、醛基等多个官能团时,和氢气的加成反应可同时进行,也可以有选择地进行,看信息而定
有机反应类型——消去反应
原理:“无进有出”
包括:醇消去H2O生成烯烃、
卤代烃消去HX生成烯烃
有机反应类型——消去反应
说明:
消去反应的实质:—OH或—X与所在碳相邻的碳原子上的-H结合生成H2O或HX而消去
不能发生消去反应的情况:—OH或—X所在的碳无相邻碳原子,或相邻碳原子上无氢(注意区分不能消去和不能氧化的醇)
有不对称消去的情况,由信息定产物
消去反应的条件:醇类是浓硫酸+加热;
卤代烃是NaOH醇溶液+加热
有机反应类型——氧化反应
原理:有机物得氧或去氢
包括:
燃烧反应、被空气(氧气)氧化、(醇是去氢氧化)
被酸性KMnO4溶液氧化,
醛基的银镜反应和被新制Cu(OH)2悬浊液氧化
烯烃被臭氧氧化
(O3,Zn/HCl,双键断裂,原双键碳变为C=O)
有机反应类型——氧化反应
说明:
有机物一般都可以发生氧化反应,此过程发生了碳碳键或碳氧键的断裂
醇氧化的规律:
伯醇氧化生成醛,如CH3CH2OH
仲醇氧化生成酮,如(CH3)2CHOH
叔醇不能被氧化,如(CH3)3COH
多官能团物质被氧化的顺序看信息
有机反应类型——还原反应
原理:有机物得氢或去氧
包括:烯、炔、苯环、醛、油脂等和氢气加成,
硝基被还原为氨基
(如硝基苯被Fe+HCl还原为苯胺)
说明:“氧化”和“还原”反应是针对有机物而言的,有机物被氧化则定义为氧化反应,有机物被还原则定义为还原反应
有机反应类型——加聚反应
类型(联系书上提到的高分子材料):
乙烯型加聚
聚丙烯、聚苯乙烯、聚氯乙烯、
聚丙烯腈、聚甲基丙烯酸甲酯(有机玻璃)
1,3-丁二烯型加聚(破两头,移中间)
天然橡胶(聚异戊二烯)
氯丁橡胶(聚一氯丁二烯)
含有双键的不同单体间的共聚
乙丙树脂(乙烯和丙烯共聚),
丁苯橡胶(丁二烯和苯乙烯共聚)
有机反应类型——加聚反应
说明
单体通常是含有C=C或C≡C的化合物
链节与单体的相对分子质量相等
产物中仅有高聚物,无其它小分子,但生成的高聚物因n值不同,是混合物
由加聚产物判断单体的“二、四”法
有机反应类型——缩聚反应
类型
酚醛缩聚(高聚物链节中含酚羟基)
苯酚和甲醛缩聚成酚醛树脂(电木)
氨基酸缩聚(高聚物链节中含酰胺键)
氨基酸缩合成多肽或蛋白质
醇酸缩聚(高聚物链节中含酯基)
乙二醇和乙二酸(或对苯二甲酸)的缩聚
有机反应类型——缩聚反应
说明
缩聚反应生成高分子和小分子,如H2O
若高分子化合物的链节并非完全以碳原子连接,如有酚羟基、-COO-、-CO-NH-等,则该高分子是缩聚反应的产物
判断缩聚反应的单体(水解法):
先判断缩聚类型,再解聚
解聚方法:先断开羰基与氧原子(或氮原子)之间的键,然后给羰基加上羟基,给氧或氮接上氢原子,链节两端的羰基、氧或氮也按此法接上羟基或氧原子
有机反应类型——显色反应
包括
苯酚遇FeCl3溶液显紫色
淀粉遇碘单质显蓝色
含苯环的蛋白质遇浓硝酸凝结显黄色
多羟基物质(甘油、葡萄糖)与新制Cu(OH)2悬浊液生成绛蓝色物质
有机反应类型——酯化反应拓展
机理:一般为羧酸脱羟基,醇脱氢
类型
一元羧酸和一元醇反应生成普通酯
二元羧酸和二元醇
部分酯化生成普通酯和1分子H2O,
或生成环状酯和2分子H2O,
或生成高聚酯和2n
H2O
羟基羧酸自身反应既可以部分酯化生成普通酯,也可以生成环状酯,还可以生成高聚酯。如乳酸分子
有机反应类型——酯化反应拓展
乙二酸和乙二醇酯化
有机反应类型——酯化反应拓展
其它酯
硝化甘油(三硝酸甘油酯)
硝酸纤维(纤维素硝酸酯)
油脂(硬脂酸甘油酯、软脂酸甘油酯、油酸甘油酯)
苯酚中的羟基也能发生酯化反应(且水解后还消耗NaOH)
有机反应类型——知识归纳
反应条件不同,反应不同
温度不同,产物和反应类型不同:
如乙醇在浓硫酸140℃和170℃的反应
溶剂不同,产物和反应类型不同:
如溴乙烷在NaOH的水溶液和醇溶液下的反应
催化剂不同,反应不同:
如甲苯在铁催化和光照条件下和氯气的取代反应
有机反应类型——知识归纳
书写有机化学反应的注意事项
写有机物的结构简式及反应条件
不漏写除了有机物外的其它无机小分子
如酯化反应、硝化反应、醇催化氧化、缩聚反应生成的H2O;卤代反应生成的HX等
配平:如醇、醛的催化氧化、银镜反应
专用名词不能出错
如,苯写“笨”、“酯”和“脂”混用、“硝化”写“消化”,
“水浴”写成“水狱”,“褪色”写成“腿色”
有机反应类型——知识归纳
反应条件
常
见
反
应
催化剂加热加压
乙烯水化、油脂氢化
催化剂
加热
烯、炔、苯环、醛加氢,
烯、炔和HX加成,醇的消去和氧化,乙醛和氧气反应,酯化反应
水浴加热
制硝基苯、银镜反应、蔗糖水解、
乙酸乙酯水解
只用催化剂
苯的溴代
只需加热
卤代烃消去、乙醛和Cu(OH)2反应
不需外加
条件
制乙炔,烯与炔加溴,烯、炔及苯的同系物被KMnO4氧化,苯酚的溴代,卤代烃的水解
有机反应类型——知识归纳
反应条件
反应类型
NaOH水溶液、加热
卤代烃或酯类的水解反应
NaOH醇溶液、加热
卤代烃的消去反应
稀H2SO4、加热
酯和糖类的水解反应
浓H2SO4、加热
酯化反应或苯环上的硝化反应
浓H2SO4、170℃
醇的消去反应
浓H2SO4、140℃
醇生成醚的取代反应
溴水
不饱和有机物的加成反应
浓溴水
苯酚的取代反应
有机反应类型——知识归纳
反应条件
反应类型
液Br2、Fe粉
苯环上的取代反应
X2、光照
烷烃或芳香烃烷基上的卤代
O2、Cu、加热
醇的催化氧化反应
O2或Ag(NH3)2OH或新制Cu(OH)2
醛的氧化反应
酸性KMnO4溶液
不饱和有机物或苯的同系物侧链上的氧化反应
H2、催化剂
不饱和有机物的加成反应
三、消去反应
①
是一类有机反应;
②
消去反应发生在分子内
③
发生在相邻的两个碳原子上;
④
消去反应会脱去小分子,即生成小分子;
⑤
消去后生成的有机物会产生双键或叁键;
⑥
消去前后的有机物的分子结构变发生变化,它与加成反应相反,因此,分子结构的变化正好与加成反应的情况相反。
具体的消去反应
卤代烃消去
C2H5Br+
NaOH→
2.
醇消去
C2H5OH→
四、聚合反应
?1?
加成聚合反应:简称加聚反应
A.CH2=CH2
B.CH3-CH=CH2
C.CH2=CHCl
D.CF2=CF2
E.C6H5-CH=G.
F.HCHO
(2).缩聚反应
双官能团的有机物、苯酚和甲醛氨基酸、醇和羧酸
nHOOCCOOH+nHOCH2CH2OH→
五、氧化反应
醇氧化成醛:C2H5OH
+
O2→
醛、甲酸、甲酸酯、葡萄糖、
麦芽糖的氧化
CH3CHO+
Ag(NH3)2OH→
使酸性高锰酸钾溶液褪色:
乙烯、乙炔
甲苯、苯酚、乙醛
六、还原反应
去氧、加氢是有机化学里的还原反应
不饱和烃及不饱和化合物的加氢,
油酯的氢化;
苯加氢变为环己烷,
苯乙烯加氢变成乙基环己烷
七、其它反应
1.裂化(解)反应
①
甲烷的高温分解
②
石油的裂化
石油的裂解
2.显色反应
(1)苯酚与铁盐溶液络合呈紫色
(2)蛋白质与浓硝酸作用呈黄色
(3)碘遇淀粉变蓝
有机化学
有机物的基本反应类型
有机化学反应:
有机反应主要包括八大基本类型:
取代反应、加成反应、消去反应、氧化反应、还原反应、加聚反应、缩聚反应、显色反应,
有机反应类型——取代反应
原理:“有进有出”
包括:卤代、硝化、酯化、水解、分子间脱水
一、取代反应
①
是一类有机反应;
②
是原子或原子团与另一原子或原子团的交换;
③
两种物质反应,生成两种物质,有进有出的;
④
该反应前后的有机物的空间结构没有发生变
化;
⑤
取代反应总是发生在单键上;
⑥
这是饱和化合物的特有反应。
有机反应类型——取代反应
1、卤代反应
烷烃的卤代,苯系芳烃的卤代,苯酚的卤代。
CH4+
Cl2→(条件、现象、产物、物质的量)
C
H
+
2、硝化反应:
苯的硝化:
3、磺化反应:
苯的磺化:
4、酯化反应:
醇和羧酸酯化,醇和无机酸的酯化
CH3COOH+C2H5OH →
HOOCCOOH+C2H5OH →
HOOCCOOH+HOCH2CH2OH→
C2H5OH+HNO3→
(条件、现象、应用)
5、水解反应
(1)H2NCH2CONHCH2COOH+H2O→
(2)C12H22O11(蔗糖)+H2O→
(3)
C12H22O11(麦芽糖)+H2O
→
(4)(C6H10O5)n(淀粉)+H2O
→
(5)(C6H10O5)n(纤维素)+H2O
→
(条件、现象、应用)
6、皂化反应
NaOH→
(条件、现象、应用)
7、其它反应
(1)CaC2+H2O→
(2)2C2H5OH→
(3)C2H5OH+HBr→
(4)CH3COONa+
NaOH→
(条件、现象、应用)
有机反应类型——加成反应
原理:“有进无出”
包括:烯烃及含C=C的有机物、炔烃及含C≡C的有机物与H2、X2、HX、H2O加成、苯环、醛基、不饱和油脂与H2加成
二、加成反应
①
是一类有机反应;
②
加成反应发生在不饱和?碳?原子上;
③该反应中加进原子或原子团,只生成一种有机物?相当于化合反应),只进不出。
④加成前后的有机物的结构将发生变化,烯烃变烷烃,结构由平面形变立体形;炔烃变烯烃,结构由直线形变平面形;
⑤加成反应是不饱和化合物的较特有反应,另外,芳香族化合物也有可能发生加成反应。
有机反应类型——加成反应
和H2加成的条件一般是催化剂(Ni)+加热
和水加成时,一般在一定的温度、压强和催化剂条件下
不对称烯烃或炔烃和H2O、HX加成时可能产生两种产物
醛基的C=O只能和H2加成,不能和X2加成,而羧基和酯的C=O不能发生加成反应
若一种物质中同时存在C=C、醛基等多个官能团时,和氢气的加成反应可同时进行,也可以有选择地进行,看信息而定
(条件、现象、应用)
(1)C=C与H2、X2、HX、H2O:
(2)C≡C与H2、X2、HX、H2O:
(3)苯与H2
(4)醛与氢气加成:
(5)油脂氢化:
有机反应类型——消去反应
原理:“无进有出”
包括:醇消去H2O生成烯烃、
卤代烃消去HX生成烯烃
有机反应类型——消去反应
说明:
消去反应的实质:—OH或—X与所在碳相邻的碳原子上的-H结合生成H2O或HX而消去
不能发生消去反应的情况:—OH或—X所在的碳无相邻碳原子,或相邻碳原子上无氢(注意区分不能消去和不能氧化的醇)
有不对称消去的情况,由信息定产物
消去反应的条件:醇类是浓硫酸+加热;
卤代烃是NaOH醇溶液+加热
有机反应类型——氧化反应
原理:有机物得氧或去氢
包括:
燃烧反应、被空气(氧气)氧化、(醇是去氢氧化)
被酸性KMnO4溶液氧化,
醛基的银镜反应和被新制Cu(OH)2悬浊液氧化
烯烃被臭氧氧化
(O3,Zn/HCl,双键断裂,原双键碳变为C=O)
有机反应类型——氧化反应
说明:
有机物一般都可以发生氧化反应,此过程发生了碳碳键或碳氧键的断裂
醇氧化的规律:
伯醇氧化生成醛,如CH3CH2OH
仲醇氧化生成酮,如(CH3)2CHOH
叔醇不能被氧化,如(CH3)3COH
多官能团物质被氧化的顺序看信息
有机反应类型——还原反应
原理:有机物得氢或去氧
包括:烯、炔、苯环、醛、油脂等和氢气加成,
硝基被还原为氨基
(如硝基苯被Fe+HCl还原为苯胺)
说明:“氧化”和“还原”反应是针对有机物而言的,有机物被氧化则定义为氧化反应,有机物被还原则定义为还原反应
有机反应类型——加聚反应
类型(联系书上提到的高分子材料):
乙烯型加聚
聚丙烯、聚苯乙烯、聚氯乙烯、
聚丙烯腈、聚甲基丙烯酸甲酯(有机玻璃)
1,3-丁二烯型加聚(破两头,移中间)
天然橡胶(聚异戊二烯)
氯丁橡胶(聚一氯丁二烯)
含有双键的不同单体间的共聚
乙丙树脂(乙烯和丙烯共聚),
丁苯橡胶(丁二烯和苯乙烯共聚)
有机反应类型——加聚反应
说明
单体通常是含有C=C或C≡C的化合物
链节与单体的相对分子质量相等
产物中仅有高聚物,无其它小分子,但生成的高聚物因n值不同,是混合物
由加聚产物判断单体的“二、四”法
有机反应类型——缩聚反应
类型
酚醛缩聚(高聚物链节中含酚羟基)
苯酚和甲醛缩聚成酚醛树脂(电木)
氨基酸缩聚(高聚物链节中含酰胺键)
氨基酸缩合成多肽或蛋白质
醇酸缩聚(高聚物链节中含酯基)
乙二醇和乙二酸(或对苯二甲酸)的缩聚
有机反应类型——缩聚反应
说明
缩聚反应生成高分子和小分子,如H2O
若高分子化合物的链节并非完全以碳原子连接,如有酚羟基、-COO-、-CO-NH-等,则该高分子是缩聚反应的产物
判断缩聚反应的单体(水解法):
先判断缩聚类型,再解聚
解聚方法:先断开羰基与氧原子(或氮原子)之间的键,然后给羰基加上羟基,给氧或氮接上氢原子,链节两端的羰基、氧或氮也按此法接上羟基或氧原子
有机反应类型——显色反应
包括
苯酚遇FeCl3溶液显紫色
淀粉遇碘单质显蓝色
含苯环的蛋白质遇浓硝酸凝结显黄色
多羟基物质(甘油、葡萄糖)与新制Cu(OH)2悬浊液生成绛蓝色物质
有机反应类型——酯化反应拓展
机理:一般为羧酸脱羟基,醇脱氢
类型
一元羧酸和一元醇反应生成普通酯
二元羧酸和二元醇
部分酯化生成普通酯和1分子H2O,
或生成环状酯和2分子H2O,
或生成高聚酯和2n
H2O
羟基羧酸自身反应既可以部分酯化生成普通酯,也可以生成环状酯,还可以生成高聚酯。如乳酸分子
有机反应类型——酯化反应拓展
乙二酸和乙二醇酯化
有机反应类型——酯化反应拓展
其它酯
硝化甘油(三硝酸甘油酯)
硝酸纤维(纤维素硝酸酯)
油脂(硬脂酸甘油酯、软脂酸甘油酯、油酸甘油酯)
苯酚中的羟基也能发生酯化反应(且水解后还消耗NaOH)
有机反应类型——知识归纳
反应条件不同,反应不同
温度不同,产物和反应类型不同:
如乙醇在浓硫酸140℃和170℃的反应
溶剂不同,产物和反应类型不同:
如溴乙烷在NaOH的水溶液和醇溶液下的反应
催化剂不同,反应不同:
如甲苯在铁催化和光照条件下和氯气的取代反应
有机反应类型——知识归纳
书写有机化学反应的注意事项
写有机物的结构简式及反应条件
不漏写除了有机物外的其它无机小分子
如酯化反应、硝化反应、醇催化氧化、缩聚反应生成的H2O;卤代反应生成的HX等
配平:如醇、醛的催化氧化、银镜反应
专用名词不能出错
如,苯写“笨”、“酯”和“脂”混用、“硝化”写“消化”,
“水浴”写成“水狱”,“褪色”写成“腿色”
有机反应类型——知识归纳
反应条件
常
见
反
应
催化剂加热加压
乙烯水化、油脂氢化
催化剂
加热
烯、炔、苯环、醛加氢,
烯、炔和HX加成,醇的消去和氧化,乙醛和氧气反应,酯化反应
水浴加热
制硝基苯、银镜反应、蔗糖水解、
乙酸乙酯水解
只用催化剂
苯的溴代
只需加热
卤代烃消去、乙醛和Cu(OH)2反应
不需外加
条件
制乙炔,烯与炔加溴,烯、炔及苯的同系物被KMnO4氧化,苯酚的溴代,卤代烃的水解
有机反应类型——知识归纳
反应条件
反应类型
NaOH水溶液、加热
卤代烃或酯类的水解反应
NaOH醇溶液、加热
卤代烃的消去反应
稀H2SO4、加热
酯和糖类的水解反应
浓H2SO4、加热
酯化反应或苯环上的硝化反应
浓H2SO4、170℃
醇的消去反应
浓H2SO4、140℃
醇生成醚的取代反应
溴水
不饱和有机物的加成反应
浓溴水
苯酚的取代反应
有机反应类型——知识归纳
反应条件
反应类型
液Br2、Fe粉
苯环上的取代反应
X2、光照
烷烃或芳香烃烷基上的卤代
O2、Cu、加热
醇的催化氧化反应
O2或Ag(NH3)2OH或新制Cu(OH)2
醛的氧化反应
酸性KMnO4溶液
不饱和有机物或苯的同系物侧链上的氧化反应
H2、催化剂
不饱和有机物的加成反应
有机反应类型——加成反应
原理:“有进无出”
包括:烯烃及含C=C的有机物、炔烃及含C≡C的有机物与H2、X2、HX、H2O加成、苯环、醛基、不饱和油脂与H2加成
有机反应类型——加成反应
和H2加成的条件一般是催化剂(Ni)+加热
和水加成时,一般在一定的温度、压强和催化剂条件下
不对称烯烃或炔烃和H2O、HX加成时可能产生两种产物
醛基的C=O只能和H2加成,不能和X2加成,而羧基和酯的C=O不能发生加成反应
若一种物质中同时存在C=C、醛基等多个官能团时,和氢气的加成反应可同时进行,也可以有选择地进行,看信息而定
有机反应类型——消去反应
原理:“无进有出”
包括:醇消去H2O生成烯烃、
卤代烃消去HX生成烯烃
有机反应类型——消去反应
说明:
消去反应的实质:—OH或—X与所在碳相邻的碳原子上的-H结合生成H2O或HX而消去
不能发生消去反应的情况:—OH或—X所在的碳无相邻碳原子,或相邻碳原子上无氢(注意区分不能消去和不能氧化的醇)
有不对称消去的情况,由信息定产物
消去反应的条件:醇类是浓硫酸+加热;
卤代烃是NaOH醇溶液+加热
有机反应类型——氧化反应
原理:有机物得氧或去氢
包括:
燃烧反应、被空气(氧气)氧化、(醇是去氢氧化)
被酸性KMnO4溶液氧化,
醛基的银镜反应和被新制Cu(OH)2悬浊液氧化
烯烃被臭氧氧化
(O3,Zn/HCl,双键断裂,原双键碳变为C=O)
有机反应类型——氧化反应
说明:
有机物一般都可以发生氧化反应,此过程发生了碳碳键或碳氧键的断裂
醇氧化的规律:
伯醇氧化生成醛,如CH3CH2OH
仲醇氧化生成酮,如(CH3)2CHOH
叔醇不能被氧化,如(CH3)3COH
多官能团物质被氧化的顺序看信息
有机反应类型——还原反应
原理:有机物得氢或去氧
包括:烯、炔、苯环、醛、油脂等和氢气加成,
硝基被还原为氨基
(如硝基苯被Fe+HCl还原为苯胺)
说明:“氧化”和“还原”反应是针对有机物而言的,有机物被氧化则定义为氧化反应,有机物被还原则定义为还原反应
有机反应类型——加聚反应
类型(联系书上提到的高分子材料):
乙烯型加聚
聚丙烯、聚苯乙烯、聚氯乙烯、
聚丙烯腈、聚甲基丙烯酸甲酯(有机玻璃)
1,3-丁二烯型加聚(破两头,移中间)
天然橡胶(聚异戊二烯)
氯丁橡胶(聚一氯丁二烯)
含有双键的不同单体间的共聚
乙丙树脂(乙烯和丙烯共聚),
丁苯橡胶(丁二烯和苯乙烯共聚)
有机反应类型——加聚反应
说明
单体通常是含有C=C或C≡C的化合物
链节与单体的相对分子质量相等
产物中仅有高聚物,无其它小分子,但生成的高聚物因n值不同,是混合物
由加聚产物判断单体的“二、四”法
有机反应类型——缩聚反应
类型
酚醛缩聚(高聚物链节中含酚羟基)
苯酚和甲醛缩聚成酚醛树脂(电木)
氨基酸缩聚(高聚物链节中含酰胺键)
氨基酸缩合成多肽或蛋白质
醇酸缩聚(高聚物链节中含酯基)
乙二醇和乙二酸(或对苯二甲酸)的缩聚
有机反应类型——缩聚反应
说明
缩聚反应生成高分子和小分子,如H2O
若高分子化合物的链节并非完全以碳原子连接,如有酚羟基、-COO-、-CO-NH-等,则该高分子是缩聚反应的产物
判断缩聚反应的单体(水解法):
先判断缩聚类型,再解聚
解聚方法:先断开羰基与氧原子(或氮原子)之间的键,然后给羰基加上羟基,给氧或氮接上氢原子,链节两端的羰基、氧或氮也按此法接上羟基或氧原子
有机反应类型——显色反应
包括
苯酚遇FeCl3溶液显紫色
淀粉遇碘单质显蓝色
含苯环的蛋白质遇浓硝酸凝结显黄色
多羟基物质(甘油、葡萄糖)与新制Cu(OH)2悬浊液生成绛蓝色物质
有机反应类型——酯化反应拓展
机理:一般为羧酸脱羟基,醇脱氢
类型
一元羧酸和一元醇反应生成普通酯
二元羧酸和二元醇
部分酯化生成普通酯和1分子H2O,
或生成环状酯和2分子H2O,
或生成高聚酯和2n
H2O
羟基羧酸自身反应既可以部分酯化生成普通酯,也可以生成环状酯,还可以生成高聚酯。如乳酸分子
有机反应类型——酯化反应拓展
乙二酸和乙二醇酯化
有机反应类型——酯化反应拓展
其它酯
硝化甘油(三硝酸甘油酯)
硝酸纤维(纤维素硝酸酯)
油脂(硬脂酸甘油酯、软脂酸甘油酯、油酸甘油酯)
苯酚中的羟基也能发生酯化反应(且水解后还消耗NaOH)
有机反应类型——知识归纳
反应条件不同,反应不同
温度不同,产物和反应类型不同:
如乙醇在浓硫酸140℃和170℃的反应
溶剂不同,产物和反应类型不同:
如溴乙烷在NaOH的水溶液和醇溶液下的反应
催化剂不同,反应不同:
如甲苯在铁催化和光照条件下和氯气的取代反应
有机反应类型——知识归纳
书写有机化学反应的注意事项
写有机物的结构简式及反应条件
不漏写除了有机物外的其它无机小分子
如酯化反应、硝化反应、醇催化氧化、缩聚反应生成的H2O;卤代反应生成的HX等
配平:如醇、醛的催化氧化、银镜反应
专用名词不能出错
如,苯写“笨”、“酯”和“脂”混用、“硝化”写“消化”,
“水浴”写成“水狱”,“褪色”写成“腿色”
有机反应类型——知识归纳
反应条件
常
见
反
应
催化剂加热加压
乙烯水化、油脂氢化
催化剂
加热
烯、炔、苯环、醛加氢,
烯、炔和HX加成,醇的消去和氧化,乙醛和氧气反应,酯化反应
水浴加热
制硝基苯、银镜反应、蔗糖水解、
乙酸乙酯水解
只用催化剂
苯的溴代
只需加热
卤代烃消去、乙醛和Cu(OH)2反应
不需外加
条件
制乙炔,烯与炔加溴,烯、炔及苯的同系物被KMnO4氧化,苯酚的溴代,卤代烃的水解
有机反应类型——知识归纳
反应条件
反应类型
NaOH水溶液、加热
卤代烃或酯类的水解反应
NaOH醇溶液、加热
卤代烃的消去反应
稀H2SO4、加热
酯和糖类的水解反应
浓H2SO4、加热
酯化反应或苯环上的硝化反应
浓H2SO4、170℃
醇的消去反应
浓H2SO4、140℃
醇生成醚的取代反应
溴水
不饱和有机物的加成反应
浓溴水
苯酚的取代反应
有机反应类型——知识归纳
反应条件
反应类型
液Br2、Fe粉
苯环上的取代反应
X2、光照
烷烃或芳香烃烷基上的卤代
O2、Cu、加热
醇的催化氧化反应
O2或Ag(NH3)2OH或新制Cu(OH)2
醛的氧化反应
酸性KMnO4溶液
不饱和有机物或苯的同系物侧链上的氧化反应
H2、催化剂
不饱和有机物的加成反应
三、消去反应
①
是一类有机反应;
②
消去反应发生在分子内
③
发生在相邻的两个碳原子上;
④
消去反应会脱去小分子,即生成小分子;
⑤
消去后生成的有机物会产生双键或叁键;
⑥
消去前后的有机物的分子结构变发生变化,它与加成反应相反,因此,分子结构的变化正好与加成反应的情况相反。
具体的消去反应
卤代烃消去
C2H5Br+
NaOH→
2.
醇消去
C2H5OH→
四、聚合反应
?1?
加成聚合反应:简称加聚反应
A.CH2=CH2
B.CH3-CH=CH2
C.CH2=CHCl
D.CF2=CF2
E.C6H5-CH=G.
F.HCHO
(2).缩聚反应
双官能团的有机物、苯酚和甲醛氨基酸、醇和羧酸
nHOOCCOOH+nHOCH2CH2OH→
五、氧化反应
醇氧化成醛:C2H5OH
+
O2→
醛、甲酸、甲酸酯、葡萄糖、
麦芽糖的氧化
CH3CHO+
Ag(NH3)2OH→
使酸性高锰酸钾溶液褪色:
乙烯、乙炔
甲苯、苯酚、乙醛
六、还原反应
去氧、加氢是有机化学里的还原反应
不饱和烃及不饱和化合物的加氢,
油酯的氢化;
苯加氢变为环己烷,
苯乙烯加氢变成乙基环己烷
七、其它反应
1.裂化(解)反应
①
甲烷的高温分解
②
石油的裂化
石油的裂解
2.显色反应
(1)苯酚与铁盐溶液络合呈紫色
(2)蛋白质与浓硝酸作用呈黄色
(3)碘遇淀粉变蓝
